|
Патентная документация ЕАПВ |
|
||
| Запрос: | ea000008339b*\id |
|
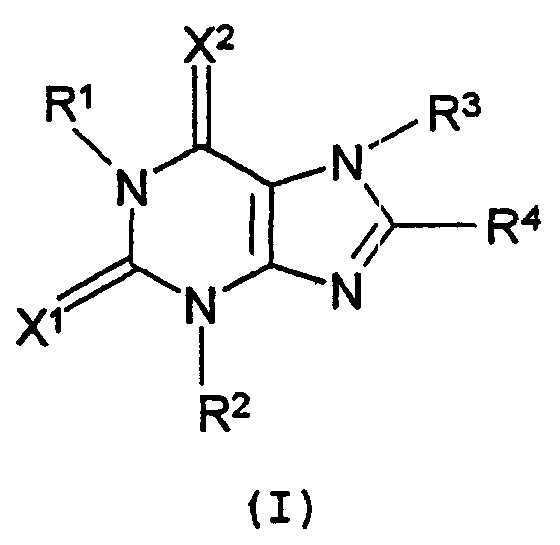
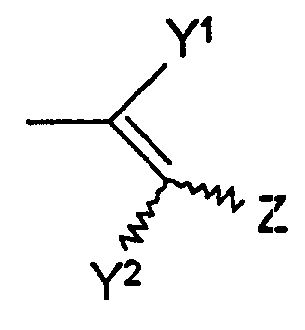
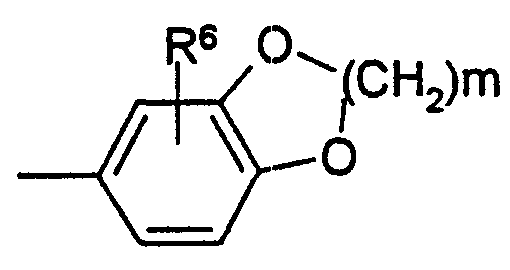
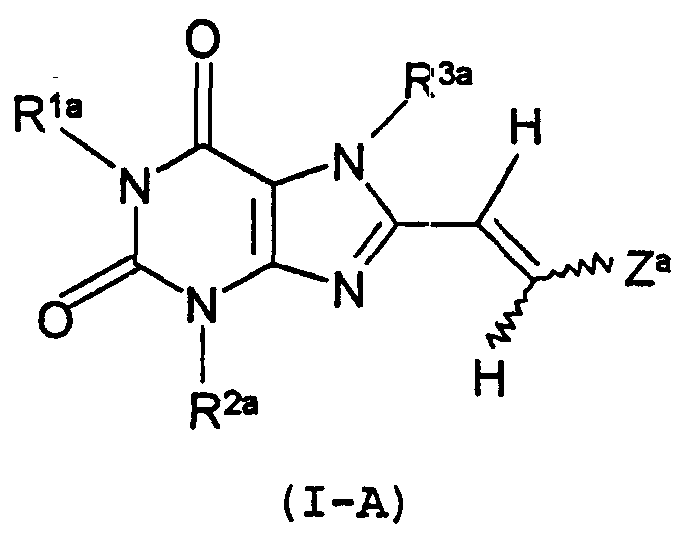
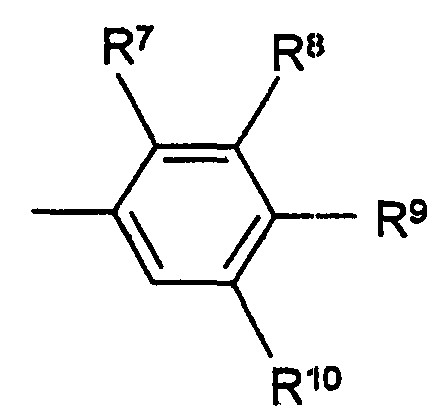
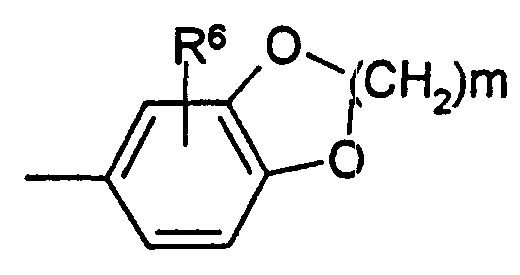
Термины запроса в документе Реферат 1. Способ лечения синдрома усталых ног, включающий введение нуждающемуся в этом пациенту эффективного количества по меньшей мере одного антагониста рецептора А 2A аденозина, представленного следующей формулой (I) в которой R 1 , R 2 и R 3 независимо обозначают водород, (C 1 -C 8 )алкил, (C 2 -C 8 )алкенил или (C 2 -C 8 )алкинил; R 4 обозначает (C 3 -C 8 )циклоалкил, группу -(CH 2 ) n -R 5 (в которой R 5 обозначает замещенный или незамещенный (C 6 -C 14 )арил, или замещенную или незамещенную гетероциклическую группу, а n обозначает целое число от 0 до 4) или группу {в которой Y 1 и Y 2 независимо обозначают водород, галоген или (C 1 -C 8 )алкил; и Z обозначает замещенный или незамещенный (С 6 -С 14 )арил, или группу (в которой R 6 обозначает водород, гидрокси, (C 1 -C 8 )алкил, (C 1 -C 8 )алкокси, галоген, нитро- или аминогруппу; и m обозначает целое число от 1 до 3)}; и X 1 и X 2 , независимо, обозначают О или S. 2. Способ лечения синдрома усталых ног по п.1, в котором антагонист рецептора А 2A аденозина представляет собой соединение формулы (I-А) в которой R la и R 2a независимо обозначают метил или этил; R 3a обозначает водород или (C 1 -C 8 )алкил; и Z a обозначает группу (в которой по меньшей мере один из R 7 , R 8 и R 9 обозначают (C 1 -C 8 )алкил или (C 1 -C 8 )алкокси, а другие обозначают атом водорода; R 10 обозначает водород или (C 1 -C 8 )алкил) или группу (в которой R 6 и m соответственно имеют значения, указанные выше). 3. Способ лечения синдрома усталых ног по п.1, в котором антагонист рецептора А 2A аденозина представляет собой соединение (Е)-8-(3,4-диметоксистирил)-1,3-диэтил-7-метилксантин. 4. Применение антагониста рецептора А 2A аденозина, охарактеризованного в любом из пп.1-3, для получения терапевтического средства для лечения синдрома усталых ног. 5. Терапевтическое средство для лечения синдрома усталых ног, содержащее антагонист рецептора А 2A аденозина, охарактеризованный в любом из пп.1-3. 6. Способ лечения ночного миоклонуса, включающий введение эффективного количества антагониста рецептора А 2A аденозина, охарактеризованного в любом из пп.1-3, нуждающемуся в этом пациенту.
Полный текст патента (57) Реферат / Формула: в которой R 1 , R 2 и R 3 независимо обозначают водород, (C 1 -C 8 )алкил, (C 2 -C 8 )алкенил или (C 2 -C 8 )алкинил; R 4 обозначает (C 3 -C 8 )циклоалкил, группу -(CH 2 ) n -R 5 (в которой R 5 обозначает замещенный или незамещенный (C 6 -C 14 )арил, или замещенную или незамещенную гетероциклическую группу, а n обозначает целое число от 0 до 4) или группу {в которой Y 1 и Y 2 независимо обозначают водород, галоген или (C 1 -C 8 )алкил; и Z обозначает замещенный или незамещенный (С 6 -С 14 )арил, или группу (в которой R 6 обозначает водород, гидрокси, (C 1 -C 8 )алкил, (C 1 -C 8 )алкокси, галоген, нитро- или аминогруппу; и m обозначает целое число от 1 до 3)}; и X 1 и X 2 , независимо, обозначают О или S. 2. Способ лечения синдрома усталых ног по п.1, в котором антагонист рецептора А 2A аденозина представляет собой соединение формулы (I-А) в которой R la и R 2a независимо обозначают метил или этил; R 3a обозначает водород или (C 1 -C 8 )алкил; и Z a обозначает группу (в которой по меньшей мере один из R 7 , R 8 и R 9 обозначают (C 1 -C 8 )алкил или (C 1 -C 8 )алкокси, а другие обозначают атом водорода; R 10 обозначает водород или (C 1 -C 8 )алкил) или группу (в которой R 6 и m соответственно имеют значения, указанные выше). 3. Способ лечения синдрома усталых ног по п.1, в котором антагонист рецептора А 2A аденозина представляет собой соединение (Е)-8-(3,4-диметоксистирил)-1,3-диэтил-7-метилксантин. 4. Применение антагониста рецептора А 2A аденозина, охарактеризованного в любом из пп.1-3, для получения терапевтического средства для лечения синдрома усталых ног. 5. Терапевтическое средство для лечения синдрома усталых ног, содержащее антагонист рецептора А 2A аденозина, охарактеризованный в любом из пп.1-3. 6. Способ лечения ночного миоклонуса, включающий введение эффективного количества антагониста рецептора А 2A аденозина, охарактеризованного в любом из пп.1-3, нуждающемуся в этом пациенту.
008339 Область техники, к которой относится изобретение Настоящее изобретение относится к способам лечения синдрома усталых ног или связанных с ним заболеваний. Способ лечения предпочтительно представляет собой введение фармацевтического агента, содержащего терапевтически эффективное количество антагониста рецептора А2д аденозина. Более предпочтительно антагонист рецептора А2А аденозина представляет собой производное ксантина. Еще более предпочтительно антагонист рецептора А2А аденозина представляет собой производное ксантина, описанное подробно в данном описании. Уровень техники Синдром усталых ног Синдром усталых ног (RLS) является характерным, но часто ошибочно диагностируемым сенсорно-двигательным заболеванием. Процент заболеваемости RLS является высоким и занимает седьмое место среди наиболее часто диагностируемых скелетно-мышечных заболеваний из 103 диагнозов, относящихся к такого рода состояниям [Arch. Intern. Med., 161, 483-484 (2001)]. Синдром RLS часто характеризуется как расстройство сна и диагностируется как причина бессонницы [Sleep Med., 2, 367-369 (2001); и Sleep, 23, 237-241 (222)]. Хотя RLS был описан впервые в XVII веке, классические признаки, которые определяют синдром, первый раз были представлены в 1945 г. [The London practice of Physick. London: Bassett et al. Eds. (1962); и Acta Med. Scand. Suppl., 158, 1-123 (1945)]. Несмотря на годы, прошедшие с тех пор как синдрому RLS было впервые дано медицинское определение, диагностика и лечение его остаются недостаточно оптимальными. Даже при том, что это заболевание может поражать до 10% населения США, оно часто не распознается или ошибочно диагностируется. В некоторых случаях обнаруживают, что причиной может являться железо-дефицитная анемия, и тогда RLS излечивают. Однако в целом, двигательная усталость плохо диагностируется и лечится [IJCP, 55, 320-322 (2001)]. Несмотря на то, что этиология RLS неизвестна, основная анатомическая локализация функциональной патологии при RLS по всей вероятности располагается в спинальной системе [Disord., 13 (suppl 2), 294 (1998)]. Несколько новых диагностических методов могут помочь в идентификации RLS [J.Neurol., 249, 164-170 (2002); и Clin. Neurophys., 113, 571-578 (2002)]. Признаки, присущие RLS, включают дизестезию в глубине конечности, которая вынуждает человека двигаться для того, чтобы уменьшить это ощущение, которое возникает и усиливается при отдыхе, прежде всего в вечернее время и ночные часы [HealthNews, Greene, June, 10 (2001)]. В 1995 г. Международная группа исследования RLS (International RLS Study Group) опубликовала основные и сопутствующие признаки этого заболевания [Mov. Dis., 10), 634-642 (1995)]. В качестве недавних публикаций см. Latorre & Irr 2001 http://www.emedicine.com/NEURO/topic509.htm; 2001 Medical Bulletin, Restless Legs Syndrome Foundation, Inc.; и Am.J.Med.Sci., 319, 397-403 (2000). Дополнительные критерии RLS включают непроизвольные ритмичные сократительные движения, появляющиеся особенно в ночные часы, и, в частности, во время I и II стадий сна; и расстройство сна, которое вызывает дневную усталость. Хотя синдром RLS встречается как компонент некоторых заболеваний, он не является показательным признаком этих заболеваний [Sleep, 23, 361-367 (2000); Arch. Neurol., 59, 421-424 (2002); J. Neurol. Sci., 196, 33-36 (2002); и J. Neurol. Neurosurg. Psych., 72, 555 (2002)]. Согласно данным организации Restless Legs Syndrome Foundation (www.rls.org), взрослые больные RLS обычно имеют все четыре основных признака, описанных ниже. Первое, беспокоящее, обычно безболезненное, ощущение глубоко в ногах, вызывающее непреодолимую потребность в движении. Второе, симптомы усиливаются или появляются исключительно тогда, когда страдающий пациент находится в состоянии покоя, и эти ощущения обычно уменьшаются при произвольном движении пораженной конечности. Третье, симптомы усиливаются в вечернее и ночное время, особенно, когда больной принимает лежачее положение. И, четвертое, движения пальцев ноги, ступней или самих ног (называемые усталостью ног), как правило, проявляются тогда, когда больной сидит или ложится в вечернее время. Эта усталость может восприниматься как беспокойство или нервозность. Дизестезия и сопутствующая ей потребность двигаться возникают наиболее часто вечером или в первой половине ночи (между 6 часами вечера и 4 часами утра) [Sleep, 22, 901-912 (1999); и Mov. Disord., 14, 102-110 (1999)]. Пациентов меньше беспокоят симптомы в дневное время, и, даже в случае тяжелого состояния, часто испытывают облегчение ближе к рассвету. У более двух третей больных RLS эти симптомы со временем прогрессируют и могут оказаться настолько тяжелыми, что приводят к потере дееспособности, нарушению сна и оказывают негативное влияние на жизнь пациентов и его благополучие. Взрослые больные RLS почти всегда описывают эти неприятные ощущения или скованность, которые происходят главным образом в ногах, как напоминающие воздействие электрического тока, движение воды, ползание насекомых или покалывание, боль или хватание. Было предложено много других разнообразных описаний, но некоторые больные не могут описать вообще свои ощущения, кроме ощущения потребности двигать ногой [Neurol., 47, 1435-1441 (1996)]. Существенно меньшее количество больных с синдромом RLS (приблизительно 20-30%) испытывают аналогичные ощущения в руках, но это характерно обычно для больных с более тяжелой степенью поражения на поздней клинической стадии этого заболевания [Eur. Neurol., 45, 67-74 (2001); и Eur. - 1 - 008339 Neurol., 44, 133-138 (2000)]. Реже эти ощущения испытывают по всему туловищу или где-либо в другом месте. Как правило, ощущения не описываются как болезненные, но если непосредственно спросить больных, то меньшинство (приблизительно 20%) опишет свои ощущения как болезненные. Появлению этих неприятных ощущений при RLS способствует бездействие или отдых, такое как лежание в кровати, поездка в автомашине или перелет в самолете или пребывание в театре. Некоторые больные жалуются на увеличивающееся чувство дискомфорта и непроизвольное подергивание конечности, когда они находятся в неподвижном состоянии. Появляется потребность переместить ноги, потому что часто приходит облегчение после перемещения. Чтобы удовлетворить потребность в движении, больные, в типичных случаях, начинают ходить, хотя они могут попытаться получить облегчение посредством выполнения разнообразных движений, таких как раскачивание, встряхивание, вытягивание, шаг на месте, расхаживание или сгибание. Некоторые больные получают облегчение просто когда они стоят. Эти разнообразные движения, которые больной выбирает для облегчения симптомов, находятся под его собственным контролем и могут быть прекращены по команде. Однако прекращение движений может сильно увеличить чувство дискомфорта больного и некоторые тяжело больные пациенты в состоянии остановить эти повторяющиеся движения за более короткий период времени, если они являются симптоматическими. В редких случаях, движения могут возникать как доминирующие симптомы, только при этом степень понимания необходимости двигаться очень низка. В большинстве случаев, причина возникновения RLS неизвестна. Такая идиопатическая болезнь может быть наследственной болезнью и в этом случае она передается аутосомно-доминантным путем. В некоторых семьях отмечается постепенное уменьшение возраста начала заболевания в последующих поколениях. Больные с наследственной болезнью RLS имеют тенденцию к наступлению болезни в более раннем возрасте и к более медленному ее развитию. Несмотря на использование допаминергических агентов для лечения RLS, гены, вовлеченные в допаминергическую нейротрансмиссию, как оказалось, не оказывают никакого влияния на RLS [Neurol., 57, 1304-1306 (2001)]. Признаки, связанные с RLS Симптомы RLS могут привести к проблемам засыпания и сна, что приводит к значительной усталости в дневное время. Хроническое недосыпание и, как следствие, сонливость в течение дня, могут сказаться на работоспособности пациентов, на участии их в общественной жизни, на том, как они проводят время на отдыхе и могут быть причиной изменения настроения, что может сказаться на их личных взаимоотношениях. Заболевание RLS может стать причиной другого состояния, которое, когда оно есть, ухудшает основной RLS. Это называется вторичным RLS. Во время беременности, особенно в течение последних нескольких месяцев, у 15% женщин развивается RLS. После родов симптомы его исчезают. Другими причинами могут быть следующие: дефицит железа, фолатов, витамина В12 или магния. Дефицит железа, фолатов и В12 может привести к анемии. Дефицит магния встречается редко, за исключением случаев, когда придерживаются необычных диет. Синдром RLS может быть начальным симптомом дефицита железа. Полиневропатия также может привести к RLS. Полиневропатия может быть вызвана злоупотреблением алкоголя, амилоидозом, сахарным диабетом, пояснично-крестцовой радикулопатией, болезнью Лайма, ревматоидным артритом, уремией или дефицитом витамина В12. Операция на желудке, которая приводит к плохому усвоению пищи. Хроническая обструктивная болезнь легких (COPD) может привести к изменению химического состава крови, такому как ацидоз или алкалоз, низкая насыщенность кислородом или задержка диоксида кремния. Эти химические изменения в крови могут в свою очередь раздражать периферические нервы и привести к заболеванию RLS. Хроническая венозная недостаточность или варикозная болезнь вен. Потребление некоторых наркотиков, таких как алкоголь, кофеин, противосудорожные агенты, антидепрессанты, бета-блокаторы, литиевые препараты или основные транквилизаторы. Синдром отмены некоторых лекарств, таких как сосудорасширяющие средства, седативные или антидепрессантные средства. Миелопатия или миелит. Гипотиреоз или гипертиреоз. Гипопаратиреоз или гиперпаратиреоз. Острая перемежающаяся порфирия. Печеночная недостаточность. Рак. Хотя RLS диагностируют наиболее часто у людей среднего возраста, многие больные с RLS, в частности, с первичным RLS, могут отследить свои симптомы начиная с детского возраста. Эти симптомы возможно назывались возрастными болями конечностей у ребенка или, как считали, у ребенка была гиперактивность, потому что он с трудом мог сидеть спокойно. Не существует какого-либо лабораторного теста, который мог бы подтвердить диагноз RLS. Однако, тщательное обследование больного, включающее результаты необходимых лабораторных исследований, может обнаружить временные нарушения, такие как дефицит железа, который может быть связан с заболеванием RLS. Некоторым больным может потребоваться проведение ночного мониторинга для того, чтобы определить другие причины нарушения сна. - 2 - 008339 Лечение Если выясняется, что дефицит основного железа или витамина является причиной синдрома усталых ног у больного, то дополнительное введение железа, витамина В12 или фолата (как указано) может оказаться достаточным для облегчения симптомов. Современные рекомендации включают анализ уровня ферритина в сыворотке (чтобы определить статус накопления железа) и дополнительное введение железа, если уровень ферритина ниже 50 мкг/л. У больных с варикозным заболеванием вен отмечалось улучшение вследствие применения склерозирующих агентов. Больные с уремией могут почувствовать облегчение после трансплантации почек или коррекции анемии с помощью эритропоетина. Оказалось, что применение некоторых лекарственных средств усиливает симптомы RLS. Такими лекарственными средствами являются блокаторы кальциевых каналов, большинство противорвотных средств, некоторые средства против простуды и аллергии, основные транквилизаторы, фенитоин и большинство антидепрессантов. К сожалению в большинстве случаев симптомы RLS либо изначально не устраняются в результате лечения основных заболеваний и изменения образа жизни, либо через некоторое время прогрессируют так, что улучшение становится незначительным с помощью этих методов. В обоих случаях может возникнуть необходимость в применении лекарственных средств. Ни одно лекарство для лечения RLS не было одобрено Администрацией США по Продуктам питания и Лекарствам (Food and Drug Administration), однако, некоторые лекарственные средства прошли клинические испытания на больных RLS и были одобрены для лечения других болезней. Эти лекарственные средства делятся на четыре основных класса: допаминергические агенты, седативные средства, болеутоляющие средства и противосудорожные средства. Каждое лекарственное средство или класс лекарственных средств имеет свои преимущества, ограничения и профиль побочного эффекта. Выбор лекарственного средства зависит от продолжительности и серьезности симптомов. Обычно лечение начинают с низкой дозы за час или два до сна. Если появляется привыкание к какому-либо лекарству, то его можно заменить лекарством другого класса. Допаминергические агенты Основным и первоочередным в лечении RLS является использование допаминергических агентов [Expert Opin. Investig. Drugs, 116 501-514 (2002); Neurol., 58. (Suppl.1), S87-S92 (2002); и Danek et al. In Neurological Disorders: Course and Treatment Academic Press, pp. 819-823 (1996)]; вовлечение измененной активности допаминергических диэнцефальных спинальных нейронов, которое возникает в области A11 мозга [Brain Res., 342, 340-351 (1985)]. Хотя допаминергические агенты используются для лечения болезни Паркинсона, синдром RLS не считается проявлением болезни Паркинсона [J.Neurol. Sci., 196, 33-36 (2002)]. Все эти препараты начинают принимать в малых дозах и увеличивают их очень медленно, чтобы уменьшить возможные побочные эффекты. Из-за побочных эффектов, ухудшающих состояние пациента, вызванных продолжительной допаминергической активацией, постоянный прием этого класса лекарственных средств для лечения RLS не был одобрен. Для лечения RLS описаны разнообразные допаминергические агенты. В их числе находятся карби-допа, леводопа, карбидопа с леводопой (Sinemet), ропинирол, прамипексол, каберголин, энтакапон и пи-рибедил [Mov. Dis., 17, 421 (2002); Mov., Dis., 16, 579-581 (2001); Eur. Neurol., 46 (suppl 1), 24-26 (2001); патент US 6194445; 6114326; 6001861; 5945424; и описание к патенту US 2001/0029262]. Допаминергические агенты могут быть причиной побочного эффекта известного как аугментация или появление обратного эффекта. Аугментация обозначает более раннее проявление симптомов в вечернее время, чем это было до начала лечения, появление симптомов в течение дня, в других частях тела и усиление симптомов. Единственное средство состоит в прекращении приема лекарства. Другие побочные эффекты включают тошноту, головокружение, сонливость, бессоницу, запор, постуральную гипотонию, астению и галлюцинацию. Седативные средства Седативные средства наиболее эффективны для уменьшения проявлений симптомов RLS в ночное время. Их применяют или на ночь перед сном в дополнение к допаминергическому агенту, или для лиц, которые страдают в основном проявлениями симптомов в ночное время. Наиболее распространенным успокоительным средством является клонозепам (Klonopin). Другие предложенные препараты, такие как антигистаминные и антагонисты рецепторов NK1, могут действовать благодаря их седативному эффекту. Болеутоляющие средства Болеутоляющие средства принимаются наиболее часто больными, которые страдают тяжелыми повторяющимися симптомами RLS. Некоторые примеры лекарственных средств этого класса включают кодеин, Дарвон или Дарвосет (пропоксифен); Долофин (метадон); Перкосет (оксикодон); Ультрам (тра-мадол); и Викодин (гидрокодон). Было обнаружено, что наиболее эффективными для облегчения симптомов являются спиоидные средства, и такое смягчение было достигнуто путем внутриоболочечного введения морфина или бупивакаина [Acta Anaesthesiol. Scand., 46, 114-117 (2002)]. Опиоидные соединения являются сильнодействующими суппрессорами в отношении RLS и PLMS, но риск злоупотребления ими и привыкания к ним ограничивает их применение. Побочными эффектами и неблагоприятными ре - 3 - 008339 акциями могут быть головокружение, седативный эффект, тошнота, рвота, запор, галлюцинация и головная боль. Противосудорожные средства Эти лекарственные средства особенно эффективны лишь для некоторых, т. е. не для всех больных, у которых отмечаются симптомы в ночное время, в частности, у лиц, имеющих болевые синдромы, связанные с RLS. Габапентин (Neurontin), являющийся противосудорожным средством, зарекомендовал себя многообещающим средством для лечения симптомов RLS [Neurol., 57, 1717-1719 (2001)]. Прочие средства лечения Другие предложенные методы лечения включают чрескожную электрическую стимуляцию нерва, адаптационную терапию и различные процедуры для уменьшения венозной недостаточности, однако, ни по одному из этих вспомогательных методов не было четко установлено, что они эффективны [Health Technol. Assess., 1, 1-135 (1997); Sleep, 19, 442-444 (1996); и Dermatol. Surg., 21 328-332 (1995)]. В частности, проба Эдинбурга показала, что большинство симптомов в нижних конечностях (включая RLS) по всей вероятности имеют не венозное происхождение и хирургическая операция на венах (т.е. склеротерапия или "стриппинг" вены) вряд ли может облегчить симптомы [Brit. Med. J. 318, 353-35 (1999)]. Одна группа врачей выступает за медицинскую терапию состояния, которое они называют "гипотоническая флебопатия" (мягкая форма венозной недостаточности), однако, их клиническое описание совпадает практически полностью с симптомами RLF [Minerva Cardioangiol., 48, 277-285 (2000)]. Были предложены дополнительные фармацевтические агенты для лечения RLS. Они включают антагонисты 5НТ; a2 антагонисты, такие как Миртазапин; антагонисты NKl-рецептора; антигистаминные агенты и экстракт травы валерьяны [Neurol., 53, 1154 (1999); патенты US 6346283; 6329401; 6319927; 6281207; 6214837; и описание к патентам US 2002/0035057; 2001/0034320; 2002/0010201]. Однако Миртазапин может быть причиной RLS [Psych. Clin. Neurosci., 56, 209-210 (2002)]. Дети Последние публикации также указывают на связь между RLS и симптомами расстройства внимания и гиперактивности [Sleep, 25, 213-218 (2002)]. В ряде сообщений и в одном медицинском случае проведена оценка лечения детей. Эти сообщения содержат конкретные ответы в отношении установления и строгого соблюдения режима сна детей, ограничения приема кофеина и использования таких лекарств как клоназепам, карбидопа/леводопа, перголид или клонидин [Picchietti In Wilson, ed. Sleep thief: restless legs syndrome. Orange Park, FL: Galaxy Books pp. 82-94 (1996); Pediatr. Neurol., 22, 182-186 (2000); Sleep Res., 22, 70 (1993); Pediatr Neurol., 11, 241-245 (1994); и Sleep, 22, 297-300 (1999)]. Бензодиазепиновые, противосудорожные, альфа-адренергические агенты и опиоидные препараты широко использовались при лечении детей в случае других заболеваний, отличных от RLS, также как постоянно использовалась леводопа в случае допа-реактивной дистонии (J. Am. Acad. Child Adolesc. Psych., 33, 424-426 (1994); и Neurol., 41, 174-181 (1991)]. Открытое маркированное испытание перголида для лечения пяти детей с заболеванием RLS показало, что не только параметры сна, но также и показатели внимания и импульсивности у детей улучшились [Pediatr. Neurol., 22, 182-186 (2000)]. ПДКС (PLMS) Приблизительно 80% пациентов, страдающих синдромом RLS, имеют односторонние или двусторонние периодические движения конечностей во время сна (ПДКС), также называемые ночным миокло-нусом. У больных, не страдающих RLS, также наблюдаются ППКС. Эти подергивания стереотипны, повторяющиеся, наблюдается также небольшое сгибание конечностей (только ног или чаще ног, чем рук) на начальных стадиях сна. Движения происходят полуритмично с интервалом от 5 до 60 с и длятся приблизительно от 1,5 до 2,5 с. На нижних конечностях наблюдается повторяемый изгиб назад большого пальца с веерообразным раскрытием маленьких пальцев, при одновременном сгибании щиколоток, колена и бедра. Движения рук обычно состоят в сгибании сустава предплечья вместе с суставом запястья. Число движений может меняться от ночи к ночи. ППКС может происходить и тогда, когда пациенты бодрствуют, и называют это явление дискине-зией. Такая дискинезия является необычной и может наблюдаться у 50% людей больных RLS. ППКС увеличивается с возрастом. У тридцати пяти и более процентов людей в возрасте 65 лет и старше наблюдаются ПДКС. ПДКС происходят и у более мол: одых людей, хотя это менее характерно. Мужчины и женщины в равной мере подвержены этим симптомам. Точная причина ПДКС до сих пор остается неизвестной. Основные механизмы по всей вероятности вовлекают факторы, лежащие в нервной системе, однако, изучение не обнаружило никакой соответствующей патологии. Симптомы ПДКС не рассматриваются с медицинской точки зрения как серьезные. Тем не менее, они могут воздействовать как фактор, способствующий хронической бессоннице и/или дневной усталости, поскольку они могут стать причиной пробуждения в ночной период. Иногда, ПДКС может служить показателем серьезного медицинского заболевания, такого как болезнь почек, диабет или анемия. Ряд лекарственных средств показали себя эффективными для лечения ПДКС, однако, лечение является тогда необходимым, когда ПДКС сопровождается синдромом усталых ног (RLS), бессонницей или усталостью в дневное время. - 4 - 008339 Рецепторы А2А аденозина Аденозин, как известно, действует через четыре главных подтипа рецепторов Ль А2А, А2В, А3, которые были охарактеризованы в соответствии с их первичными последовательностями [Pharmacol. Rev., 46, 143-156 (1994)]. Рецепторы А2Л аденозина находятся в избыточном количестве в оболочке хвостатого ядра, прилежащем ядре и обонятельном бугорке у некоторых видов [Brain Res., 519, 333-337 (1990)]. Были синтезированы различные антагонисты рецептора А2А (патент US 6262106, 6222035, 6197788, 5756735, 5703085, 5670498, 5565460 и 5484920). В оболочке хвостатого ядра рецепторы А2А аденозина локализованы на нескольких нейронах и показали себя способными модулировать нейротрансмиссию у-аминобутановой кислоты (GABA), ацетил-холина и глутамата [J. Neurochem., 66, 1882-1888 (1996); J. Neurosci., 16, 605-611 (1996); Neuroscience, 100, 53-62 (2000); Trends Pharmacol. Sci., 13, 338-344 (1997); и Biosci. Biotechnol. Biochera., 65, 1447-1457 (2001)]. Эти функции рецептора А2А способствует регулированию моторного поведения, так как агони-сты рецептора А2А ингибируют двигательную активность и вызывают оцепенение у грызунов [Adv. Neurol., 80, 121-123 (1999); и Psychopharmacology, 147, 90-95 (1999)]. В отличие от этого, антагонисты рецептора А2А аденозина предотвращают нарушение моторной активности рецептора допамина D2 у голой мыши [J. Neurosci., 20, 5848-58852 (2000)]. Антагонисты рецептора А2А были исследованы на обезьянах, страдающих паркинсонизмом, и показали свою эффективность для лечения симптомов болезни Паркинсона [Ann. Neurol., 43, 507-513 (1998); NeuroReport, 9, 2857-2860 (1998); и Exp. Neurol., 162, 321-327 (2000)]. Было показано, что антагонист KW-6002 рецептора А2А аденозина усиливает антипаркинсоническую активность без возникновения гиперфункции и без появления дискинезии [Neurology, 52, 1673-1677 (1999)]. Согласно последним сведениям нейропротекторное действие антагониста KW-6002 рецептора А2А аденозина продемонстрировано на МРТР-наведенной допаминергической нейродегенерации [J. Neurochem., 80, 2620270 (2002); и J. Neurosci., 21, RC143 (1-6) (2001)] . Сущность изобретения Настоящее изобретение относится к способам лечения синдрома усталых ног или связанных с ним расстройств путем введения фармацевтического агента, содержащего терапевтически эффективное количество антагониста рецептора А2А аденозина, нуждающемуся в этом пациенту. Настоящее изобретение относится также к применению антагониста рецептора А2А аденозина для получения терапевтического агента, предназначенного для лечения синдрома усталых ног, а также к терапевтическим агентам для лечения синдрома усталых ног, содержащему антагонист рецептора аденозина. Предпочтительно, антагонистом рецептора аденозина является производное ксантина или его фармацевтически приемлемая соль. Более предпочтительно, антагонистом рецептора аденозина является производное ксан-тина или его фармацевтически приемлемая соль, описанные ниже. Подробное описание изобретения Настоящее изобретение относится к следующим объектам (1)-(26). (1) Способ лечения синдрома усталых ног, включающий введение эффективного количества по меньшей мере одного антагониста рецептора аденозина нуждающемуся в этом пациенту. (2) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора аденозина представляет собой производное ксантина или его фармацевтически приемлемую соль. (3) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (2), в котором производное ксантина представляет собой соединение формулы (I) 1 2 3 в которой R1, R2 и R3 независимо обозначают водород, низший алкил, низший алкенил или низший алки-нил; R4 обозначает циклоалкил, группу -(CH2)n-R5 (в которой R5 обозначает замещенный или незамещенный арил, или замещенную, или незамещенную гетероциклическую группу; и n обозначает целое число от 0 до 4); или группу {в которой Y1 и Y2 независимо обозначают водород, галоген или низший алкил; и Z обозначает заме II /R3 - 5 - 008339 щенный или незамещенный арил, или группу (в которой R6 обозначает водород, гидрокси, низший алкил, низший алкокси, галоген, нитро- или аминогруппу; и m обозначает целое число от 1 до 3)}; и X1 и X2 независимо обозначают О или S. (4) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (2), в котором производное ксантина представляет собой соединение формулы (I-A) JU н U-A) в которой Rla и R2a независимо обозначают метил или этил; R3a обозначает водород или низший алкил; и Za обозначает группу R7 R* R10 (в которой по меньшей мере один из радикалов R7, R8 и R9 обозначают низший алкил или низший алкокси, а другие обозначают водород; R10 обозначает водород или низший алкил) или группу i!/°-(CH2)m (в которой R6 и m соответственно имеют значения, указанные выше). (5) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (2), в котором производное ксантина представляет собой соединение формулы (I-B) R2b (I-B) в которой R1b и R2b независимо обозначают водород, пропил, бутил, низший алкенил или низший алки-нил; R3b обозначает водород или низший алкил; Zb обозначает замещенный или незамещенный нафтил, или группу (в которой R6 и m имеют соответственно значения, указанные выше); и Y1 и Y2 имеют соответственно значения, указанные выше. (6) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (2), в котором производное ксантина представляет собой (Е)-8-(3,4-диметоксистирил)-1,3-диэтил-7-метилксантин. (7) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора аденозина представляет собой соединение формулы (II) - 6 - 008339 NHQ2 R13 R12 (II) в которой R11 обозначает замещенный или незамещенный арил или замещенную или незамещенную гетероциклическую группу; R12 обозначает водород, галоген, низший алкил, замещенный или незамещенный арил, или замещенную или незамещенную гетероциклическую группу; R13 обозначает водород, галоген или X2R14 (в которой X2 обозначает О или S; R14 обозначает замещенный или незамещенный низший алкил, замещенный или незамещенный арил, замещенную или незамещенную гетероциклическую группу или замещенный или незамещенный аралкил); и Q2 обозначает водород или 3,4-диметоксибензил {например, 5-амино-7-(4-бензоилпиперазинил)-2-(2-фурил)[1,2,4]триазоло[1,5-с]пиримидин}, или его фармацевтически приемлемую соль. (8) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2д аденозина представляет собой соединение формулы (III) NHQ3 R20 fVV-R15 (III) в которой R15 обозначает замещенный или незамещенный арил или замещенный или незамещенный ге-тероарил; R16 обозначает водород, галоген, замещенный или незамещенный низший алкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; m3 и n3 независимо обозначают целое число от 0 до 4; Q3 обозначает водород или 3,4-диметоксибензил; R20 обозначает водород, галоген, гидрокси или замещенный, или незамещенный низший алкил; R17 обозначает гидрокси, гидрокси-замещенный низший алкил, замещенный или незамещенный низший алкокси или имидазо[1,2-а]пири-дил; R18 и R19 независимо обозначают водород, замещенный или незамещенный низший алкил или замещенный или незамещенный арил; или R18 и R19 вместе с соседним атомом углерода образуют замещенный или незамещенный циклоалкил {например, 5-амино-2-(2-фурил)-7-(4-(2-гидрокси-2-метилпропил) пиперазинил)[1,2,4]триазоло[1,5-с]пиримидин}, или его фармацевтически приемлемую соль. (9) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (IV) NH2 r2iANAN^A (IV) в которой Z4 обозначает О или S; R21 обозначает Ph-(СН2)n4Y4 (в которой Ph обозначает фенил, замещенный или незамещенный галогеном или низшим алкилом; Y4 обозначает простую связь, О или S; и n4 обозначает целое число от 0 до 5) { например, 7-амино-2-(2-фурил)-5-фенокси[1,2,4]-триазоло[1,5-а]пи-римидин}, или его фармацевтически приемлемую соль. (10) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (V) NHR22 N^N 24 в которой R22 обозначает водород, замещенный или незамещенный низший алкил или замещенный или незамещенный низший алканоил; R23 обозначает водород, замещенный или незамещенный низший алкил или замещенный или незамещенный низший алкенил, замещенный или незамещенный циклоалкил, замещенный или незамещенный арил, замещенный или незамещенный аралкил или замещенную или незамещенную гетероциклическую группу; R24 обозначает замещенную или незамещенную гетероциклическую группу; X5 обозначает простую связь, О, S, S(O), S(O)2 или NR25 (в которой R25 обозначает водород - 7 - 008339 или замещенный или незамещенный низший алкил); и А обозначает N или CR26 (в которой R26 обозначает водород или замещенный или незамещенный низший алкил), или его фармацевтически приемлемую соль. (11) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (VI) I ¦ 1 I ч I (VI) в которой R27 обозначает замещенный или незамещенный арил, или замещенную или незамещенную гетероциклическую группу; Y6 обозначает О, S или NR29 (в которой R29 обозначает водород, замещенный или незамещенный низший алкил, замещенный или незамещенный циклоалкил или замешенный или незамещенный арил), R28 обозначает водород, замещенный или незамещенный низший алкил, замещенный или незамещенный низший алкенил, замещенный или незамещенный низший алкинил, замещенный или незамещенный циклоалкил, замещенный или незамещенный арил, замещенный или незамещенный аралкил или замещенную или незамещенную гетероциклическую группу; и В вместе с двумя соседними атомами углерода образует замещенный или незамещенный углеродный цикл или гетероцикл, или его фармацевтически приемлемую соль. (12) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (VII) (VII) в которой R30 обозначает замещенный или незамещенный низший алкил или замещенный или незамещенный арил; W обозначает СН2СН2, СН=СН или СС; R31 обозначает водород, гидрокси, замещенный или незамещенный низший алкил, замещенную или незамещенную аминогруппу или замещенную или незамещенную гетероциклическую группу; R32 обозначает водород, замещенный или незамещенный циклоалкил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, или замещенный, или незамещенный низший алкенил; R33 обозначает водород, замещенный или незамещенный низший алкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, или замещенный, или незамещенный низший алкенил, или замещенный, или незамещенный низший алкинил {например, 4-[6-амино-8-(3-фторфенил)-9-метил-9Н-2-фторфенил]-2-метил-3-бутин-2-ол}, или его фармацевтически приемлемую соль. (13) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (VIII) R35 R41 R36 R4J-f 4-7 ?_R37 _R39 R43_ N=( в которой R35 обозначает водород или низший алкил; R36 и R37 независимо обозначают водород, заме- 38 39 40 41 щенный или незамещенный низший алкил, или замещенный, или незамещенный арил; и R , R , R , R , R42 и R43 независимо обозначают водород, замещенный или незамещенный низший алкил, замещенный или незамещенный арил, или замещенную, или незамещенную гетероциклическую группу, или его фармацевтически приемлемую соль. (14) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2д. аденозина представляет собой соединение формулы (IX) - 8 - 008339 ^N/ -N (IX) в которой X9 обозначает СН или N; R44 обозначает низший алкил, замещенный или незамещенный арил или замещенную или незамещенную гетероциклическую группу; R45 обозначает замещенный или незамещенный низший алкил или замещенную или незамещенную гетероциклическую группу; и R46 обозначает гидрокси, галоген или замещенный или незамещенный низший алкил {например, 3-[2-(тиазол-2-илметил)-3-оксо-2,3-дигидропиридазин-6-ил]-2-фенилпиразоло[1,5-а]пиридин}, или его фармацевтически приемлемую соль. (15) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (X) 47 К п49 R52 _У II N R51 (X) в которой X10 обозначает О или независимо обозначает водород, низший алкил, арил, гидро- кси, алкокси, циано- или нитрогруппу, или вместе образуют карбонильную, оксимную, имино- или гид-разоновую группу; R49 обозначает низший алкил или арил; и R50, R51 и R52 независимо обозначают гид-рокси, галоген, замещенный или незамещенный низший алкил, замещенный или незамещенный арил, нитро-, циано- или алкоксигруппу {например, (2R)-2-(1-гидрокси-2-пропиламино)тиено[3,2-d]пирими-дин-4-ил-2-тиенилметанон}; или его фармацевтически приемлемую соль. (16) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (XI) R53 wl1 (XI) в которой R53 обозначает водород, гидрокси, галоген, замещенную или незамещенную аминогруппу, замещенный или незамещенный низший алкил; R54 обозначает водород, галоген, замещенную или незамещенную аминогруппу, замещенный или незамещенный низший алкинил, замещенный или незамещенный низший алкенил, замещенный или незамещенный низший алкил или замещенный или незамещенный низший алкокси; R55 обозначает замещенный или незамещенный низший алкил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил; Аг обозначает замещенный или незамещенный арил, или замещенный или незамещенный гетероарил; и Q11 и W11 независимо обозначают N или СН {например, 5-[6-амино-8-(3-фторфенил)-9Н-9-пуринил]-1-метил-1,2-дигидро-2-пирими-дин}; или его фармацевтически приемлемую соль. (17) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (XII) NH2 f Г у-R N (XII) в которой R56 обозначает замещенный или незамещенный арил, замещенный или незамещенный цикло-алкенил, или замещенный или незамещенный гетероарил; X12 обозначает простую связь или С(О); и R57 обозначает замещенный или незамещенный низший алкил; или его фармацевтически приемлемую соль. (18) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2A аденозина представляет собой соединение формулы (XIII) - 9 - 008339 {XIII} в которой А13 обозначает простую связь, -S-, -N(R63)- (в которой R63 обозначает водород или низший алкил), -(СН2)2-, -СН=СН-, -СС- или -O-; X13 и Y13 независимо обозначают N или СН; R58 обозначает водород, замещенный или незамещенный низший алкил, низший алкенил, низший алкинил, галоген, циано или циклоалкил; R59 обозначает водород, галоген, циано, нитро, замещенный или незамещенный низший алкил, низший алкенил или замещенный или незамещенный арил; R60 обозначает низший алкил, замещенный или незамещенный арил, или замещенный, или незамещенный гетероарил; и R61 и R62 независимо обозначает водород, или замещенный или незамещенный арил, или его фармацевтически приемлемую соль. (19) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (XIV) R65 (XIV) в которой R64 обозначает замещенный или незамещенный низший алкокси, замещенный или незамещенный арил, или замещенный, или незамещенный гетероарил; R65 и R67 независимо обозначают водород, циано или S^^m^ R66 обозначает водород, галоген, замещенный или незамещенный арил, замещенный или незамещенный гетероарил или замещенную или незамещенную аминогруппу; R68 обозначает замещенную или незамещенную аминогруппу {например, 2-(4,5-дигидрофуран-2-ил)-7-м-толил-[1,2,4] триазоло[1,5-а]пиридин-5-иламин}; или его фармацевтически приемлемую соль. (20) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (XV) (XV) в которой А15 обозначает замещенный или незамещенный арил, или замещенный, или незамещенный гетероарил; В15 обозначает замещенный или незамещенный гетероарил; R69 и R70 независимо обозначает водород или замещенную или незамещенную аминогруппу; или его фармацевтически приемлемую соль. (21) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (XVI) H2N^N_R74 R7lAf^R73 R72 (XVI) в которой R71 обозначает циано-, карбоксигруппу или замещенный или незамещенный карбамоил; R72 обозначает водород, гидрокси, замещенный или незамещенный низший алкокси, замещенный или незамещенный арил, или замещенный, или незамещенный гетероарил; R73 и R74 независимо обозначают замещенный или незамещенный арил, или замещенную, или незамещенную гетероциклическую группу, или его фармацевтически приемлемую соль. (22) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (XVII) - 10 - 008339 (XVII) в которой R75 обозначает водород, гидрокси, галоген, низший алкил, низший алкокси, бензилокси или OCF3; R76 и R77 независимо обозначают водород, галоген, низший алкил или низший алкокси; R78 обозначает водород, галоген, низший алкил, низший алкенил, карбокси, низший алканоил, низший алкокси-карбонил, (CH2)ni7-OH (в которой n17 обозначает целое число от 0 до 4), замещенный или незамещенный фенил, 2,3-дигидро-1Н-индолил, азепан-1-ил или 1,4-оксазепан-4-ил; R79 обозначает замещенный или незамещенный фенил; и X17 обозначает О, S или 2Н {например, 4-гидроксиметил-К-(4-метокси-7-фенил-бензотиазол-2-ил)бензамид}; или его фармацевтически приемлемую соль. (23) Способ лечения синдрома усталых ног согласно вышеуказанному абзацу (1), в котором антагонист рецептора А2А аденозина представляет собой соединение (-)-(1^,2^)-а-2-пиперидинил-2,8-бис(трифторметил)-4-хинолинметанол или его фармацевтически приемлемую соль. (24) Применение антагониста рецептора А2А аденозина, описанного в любом из абзацев (1)-(23), для получения терапевтического агента для лечения синдрома усталых ног. (25) Терапевтический агент для лечения синдрома усталых ног, содержащий антагонист рецептора А2А аденозина, описанный в любом из абзацев (1)-(23). (26) Способ лечения ночного миоклонуса, включающий введение эффективного количества антагониста рецептора А2А аденозина, описанного в любом из абзацев (1)-(23) нуждающемуся в этом пациенту. Антагонист рецептора А2А аденозина используется в способе согласно изобретению без ограничений пока он обладает антагонистической активностью к рецептору А2А. Антагонистическая активность к рецептору А2А подразумевает ингибирование, подавление или прерывание действия по меньшей мере одного медиатора биологической активности аденозина, путем, например, связывания с А2А-аденозиновым рецептором, или путем влияния на связывание или препятствуя связыванию аденозина с рецептором. Примеры соединений антагониста рецептора А2А аденозина включают соединения, раскрытые в документах US 5484920, US 5703085, WO 92/06976, WO 94/01114, US 5565460, WO 98/42711, WO 00/17201, WO 99/43678, WO 99/26627, WO 01/92264, WO 99/35147, WO 00/13682, WO 00/13681, WO 00/69464, WO 01/40230, WO 01/2409, WO 01/02400, EP 1054012, WO 01/62233, WO 01/17999, WO 01/80893, WO 02/14282, WO 01/97786 и др. Более конкретно, примеры включают соединения, представленные выше в общих формулах (I), (I-A), (I-B) или (II)-(XVII), (-)-(1^,2^)-а-2-пиперидинил-2,8-бис(трифторметил)-4-хинолинметанол и их фармацевтически приемлемые соли. Предпочтительным антагонистом рецептора А2А аденозина, используемым в способе согласно изобретению, является (Е)-8-(3,4-диметоксистирил)-1,3-диэтил-7-метилксантин (далее называется как соединение А) следующей формулы: С2Н5 В определении каждой группы формул (I), (I-A), (I-B) и (II)-(XVII) низшие алкилы и алкильные части низшего алкокси, гидрокси-замещенного низшего алкила, низшего алканоила и низшего алкоксикар-бонила включают прямые или разветвленные алкильные группы, содержащие 1-8 атомов углерода, такие как метил, этил, пропил, изопропил, бутил, изобутил, втор. бутил, трет. бутил, пентил, неопентил, гексил, гептил или октил. Низший алкенил включает прямые или разветвленные алкенильные группы, содержащие 2-8 атомов углерода, такие как винил, аллил, метакрил, кротил, 3-бутенил, 2-пентенил, 4-пентенил, 2-гексенил, 5-гексенил, 2-гептенил и 2-октенил. Низший алкинил включает прямые или разветвленные алкинильные группы, содержащие 2-8 атомов углерода, такие как этинил, пропаргил, 2-бутинил, 3-бутинил, 2-пентинил, 4-пентинил, 2-гексинил, 5-гексинил, 4-метил-2-пентинил, 2-гептинил и 2-октинил. Циклоалкил включает циклоалкильные группы, содержащие 3-8 атомов углерода, такие как цикло-пропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Циклоалкенил включает циклоалкенильные группы, содержащие 4-8 атомов углерода, такие как циклобутенил, циклопентенил, циклогексенил, циклогептенил и циклооктенил. Арил включает арильные группы, содержащие 6-14 атомов углерода, такие как фенил или нафтил. Аралкил включает группы, содержащие 7-15 атомов углерода, такие как бензил, фенетил, бензгидрил и нафтилметил. Примерами ге - 11 - 008339 тероарила являются фурил, тиенил, пирролил, пиранил, тиопиранил, пиридил, тиазолил, имидазолил, пиримидил, пиридазинил, пиридазиноил, триазинил, индолил, хинолил, пуринил и бензотиазолил. Примерами гетероциклической группы являются пирролидинил, пиперидино, пиперидинил, пиперазинил, морфолино, морфолинил, тиоморфолино, тиоморфолинил, гомопиперидино, гомопиперидинил, гомопи-перазинил, тетрагидропиридинил, тетрагидрохинолинил, тетрагидроизохинолинил, тетрагидрофуранил, тетрагидропиранил, имидазолидинил, тиазолидинил и оксазолидинил в дополнение к группам, перечисленным в качестве примеров гетероарила. Галогенами являются атомы фтора, хлора, брома и йода. Углеродный цикл, образованный комбинацией В с двумя ближайшими атомами углерода, содержит 4-8 атомов углерода и по меньшей мере одну двойную связь, например, циклобутен, циклопентен, циклогексен, циклогептен и циклооктен. Примерами гетероциклического цикла, образованного комбинацией В с двумя ближайшими атомами углерода, являются пиррол, пиран, тиопиран, пиридин, тиазол, имидазол, пиримидин, триазин, индол, хинолин, бензотиазол, пирролин, тетрагидропиридин, тетрагидропиразин, тет-рагидрохинолин и тетрагидроизохинолин. Каждый из замещенного низшего алкила, замещенного низшего алкокси, замещенного низшего ал-каноила и замещенного низшего алкенила содержит, например, 1-3 независимо выбранных заместителя. Примерами заместителей являются группы гидрокси, замещенный или незамещенный низший алкокси, атом галогена, нитро, амино, низший алкиламино, ди(низший алкил)амино, трифторметил, трифторме-токси, бензилокси, фенил и фенокси. Низший алкил и алкильные части низшего алкокси, низшей алки-ламиногруппы и ди(низший алкил)аминогруппы имеют те же значения, что указанные выше для низшего алкила. Галоген имеет то же значение, что и галоген, описанный выше. Примерами заместителя в замещенном низшем алкокси являются гидрокси, низший алкокси, галоген, аминогруппа, азидная группа, карбоксильная и низшая алкоксикарбонильная группа. Алкильные части низшего алкокси в группах низший алкокси и низший алкоксикарбонил имеют те же значения, которые указаны выше для низшего алкила и галоген имеет также те же значения, которые указаны выше для галогена. Каждый из замещенного арила, замещенного нафтила, замещенного фенила, замещенного аралкила, замещенного гетероцикла, замещенного гетероарила, замещенного циклоалкила, замещенного циклоал-кенила, замещенного углеродного цикла, образованного комбинацией В с двумя соседними атомами углерода и замещенного гетероцикла, образованного комбинацией В с двумя соседними атомами углерода содержат, например, 1-4 независимо выбранных заместителя. Примерами заместителей являются группы низший алкил, гидрокси, замещенный или незамещенный низший алкокси, галоген, нитро, амино, низший алкиламино, ди(низший алкил)амино, трифторметил, трифторметокси, бензилокси, фенил и фенок-си. Низший алкил и алкильные части низшего алкокси, низшего алкиламино и ди(низшего алкил)амино имеют те же значения, что указаны выше для низшего алкила. Галоген имеет те же значения, что указаны выше для галогена. Примерами заместителя в замещенном низшем алкокси являются гидрокси, низший алкокси, галоген, группы амино, азидо, карбокси и низший алкоксикарбонил. Алкильная часть низшего алкила в низшем алкокси и низшем алкоксикарбониле имеют те же самые значения, что указаны выше для низшего алкила, и галоген имеет значения, указанные выше для галогена. Каждый из замещенной аминогруппы и замещенного карбамоила имеет 1 или 2 независимо выбранных заместителей. Примерами заместителей являются замещенный или незамещенный низший ал-кил или замещенный или незамещенный низший алкокси. Низший алкил и алкильные части низшего алкокси имеют значения, указанные выше для низшего алкила. Примерами заместителя замещенного низшего алкила и замещенного низшего алкокси являются группы гидрокси, низший алкокси, галоген, амино, азидо, карбокси или низший алкоксикарбонил. Алкильная часть низшего алкила и низшего ал-коксикарбонила имеет значения, указанные выше для низшего алкила, и галоген имеет значения, указанные выше для галогена. В дальнейшем описании соединения, представленные формулами (I), (I-A), (I-B) и (II)-(XVII) будут обозначены как соединения (I), (I-A), (I-B) и (II)-(XVII) соответственно. Фармацевтически приемлемыми солями соединений (I), (I-A), (I-B) и (II)-(XVII) являются фармацевтически приемлемые кислотно-аддитивные соли, соли с металлами, аммониевые соли, аддитивные соли с органическим амином и аддитивные аминокислотные соли. Фармацевтически приемлемые кислотно-аддитивные соли включают аддитивные соли с минеральной кислотой, такие как гидрохлорид, сульфат, нитрат и фосфат, и аддитивные соли с органическими кислотами, такие как ацетат, малеат, фумарат и цитрат; фармацевтически приемлемые соли с металлами включают соли со щелочными металлами, такие как натриевая и калиевая соль, со щелочно-земельными металлами, такие как соль магния и кальция, алюминия и цинка; фармацевтически приемлемые соли аммония включают соли аммония и тетраметиламмония; фармацевтически приемлемые аддитивные соли с органическим амином включают соли с морфолином или пиперидином; и фармацевтически приемлемые аддитивные соли с аминокислотой включают аддитивные соли с лизином, глицином или фенилалани-ном. Соединения (I), (I-A), (I-B) и (II)-(XVII) и их фармацевтически приемлемые соли могут быть получены в соответствии с методами, описанными в документах US 5484920, US 5703085, WO 92/06976, WO 94/01114, US 5565460, WO 98/42711, WO 00/17201, WO 99/43678, WO 99/26627, WO 01/92264, WO - 12 - 008339 99/35147, WO 00/13682, WO 00/13681, WO 00/69464, WO 01/40230, WO 01/02409, WO 01/02400, EP 1054012, WO 01/62233, WO 01/17999, WO 01/80893, WO 02/14282, WO 01/97786 и др. Фармацевтические композиции для введения в соответствии с настоящим изобретением содержат по меньшей мере один антагонист рецептора аденозина в качестве активного ингредиента (ингредиентов), возможно в сочетании с фармацевтически приемлемым носителем (носителями). Такие композиции могут вводиться любым методом, предназначенным для достижения поставленной цели. Количество и схема приема композиции в соответствии с изобретением может быть легко определена обычным специалистом данной области для лечения пациента, который болен RLS. Фармацевтические композиции, описанные здесь, могут быть введены любым подходящим способом, включающим, без ограничения, оральный, интраназальный, внутрилегочный, парентеральный путь, такой как подкожный, внутривенный, внутримышечный, интраперитональный, интрадуоденальный, чре-скожный или через рот. Вводимая доза соответствует эффективному количеству и зависит от возраста пациента, состояния его здоровья и веса, от типа предыдущего или текущего лечения, если они проводились, частоты лечения и от желаемого результата. Обычно учитывают некоторые факторы при определении соответствующей дозы. Такими факторами являются возраст, пол и вес пациента, состояние в момент лечения, тяжесть состояния и форма лекарственного средства, принимаемого пациентом. Под "эффективным количеством" понимается количество, достаточное для достижения положительного эффекта или желаемого клинического результата. Эффективное количество может вводиться в одной или более дозах. С точки зрения лечения эффективным количеством является количество, которое достаточно для временного облегчения, улучшения, стабилизации, возвращения к прежнему состоянию или замедления развития болезни или расстройства, или, другими словами, для снижения патологических последствий болезни или расстройства. Обычно эффективное количество определяется врачом в зависимости от случая и доступно специалисту своей области. В дополнение к активному ингредиенту (ингредиентам) фармацевтические композиции в соответствии с изобретением могут содержать подходящий фармацевтически приемлемый носитель, такой как эксципиент, который облегчает переработку активного ингредиента (ингредиентов) в фармацевтически приемлемый препарат. Предпочтительно, препараты, особенно те, которые могут вводиться орально и которые могут быть использованы для предпочтительной формы введения, такой как таблетки, пастилки и капсулы, а также препараты, которые могут быть введены ректально, такие как свечи, а также подходящие растворы для введения путем инъекций или орально, содержат от приблизительно 0,1 до 99%, предпочтительно, от приблизительно 20 до 85% активного ингредиента (ингредиентов) вместе с эксци-пиентом. Жидкие препараты можно, например, получить путем растворения или диспергирования активного соединения в жидком эксципиенте, таком как вода, соляной раствор, водный раствор декстрозы, глицерин или этанол. Фармацевтическая композиция может также содержать другой лекарственный агент(агенты), фармацевтический агент(агенты), носитель (носители) или вспомогательное вещество (вещества), такое как смачиватель или эмульгатор, или буферный агент(агенты) для поддержания рН. Фармацевтические композиции согласно изобретению вводят способом, подходящим для данной формы композиции. Типичный путь введения включает подкожный путь, внутримышечный, интрапери-тональный, чрескожный, оральный, интраназальный и внутрилегочный (т. е. с помощью аэрозоля). Фармацевтические композиции согласно изобретению, предназначенные для человека, вводятся обычно оральным путем. Фармацевтические композиции для введения оральным или интраназальным путем, или путем местного нанесения, могут выпускаться в твердой, полутвердой или жидкой формах, включающих таблетки, капсулы, порошки, жидкости и суспензии. Фармацевтические композиции для инъекций могут выпускаться в виде жидких растворов, суспензий, эмульсий или в жидких формах, подходящих для растворения или суспензирования в жидкости перед инъекцией. Для введения через дыхательные пути предпочтительной композицией является та, которая образует твердый, порошкообразный или жидкий аэрозоль с использованием соответствующего аэрозольного устройства. Хотя и необязательно, фармацевтическую композицию предпочтительно выпускают в виде единичной дозы для введения в точном количестве. Настоящее изобретение предусматривает также формы с замедленным высвобождением или с отсроченным высвобождением, когда относительно адекватные уровни активного ингредиента (ингредиентов) предусматривают введение в течение более длительного периода. Предпочтительно, антагонист рецептора А2А аденозина может вводиться в количестве предпочтительно от 0,001 до предпочтительно 20,0 мг на 1 кг веса больного. Более предпочтительно, интервал доз составляет от приблизительно 0,01 до приблизительно 10 мг на 1 кг веса больного. Так как антагонист рецептора А2А аденозина согласно изобретению возможно будет выводиться из кровотока, то повторный прием фармацевтической композиции показан и является предпочтительным. Антагонист рецептора аденозина может вводиться способом, совместимым с дозировкой композиции и в таком количестве, которое является терапевтически эффективным. Общая доза зависит от возраста, веса и состояния больного и от пути введения. Фармацевтические композиции, используемые для способов согласно изобретению, получают из - 13 - 008339 вестным методом. Получение фармацевтической композиции осуществляют в соответствии с общепринятыми процедурами для получения фармацевтических композиций [например, Remington's Pharmaceutical Sciences 18th Edition (1990), E.W.Martin ed., Mack Publishing Co., Pa]. В зависимости от цели применения и способа введения может оказаться желательным обработать далее активный ингредиент при получении фармацевтических композиций. Соответствующий метод может включать стерилизацию, смешивание с соответствующими нетоксичными и безопасными смешивающимися компонентами, разделение на единичные дозы и упаковку. Фармацевтические препараты для орального введения могут быть получены смешиванием активного ингредиента (ингредиентов) с твердым эксципиентом (эксципиентами), возможно, измельчением полученной смеси и, при желании или необходимости, обработкой смеси гранул после добавления необходимого вспомогательного вещества (веществ) для получения таблеток. Подходящими эсципиентами могут быть наполнители, такие как сахариды, например, лактоза, сахароза, маннит или сорбит; производные целлюлозы; соединения цинка; и/или фосфаты кальция, такие как трифосфат кальция или гидрофосфат кальция; связующие вещества, такие как крахмальная паста, в которой используется, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал или картофельный крахмал; желатин; трагакант; и/или поливинилпирролидон. Вспомогательными веществами могут быть регуляторы текучести и смазывающие вещества, такие как диоксид кремния, тальк, стеариновая кислота или ее соли и/или полиэтиленгликоль. Таблетки, твердые капли или капсулы могут быть покрыты подходящим покрывающим веществом, которое, при желании, придаст стойкость к желудочному соку. С этой целью можно использовать концентрированный раствор сахарида, который может содержать гуммиарабик, тальк, поливинилпирролидон, полиэтиленгли-коль и/или диоксид титана, растворы лаков и соответствующие органические растворители или смеси растворителей. Для нанесения стойкого к желудочному соку покрытия, т. е. получения энтеросолюбиль-ной оболочки, используются растворы соответствующих соединений целлюлозы, таких как фталат аце-тилцеллюлозы или фталат гидроксипропилметилцеллюлозы. В таблетки или покрывающие вещества могут добавляться красящие вещества или пигменты, например, для идентификации или для характеристики комбинации доз активного соединения. Другие фармацевтические препараты, которые могут использоваться для орального введения, включают желатиновые капсулы, пригодные для прохождения, а также мягкие герметичные капсулы, выполненные из желатины и пластификатора, такого как глицерин или сорбит. Капсулы, пригодные для прохождения, могут содержать активный ингредиент(ы) в форме гранул, которые могут быть смешаны с наполнителем(ями), такими как лактоза, связующие вещества, такие как крахмал, и/или смазывающее вещество(а), такое как тальк или стеарат магния и, возможно, стабилизатор(ы). В мягких капсулах активный ингредиент(ы) предпочтительно растворен или суспендирован в соответствующих жидкостях, таких как жирные масла или жидкий парафин. Дополнительно можно вводить стабилизатор(ы). Антагонисты рецептора аденозина могут также вводиться согласно изобретению в форме им-плантата, который смешивают с биодеградируемым носителем, представляющим собой регулятор текучести. В качестве альтернативного варианта, активные ингредиенты могут изготавливаться в виде транс-дермального пластыря для непрерывного высвобождения активного ингредиента (ингредиентов). Способы изготовления имплантатов и пластырей хорошо известны в данной области техники [Remington's Pharmaceutical Sciences 18th Edition (1990), E.W.Martin ed., Mack Publishing Co., Pa; и Kydonieus ed. (1992) Treatise on controlled drug delivery Marcel Dekker, NY]. Ниже представлены не ограничивающие примеры, иллюстрирующие настоящее изобретение. Все документы, цитированные в описании, включены в него в виде ссылки. Пример 1. Модель животного: лечение RLS с помощью антагониста рецептора аденозина. Соединение А, являющееся новым потенциальным антагонистом рецептора аденозина, показало себя эффективным при лечении симптомов болезни Паркинсона на модели животного и при лечении ранней стадии II, проведенном на пациентах с болезнью Паркинсона. Способность соединения А взаимодействовать с допаминергической и GABA-эргической системами среднего мозга является основой для лечения RLS. Было отмечено, что двустороннее поражение с помощью 6-OHDA ядра A11, вызывающее поведенческую реакцию, коррелирует с клиническим состоянием RLS, т.е. увеличивается среднее число эпизодов стояния и увеличивается общее время стояния [Ondo et al., Mov. Dis., 15, 154-158 (2000)]. Особенно отмечается, что лечение пораженных животных с помощью допаминового агониста, такого как прами-пексол, приводит в результате к снижению эпизодов стояния и уменьшению общего времени стояния. Эти данные согласовывались с теми, которые ожидались при лечении RLF на модели животного. Для оценки эффективности антагониста рецептора аденозина на модельной системе животного был использован метод Ondo et al. (2000). Крысы были анестезированы стереотаксическим методом путем введения инъекции 6-OHDA в объеме приблизительно 8 мкг, растворенных в рассоле, забуференном фосфатом (PBS), содержащим 0,01-0,05 вес./об.% аскорбиновой кислоты в правое и левое ядро A11. Контрольной группе крыс также была сделана инъекция носителя, но без 6-OHDA. Спустя 2-12 недель после инъекции 6-OHDA или носителя, за животным наблюдали в течение 30 - 14 - 008339 120 мин и его поведение оценивалось по числу раз стояния на двух ногах и по общему времени стояния на двух ногах. Измерялась также общая продолжительность сна. Последующее проведение электроэнцефалографии или электромиографии позволило дать объяснения поведению, которое было характерно для пораженного и не пораженного болезнью животного. Анализировались эффекты, вызванные фармакологическими действиями над пораженным животным. Введение антагониста рецептора аденозина противодействовало изменениям в поведении, наблюдаемым у пораженных животных. Лечение пораженных животных с помощью носителя или прами-пексола служило соответственно отрицательным или положительным контролем. После завершения поведенческих и лекарственных тестов и завершения контрольного лечения, крыс умерщвляли и извлекали целиком их мозг. Венечные срезы диэнцефальных участков мозга, содержащих группы ядер A11, помещали в криостат и затем полученные срезы обрабатывали тирозингидрок-силазой (ТН) по методу иммуногистологической химии. Окрашенные срезы наблюдали под оптическим микроскопом для того, чтобы удостовериться в истинном поражении ядер A11. Результаты контроля сравнивались с антагонистом A2A в свете обнаруженного поражения. Пример 2. Клинические испытания на людях: лечение RLS антагонистом А^. В этом исследовании оценивалась эффективность соединения А при лечении RLS. Всех пациентов в количестве 45 человек, у которых был диагностирован RLS и PLMS средней и высокой степени тяжести, разделили на 3 группы. Пациенты, которые не поддались какому-то одному или комбинированному методу лечения, не отбирались для этого исследования. Базовая линия симптомов RLS и PLMS устанавливалась самим пациентом, принявшим лекарство, по визуальной аналоговой шкале, клинической шкале оценки впечатления и полисомнографом. Пациенты первой группы получали 5 мг соединения А, второй группы - 20 мг и третьей группы - 80 мг один раз в день в течение 8 недель. Еженедельная оценка проводилась в течение всего периода лечения. Величина оценки на неделе 8 сравнивались с величинами значений базовой линии методом статистического анализа. Пример 3. Клинические испытания на людях: лечение RLS антагонистом. С целью оценки эффективности исследуемого антагониста при лечении RLS клиническое испытание начиналось и проводилось в соответствии со стандартными процедурами. Вкратце, для определения эффективности соединения А при лечении RLS измерялось у пациентов общее число баллов по Международной рейтинговой шкале RLS [International RLS Rating Scale (IRLSRS)] и общий показатель PLMS (полисомнография; показатель PLMS представляет собой число периодических движений конечности в час во время сна) [Understanding and Diagnosing Restless Legs Syndrome (2003), Restless Legs Syndrome Foundation, 819 Second Street, SW Rochester, MN 55902]. Балльная оценка по шкале IRLSRS проводилась в соответствии с Инструкциями для эксперта (максимальный общий балл по IRLSRS составляет 40). Эксперту предписывалось получить от пациента оценки его/ее симптомов, вытекающие из следующих ниже десяти вопросов. Именно пациент, а не эксперт, должен сделать себе оценку, однако только эксперт должен уточнить любую неясность, возникшую у пациента в связи с вопросами. Один из двух, либо пациент либо эксперт, заносит ответы в соответствии с установленной формой. Для вопросов 1, 2, 4, 5, 6, 9 и 10 используется следующая шкала оценок: (4) очень тяжелое, (3) тяжелое, (2) умеренное, (1) легкое и (0) отсутствие. 1. В целом, как бы вы оценили дискомфорт в руках или ногах, связанный с RLS? 2. В целом, как вы оцениваете потребность в движении? 3. В целом, намного ли снижается у вас ощущение дискомфорта в ноге или руке, пораженной RLS, когда вы начинаете ходить? (4) нет облегчения, (3) небольшое облегчение, (2) умеренное облегчение, (1) полное или почти полное облегчение, (2) отсутствие симптомов RLS, поэтому вопрос снимается. 4. В целом, насколько серьезны у вас нарушения сна при симптомах RLS? 5. Насколько велики у вас усталость и сонливость при симптомах RLS? 6. Насколько тяжелым в целом является для вас заболевание RLS? 7. Насколько часто возникают у вас симптомы RLS? (4) очень тяжелое (обозначающее 6-7 дней в неделю), (3) тяжелое (обозначающее 4-5 дней в неделю), (2) умеренное (обозначающее 2-3 дня в неделю), (1) легкое (1 день в неделю или меньше), (0) не возникают. 8. Если вы ощущаете симптомы RLS, насколько они тяжелы, в среднем? (4) очень тяжелое (обозначающее 8 ч в сутки и более), (3) тяжелое (обозначающее 3-8 ч в сутки), (2) умеренное (обозначающее 1-3 ч в сутки), - 15 - 008339 (1) легкое (означающее менее 1 ч в сутки), (0) отсутствие симптомов. 9. В целом, в какой степени отражаются симптомы RLS на способности к выполнению ваших ежедневных обязанностей, например, удовлетворительно ли выполняются дела в семье, дома, общественные дела, в школе или на работе? 10. Насколько резко происходит смена вашего настроения при симптомах RLS, например, сердитесь ли вы, подавлены, опечалены, озабочены или раздражены? Пациентам с установленным диагнозом идиопатического RLS не давали лекарства с момента скрининга до конца лечения. После того, как прием всех лекарств RLS подошел к концу, пациенты проходили скрининг на переносимость. На неделе 2 пациентов помещали в больницу на ночь, предшествующую дню посещения, для того, чтобы они адаптировались к условиям сна в обстановке лаборатории. После скрининга измеряли общий балл по IRLESS и общий показатель PLMS в день-1 для установления базовой линии и определения диапазона отклонения RLS. К исследованию были допущены только пациенты со степенью тяжести RLS от умеренной до тяжелой (общий балл по IRLSRS 15 и выше). Пациенты, у которых было отмечено 35% отклонение и выше в баллах по шкале IRLSRS и/или согласно полисомно-графии от значений в неделю 1 посещения и в день-1 посещения (базовая линия), не участвовали в дальнейшем исследовании. Лечение с помощью соединения А (80 мг, один раз в день) начиналось на следующий день после посещения в день-1 и продолжалось в течение следующих 6 недель. Последняя доза соединения А принималась в день посещения на неделе 6. В неделю 8 пациентам давались оценки RLS (общий балл по шкале IRLSRS и общий показатель PLMS). Показатель ингибирования по каждому баллу рассчитывался по следующему соотношению: Показатель ингибирования (%) = {[(Балл в День-1)-(Балл в Неделю 8)]/(Балл в День-1)} х 100. Результаты сведены в табл. 1. Таблица 1 Базовая линия Неделя 8 Показатель (День-1) среднее (SD) ингтибиров ания среднее (SD) (%) IRLSRS Общий балл 1 32, 5 (4, 39) 23 (8, 04) 29,2 PLMS общий показатель 45 (15,41) 24, 67 (23, 89) 45, 2 N=4 Как показывает табл. 1, общий балл IRLSRS и общий показатель PLMS уменьшились в неделю 8 по сравнению с соответствующей базовой линией. Так, 80 мг соединения А, принимаемые 1 раз в день в течение 6 недель, вызывали облегчение симптомов RLS и улучшали состояние пациентов, страдающих RLS в умеренной и тяжелой степени. Эти результаты подтверждают, впервые, что антагонист рецептора А2А аденозина является эффективным для лечения RLS. Некоторые способы осуществления изобретения описаны в следующих примерах. Пример 1. Таблетки. Таблетки, имеющие следующий ниже состав, получают традиционным способом. Соединение А (40 г) смешивают с 286,8 г лактозы и 60 г картофельного крахмала с последующим добавлением 120 г 10% водного раствора гидроксипропилцеллюлозы. Полученную смесь перемешивают, гранулируют и сушат традиционным способом. Гранулы подвергают очистке для получения гранул, используемых для изготовления таблеток. После смешивания гранул с 1,2 г стеарата магния смесь формуют в виде таблеток, каждая из которых содержит 20 мг активного ингредиента, с использованием табле-тирующих машин (Модель RT-15, Kikusui), снабженных пестиками диаметром 8 мм. Состав таблетки представлен в табл. 2. Таблица 2 Соединение А 2 0 мг Лактоза 143, 4 мг Картофельный крахмал 30 мг Гидроксипропилцеллюлоза 6 мг Стеарат магния 0, 6 мг 200 мг - 16 - 008339 Пример 2. Капсулы. Капсулы, имеющие следующий ниже состав, получают традиционным способом. Соединение А (200 г) смешивают с 995 г Avicel и 5 г стеарата магния. Смесь помещают в твердые капсулы No 4, каждая из которых имеет объем 12 0 мг, с использованием устройства для наполнения капсул (Модель LZ-64, Zanashi), и получают капсулы, каждая из которых содержит 20 мг активного ингредиента. Состав капсулы представлен в табл. 3. Таблица 3 Соединение А 2 0 мг Avicel 99, 5 мг Стеарат магния 0,5 мг 12 0 мг Пример 3. Инъекционные растворы. Инъекционные растворы, имеющие следующий ниже состав, получают традиционным способом. Соединение А (1 г) растворяют в 100 г очищенного соевого масла с последующим добавлением 12 г очищенного лецитина яичного желтка и 25 г глицерина для инъекций. Полученную смесь доводят до объема 1000 мл с помощью дистиллированной воды для инъекций, тщательно смешивают и эмульгируют традиционным способом. Образующуюся дисперсию подвергают асептической фильтрации с использованием одноразовых мембранных фильтров толщиной 0,2 мкм и затем разливают в асептических условиях в стеклянные емкости объемом 2 мл и получают инъекционные растворы, содержащие 2 мг активного ингредиента в каждой емкости. Состав инъекционного раствора представлен в табл. 4. Таблица 4 Соединение А 2 мг Соевое масло очищенное 200 мг Очищенный лецитин яичного желтка 2 4 мг Глицерин для инъекции 50 мг Дистиллированная вода для инъекции 1,72 мл 2,00 мл ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения синдрома усталых ног, включающий введение нуждающемуся в этом пациенту эффективного количества по меньшей мере одного антагониста рецептора А2Л. аденозина, представленного следующей формулой (I) в которой R1, R2 и R3 независимо обозначают водород, (^-^алки, (^-^алкен^т или (^-^алки-нил; R4 обозначает (C3-C8)циклоалкил, группу -(CH2)n-R5 (в которой R5 обозначает замещенный или незамещенный (C^Cn^im, или замещенную или незамещенную гетероциклическую группу, а n обозначает целое число от 0 до 4) или группу " Z {в которой Y1 и Y2 независимо обозначают водород, галоген или (^-^алкал; и Z обозначает замещенный или незамещенный (С6-С14)арил, или группу - 17 - 008339 (в которой R6 обозначает водород, гидрокси, (СгС8)алкил, (CrC8)алкокси, галоген, нитро- или аминогруппу; и m обозначает целое число от 1 до 3)}; и X1 и X2, независимо, обозначают О или S. 2. Способ лечения синдрома усталых ног по п.1, в котором антагонист рецептора А2А аденозина представляет собой соединение формулы (I-A) (I-A) в которой Rla и R2a независимо обозначают метил или этил; R3a обозначает водород или (С1-С8)алкил; и Za обозначает группу R7 RB R10 (в которой по меньшей мере один из R7, R8 и R9 обозначают (С1-С8)алкил или (С1-С8)алкокси, а другие обозначают атом водорода; R10 обозначает водород или (СгС8)алкил) или группу ?е п. (СН2)т (в которой R6 и m соответственно имеют значения, указанные выше). 3. Способ лечения синдрома усталых ног по п.1, в котором антагонист рецептора А2А аденозина представляет собой соединение (Е)-8-(3,4-диметоксистирил)-1,3-диэтил-7-метилксантин. 4. Применение антагониста рецептора аденозина, охарактеризованного в любом из пп.1-3, для получения терапевтического средства для лечения синдрома усталых ног. 5. Терапевтическое средство для лечения синдрома усталых ног, содержащее антагонист рецептора аденозина, охарактеризованный в любом из пп.1-3. 6. Способ лечения ночного миоклонуса, включающий введение эффективного количества антагониста рецептора аденозина, охарактеризованного в любом из пп.1-3, нуждающемуся в этом пациенту. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6 - 18 - 
|