|
Патентная документация ЕАПВ |
|
||
| Запрос: | ea000008303b*\id |
|
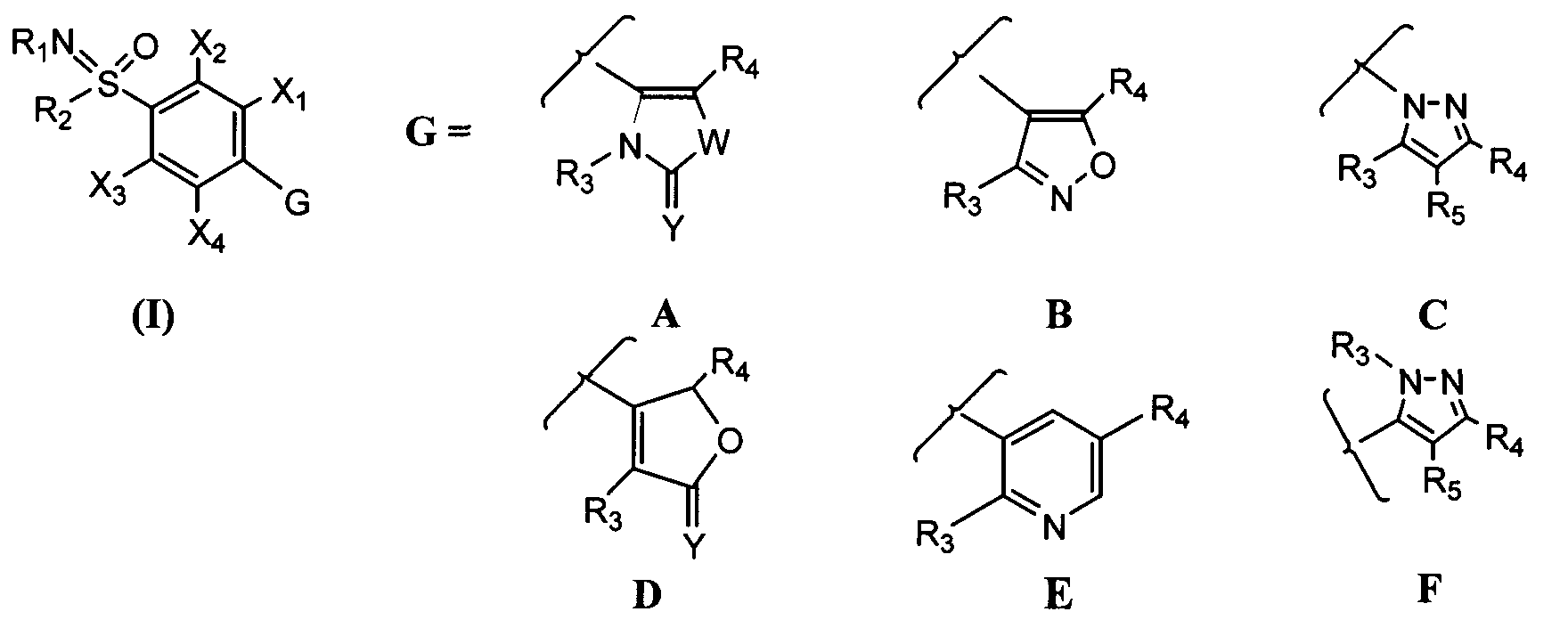
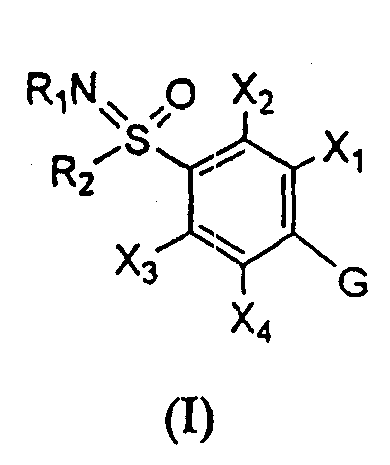
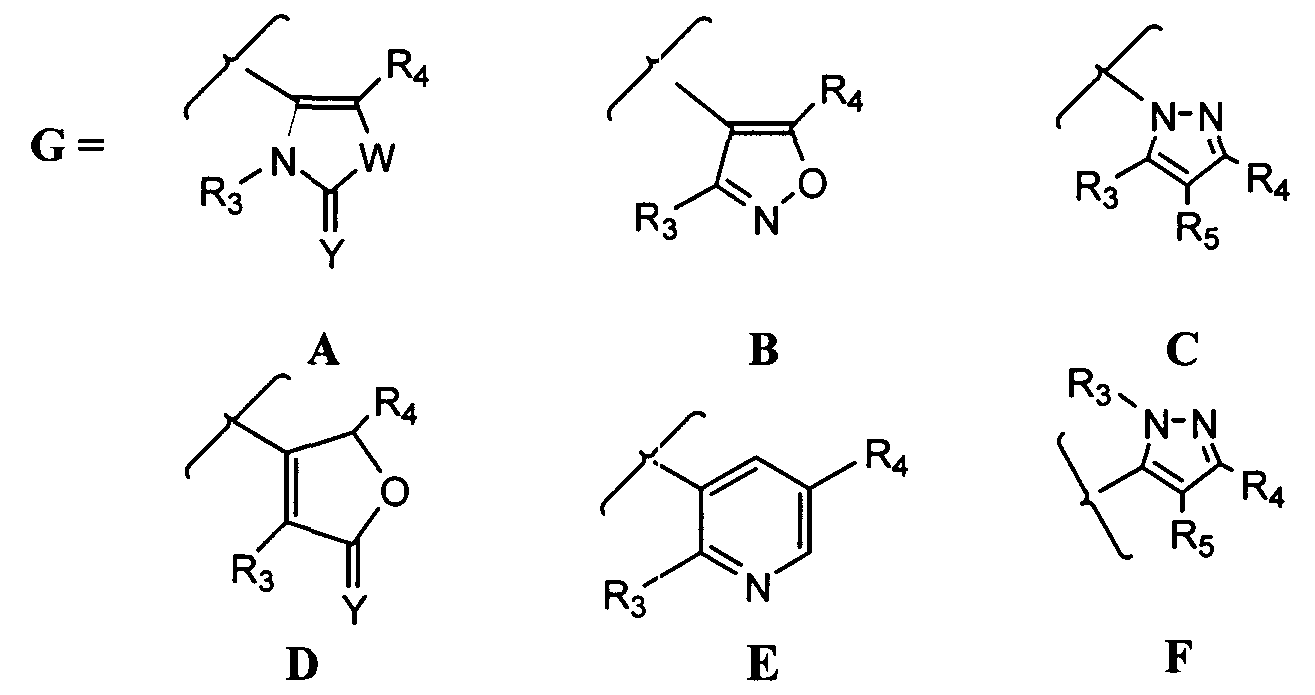
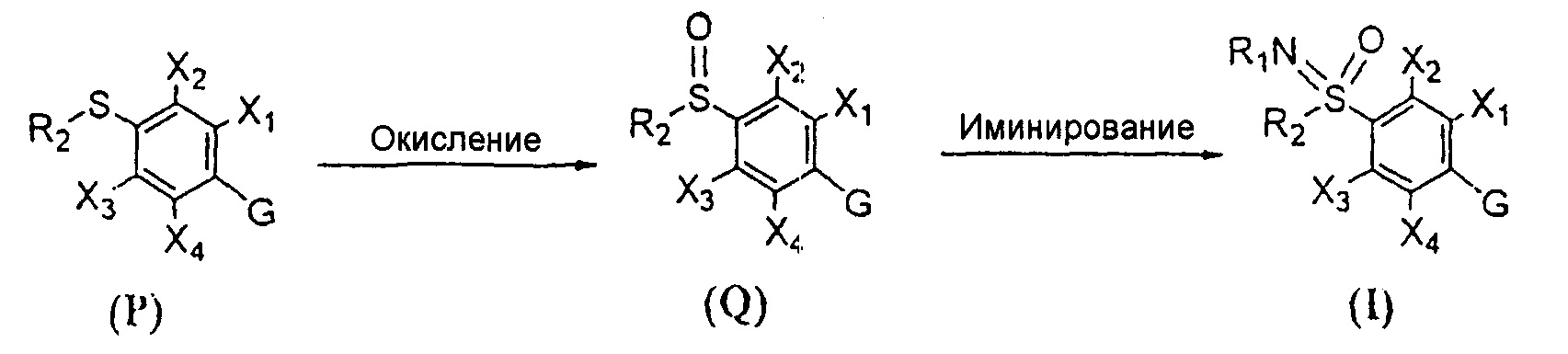
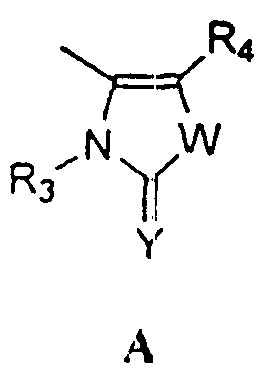
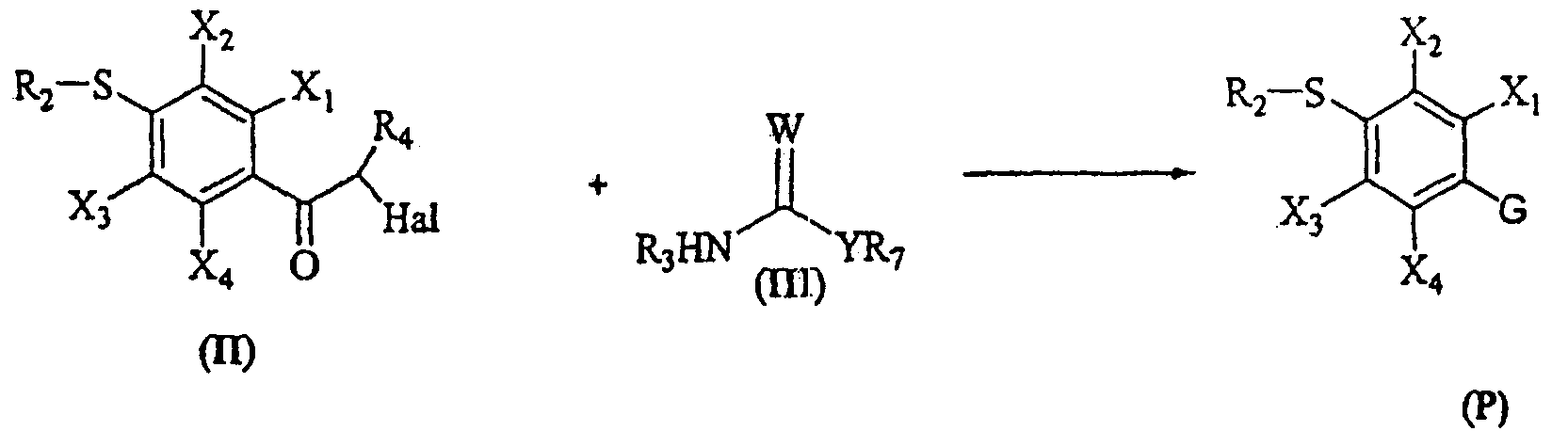
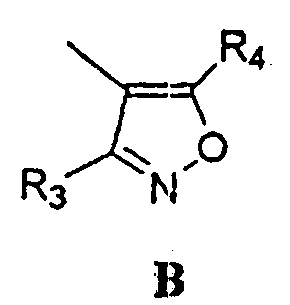
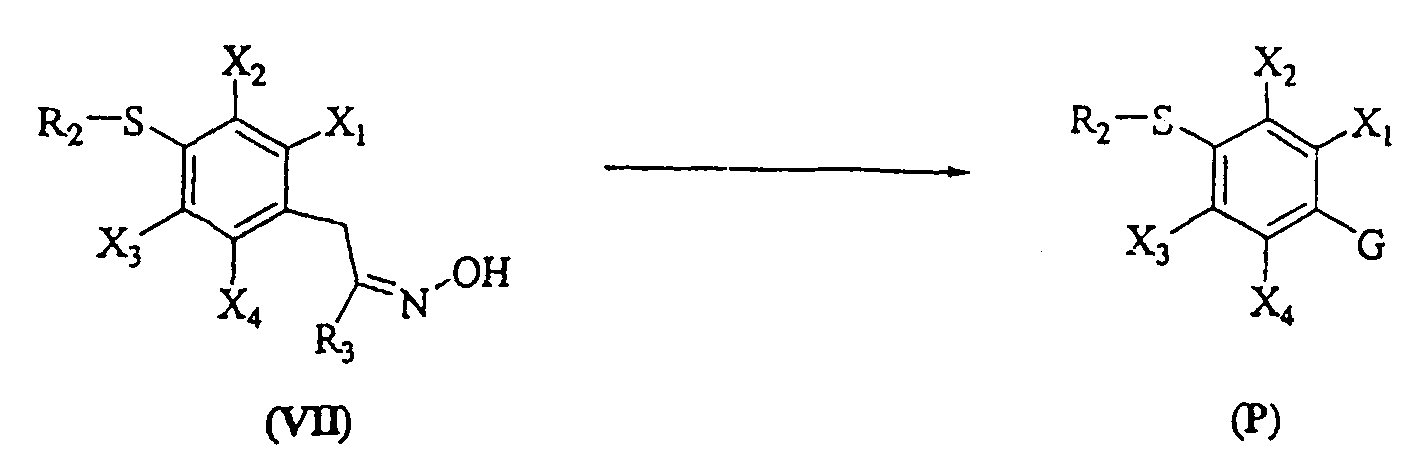
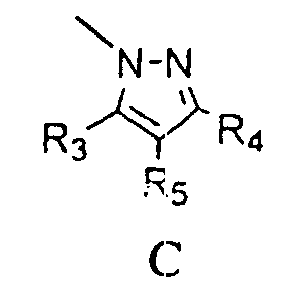
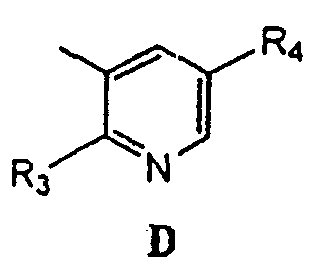
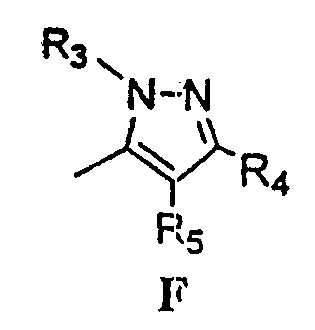
Термины запроса в документе Реферат 1. Соединение формулы (I), где G представляет собой группы А, В, С, D, Е или F, описанные ниже: где R 1 представляет собой водород, ацильную, галогенацильную группу; R 2 представляет собой (C 1 -С 3 )алкил; X 1 , X 2 , Х 3 , Х 4 могут быть одинаковыми или различными и представляют собой водород или галоген; и если G представляет собой гетероцикл "D", то по меньшей мере одна из групп, определенных как X 1 , X 2 , Х 3 , Х 4 , не является водородом; R 3 выбран из замещенных или незамещенных арильных или гетероарильных групп, где заместители арильных групп выбраны из галогена, нитро, гидроксила, (C 1 -C 3 )алкила, (C 1 -C 3 )алкокси, гидрокси (C 1 -C 3 )алкокси, а заместители гетероарильных групп выбраны из (C 1 -C 3 )алкильных групп; R 4 выбран из атома водорода, атома галогена, карбокси, прямой или разветвленной (C 1 -С 3 )алкильной, гидрокси(C 1 -C 3 )алкильной, алкокси (C 1 -C 3 )алкильной, галоген(C 1 -C 3 )алкильной и фенильной групп, и R 5 представляет собой водород; Y представляет собой О; W представляет собой О или S; его таутомеры, фармацевтически приемлемые соли и сольваты. 2. Соединение по п.1, где указанными фармацевтически приемлемыми солями являются соли винной кислоты, миндальной кислоты, фумаровой кислоты, яблочной кислоты, молочной кислоты, малеиновой кислоты, салициловой кислоты, лимонной кислоты, аскорбиновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты, гидроксинафтойной кислоты, метансульфоновой кислоты, уксусной кислоты, бензойной кислоты, янтарной кислоты, пальмитиновой кислоты, хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты и азотной кислоты. 3. Фармацевтическая композиция, содержащая соединения по п.1 или их фармацевтически приемлемые соли или сольваты и фармацевтически приемлемый носитель, разбавитель, наполнитель. 4. Фармацевтическая композиция по п.3 в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 5. Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение по п.2 или его сольват и фармацевтически приемлемый носитель, разбавитель, наполнитель. 6. Фармацевтическая композиция по п.5, содержащая соединение по п.2 и изготовленная в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 7. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли. 8. Способ по п.7, где указанное соединение вводят перорально, интраназально, парентерально, местно, чрескожно или ректально. 9. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.2. 10. Способ по п.9, где указанное соединение вводят перорально, интраназально, парентерально, местно, чрескожно или ректально. 11. Соединение по п.1, выбранное из 5-(4-фторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-хлорфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-н-пропоксифенил)-3-трифторметил-1Н-пиразола; 5-(4-этоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-гидроксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-хлор-4-фторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3,4-дифторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-фтор-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метокси-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-хлор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-бром-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-метокси-4-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(2-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразола; 1-(3-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-фенил-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(1-нафтил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-3-метил-1-(4-метилсульфоксиминилфенил)-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-нитрофенил)-3-трифторметил-1Н-пиразола; 5-(3-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3,5-дифтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-гидрокси-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразол-3-карбоновой кислоты; 3-(гидроксиметил)-5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразола; 5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразол-3-илметилгидросульфата; 5-{4-(2-гидроксиэтокси)фенил}-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-пиридил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(3-пиридил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(2-пиридил)-3-трифторметил-1Н-пиразола; 5-(4-изопропоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(2-тиофенил)-3-трифторметил-1Н-пиразола; 5-(4-метилсульфоксиминилфенил)-1-фенил-3-трифторметил-1Н-пиразола; 1-(4-метоксифенил)-5-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-этил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 5-метоксиметил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 3-(4-фторфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-(4-хлорфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-этил-4-(4-метилсульфоксиминилфенил)-5-фенилизоксазола; 5-хлор-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 5-метил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 3-(4-метоксифенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-(3,4-дихлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-хлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-фенил-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(3,4-дифторфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(3,4-диметоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-метоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-метилфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 5-хлор-3-(4-метилсульфоксиминилфенил)-6'-метил[2,3']бипиридинила; 5-хлор-3-(4-метилсульфоксиминилфенил)-[2,3']бипиридинила; 3-(3-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-она; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-она; 3-(2-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 3-(4-бромфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 4-(4-метилсульфоксиминилфенил)-3-фенил-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(N-хлорацетил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(N-ацетил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(N-метилсульфонил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-{N-(4-метилфенил)сульфонил}метилсульфоксиминилфенил]-3Н-оксазол-2-она. 12. Соединение по п.11, где указанными фармацевтически приемлемыми солями являются соли винной кислоты, миндальной кислоты, фумаровой кислоты, яблочной кислоты, молочной кислоты, малеиновой кислоты, салициловой кислоты, лимонной кислоты, аскорбиновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты, гидроксинафтойной кислоты, метансульфоновой кислоты, уксусной кислоты, бензойной кислоты, янтарной кислоты, пальмитиновой кислоты, хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты и азотной кислоты. 13. Фармацевтическая композиция, содержащая соединение по п.11 или 12 или его сольват и фармацевтически приемлемый носитель, разбавитель, наполнитель. 14. Фармацевтическая композиция по п.13 в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 15. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.11-12 или его фармацевтически приемлемой соли. 16. Применение соединения по пп.1-2 и 11-12 для лечения воспалений и ассоциированных с воспалением заболеваний. 17. Способ получения соединений формулы (I) G представляет собой группы А, В, С, D, Е или F, описанные ниже: где R 1 представляет собой водород, ацильную, галогенацильную группу; R 2 представляет собой (C 1 -C 3 )алкил; X 1 , X 2 , Х 3 , Х 4 могут быть одинаковыми или различными и представляют собой водород или галоген; и если G представляет собой гетероцикл D, то по меньшей мере одна из групп, определенных как X 1 , X 2 , Х 3 , Х 4 , не является водородом; R 3 выбран из замещенных или незамещенных арильных или гетероарильных групп, где заместители арильных групп выбраны из галогена, нитро, гидроксила, (C 1 -C 3 )алкила, (C 1 -C 3 )алкокси, гидрокси(C 1 -C 3 )алкокси, а заместители гетероарильных групп выбраны из (C 1 -C 3 )алкильных групп; R 4 выбран из атома водорода, атома галогена, карбокси, прямой или разветвленной (C 1 -С 3 )алкильной, гидрокси(C 1 -C 3 )алкильной, алкокси(C 1 -C 3 )алкильной, галоген(C 1 -C 3 )алкильной и фенильной групп, и R 5 представляет собой водород; Y представляет собой О; W представляет собой О или S; и где указанный способ предусматривает окисление соединения формулы (Р) с получением соединения формулы (Q), которое подвергают иминированию подходящими реагентами и получают соединение формулы (I), которое может быть затем, если это необходимо, превращено в его фармацевтически приемлемые соли. 18. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия галогенкетона формулы (II) с соединением формулы (III) с получением меркапто-соединения формулы (Р) 19. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий превращение оксима формулы (VII) в меркапто-соединение формулы (Р) 20. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия гидразина формулы (XI) с 1,3-дикетоном формулы (XII) с получением меркапто-соединения формулы (Р) 21. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия соединения формулы (XVII) с соединением формулы (XVIII) с получением меркапто-соединения формулы (Р) 22. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия соединения формулы (XXI) с соединением формулы (XXII) с получением меркапто-соединения формулы (Р)
Полный текст патента (57) Реферат / Формула: где R 1 представляет собой водород, ацильную, галогенацильную группу; R 2 представляет собой (C 1 -С 3 )алкил; X 1 , X 2 , Х 3 , Х 4 могут быть одинаковыми или различными и представляют собой водород или галоген; и если G представляет собой гетероцикл "D", то по меньшей мере одна из групп, определенных как X 1 , X 2 , Х 3 , Х 4 , не является водородом; R 3 выбран из замещенных или незамещенных арильных или гетероарильных групп, где заместители арильных групп выбраны из галогена, нитро, гидроксила, (C 1 -C 3 )алкила, (C 1 -C 3 )алкокси, гидрокси (C 1 -C 3 )алкокси, а заместители гетероарильных групп выбраны из (C 1 -C 3 )алкильных групп; R 4 выбран из атома водорода, атома галогена, карбокси, прямой или разветвленной (C 1 -С 3 )алкильной, гидрокси(C 1 -C 3 )алкильной, алкокси (C 1 -C 3 )алкильной, галоген(C 1 -C 3 )алкильной и фенильной групп, и R 5 представляет собой водород; Y представляет собой О; W представляет собой О или S; его таутомеры, фармацевтически приемлемые соли и сольваты. 2. Соединение по п.1, где указанными фармацевтически приемлемыми солями являются соли винной кислоты, миндальной кислоты, фумаровой кислоты, яблочной кислоты, молочной кислоты, малеиновой кислоты, салициловой кислоты, лимонной кислоты, аскорбиновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты, гидроксинафтойной кислоты, метансульфоновой кислоты, уксусной кислоты, бензойной кислоты, янтарной кислоты, пальмитиновой кислоты, хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты и азотной кислоты. 3. Фармацевтическая композиция, содержащая соединения по п.1 или их фармацевтически приемлемые соли или сольваты и фармацевтически приемлемый носитель, разбавитель, наполнитель. 4. Фармацевтическая композиция по п.3 в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 5. Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение по п.2 или его сольват и фармацевтически приемлемый носитель, разбавитель, наполнитель. 6. Фармацевтическая композиция по п.5, содержащая соединение по п.2 и изготовленная в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 7. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли. 8. Способ по п.7, где указанное соединение вводят перорально, интраназально, парентерально, местно, чрескожно или ректально. 9. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.2. 10. Способ по п.9, где указанное соединение вводят перорально, интраназально, парентерально, местно, чрескожно или ректально. 11. Соединение по п.1, выбранное из 5-(4-фторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-хлорфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-н-пропоксифенил)-3-трифторметил-1Н-пиразола; 5-(4-этоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-гидроксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-хлор-4-фторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3,4-дифторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-фтор-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метокси-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-хлор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-бром-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-метокси-4-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(2-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразола; 1-(3-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-фенил-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(1-нафтил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-3-метил-1-(4-метилсульфоксиминилфенил)-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-нитрофенил)-3-трифторметил-1Н-пиразола; 5-(3-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3,5-дифтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-гидрокси-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразол-3-карбоновой кислоты; 3-(гидроксиметил)-5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразола; 5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразол-3-илметилгидросульфата; 5-{4-(2-гидроксиэтокси)фенил}-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-пиридил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(3-пиридил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(2-пиридил)-3-трифторметил-1Н-пиразола; 5-(4-изопропоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(2-тиофенил)-3-трифторметил-1Н-пиразола; 5-(4-метилсульфоксиминилфенил)-1-фенил-3-трифторметил-1Н-пиразола; 1-(4-метоксифенил)-5-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-этил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 5-метоксиметил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 3-(4-фторфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-(4-хлорфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-этил-4-(4-метилсульфоксиминилфенил)-5-фенилизоксазола; 5-хлор-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 5-метил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 3-(4-метоксифенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-(3,4-дихлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-хлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-фенил-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(3,4-дифторфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(3,4-диметоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-метоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-метилфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 5-хлор-3-(4-метилсульфоксиминилфенил)-6'-метил[2,3']бипиридинила; 5-хлор-3-(4-метилсульфоксиминилфенил)-[2,3']бипиридинила; 3-(3-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-она; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-она; 3-(2-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 3-(4-бромфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 4-(4-метилсульфоксиминилфенил)-3-фенил-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(N-хлорацетил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(N-ацетил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(N-метилсульфонил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-{N-(4-метилфенил)сульфонил}метилсульфоксиминилфенил]-3Н-оксазол-2-она. 12. Соединение по п.11, где указанными фармацевтически приемлемыми солями являются соли винной кислоты, миндальной кислоты, фумаровой кислоты, яблочной кислоты, молочной кислоты, малеиновой кислоты, салициловой кислоты, лимонной кислоты, аскорбиновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты, гидроксинафтойной кислоты, метансульфоновой кислоты, уксусной кислоты, бензойной кислоты, янтарной кислоты, пальмитиновой кислоты, хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты и азотной кислоты. 13. Фармацевтическая композиция, содержащая соединение по п.11 или 12 или его сольват и фармацевтически приемлемый носитель, разбавитель, наполнитель. 14. Фармацевтическая композиция по п.13 в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 15. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.11-12 или его фармацевтически приемлемой соли. 16. Применение соединения по пп.1-2 и 11-12 для лечения воспалений и ассоциированных с воспалением заболеваний. 17. Способ получения соединений формулы (I) G представляет собой группы А, В, С, D, Е или F, описанные ниже: где R 1 представляет собой водород, ацильную, галогенацильную группу; R 2 представляет собой (C 1 -C 3 )алкил; X 1 , X 2 , Х 3 , Х 4 могут быть одинаковыми или различными и представляют собой водород или галоген; и если G представляет собой гетероцикл D, то по меньшей мере одна из групп, определенных как X 1 , X 2 , Х 3 , Х 4 , не является водородом; R 3 выбран из замещенных или незамещенных арильных или гетероарильных групп, где заместители арильных групп выбраны из галогена, нитро, гидроксила, (C 1 -C 3 )алкила, (C 1 -C 3 )алкокси, гидрокси(C 1 -C 3 )алкокси, а заместители гетероарильных групп выбраны из (C 1 -C 3 )алкильных групп; R 4 выбран из атома водорода, атома галогена, карбокси, прямой или разветвленной (C 1 -С 3 )алкильной, гидрокси(C 1 -C 3 )алкильной, алкокси(C 1 -C 3 )алкильной, галоген(C 1 -C 3 )алкильной и фенильной групп, и R 5 представляет собой водород; Y представляет собой О; W представляет собой О или S; и где указанный способ предусматривает окисление соединения формулы (Р) с получением соединения формулы (Q), которое подвергают иминированию подходящими реагентами и получают соединение формулы (I), которое может быть затем, если это необходимо, превращено в его фармацевтически приемлемые соли. 18. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия галогенкетона формулы (II) с соединением формулы (III) с получением меркапто-соединения формулы (Р) 19. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий превращение оксима формулы (VII) в меркапто-соединение формулы (Р) 20. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия гидразина формулы (XI) с 1,3-дикетоном формулы (XII) с получением меркапто-соединения формулы (Р) 21. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия соединения формулы (XVII) с соединением формулы (XVIII) с получением меркапто-соединения формулы (Р) 22. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия соединения формулы (XXI) с соединением формулы (XXII) с получением меркапто-соединения формулы (Р)
008303 Область, к которой относится изобретение Настоящее изобретение относится к новым соединениям общей формулы (I), к их аналогам, производным, таутомерным формам, фармацевтически приемлемым солям; к фармацевтическим композициям, содержащим эти соединения, где G представляет собой замещенные или незамещенные одинарные или конденсированные группы, выбранные из арильной, гетероарильной или гетероциклической групп. Предпочтительно, G представляет собой группы А, В, С, D, Е и F, определенные ниже. Настоящее изобретение также относится к способу получения соединений общей формулы (I), их аналогов, производных, таутомерных форм, фармацевтически приемлемых солей, фармацевтических композиций, содержащих указанные соединения, и новых промежуточных соединений, участвующих в их синтезе. R3s . N-N \ Rs F Соединения настоящего изобретения могут быть использованы для лечения воспалительных заболеваний, предпочтительно, таких заболеваний, в которых патофизиологическую роль играют простагландины. Такая роль простагландинов приводит к ряду заболеваний, которыми являются ревматоидный артрит и остеоартрит, гипертермия, астма, резорбция кости, сердечно-сосудистые заболевания, дисменорея, преждевременные роды, нефрит, нефроз, атеросклероз, гипотензия, инсульт, боли, рак и болезнь Альцгеймера. Предпосылки создания изобретения Воспаление представляет собой расстройство, характеризующееся покраснением, повышением температуры, опуханием и болями. В таком воспалительном процессе главную роль играют про-стагландины, а поэтому общей целью при лечении воспаления является ингибирование продуцирования простагландинов, а в частности, PGG2, PGH2 и PGE2. Однако НСПВС (нестероидные противовоспалительные средства), которые обычно используются для ослабления болей и лечения воспалений, индуцируемых простагландинами, также влияют на другие регулируемые простагландинами процессы, не ассоциированные с воспалением. Такое действие НСПВС приводит к тяжелым побочным эффектам, включая опасные для жизни язвы желудка, диспепсию и нефротоксичность, что ограничивает терапевтическое применение этих лекарственных средств. Ранее было обнаружено, что НСПВС предотвращают продуцирование простагландинов у человека посредством ингибирования ферментов в метаболическом пути арахидоновой кисло-ты/простагландина, включая фермент циклооксигеназу (СОХ). В начале 1990-х годов было продемонстрировано, что СОХ существует в виде двух различных изоформ, СОХ-1 и СОХ-2 (PNAS (1991) 88, 2692-96), а недавно в головном мозге была обнаружена третья изоформа СОХ-3 (PNAS (2002) 99, 13926-13931). СОХ-1 и СОХ-2 обладают различными физиологическими и патофизиологическими функциями. СОХ-1 представляет собой конститутивную изоформу и является, главным образом, ответственной за синтез цитопротективных простагландинов в желудочно-кишечном тракте, а также за синтез тромбоксана, который приводит к стимуляции агрегации тромбоцитов в крови. СОХ-2, очевидно, представляет собой индуцибельную изоформу, которая стимулируется в ответ на действие эндотоксинов, цитокинов и митогенов. Важно отметить, что СОХ-2 играет главную роль в биосинтезе простагландинов в воспалительных клетках (моноцитах/макрофагах) и в центральной нервной системе. (Current Medicinal Chemistry (2000) 7, 1041-62). Использование COX-2 в качестве противоракового средства обсуждается в работе Curr. Drug. Targets 2001 Mar; 2 (1):79-106. Следовательно, различие в функциях СОХ-1 и СОХ-2 может быть использовано в целях предотвращения развития токсичности, ассоциированной, в частности, с действием НСПВС в желудочно-кишечном тракте, и может быть положено в основу при разработке лекарственных средств, которые представляли бы собой селективные ингибиторы СОХ-2, действующие как противовоспалительные, обезболивающие и/или жаропонижающие средства. Очевидно, что эти соединения должны обладать минимальным, или вообще не обладать, токсическим действием, ассоциированным с ингибированием СОХ-1 в желудочно-кишечном тракте и в кроветворных тканях, в отличие почти от всех существующих в настоящее время НСПВС, большинство из которых ингибируют как СОХ-1, так и СОХ-2, причем их специфичность в отношении ингибирования СОХ-1 значительно выше, чем в отношении СОХ-2. Целекоксиб и рофекоксиб являются первыми двумя селективными ингибиторами СОХ-2, апробированными на ограниченном рынке и используемыми для лечения некоторых воспалитель - 1 - 008303 ных состояний. Хотя идея селективного ингибирования СОХ-2 для повышения эффективности и безопасности лекарственных средств является чрезвычайно привлекательной, однако, недавно проведенные клинические исследования ставят под сомнение продолжительное действие селективных ингибиторов СОХ-2. Долгосрочные клинические исследования (BMJ (2002) 324, 1287-88) не подтвердили, что целекоксиб обладает лучшими свойствами, чем другие НСПВС. С другой стороны, высокоселективные ингибиторы СОХ-2 оказывают неблагоприятное действие на сердечно-сосудистую систему, в отличие от неселективных ингибиторов СОХ (Science (2002) 296, 539-541; JAMA (2001) 268, 954959). В нижеуказанных работах описаны противовоспалительные соединения, которые являются селективными ингибиторами СОХ-2. Все возрастающее число публикаций и патентов, появляющееся в настоящее время, свидетельствует о непрекращающихся попытках получить безопасное и эффективное противовоспалительное средство. Такие новые соединения и методы их получения описаны в ЕР1006114, ЕР1099695, ЕР418845, ЕР554829, ЕР0863134, ЕР0714895, ЕР0799523, GB2294879, US5474995, US5486534, US5510368, US5686460, US5691374, US5710140, US5723485, US5776967, US5981576, US5922742, US6083969, US6071954, US6071936, US6133292, US6143892, US6274590, WO9415932, WO9427980, WO9500501, WO9515315, WO9515316, WO9515317, WO9515318, WO9518799, WO9603387, WO9603392, WO9606840, WO9609304, WO9610012, WO9616934, WO9619469, WO9621667, WO9623786, WO9624585, WO9625405, WO9631509, WO9636623, WO9637467, WO9638418, WO9636617, WO9703667, WO9703953, WO9713755, WO9714691, WO9716435, WO9727181, WO9734882, WO9737984, WO9746524, WO97727181, WO9804527, WO9807425, WO9807714, WO9811080, WO9813483, WO9816227, WO9821195, WO9822442, WO9825896, WO9841511, WO9841516, WO9843966, WO9852940, WO9910331, WO9910332, WO9912930, WO9915503, WO9923087, WO9935130, WO0026216, WO0052008, WO0024719, WO0134577, WO0140216. Помимо СОХ, фермент липоксигеназа (LOX) также играет важную роль в воспалительном процессе, так, например, продукты 5-LOX, такие как LTB4, LTC4 и LTD4 участвуют в различных патологических процессах (Pharmacol Rev. (2003) 55, 195-227). Поэтому ингибирование активности 5-LOX может оказывать благоприятное воздействие на воспалительный процесс. Исследования показали, что двойные ингибиторы СОХ и LOX могут иметь лучший профиль безопасности (Pharmacol. Res. (2001), 43 429-436), чем неселективные НСПВС. Соединения настоящего изобретения могут быть использованы для лечения воспалительных состояний, вызываемых повышенными активностями ферментов СОХ и/или LOX. Известно, что в воспалительных процессах участвуют цитокины. Фактор некроза опухоли а (TNF-а) был описан как ключевой медиатор провоспаления при аутоиммунных заболеваниях. Этот 26 кДа-фермент является мембрано-ассоциированным ферментом, до тех пор, пока он не подвергается процессингу под действием TNF-а-конвертирующего фермента (ТАСЕ) с образованием менее крупной (17 кДа) растворимой формы. Соединения настоящего изобретения могут быть также использованы для лечения воспалительных заболеваний, таких как артрит, благодаря ингибированию TNF-a или ТАСЕ, либо благодаря ингибированию продуцирования фактора некроза опухоли а. Краткое описание изобретения В настоящем изобретении описана группа новых соединений, которые могут быть использованы для лечения воспалительных заболеваний, ассоциированных с действием цитокинов, а в частности, заболеваний, опосредованных действием TNF-a и заболеваний, опосредованных действием циклооксигеназы, таких как воспалительные заболевания и боли. Новые соединения представлены общей формулой (I), где G представляет собой замещенные или незамещенные одинарные или конденсированные группы, выбранные из арильной, гетероарильной или гетероциклической групп, содержащих один или несколько гетероатомов, выбранных из О, S, N, а предпочтительно G представляет собой группы А, В, С, D, Е и F, представленные ниже. D Е - 2 - 008303 Соединения настоящего изобретения могут быть использованы для лечения человека или животных, а в частности, для ослабления болей, снижения температуры или лечения воспалений, для ингибирования индуцированного простаноидами сокращения гладких мышц или для предупреждения рака прямой и толстой кишки. Указанные соединения также могут быть использованы для ослабления боли, снижения температуры и лечения воспалений при различных состояниях, включая ревматическую лихорадку и невропатические боли, симптомы, ассоциированные с гриппом или с другими вирусными инфекциями, насморк, боли в нижней части спины и шеи, дисменорею, головную боль, зубную боль, растяжения и повреждения тканей, миозит, невралгию, синовиит, бурсит, тендинит, поражения в результате хирургического вмешательства и лечения зубов, послеоперационные воспаления, включая хирургические операции на глазах, такие как операции по поводу катаракты и операции по исправлению дефектов рефракции глаза, а также мышечные спазмы при менструациях и преждевременные роды. Эти соединения могут быть также использованы для лечения артрита, например, ревматоидного артрита, спондилоартропатии, подагрического артрита, остео-артрита, системной красной волчанки и ювенильного артрита; воспалительных заболеваний кожи, таких как псориаз, экзема, ожоги и дерматит; причем, указанные соединения обладают более высокой эффективностью, активностью, и минимальным токсическим действием. Главной целью настоящего изобретения является получение новых соединений общей формулы (I), их аналогов, производных, таутомерных форм, фармацевтически приемлемых солей, фармацевтически приемлемых сольватов и фармацевтических композиций, содержащих указанные соединения или их смеси. Другой целью настоящего изобретения является разработка способа получения новых соединений общей формулы (I), их аналогов, производных, таутомерных форм, фармацевтически приемлемых солей, фармацевтически приемлемых сольватов и фармацевтических композиций, содержащих эти соединения. Еще одной целью настоящего изобретения является получение фармацевтических композиций, содержащих соединения общей формулы (I), их аналоги, производные, таутомерные формы, фармацевтически приемлемые соли, сольваты и их смеси с фармацевтически приемлемыми носителями, растворителями, разбавителями и другими средами, обычно используемыми для изготовления фармацевтических композиций. Настоящее изобретение также относится к разработке способа лечения заболеваний, опосредуемых циклооксигеназой, где указанный способ предусматривает введение млекопитающему терапевтически эффективного и нетоксичного количества соединения формулы (I) или фармацевтически приемлемых композиций, содержащих указанное соединение. Подробное описание изобретения Новые соединения настоящего изобретения определены нижеследующей общей формулой (I), где G представляет собой замещенные или незамещенные одинарные или конденсированные группы, выбранные из арильной, гетероарильной или гетероциклической групп, содержащих один или несколько гетероатомов, выбранных из О, S, N, а предпочтительно, G представляет собой группы А, В, С, D, Е и F, описанные ниже: D ? где R1 представляет собой водород, замещенные или незамещенные группы, выбранные из алкиль-ной, аралкильной, ацильной, алкилсульфонильной, арилсульфонильной групп; R2 представляет собой алкил, аралкил, алкокси или NHR, где R представляет собой водород или низшие алкильные группы, которые могут быть соответствующим образом замещенными; Х1, Х2, Х3, Х4 могут быть одинаковыми или различными и представляют собой водород, циано, нитро, галоген, карбоксил, формил, гидразино, азидо, амино, тио, гидрокси или замещенные или незамещенные группы, выбранные из следующих групп: алкила, который может быть прямым или разветвленным, алкенила, циклоалкила, алкокси, циклоалкокси, циклоалкоксиалкила, галогеналкок-си, гидроксиалкила, алкоксиалкила, тиоалкила, карбоксиалкила, галогеналкила, аминоалкила, циа-ноалкила, алкилтио, алкилсульфинила, алкилсульфонила, алкоксикарбонилалкила, ацила, ацилокси, - 3 - 008303 ацилоксиалкила, аралкила, арилокси, аралкокси, арилоксиалкила, аралкоксиалкила, аралкенила, ациламино, алкиламино, диалкиламино, аралкиламино, алкоксиамино, гидроксиламино, алкокси-карбонила, аралкоксикарбонила; где две смежные группы могут образовывать метилендиокси- или этилендиоксигруппу, и где, в случае, если G представляет собой гетероцикл "D", то по крайней мере одна из групп, определенных X1, X2, Х3, Х4, не является водородом; R3 выбран из замещенных или незамещенных алкильных групп и замещенных или незамещенных одинарных или конденсированных групп, выбранных из арильной, аралкенильной, гетероарильной или гетероциклильной групп; R4 и R5 выбраны из атома водорода, атома галогена, карбокси, и замещенных или незамещенных групп, выбранных из прямой или разветвленной алкильной, галогеналкильной, полигалогеналкиль-ной, алкоксикарбонильной, гидроксиалкильной, алкоксиалкильной и фенильной групп; Y представляет собой О или S; W представляет собой О или S. Подходящие заместители на группах R3 и R4 могут быть выбраны из циано, нитро, галогена, карбоксила, гидразино, азидо, формила, амино, тио, гидрокси, ONO2 или алкил-ОNO2, или замещенных или незамещенных групп, выбранных из следующих групп: алкила, который может быть прямым или разветвленным, пергалогеналкила, алкокси, гидразиноалкила, алкилгидразидо, ацила, ацилокси, оксо, карбоксиалкила, галогеналкила, аминоалкила, галогеналкокси, гидроксиалкила, ал-коксиалкила, тиоалкила, алкилтио, алкилсульфинила, алкилсульфонила, алкилсульфоксиминила, арила, аралкила, арилокси, аралкокси, арилоксиалкила, аралкоксиалкила, арилоксикарбонила, ал-коксикарбонила, аралкоксикарбонила, алкоксикарбонилалкила, амидино, карбоксамидоалкила, аци-ламино, цианоамидино, цианоалкила, N-аминокарбонилалкила, N-ариламинокарбонила, карбокси-алкиламинокарбокси, N-алкиламино, N,N-диалкиламино, N-ариламино, N-аралкиламино, N-алкил-N-аралкиламино, N-алкил-N-ариламино, N-алкиламиноалкила, М,N-диалкиламиноалкила, N-арил-аминоалкила, N-аралкиламиноалкила, N-алкил-N-аралкиламиноалкила, ^алкил-^ариламино-алкила, арилтио, аралкилтио, N-алкиламиносульфонила, N-ариламиносульфонила, арилсульфонила, ^^диалкиламиносульфонила, N-алкил-N-ариламиносульфонила, алкоксикарбонила, аминокарбо-нила, циклоалкила, гетероциклила, гетероциклилалкила, гетероарила, гетероаралкила, гетероарал-кокси и сульфамила, где две смежные группы могут образовывать метилендиокси- или этилендиок-сигруппу. Подходящие заместители на группах X1, Х2, Х3, Х4 могут быть выбраны из циано, нитро, галогена, карбоксила, гидразино, азидо, формила, амино, тио, гидрокси или замещенных или незамещенных групп, выбранных из следующих групп: алкила, который может быть прямым или разветвленным; алкокси, алкоксикарбонила, ацила, ациламино, ацилокси, гидразиноалкила, алкилгидрази-до, карбоксиалкила, галогеналкила, аминоалкила, галогеналкокси, гидроксиалкила, алкоксиалкила, тиоалкила, алкилтио, алкилсульфинила, алкилсульфонила, арила, аралкила, арилокси, аралкокси, арилоксиалкила, аралкоксиалкила, алкоксикарбонила, амидино. Термин "алкил", используемый в настоящем описании отдельно или в комбинации с другими терминами, такими как "галогеналкил", "гидроксиалкил", "алкилтио", "алкилсульфонил" и т.п., включает прямые или разветвленные радикалы, содержащие от одного до десяти атомов углерода. Более предпочтительными алкильными радикалами являются "низшие алкильные" радикалы, имеющие от одного до шести атомов углерода. Примерами таких радикалов являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, изоамил, гексил, изогек-сил, гептил, октил и т.п. Термин "алкенил" включает прямые или разветвленные радикалы, имеющие по крайней мере одну углерод-углеродную двойную связь, и содержащие от двух до десяти атомов углерода, или, предпочтительно, от двух до шести атомов углерода. Примерами таких радикалов являются этенил, н-пропенил, бутенил и т.п. Термин "галоген" означает атомы фтора, хлора, брома или йода. Термин "галогеналкил" означает радикалы, где один или несколько атомов углерода алкила замещены атомами галогена, определенными выше. Примерами являются моногалогеналкил, дига-логеналкил, полигалогеналкил или аналогичные радикалы. Моногалогеналкильный радикал, например, может иметь любой из атомов йода, брома, хлора или фтора. Дигалоген- и полигалогеналкиль-ные радикалы могут иметь два или более одинаковых атома галогена или комбинацию из различных галогеновых радикалов. Алкильная группа в галогеналкильной группе представляет собой низшую алкильную группу и называется "низшей галогеналкильной" группой. "Низший галогеналкил" означает радикалы, имеющие 1-6 атомов углерода. Примерами гало-геналкильных радикалов являются фторметил, дифторметил, трифторметил, хлорметил, дихлорме-тил, трихлорметил, трихлорэтил, пентафторэтил, дифторхлорметил, дихлорфторметил, дифторэтил, дифторпропил и т.п. Термин "гидроксиалкил" включает прямые или разветвленные алкильные радикалы, имеющие от одного до десяти атомов углерода, один из которых может быть замещен одним или несколькими гидроксильными радикалами. Более предпочтительными гидроксиалкильными радикалами являются "низшие гидроксиалкильные" радикалы, имеющие от одного до шести атомов углерода и один - 4 - 008303 или несколько гидроксильных радикалов. Примерами таких радикалов являются гидроксиметил, гидроксиэтил, гидроксипропил, гидроксибутил, гидроксипентил и гидроксигексил. Термины "алкокси" и "алкоксиалкил" включают линейные или разветвленные оксисодержа-щие радикалы, каждый из которых имеет алкильные части примерно из одного-десяти атомов углерода, такие как метоксирадикал. Предпочтительными алкоксирадикалами являются такие радикалы, как "низшие алкокси", имеющие от одного до шести атомов углерода. Примерами таких радикалов являются метокси, этокси, пропокси, бутокси и трет-бутокси. Термин "алкоксиалкил" также включают алкильные радикалы, имеющие два или более алкок-си-радикалов, связанных с алкильным радикалом, то есть образующих моноалкоксиалкильные и диалкоксиалкильные радикалы. Предпочтительными алкоксиалкильными радикалами являются " низшие алкоксиалкильные" радикалы, имеющие от одного до шести атомов углерода и один или два алкоксирадикала. Примерами таких радикалов являются метоксиметил, метоксиэтил, этокси-этил, метоксибутил, метоксипропил и т. п. "Алкокси-" или "алкоксиалкильные" радикалы могут, кроме того, иметь замещение одним или несколькими атомами галогена, такими как фтор, хлор или бром с образованием радикалов "галогеналкокси" или "галогеналкоксиалкил". Примерами таких радикалов являются фторметокси, хлорметокси, трифторметокси, трифторэтокси, фторэтокси и т.п. Термин "арил", используемый отдельно или в комбинации, включает карбоциклическую ароматическую систему, содержащую один, два или три цикла, где эти циклы могут быть присоединены друг к другу в боковой группе, либо они могут быть конденсированными. Термин "арил" включает ароматические радикалы, такие как фенил, нафтил, тетрагидронаф-тил, индан и бифенил. Термин "гетероциклический" радикал включает насыщенные, частично насыщенные и ненасыщенные циклические радикалы, в которых гетероатомы выбраны из атомов азота, серы и кислорода. Примерами насыщенных гетероциклических радикалов являются насыщенная 3-7-членная гетероциклическая группа, содержащая один или несколько гетероатомов, выбранных из О, N или S. Примерами таких групп являются, но не ограничиваются ими, азиридинил, азетидинил, пирроли-динил, имидазолидинил, пиперидинил, пиперазинил, 2-оксопиперидинил, 4-оксопиперидинил, 2-оксопиперазинил, 3-оксопиперазинил, морфолинил, тиоморфолинил, 2-оксоморфолинил, азепинил, диазепинил, оксазепинил, тиазепинил, оксазолидинил, тиазолидинил и т.п., а примерами частично насыщенных гетероциклических радикалов являются дигидротиофен, дигидропиран, дигидрофуран, дигидротиазол и т. п.; термин "гетероарил" включает ненасыщенные гетероциклические радикалы. Примерами ненасыщенных гетероциклических радикалов, также называемых "гетероарильными" радикалами, являются ненасыщенные 5-6-членные гетеромоноциклические группы, конденсированные полициклические гетероарильные группы или конденсированные полициклические гетероциклические группы, содержащие один или несколько гетероатомов, выбранных из О, N, S. Примерами таких групп являются, но не ограничиваются ими, пирролил, пирролинил, имидазолил, пира-золил, 2-пиридил, 3-пиридил, 4-пиридил, пиримидил, пиразинил, пиридазинил, триазолил (например, 4Н-1,2,4-триазолил, 1 Н-1,2,3-тетразолил и т.п.), индолил, изоиндолил, дигидроиндолил, бензо-фурил, 2,3-дигидробензофурил, хроманил, бензопиран, тиохроманил, бензотиопиран, бензодиоксо-лил, бензодиоксанил, пиридил, тиенил, бензотиенил, оксазолил, бензимидазолил, хинолил, изохи-нолил, индазолил, бензотриазолил, тетразолпиридазинил, пиранил, 2-фурил, 3-фурил, фталазинил, хиназолинил, хинолинил, изохинолинил, бензоксазолил, бензоксадиазолил, тиазолил, тиадиазолил, бензотиазолил, бензотиадиазолил, бензофуран, бензотиофен и т.п. Вышеуказанные "гетероциклические" или "гетероарильные" группы могут иметь 1-4 заместителя, такие как низший алкил, галоге-налкил, дигалогеналкил, тригалогеналкил, гидрокси, оксо, амино и низший алкиламино, низший алкокси, галоген, низший тиоалкил, ацил, ациламино. Предпочтительными гетероциклическими радикалами являются 5-10-членные конденсированные или неконденсированные радикалы, а более предпочтительными примерами гетероарильных радикалов являются бензофурил, 2,3-дигидробензофурил, бензотиенил, индолил, дигидроиндолил, хроманил, бензопиран, тиохроманил, бензотиопиран, бензодиоксолил, бензодиоксанил, пиридил, тиенил, тиазолил, оксазолил, фурил, пиразинил, фталазинил, хиназолинил, хинолинил, изохинолинил, бензоксазолил, бензотиазолил и т.п. Термин "гидразино", используемый отдельно или в комбинации с другими радикалами, означает -NHNH-, соответствующим образом замещенный другими радикалами, такой как алкилгидра-зино, где алкильная группа, определенная выше, присоединена к гидразиногруппе. Термин "сульфонил", используемый отдельно или в комбинации с другими терминами, такими как алкилсульфонил, означает, соответственно, двухвалентные радикалы -SO2-. Термин "алкил-сульфонил" включает алкильные радикалы, связанные с сульфонильным радикалом, где алкил определен выше. Более предпочтительными алкилсульфонильными радикалами являются низшие ал-килсульфонильные радикалы, имеющие от одного до шести атомов углерода. Примерами таких низших алкилсульфонильных радикалов являются метилсульфонил, этилсульфонил и пропилсуль-фонил. Термин "арилсульфонил" включает арильные радикалы, определенные выше, и связанные с - 5 - 008303 сульфонильным радикалом. Примерами таких радикалов являются фенилсульфонил. Термины "сульфамид", "аминосульфонил" и "сульфонамидил", используемые отдельно или с другими терминами, такими как "N-алкиламиносульфонил", "N-ариламиносульфонил", "N,N-диалкиламиносульфонил" и "N-алкил-N-ариламиносульфонил" означают сульфонильный радикал, замещенный аминовым радикалом с образованием сульфонамида (SO2NH2). Термины "N-ариламиносульфонил" и "N,N-диалкиламиносульфонил" означают сульфамильные радикалы, замещенные, соответственно, одним алкильным радикалом или двумя алкильными радикалами. Более предпочтительными алкиламиносульфонильными радикалами являются "низшие алкиламиносуль-фонильные" радикалы, имеющие от одного до шести атомов углерода. Примерами таких низших алкиламиносульфонильных радикалов являются N-метиламиносульфонил, N-этиламиносульфонил, N-метил-N-этиламиносульфонил и т.п. Термины "N-ариламиносульфонил" и "N^iaui-N-ариламиносульфонил" означают сульфамильные радикалы, замещенные, соответственно, одним арильным радикалом или одним алкильным и одним арильным радикалами. Предпочтительными N-алкил-^ариламиносульфонильными радикалами являются низшие ^алкил-^арилсульфонильные радикалы, имеющие алкильные радикалы с 1-6 атомами углерода. Примерами таких низших N-алкил-N-арилсульфонильных радикалов являются N-этилфениламиносульфонил и т.п. Термины "карбокси" или "карбоксил", используемые отдельно или с другими терминами, такими как "карбоксиалкил" означают -CO2H. Термины "алканоил" или "ацил" включают радикалы, происходящие от карбоновых кислот, и такими радикалами являются, но не ограничиваются ими, замещенные или незамещенные группы, выбранные из формила, ацетила, пропионила (пропаноила), бутаноила (бутирила), изобутаноила (изобутирила), валерила (пентаноила), изовалерила, пивалоила, гексаноила, бензоила или т.п. Термин "карбонил", используемый отдельно или с другими терминами, такими как "алкилкарбонил", означают -(C=O)-. Термин "алкилкарбонил" включает радикалы, имеющие карбонильный радикал, замещенный алкильным радикалом, таким как ацил или алканоил, определенные выше. Термин "алкилкарбонилалкил" означает алкильный радикал, замещенный "ал-килкарбонильным" радикалом. Термин "алкоксикарбонил" означает радикал, содержащий алкокси-радикал, определенный выше и связанный посредством атома кислорода с карбонильным радикалом. Предпочтительно, термин "низший алкоксикарбонил" включает алкоксирадикалы, имеющие от 1 до 6 атомов углерода. Примерами таких сложноэфирных радикалов как "низший алкоксикарбо-нил" являются замещенный или незамещенный метоксикарбонил, этоксикарбонил, пропоксикарбо-нил, бутоксикарбонил и гексилоксикарбонил. Термин "алкоксикарбонилалкил" включает радикалы, содержащие "алкоксикарбонил", определенный выше и присоединенный к алкильному радикалу. Предпочтительными алкоксикарбонилалкильными радикалами являются "низшие алкоксикарбони-лалкилы", имеющие низшие алкоксикарбонильные радикалы, определенные выше и связанные с алкилом, содержащим от 1 до 6 атомов углерода, например, метоксикарбонилметил, трет-бутоксикарбонилэтил и метоксикарбонилэтил. Термин "аминокарбонил", используемый отдельно или с другими терминами, такими как "аминокарбонилалкил", "N-алкиламинокарбонил", "N-ариламинокарбонил", "N,N-диалкиламинокарбонил", "N-алкил-N-ариламинокарбонил", "^алкил-^ гидроксиаминокарбонил" и '^-алкил^-гидроксиаминокарбонилалкил", означает аминокарбониль-ный радикал, который является замещенным или незамещенным. Термины "N-алкиламинокарбонил" и "^^диалкиламинокарбонил" означают аминокарбонильные радикалы, замещенные одним алкильным радикалом и двумя алкильными радикалами соответственно. Предпочтительным является "низший алкиламинокарбонил", имеющий низшие алкильные радикалы, определенные выше и присоединенные к аминокарбонильному радикалу. Термины "N-ариламинокарбонил" и "N-алкил-N-ариламинокарбонил" означают аминокарбонильные радикалы, замещенные соответственно одним арильным радикалом или одним алкильным и одним арильным радикалом. Термин "аминокарбонилалкил" включает алкильные радикалы, замещенные аминокар-бонильными радикалами. Термин "амидино" означает радикал -C(=NH)-NH2. Термин "цианоамидино" означает радикал -C(=N-CN)-NH2. Термин "гетероциклилалкил" включает алкильные радикалы, замещенные гетероциклической группой. Более предпочтительными гетероциклилалкильными радикалами являются " низшие гетероциклилалкильные радикалы", имеющие от 1 до 6 атомов углерода, и гетероциклический радикал. Примерами являются такие радикалы, как пирролидинилметил, пиридилметил и тие-нилметил. Термин "аралкил" включает арилзамещенные алкильные радикалы. Предпочтительными аралкильными радикалами являются "низшие аралкильные" радикалы, имеющие арильные радикалы, присоединенные к алкильным радикалам с 1-6 атомами углерода. Примерами таких радикалов являются бензил, дифенилметил, трифенилметил, фенилэтил, дифенилэтил и т.п. Арил в указанном аралкиле может быть, кроме того, замещен галогеном, алкилом, алкокси, галогеналкилом, галоге-налкокси, гидрокси, амино, ациламино, алкоксикарбонилом, алкилтио и т. п. Термины "бензил" и "фенилметил" являются взаимозаменяемыми. Термин "циклоалкил" включает радикалы, имеющие от трех до десяти атомов углерода. Более предпочтительными циклоалкильными радикалами являются "низшие циклоалкильные" радикалы, имеющие от 3 до 7 атомов углерода. Примерами таких - 6 - 008303 радикалов являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т. п. Термин "циклоалкенил" включает ненасыщенные циклические радикалы, имеющие от 3 до 10 атомов углерода, такие как циклобутенил, циклопентенил, циклогексенил, циклогептенил и т. п. Термин " алкилтио" включает радикалы, содержащие прямой или разветвленный алкильный радикал, связанный с двухвалентным атомом серы. Примерами алкилтио являются метилтио (CH3-S-), этилтио, бутилтио и т. п. Термин "алкилсульфинил" включает радикалы, содержащие прямой или разветвленный радикал, связанный с двухвалентным атомом S(=O). Термин "аминоалкил" включает алкильные радикалы, замещенные аминорадикалами. Предпочтительными аминоалкильными радикалами являются "низший аминоалкил", имеющий от 1 до 6 атомов углерода. Примерами являются аминометил, аминоэтил и аминобутил. Термин "алкиламиноалкил" включает аминоалкильные радикалы, имеющие атом азота, замещенный по крайней мере одним алкильным радикалом. Предпочтительным алкиламиноалкильными радикалами являются "низший алкиламиноалкил", имеющий от 1 до 6 атомов углерода, связанных с низшим аминоалкильным радикалом, определенным выше. Термины "N-алкиламино" и "^^диалкиламино" означают аминогруппы, замещенные одним алкильным радикалом и двумя алкильными радикалами соответственно. Предпочтительными алки-ламинорадикалами являются "низшие алкиламино"-радикалы, имеющие один или два алкильных радикала с 1-6 атомами углерода, связанных с атомом азота. Подходящим "алкиламино" может быть ^^диметиламино, ^^диэтиламино или т.п. Термин "ариламино" означает аминогруппы, замещенные одним или двумя арильными радикалами, такие как N-фениламино. Такие "ариламино"-радикалы могут быть, кроме того, замещены на арильной циклической части этого радикала. Термин "аралкиламино" означает аминогруппы, замещенные одним или двумя аралкильными радикалами, такие как N-бензиламино. Такие "аралкиламино "-радикалы могут быть, кроме того, замещены на арильной циклической части этого радикала. Термины "^алкил-^ариламино" и "^аралкил-^алкиламино" означают аминогруппы, замещенные одним аралкильным и одним алкильным радикалом, или одним арильным и одним алкиль-ным радикалом соответственно. Термины "N-ариламиноалкил" и "N-аралкиламиноалкил" означают аминогруппы, замещенные одним арильным радикалом или одним аралкильным радикалом, соответственно, где указанные аминогруппы присоединены к алкильному радикалу. Предпочтительными ариламиноалкильными радикалами являются "низший ариламиноалкил", имеющий ариламино-радикал, связанный с алки-лом, имеющим от 1 до 6 атомов углерода. Примерами таких радикалов являются N-фениламинометил и ^фенил-^метиламинометил. Термины "N-алкил-N-ариламиноалкил" и "^аралкил-^алкиламиноалкил" означают N-алкил-N-ариламино- и ^алкил-^аралкиламиногруппы соответственно, где указанная аминогруппа присоединена к алкильным радикалам. Термин "ацил", используемый отдельно или с другими терминами, такими как "ациламино", означает радикал, образованный остатком после удаления гидроксила из органической кислоты. Термин "ациламино" включает аминорадикал, замещенный ацильной группой. Примерами "ациламино"-радикала являются ацетиламино или ацетамидо (CH3C(=O)-NH-), где амин может быть, кроме того, замещен алкилом, арилом или аралкилом. Термин "арилтио" включает арильные радикалы, имеющие 6-10 атомов углерода и связанные с двувалентным атомом серы. Примером "арилтио" является фенилтио. Термин "аралкилтио" включает аралкильные радикалы, определенные выше и связанные с двувалентным атомом серы. Примером "аралкилтио" является бензилтио. Термин "арилокси" включает арильные радикалы, определенные выше и связанные с атомом кислорода. Примерами таких радикалов является фенокси. Термин "аралкокси" включает оксисодержащие аралкильные радикалы, связанные посредством атома кислорода с другими радикалами. Предпочтительными аралкоксирадикалами являются "низшие аралкокси", имеющие фенильные радикалы, связанные с низшим алкоксирадикалом, определенным выше. Термин "галогенаралкил" включает арильные радикалы, определенные выше. Термин "карбок-сигалогеналкил" включает карбоксиалкильные радикалы, определенные выше, где галогены связаны с алкильной частью. Термин "аралкенил" включает арильные радикалы, связанные с алкенильными радикалами, имеющими от 2 до 10 атомов углерода, такие как фенилбутенил, фенилэтенил или стирил. Подходящие группы и заместители на указанных группах могут быть выбраны из групп, описанных в настоящей заявке. Наиболее подходящими соединениями настоящего изобретения являются 5-(4-фторфенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(4-хлорфенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; - 7 - 008303 5-(4-метилфенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-(4-н-пропоксифенил)-3-трифторметил-1Н-пиразол; 5-(4-этоксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(4-гидроксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3-хлор-4-фторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3,4-дифторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(4-фтор-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(4-метокси-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3-хлор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3-бром-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3-метокси-4-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 1-(2-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразол; 1-(3-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-фенил-3-трифторметил-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-( 1-нафтил)-3-трифторметил-1Н-пиразол; 5-(4-метоксифенил)-3 -метил-1 -(4-метилсульфоксиминилфенил)-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-(4-нитрофенил)-3-трифторметил-1Н-пиразол; 5-(3-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3,5-дифтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(3 -гидрокси-4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-(4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-1Н-пиразол-3 -карбоновая кислота; 3-(гидроксиметил)-5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразол; 5-(4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-1Н-пиразол-3 -илметилгидросульфат; 5-{4-(2-гидроксиэтокси)фенил}-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-(4-пиридил)-3-трифторметил-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-(3-пиридил)-3-трифторметил-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-(2-пиридил)-3-трифторметил-1Н-пиразол; 5-(4-изопропоксифенил)-1 -(4-метилсульфоксиминилфенил)-3 -трифторметил-1Н-пиразол; 1-(4-метилсульфоксиминилфенил)-5-(2-тиофенил)-3-трифторметил-1Н-пиразол; 5-(4-метилсульфоксиминилфенил)-1-фенил-3-трифторметил-1Н-пиразол; 1-(4-метоксифенил)-5-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол; 5-этил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазол; 5-метоксиметил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазол; 3-(4-фторфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазол; 3-(4-хлорфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазол; 3-этил-4-(4-метилсульфоксиминилфенил)-5-фенилизоксазол; 5-хлор-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазол; 5-метил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазол; 3-(4-метоксифенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазол; 3-(3,4-дихлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-он; 3-(4-хлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-он; 3-фенил-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-он; 3-(3,4-дифторфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-он; 3-(3,4-диметоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-он; 3-(4-метоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-он; 3-(4-метилфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-он; 5-хлор-3-(4-метилсульфоксиминилфенил)-6'-метил[2,3']бипиридинил; 5-хлор-3-(4-метилсульфоксиминилфенил)-[2,3']бипиридинил; 3-(3-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-он; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-он; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-он; 3-(2-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-он; 3- (4-бромфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-он; 4- (4-метилсульфоксиминилфенил)-3-фенил-3Н-оксазол-2-он; 3-(3,4-дихлорфенил)-4-[4-(N-хлорацетил)метилсульфоксиминилфенил]-3H-оксазол-2-он; 3-(3,4-дихлорфенил)-4-[4-(N-ацетил)метилсульфоксиминилфенил]-3H-оксазол-2-он; 3-(3,4-дихлорфенил)-4-[4-(N-метилсульфонил)метилсульфоксиминилфенил]-3H-оксазол-2-он; - 8 - 008303 3-(3,4-дихлорфенил)-4-[4-{М-(4-метилфенил)сульфонил}метилсульфоксиминилфенил]-ЗН-оксазол-2-он. Настоящее изобретение также относится к получению новых соединений общей формулы (I), их таутомерных форм, производных, аналогов, фармацевтически приемлемых солей и фармацевтически приемлемых сольватов, где все символы являются такими, как они были определены выше. Указанный способ предусматривает: Окисление соединения формулы (Р) с получением соединения формулы (Q), которое подвергают иминированию подходящими реагентами и получают соединение формулы (I), которое может быть затем превращено в его фармацевтически приемлемые соли, если это необходимо. Окисление Метод В и х2 R2 ГТГ*1 Х4 (Q) RiV/°x2 Иминирование R2' Метод С х < (I) Подробное описание способа с различными группами G приводится в нижеследующих схемах: Метод В. Меркапто-соединения формулы (Р) могут быть превращены в соответствующие сульфоксиды формулы (Q) посредством взаимодействия с окислителем. Подходящие окислители могут быть выбраны из соединений, которыми являются, но не ограничиваются ими, пероксиды и пероксикислоты и их соли. Подходящий окислитель выбран из Н202, мета-пероксидов Na, K и т.п., оксона(r), пербо-рата натрия, вольфрамата натрия и т. п., перуксусной кислоты, м-хлорпербензойной кислоты, моно-пероксифталата магния и т. п. Походящими растворителями являются растворители на основе используемых окислителей, и такие растворители выбраны из воды, уксусной кислоты, ацетонитрила, дихлорметана, ацетона, ТГФ, метанола, этанола и т.п. или их смеси. Температура реакции может составлять от -78 до 40°С, в зависимости от используемого растворителя. Метод С. Сульфоксидные соединения формулы (Q) могут быть превращены в сульфоксиминовые соединения формулы (I) путем взаимодействия с подходящими иминирующими агентами, такими как азотисто-водородная кислота (HN3), которая может быть получена посредством взаимодействия NaN3 с концентрированной серной кислотой в растворителях, таких как СН2С12, СНС13 и т.п. Температура может составлять в пределах от -10°С до температуры флегмообразования используемо-го(ых) растворителя(ей). Альтернативно, сульфоксиды формулы (IV) или (V) могут быть обработаны О-замещенными гид-роксиламинами, такими как 0-мезитиленсульфонилгидроксиламин (MSH), а затем основанием, таким как KОН, NaOH, NaHCO3 и т.п. Могут быть использованы растворители, такие как СН2С12, СНС13. Схема I Соединения общей формулы (IA), где все символы являются такими, как они были определены выше, могут быть получены путем проведения одной или нескольких реакций или комбинаций реакций, проиллюстрированных ниже на схеме I, которые включают: R4 3 am Метод А OA) - 9 - 008303 i) реакцию взаимодействия соединения формулы (II), где R2, R4, Xb Х2, Х3, Х4 определены выше, a Hal представляет собой атом галогена, такой как хлор, бром или иод, с арилтиокарбаматом III, с получением соединения формулы (V), после дегидратации промежуточного соединения IV; (ii) реакцию взаимодействия соединения формулы (V) с окисляющим соединением, таким как Н2О2, перкислота и другие окислители, с получением сульфоксида формулы (VI); (iii) реакцию взаимодействия сульфоксида формулы (VI) с соответствующим иминирующим агентом, таким как HN3, O-замещенными гидроксиламинами, такими как O-мезитиленсуль-фонилгидроксиламин (MSH) и т.п., с получением сульфоксамина формулы (!Аа); (iv) необязательно, превращение соединения формулы (!Аа) в соединение формулы (IA) с использованием подходящих агентов, с получением соответствующей группы R1. Альтернативно, соединение формулы (VI) может быть превращено в соединение (IA) путем обработки соответствующими агентами; v) при желании, но необязательно, превращение соединения формулы (!Аа) или (IA) в фармацевтически приемлемые соли; Реакции, описанные выше в способах (i)-(v), могут быть осуществлены методами, описанными ниже. Метод А. Галогенкетоны формулы (II) могут быть превращены в соответствующие циклические соединения формулы (V) посредством реакции взаимодействия с соединением формулы (II), сначала с получением соединения формулы (IV) в растворителе, таком как спирт, например, метанол, этанол, изопропанол и т.п.; ацетон, ТГФ, диоксан, ацетонитрил, толуол, ксилол и т.п. или их смеси. Температура реакции может варьироваться от комнатной температуры до температуры флегмообразова-ния используемого(ых) растворителя(ей). Соединения формулы (IV) превращают в соответствующее соединение формулы (V) путем дегидратации при кипячении с обратным холодильником в подходящей среде, такой как водная спиртовая среда, содержащая минеральную кислоту, такую как НС1, H2SO4 или Н3Р04; при этом, могут быть также использованы органические кислоты, такие как PTSA в органическом растворителе, таком как толуол, ксилол и т. п., а также органическая кислота, такая как уксусная кислота, пропионовая кислота или трифторуксусная кислота. Метод В. Меркапто-соединения формулы (V) могут быть превращены в соответствующие сульфоксиды посредством взаимодействия с окислителем. Подходящие окислители могут быть выбраны из соединений, которыми являются, но не ограничиваются ими, пероксиды и пероксикислоты и их соли. Подходящий окислитель выбран из Н^2, мета-пероксидов Na, K и т.п., оксона(r), пербората натрия, вольфрамата натрия и т. п., перуксусной кислоты, м-хлорпербензойной кислоты, монопероксифтала-та магния и т. п. Походящими растворителями являются растворители на основе используемых окислителей, и такие растворители выбирают из воды, уксусной кислоты, ацетонитрила, дихлорме-тана, ацетона, ТГФ, метанола, этанола и т. п. или их смеси. Температура реакции может составлять в пределах от -78 до 40°С, в зависимости от используемого растворителя. Метод С. Сульфоксидные соединения формулы (VI) могут быть превращены в сульфоксиминовые соединения посредством взаимодействия с подходящими иминирующими агентами, такими как азо-тистоводородная кислота (HN3), которая может быть получена посредством взаимодействия NaN3 с концентрированной серной кислотой в растворителях, таких как СН2С12, СНС13 и т.п. Температура может составлять в пределах от -10°С до температуры флегмообразования используемого(ых) рас-творителя(ей). Альтернативно, сульфоксиды формулы (IV) или (V) могут быть обработаны О-замещенными гидроксиламинами, такими как O-мезитиленсульфонилгидроксиламин (MSH), а затем основанием, таким как ЮН, NaOH, NaHCO3 и т.п. Могут быть использованы растворители, такие как СН2С12, СНС13. Метод D. Сульфоксимины формулы (!Аа) могут быть превращены в соответствующие замещенные соединения формулы (IA) посредством взаимодействия с соответствующими алкилирующи-ми/ацилирующими агентами в присутствии основания. Выбор алкилирующего/ацилирующего агента зависит от нужной группы R1, например, такими агентами могут быть соответствующим образом замещенные алкилгалогениды/ацилгалогениды или ацилангидриды. Если Ri=Me, то используется смесь муравьиной кислоты и формальдегида. В качестве растворителей могут быть использованы ДМФ, ДМСО, ацетон, ТГФ, диоксан, толуол, ксилол и т.п. или их смеси. Могут быть также использованы основания, такие как K2TO3, Na2CO3, NaH, KI, n-BuLi, Et3N или их смеси. Температура реакции может составлять от 0°С до температуры флегмообразования используемого растворителя(ей). Метод Е. Сульфоксидные соединения формулы (VI) могут быть непосредственно превращены в замещенные сульфоксиминовые соединения посредством взаимодействия с подходящими реагентами, - 10 - 008303 такими как тозилазид, хлорамин Т, в растворителях, таких как этанол, метанол и т.п., с последующим подщелачиванием и с образованием групп Я1=тозил. Альтернативно, в результате реакции взаимодействия с ариламинами в присутствии t-BuOCl получают N-арилсульфоксимины. Схема II Соединения общей формулы (IB), где все символы являются такими, как они были определены выше, могут быть получены путем проведения одной или нескольких реакции или комбинаций реакций, проиллюстрированных ниже на схеме II, которые включают i) реакцию взаимодействия соединения общей формулы (VII) по крайней мере с двумя эквивалентами подходящего основания, с последующей обработкой соответствующим сложным эфиром или ангидридом, и с получением спирта общей формулы (VIII); (ii) нагревание соединения общей формулы (VIII) в соответствующем растворителе в присутствии подходящей кислоты с получением соединения общей формулы (IX); (iii) окисление соединения формулы (IX) соответствующими окислителями с получением соединения общей формулы (X); (iv) реакцию взаимодействия сульфоксида формулы (X) с соответствующими агентами, с получением соединения общей формулы (IBb); (v) необязательно, превращение соединения формулы (X) в соединение формулы (IB) с использованием подходящих агентов и с получением соответствующей группы R1. Альтернативно, соединение формулы (IBb) может быть превращено в соединение (IB) с использованием подходящих агентов; vi) при желании, но необязательно, превращение соединений формулы (IBb) или (IB) в фармацевтически приемлемые соли. Реакции, описанные в способах, проиллюстрированных выше на схемах II, могут быть осуществлены нижеследующими методами. Метод F. Оксим формулы (VII) может быть превращен в спирт формулы (VIII) посредством взаимодействия с двумя эквивалентами подходящего основания с получением дианиона, который затем аци-лируют. Могут быть использованы основания, такие как n-BuLi, гидрид натрия, LDA, LiHMDS, NaHMDS и т.п. или их смесь. Температура может составлять в пределах от -78°С до комнатной температуры. Предпочтительно, образование дианиона происходит при температуре в пределах от -78 до -40°С. Подходящими ацилирующими агентами являются сложные эфиры, ангидриды, ацилими - 11 - 008303 дазолы и т.п. Реакцию осуществляют в инертной атмосфере с использованием инертных газов, таких как N2, He или Аг. Для получения хорошего продукта и высокого выхода, очень важно, чтобы данная реакция протекала в безводных условиях. Метод G. Спирт формулы (VIII) может быть превращен в изоксазол формулы (IX) путем дегидратации в присутствии кислоты. При этом, могут быть использованы растворители, такие как этанол, ТГФ, толуол, ксилол и т.п. или их смесь. Подходящими кислотами могут быть PTSA, H2SO4, HCl, НВг, камфорсульфоновая кислота, пиридинийпаратолуолсульфоновая кислота и т. п. Для осуществления дегидратации, указанная кислота может быть использована в каталитическом, субстехиометриче-ском или стехиометрическом количестве. Температура может составлять в пределах от комнатной температуры до температуры флегмообразования растворителя(ей). Метод В. Меркапто-соединение формулы (IX) может быть превращено в сульфоксид формулы (X) посредством взаимодействия с окислителем, как описано выше в методе В схемы I. Метод С. Сульфоксидные соединения формулы (X) могут быть превращены в сульфоксиминовые соединения формулы (IBb) посредством взаимодействия с подходящими иминирующими агентами, как описано выше в методе С схемы I. Метод D. Сульфоксимины формулы (IBb) могут быть превращены в соединения формулы (IB) посредством взаимодействия с подходящими алкилирующими/ацилирующими агентами в присутствии основания, как описано выше в методе D схемы I. Метод Е. Соединения X могут быть непосредственно превращены в соединения формулы (IB) посредством взаимодействия с подходящими реагентами как описано выше в методе Е схемы I, такими как тозилазид, хлорамин Т, в растворителях, таких как этанол, метанол и т.п. с последующим подщела-чиванием и получением групп R1=тозил. Альтернативно, в результате реакции взаимодействия с ариламинами в присутствии t-BuOCl получают N-арилсульфоксимины, как описано в методе Е схемы I. Схема III Соединение общей формулы (ГС), где все символы являются такими, как они были определены выше, может быть получено способом, проиллюстрированным на схеме III, который предусматривает: (ICc) i) проведение реакции взаимодействия гидразина общей формулы (XI) с 1,3-дикетоном общей формулы (XII) с получением соединения общей формулы (XIII); - 12 - 008303 (ii) окисление соединения формулы (XIII) подходящим окислителем с получением соединения общей формулы (XIV); (iii) проведение реакции взаимодействия сульфоксида формулы (XIV) с соответствующими агентами с получением соединения общей формулы (ГСс); (iv) необязательно, превращение соединения формулы (XIV) в соединение формулы (ГС) с использованием подходящих агентов с получением соответствующей группы R1. Альтернативно, соединение формулы (ГСс) может быть превращено в соединение (ГС) с использованием соответствующих агентов; v) при желании, но необязательно, превращение соединений формулы (ГСс) или (ГС) в фармацевтически приемлемые соли. Реакции, описанные в способах, проиллюстрированных выше на схеме III, могут быть осуществлены нижеследующими методами. Метод Н. Гидразин формулы (XI) или его кислотно-аддитивные соли могут быть превращены в соединение формулы (XIII) посредством взаимодействия с соответствующим образом замещенными 1,3-дикетонами формулы (XII). При этом могут быть использованы такие реагенты, как ацетат натрия, но они не имеют решающего значения. Могут быть использованы растворители, такие как спирты, например, этанол, метанол, изопропанол и т.п., ТГФ, диоксан, толуол, ксилол, циклогексан, гептан, гексан и т.п. или их смесь. Температура может составлять в пределах от 20°С до температуры флег-мообразования растворителя, а предпочтительно от 60°С до температуры флегмообразования рас-творителя(ей). Инертная атмосфера может поддерживаться с использованием газов N2, He или аргона. Метод В. Пиразоловое соединение формулы (XIII) может быть превращено в сульфоксид формулы (XIV) посредством взаимодействия с окислителем, как описано выше в методе В схемы I. Метод С. Сульфоксидные соединения формулы (XIV) могут быть превращены в сульфоксиминовые соединения формулы (ГСс) посредством взаимодействия с подходящими иминирующими агентами, как описано выше в методе С схемы I. Метод D. Сульфоксимины формулы (ГСс) могут быть превращены в соединения формулы (IC) посредством взаимодействия с подходящими алкилирующими/ацилирующими агентами в присутствии основания, как описано выше в методе D схемы I. Метод Е. Соединения XIV могут быть непосредственно превращены в соединения формулы (IC) посредством взаимодействия с подходящими реагентами, такими как тозилазид и хлорамин Т, в растворителях, таких как этанол, метанол и т.п. с последующим подщелачиванием и получением групп R1=тозил. Альтернативно, в результате реакции взаимодействия с ариламинами в присутствии t-BuOCl получают N-арилсульфоксимины, как описано в методе Е схемы I. Схема IV Соединение общей формулы (ID), где все символы являются такими, как они были определены выше, может быть получено способом, проиллюстрированным ниже в схеме IV, который предусматривает: - 13 - 008303 Соединение формулы (XV) в вышепривиденной схеме IV может быть превращено в соединение общей формулы (ID), определенное выше, способом, предусматривающим: i) окисление соединения XV соответствующими окислителями с получением соединения общей формулы (XVI); (ii) проведение реакции взаимодействия сульфоксида формулы (XVI) с соответствующими агентами с получением соединения общей формулы (IDd); (iii) необязательно, превращение соединения формулы (IDd), полученного как описано в стадии (ii), в соединение формулы (ID) с использованием подходящих агентов и с получением соответствующей группы R1; (iv) необязательно, непосредственное превращение соединения формулы (XVI) в соединение формулы (ID) с использованием соответствующих реагентов; (v) при желании, но необязательно, превращения соединения формулы (IDd) или (ID) в фармацевтически приемлемые соли. Соединение общей формулы (ID) может быть получено способом, проиллюстрированным в схеме IV, который включает: Метод В. Лактоновое соединение формулы (XV) может быть превращено в сульфоксид формулы (XVI) посредством взаимодействия с окислителем, как описано выше в методе В схемы I. Метод С. Сульфоксидные соединения формулы (XVI) могут быть превращены в сульфоксиминовые соединения формулы (IDd) посредством взаимодействия с подходящими иминирующими агентами, как описано выше в методе С схемы I. Метод D. Сульфоксимины (IDd) могут быть превращены в соединения формулы (ID) посредством взаимодействия с подходящими алкилирующими/ацилирующими агентами в присутствии основания, как описано выше в методе D схемы I. Метод Е. Соединения XVI могут быть непосредственно превращены в соединения формулы (ID) посредством взаимодействия с подходящими реагентами, такими как тозилазид, хлорамин Т, в растворителях, таких как этанол, метанол и т.п., с последующим подщелачиванием и получением групп R1=тозил. Альтернативно, в результате реакции взаимодействия с ариламинами в присутствии t-BuOCl получают N-арилсульфоксимины, как описано в методе Е схемы I. Схема V Соединение общей формулы (IE), где все символы являются такими, как они были определены: выше, может быть получено способом, проиллюстрированным ниже в схеме V, который предусматривает: (IE) - 14 - 008303 i) проведение реакции взаимодействия соединения формулы (XVII) с соединением формулы (XVIII) с получением соединения формулы (XIX); (ii) окисление соединения формулы (XIX) подходящими окислителями с получением соединения общей формулы (XX); (iii) проведение реакции взаимодействия сульфоксида формулы (XX) с соответствующими агентами с получением соединения общей формулы (Ше); (iv) необязательно, превращение соединения формулы (Ше), полученного как описано в стадии (iii), в соединение формулы (IE) с использованием подходящих агентов и с получением соответствующей группы R1; (v) необязательно, непосредственное превращение соединения формулы (XX) в соединение формулы (IE) с использованием подходящих реагентов; (vi) при желании, но необязательно, превращение соединения формулы (Ше) или (IE) в фармацевтически приемлемые соли. Соединение общей формулы (IE) может быть получено способом, проиллюстрированным на схеме V, который включает: Метод I. Кето-соединение формулы (XVII) может быть превращено в соединение формулы (XIX) посредством взаимодействия с соединением формулы (XVIII). При этом, могут быть использованы такие реагенты, как ацетат аммония. Реакция может быть осуществлена с использованием растворителей, таких как пропионовая кислота, или без использования растворителя. Температура реакции может варьироваться в пределах от комнатной температуры до 150°С или температуры флегмообра-зования растворителя(ей). Метод В. Пиридиновое соединение формулы (XIX) может быть превращено в сульфоксид формулы (XX) посредством ззаимодействия с окислителем, как описано выше в методе В схемы I. Метод С. Сульфоксидные соединения формулы (XX) могут быть превращены в сульфоксиминовые соединения формулы (Ше) посредством взаимодействия с подходящими иминирующими агентами, как описано выше в методе С схемы I. Метод D. Сульфоксимины (IEe) могут быть превращены в соединения формулы (IE) посредством взаимодействия с подходящими алкилирующими/ацилирующими агентами в присутствии основания, как описано выше в методе D схемы I. Метод Е. Соединения XX могут быть непосредственно превращены в соединения формулы (IE) посредством взаимодействия с подходящими реагентами, такими как тозилазид, хлорамин Т, в растворителях, таких как этанол, метанол и т.п., с последующим подщелачиванием и получением групп R1=тозил. Альтернативно, врезультате реакции взаимодействия с ариламинами в присутствии t-BuOCl получают N-арилсульфоксимины, как описано в методе Е схемы I. Схема VI Соединение общей формулы (IF), где все символы являются такими, как они были определены выше, может быть получено способом, проиллюстрированным ниже в схеме VI, который предусматривает: - 15 - 008303 i) проведение реакции взаимодействия гидразина общей формулы (XXII) с 1,3-дикетоном общей формулы (XXI) с получением соединения общей формулы (XXIII); (ii) окисление соединения формулы (XXIII) подходящим окислителем с получением соединения общей формулы (XXIV); (iii) проведение реакции взаимодействия сульфоксида формулы (XXIV) с соответствующими агентами с получением соединения общей формулы (IFf); (iv) необязательно, превращение соединения формулы (XXIV) в соединение формулы (IF) с использованием подходящих агентов и с получением соответствующей группы R1. Альтернативно, соединение формулы (IFf) может быть превращено в соединение (IF) с использованием соответствующих агентов; v) при желании, но необязательно, превращение соединений формулы (IFf) или (IF) в фармацевтически приемлемые соли. Реакции, описанные выше в способах, проиллюстрированных на вышеуказанной схеме VI, могут быть осуществлены методами, описанными ниже. Метод Н. Гидразин формулы (XXII) или его кислотно-аддитивные соли могут быть превращены в соединение формулы (XXIII) посредством взаимодействия с соответствующим образом замещенными 1,3-дикетонами формулы (XXI). При этом могут быть использованы такие реагенты, как ацетат натрия, но они не имеют решающего значения. Могут быть также использованы растворители, такие как спирты, например, этанол, метанол, изопропанол и т.п., ТГФ, диоксан, толуол, ксилол, цикло-гексан, гептан, гексан и т.п. или их смесь. Температура может составлять в пределах от 20°С до температуры флегмообразования растворителя, а предпочтительно, от 60°С до температуры флег-мообразования растворителя(ей). Инертная атмосфера может поддерживаться с использованием газов N2, Не или аргона. Метод В. Пиразоловое соединение формулы (XXIII) может быть превращено в сульфоксид формулы (XXIV) посредством взаимодействия с окислителем, как описано выше в методе В схемы I. Метод С. Сульфоксидные соединения формулы (XXIV) могут быть превращены в сульфоксиминовые соединения формулы (IFf) посредством взаимодействия с подходящими иминирующими агентами, как описано выше в методе С схемы I. Метод D. Сульфоксимины (IFf) могут быть превращены в соединения формулы (IF) посредством взаимодействия с подходящими алкилирующими/ацилирующими агентами в присутствии основания, как описано выше в методе D схемы I. Метод Е. Соединения XXIV могут быть непосредственно превращены в соединения формулы (IF) посредством взаимодействия с подходящими реагентами, такими как тозилазид, хлорамин Т, в растворителях, таких как этанол, метанол и т. п., с последующим подщелачиванием и получением групп R1=тозил. Альтернативно, в результате реакции взаимодействия с ариламинами в присутствии t-BuOCl получают N-арилсульфоксимины, как описано в методе Е схемы I. Фармацевтически приемлемыми солями, составляющими часть настоящего изобретения, могут быть, но не ограничиваются ими, соли, имеющие группу карбоновой кислоты, если она присутствует в данной молекуле, такие как соли щелочных металлов, например, соли Li, Na и K; соли щелоч-но-земельных металлов, например, соли Са и Mg; соли органических оснований, таких как лизин, аргинин, гуанидин и их производные, которые могут быть, но необязательно, замещенными, диэта-ноламин, холин, трометамин и т. п.; соли аммония или замещенного аммония и соли алюминия. Могут быть использованы кислотно-аддитивные соли, которыми являются, но не ограничиваются ими, сульфаты, бисульфаты, нитраты, фосфаты, перхлораты, бораты, галогенводороды, ацетаты, тартра-ты, малеаты, фумараты, малаты, цитраты, сукцинаты, пальмоаты, метансульфонаты, бензоаты, са-лицилаты, гидроксинафтоаты, бензолсульфонаты, аскорбаты, глицерофосфаты, кетоглутараты и т.п. Фармацевтически приемлемые сольваты могут представлять собой гидраты, либо они могут содержать другие растворители кристаллизации, такие как спирты. Следует отметить, что в любой из вышеупомянутых реакций, любая реакционноспособная группа в молекуле субстрата может быть защищена в соответствии со стандартными химическими методами. Подходящими защитными группами в любой из вышеупомянутых реакций являются защитные группы, известные специалистам. Для образования и удаления таких защитных групп могут быть использованы стандартные методы, подходящие для данной защищаемой молекулы. См. T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, John Wiley & Sons, Inc., 1999, 3rd Ed., 201-245, и цитируемые там работы. Кислотно-аддитивные соли, независимо от их применения, могут быть получены путем обработки кислотами, такими как винная кислота, миндальная кислота, фумаровая кислота, яблочная - 16 - 008303 кислота, молочная кислота, малеиновая кислота, салициловая кислота, лимонная кислота, аскорбиновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, гидроксинафтойная кислота, метансульфоновая кислота, уксусная кислота, бензойная кислота, янтарная кислота, пальмитиновая кислота, хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота и т.п., в растворителях, таких как вода, спирты, эфиры, этилацетат, диоксан, ТГФ, аце-тонитрил, ДМФ или низший алкилкетон, такой как ацетон или их смеси. В другом своем аспекте, настоящее изобретение относится к фармацевтической композиции, содержащей по крайней мере одно из соединений общей формулы (I), его производные, аналоги, таутомерные формы, фармацевтически приемлемые соли и фармацевтически приемлемые сольваты, используемые в качестве активного ингредиента вместе с фармацевтически приемлемыми носителями, разбавителями и т. п. Фармацевтические композиции, содержащие соединение настоящего изобретения, могут быть получены стандартными методами, например, как описано в руководстве Remington: the Science and Practice of Pharmacy, 19th Ed., 1995. Такие композиции могут быть приготовлены в стандартных лекарственных формах, таких как капсулы, таблетки, порошки, растворы, суспензии, сиропы, аэрозоли или препараты для местного применения. Они могут содержать подходящие твердые или жидкие носители, либо они могут быть включены в подходящие стерильные среды с образованием растворов или суспензий для инъекций. Такие композиции могут содержать 0,5-20%, а предпочтительно 0,5-10 мас.% активного соединения, а остальную часть составляют фармацевтически приемлемые носители, наполнители, разбавители, растворители и т.п. Благодаря своей смешанной активности по отношению к СOХ-1/СOХ-2, соединения формулы (I) являются хорошими противовоспалительными средствами, а также селективными ингибиторами СОХ-2, обладающими меньшими побочными эффектами, чем НСПВС. Настоящее изобретение относится к соединению формулы (I), которое может быть использовано для лечения человека или животного, а в частности, для устранения болей, снижения температуры или лечения воспаления, для ингибирования индуцированного простаноидами сокращения гладкой мышцы или для предупреждения рака толстой и прямой кишки. Другой целью настоящего изобретения является использование соединения формулы (I) в целях изготовления лекарственного средства для устранения болей, снижения температуры или лечения воспаления, для ингибирования индуцированного простаноидами сокращения гладкой мышцы или для предупреждения рака толстой и прямой кишки. Соединения настоящего изобретения могут быть использованы для лечения воспаления и ассоциированных с воспалениями заболеваний путем введения индивидууму терапевтического количества соединения формулы (I) или его активной соли. Воспаление ассоциируется с рядом патологических состояний. Перечень таких патологических состояний, которые могут быть подвергнуты лечению ингибиторами циклооксигеназы и ингибиторами СОХ-2, приводится, в частности, в патентах США 5604253 и 5908852, а также в WO 9638442, WO 9603392 и WO 9714691. Такими состояниями являются боли, повышенная температура и воспаления при различных состояниях, включая ревматическую лихорадку, симптомы, ассоциированные с гриппом или другими вирусными инфекциями, насморк, боли в нижней части спины и шеи, дисменорею, головную боль, зубную боль, растяжения и повреждения тканей, мышечные спазмы при менструации и преждевременные роды. Такие соединения могут быть использованы для лечения артрита, включая, но не ограничиваясь ими, ревматоидный артрит, спондилоартропатии, подагрический артрит, остеоартрит, системную красную волчанку и ювенильный артрит. Эти соединения могут быть также использованы для лечения кожных воспалительных заболеваний, таких как псориаз, экзема, ожоги и дерматит. Соединения формулы (I) могут быть также использованы в качестве альтернативы стандартным НСПВС, а особенно, в том случае, когда такие нестероидные противовоспалительные лекарственные средства могут иметь противопоказания, например, при лечении пациентов с расстройствами желудочно-кишечного тракта, включая пептические яззы, гастриты, региональный энтерит, язвенный колит, дивертикулы, болезнь Крона, синдром воспаления кишечника и синдром раздраженного кишечника, язвенный колит, кровотечения в области желудочно-кишечного тракта и нарушения свертывания крови, заболевания почек (например, нарушение почечной функции); при лечении пациентов перед хирургической операцией или пациентов, принимающих антикоагулянты, и при лечении пациентов, чувствительных к НСПВС. Кроме того, соединения настоящего изобретения могут ингибировать опухолевые (неопластические) трансформации клеток и метастатический рост опухолей, а поэтому они могут быть использованы для лечения рака. В частности, настоящее изобретение относится к способу лечения неопла-зии опухолевых заболеваний, вызываемых простагландином, путем введения индивидууму терапевтического количества соединения (I). Так, например, соединения настоящего изобретения могут быть использованы для предупреждения и лечения рака, такого как рак толстой и прямой кишки, рак губы, ротовой полости, пищевода, молочной железы, легких, предстательной железы, мочевого - 17 - 008303 пузыря, поджелудочной железы, шейки матки и кожи, а также рак тонкого кишечника, рак желудка, рак яичника, рак шейки матки и т.п. Использование ингибиторов СОХ-2 для лечения вышеупомянутых заболеваний обсуждается в патенте США 5972986, в WO 0076983 и 9714691. Такие соединения могут быть также использованы для лечения воспалений, ассоциированных с такими заболеваниями, как сосудистые заболевания, головные боли при мигрени, нодозный периартериит, тироидит, апластическая анемия, болезнь Ходжкина, склеродома, ревматическая лихорадка, диабет типа I, нейромышечные заболевания суставов, включая тяжелую миастению, заболевание белого вещества, включая рассеянный склероз, саркоидоз, нефротический синдром, синдром Бехчета, полимиозит, гингивит, нефрит, гиперчувствительность, опухание тканей после повреждения, ишемия миокарда и т.п. Указанные соединения могут быть также использованы для лечения глазных болезней, таких как ретинит, ретинопатия, увеит, глазные фотофобии и острое поражение глазных тканей. Эти соединения могут быть также использованы для лечения воспаления легких, такого как воспаление, ассоциированное с вирусными инфекциями и кистозным фиброзом. Соединения настоящего изобретения могут быть использованы для лечения некоторых расстройств центральной нервной системы, таких как кортикальная деменция, включая болезнь Альц-геймера (Bratisl Lek Listy 2001; 102 (3):123-132) и поражение центральной нервной системы, возникающее в результате инсульта, ишемии и травм. Эти соединения могут быть также использованы для ослабления невропатических болей. Соединения настоящего изобретения могут быть использованы в качестве противовоспалительных средств, например, для лечения артрита, при этом, они обнаруживают значительно меньшие побочные эффекты. Эти соединения должны быть эффективными при лечении аллергического ринита, респираторного дистресс-синдрома, синдрома эндотокси-нового шока и атеросклероза. Соединения настоящего изобретения могут быть также использованы для лечения расстройств, опосредованных ангиогенезом. Опосредованные ангиогенезом расстройства могут быть подвергнуты лечению ингибиторами циклооксигеназы, как описано в патенте США 6025353 и в WO 0076983. Согласно этим патентам такими заболеваниями являются, например, метастазы, отторжение трансплантата роговицы, неоваскуляризация глаза, диабетическая ретинопатия, ретроленталь-ная фиброплазия, глаукома с неоваскуляризацией, язва желудка, гемангиомы у детей, ангиофиброма носоглотки, бессосудистый некроз кости и эндометриоз. Указанные соединение, помимо их использования для лечения человека, могут быть также использованы в ветеринарии для лечения домашних животных, экзотических животных и сельскохозяйственных животных, включая млекопитающих, грызунов и т.п. Более предпочтительными животными являются лошади, собаки и кошки. Соединения настоящего изобретения могут быть также использованы в комбинированной терапии, частично или полностью, вместо других стандартных противовоспалительных средств, таких как стероиды, НСПВС, ингибиторы 5-липоксигеназы, антагонисты рецептора LTB4 и ингибиторы LТА4-гидролазы. Они могут быть также использованы в комбинированной терапии вместе с опиои-дами и другими анальгетиками, включая наркотические анальгетики, антагонисты Mu-рецептора, антагонисты каппа-рецептора, ненаркотические анальгетики, ингибиторы поглощения моноамина, аденозин-регулирующие агенты, производные каннабиноидов, антагонисты вещества Р, антагонисты рецептора нейрокинина-1, блокаторы натриевых каналов и т.п. Настоящее изобретение также относится к фармацевтической композиции для лечения расстройства или состояния, которое может быть осуществлено путем ингибирования СОХ у млекопитающего, а предпочтительно, у человека, кошек, крупного рогатого скота или собак, где указанная фармацевтическая композиция содержит СОХ-ингибирующее эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли, и фармацевтически приемлемый носитель. Настоящее изобретение также относится к способу лечения расстройства или состояния, которое может быть осуществлено путем ингибирования СОХ у млекопитающего, а предпочтительно, у человека, кошек, собак и крупного рогатого скота, где указанный способ предусматривает введение млекопитающему, нуждающемуся в таком лечении СОХ-ингибирующего эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли. Настоящее изобретение также относится к способу лечения или к фармацевтической композиции для лечения воспаления и аналогичных заболеваний, где указанный способ предусматривает введение млекопитающему, включая человека, кошек, крупный рогатый скот или собак, соединения формулы (I) настоящего изобретения или его соли. Указанное ингибирующее соединение используется в комбинации с одним или несколькими другими терапевтически активными агентами, описанными ниже. A) При состояниях, где воспаление сустава ассоциируется с бактериальной, грибковой, прото-зойной и/или вирусной инфекцией, указанное ингибирующее соединение вводят в комбинации с одним или несколькими антибиотиками, противогрибковыми, антипротозойными и/или противовирусными терапевтическими агентами. (i) Если требуется многократное лечение для устранения боли и воспаления, то данное соеди - 18 - 008303 нение должно быть введено в комбинации с ингибиторами или с другими медиаторами воспаления, включающей члены следующих групп соединений: НСПВС, антагонисты Щ-рецептора, антагонисты рецепторов кинина-ЕЦ и В2; ингибиторы простангландинов, выбранные из группы, состоящей из антагонистов PGD-, PGF-, PGI2- и PGE-рецепторов; ингибиторы тромбоксана А2 (ТХА2); ингибиторы 5-, 12- и 15-липоксигеназы; ингибиторы лейкотриенов LTC4-, LTD4/LTE4- и LTB4; антиагонисты PAF-рецептора; противовоспалительные глюкокортикоиды; средства против подагры, включая колхицин; ингибиторы ксантин-оксидазы, включая аллопуринол; и средства, способствующие выведению мочевой кислоты, выбранные из пробенецида, сульфинпиразона и бензбромарона. B) При лечении млекопитающих в старом возрасте с гериатрическими расстройствами, указанное соединение вводят в комбинации со средствами, выбранными из группы, состоящей из когнитивных терапевтических средств, антигипертензивных средств и других сердечно-сосудистых средств, выбранных из диуретиков, вазодилататоров, антагонистов в-адренергических рецепторов, АСЕ-ингибиторов, взятых отдельно или в комбинации с ингибиторами нейтральной эндопептидазы, предназначенных для предупреждения последствий атеросклероза, гипертензии, ишемии миокарда, стенокардии, застойной сердечной недостаточности и инфаркта миокарда. Для лечения вышеупомянутых заболеваний, соединения формулы (I) могут быть введены, например, перорально, местно или парентерально в виде разовых лекарственных форм, содержащих стандартные нетоксические фармацевтически приемлемые носители, адъюванты и наполнители. Соединения настоящего изобретения могут быть использованы для лечения воспалительных заболеваний, вызываемых цитокинами, а в частности, TNF-a, либо путем ингибирования продуцирования TNF-a-конвертирующего фермента или ингибирования действия указанного фермента (ТАСЕ), либо путем ингибирования самого TNF-a. В общих чертах доза для введения человеку, предпочтительно, составляет от 0,01 до 100 мг на 1 кг массы тела в день, хотя эта доза может варьировать в зависимости от веса, пола и состояния индивидуума, подвергаемого лечению, тяжести заболевания, подвергаемого лечению; и конкретного способа введения. Однако предпочтительной дозой является доза, составляющая от 0,1 до 10 мг на 1 кг массы тела в день, которая вводится в виде разовых или дробных доз. Для млекопитающих, не являющихся человеком, например, собак, кошек, лошадей или крупного рогатого скота, доза должна составлять примерно от 0,01 до 20,0 мг/кг/день, а более предпочтительно примерно от 0,5 до 8,0 мг/кг/день. Соединения настоящего изобретения могут быть введены отдельно или в комбинации с фармацевтически приемлемыми носителями или разбавителями любыми способами, указанными ранее, в виде разовых или дробных доз. Более конкретно, новые соединения, описанные в настоящем изобретении, могут быть введены в виде различных лекарственных форм широкого ряда, то есть они могут быть объединены с различными фармацевтически приемлемыми инертными носителями и изготовлены в форме таблеток, капсул, лекарственных лепешек, пастилок, леденцов, порошков, спреев, кремов, жидких мазей, суппозиториев, желе, гелей, паст, лосьонов, твердых мазей, водных суспензий, растворов для инъекций, эликсиров, сиропов и т. п. Такими носителями могут быть твердые разбавители или наполнители, стерильные водные среды и различные нетоксические органические растворители и т.п. Кроме того, для перорального введения, указанные фармацевтические композиции могут быть соответствующим образом подслащены и/или ароматизированы. В основном, терапевтически эффективные соединения, описанные в настоящем изобретении, присутствуют в указанных композициях в концентрации, составляющей от 5 до 60 мас.%, а предпочтительно от 10 до 50 мас.%. Для перорального введения, таблетки могут быть изготовлены с использованием различных наполнителей, таких как микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, дика-лийфосфат и глицин вместе с различными дезинтеграторами, такими как крахмал, а более предпочтительно, кукурузный крахмал, картофельный крахмал или крахмал тапиоки, альгиновая кислота, карбонат натрия и некоторые сложные силикаты; вместе со связующими агентами, такими как по-ливинилпирролидон, сахароза, желатин и аравийская камедь; с увлажнителями, такими как, например, глицерин; агентами, замедляющими растворение, такими как, например, парафин; с ускорителями абсорбции, такими как, например, четвертичные аммониевые соединения; со смачивающими агентами, такими как цетиловый спирт и моностеарат глицерина; с абсорбентами, такими как каолин и бентонитовая глина. Кроме того, для изготовления таблеток, в качестве смазывающих агентов часто добавляют стеарат магния, лаурилсульфат натрия, тальк, стеарат кальция, твердые полиэти-ленгликоли и их смеси. В случае использования капсул, таблеток и драже, указанная лекарственная форма может также содержать буферирующие агенты. Твердые композиции аналогичного типа могут быть также использованы в качестве наполнителей и носителей в мягких и твердых желатиновых капсулах; при этом, предпочтительными материалами являются лактоза, молочный сахар или высокомолекулярные полиэтиленгликоли. Активные соединения могут быть также приготовлены в форме микрокапсул с использовани - 19 - 008303 ем одного или нескольких из вышеуказанных наполнителей. Твердые лекарственные формы, а именно таблетки, драже, капсулы, пилюли и гранулы могут иметь покрытия и оболочки, такие как энтеросолюбильные покрытия, покрытия, регулирующие высвобождение лекарственного средства, и другие покрытия, хорошо известные специалистам-фармацевтам. В таких твердых лекарственных формах, активное соединение может быть смешано по крайней мере с одним инертным разбавителем, таким как сахароза, лактоза и крахмал. Они могут также содержать добавки, например, смазывающие агенты для таблеток и другие вещества, например, стеарат магния и микрокристаллическую целлюлозу. В случае капсул, таблеток и драже, указанная композиция может также содержать бу-ферирующие агенты. Эти композиции могут быть приготовлены так, чтобы они высвобождали ак-тивный(е) ингредиент(ы) только или преимущественно в определенной области кишечного тракта, необязательно с пролонгированным действием. Это может быть достигнуто с использованием агентов для инкапсулирования, таких как, например, полимерные вещества и воски. Жидкими лекарственными формами для перорального введения являются фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Для такого перо-рального введения может оказаться желательным объединение активного ингредиента с различными подсластителями или ароматизаторами, а также, при желании, с подкрашивающими веществами или красителями. Разбавители могут быть выбраны из воды, этанола, пропиленгликоля, изопропи-лового спирта, этилкарбоната, этилацетата, бензилового спирта, бензилбензоата, 1,3-бутилен-гликоля, диметилформамида, масел, например, таких как масло из семян хлопчатника, арахисовое масло, кукурузное масло, масло из проростков, оливковое масло, касторовое масло, кунжутное масло и т. п., глицерина, тетрагидрофурфурилового спирта, полиэтиленгликолей и эфиров жирных кислот, таких как сорбитан, и их различных комбинаций. Для введения млекопитающему, не являющемуся человеком, композиция активного вещества может быть соответствующим образом модифицирована. Для парентерального введения, растворы данного соединения получают либо в кунжутном, либо в арахисовом масле или в водном полиэтиленгликоле. Водные растворы, если это необходимо, должны быть соответствующим образом забуферены, а разбавителю сначала следует придать изо-тоничность. Водные растворы являются подходящими для внутривенного введения, а масляные растворы являются подходящими для внутрисуставного, внутримышечного и подкожного введения. Вышеупомянутые композиции могут быть легко получены в стерильных условиях в соответствии со стандартными методами, хорошо известными специалистам-фармацевтам. Соединения формулы (I) могут быть также введены в виде суппозиториев для ректального или вагинального введения активного ингредиента. Эти композиции могут быть получены путем смешивания активного ингредиента с подходящим нераздражающим наполнителем, который является твердым при комнатной температуре (например, при 10-32°С), но становится жидким при температуре прямой кишки и начинает расплавляться в прямой кишке или во влагалище с высвобождением активного ингредиента. Такими веществами являются полиэтиленгликоли, масло какао, основы для суппозиториев и воск. Для буккального введения, данная композиция может быть изготовлена в виде таблеток или пастилок стандартным методом. Лекарственные формы для чрескожного и местного введения могут представлять собой мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи и ингаляторы. Пластыри для чрескожного введения могут быть изготовлены в соответствии со стандартной технологией доставки лекарственного средства и нанесены на кожу млекопитающего, подвергаемого лечению, а предпочтительно, человека или собаки. Если это необходимо, то лекарственные средства могут быть введены пациенту также в виде офтальмических растворов, ушных капель, глазных мазей и порошков. Мази, пасты, кремы и гели, помимо активного ингредиента, могут также содержать наполнители, такие как животные и растительные жиры, масла, воски, парафины, крахмал, трагакантовая камедь, производные целлюлозы, полиэтиленгликоли, силиконы, бентониты, кремниевая кислота, тальк, оксид цинка или их смеси. Порошки и спреи, помимо активного вещества, могут содержать наполнители, такие как лактоза, тальк, кремниевая кислота, гидроксид алюминия, силикаты кальция и полиамидный порошок или их смеси. Спреи, кроме того, могут содержать пропелленты, такие как хлорфторуглеводороды. Соединения настоящего изобретения были протестированы на их биологическую активность в тесте, где в подушечку лапы самцов и самок крыс Wistar вводили карагенан в соответствии со стандартным протоколом, описанным в литературе (Winter et al., Proc. Soc., Exp, Biol. Med., 111, 544 (1962); Otterness & Bliven, Laboratory Models for Testing NSAIDS, in Non-steroidal Anti-inflammatory Drugs (J.Lombardino, ed. 1985)). Описание этого протокола приводится ниже. Крысы Wistar были взяты из экспериментальной лаборатории Научно-исследовательского центра Зидус (Experimental Animal Facility of Zydus Research Centre). Животных содержали в камерах с регулируемыми условиями и давали пищу и воду ad libitum. Все протоколы экспериментов были одобрены Комитетом по этике экспериментов над животными (Institutional Animal Ethics - 20 - 008303 Committee). Затем животных распределяли по различным группам, каждая из которых содержала по 5-6 животных. После выдерживания животных в условиях голодания, животным контрольной группы вводили через желудочный зонд только носитель, а животным других групп вводили различные дозы тестируемого(ых) вещества(веществ). Каждая крыса получала один и тот же объем композиции, т.е. 2 мл/кг массы тела. Через один час после введения носителя или тестируемого вещества, всем животным под подушечку лапы инъецировали карагенан (1% мас./об. в физиологическом растворе). Через 0, 1, 3 и 5 ч после введения карагенана измеряли объем лапы. Противовоспалительную активность, выражаемую как % ингибирования опухания лапы, вычисляли путем измерения изменения объема лапы через различные интервалы времени после инъекции карагенана по отношению к соответствующим величинам, полученным на 0 ч, с использованием формулы: (PVC - PVT) % ингибирования =--X 100 PVC где PVC = среднее изменение объема лапы у контрольных животных, PVT = среднее изменение объема лапы у обработанных животных. Соединения настоящего изобретения обнаруживали 10-95% ингибирование отека лапы крыс при дозе 30 мг/кг. Соединения настоящего изобретения обладают свойствами анальгетиков и являются эффективными для устранения невропатической боли. Соединения настоящего изобретения ингибируют коферменты СОХ-1 и СОХ-2 в различной степени, как было обнаружено с помощью анализа цельной крови человека (С. Brideau, S. Kargman, S.Liu; Inflammation Research, 45, 68-74 (1996)). Ингибирующие активности репрезентативных соединений настоящего изобретения приводятся в следующей таблице: Соединение № Доза (мг/кг) % ингибирования отека лап 1 час 3 часа 179 171 154 153 158 187 112 Целекоксиб Настоящее изобретение подробно описано на нижеследующих примерах, которые приводятся лишь в иллюстративных целях и не должны рассматриваться как ограничение объема изобретения. Спектральные данные 1Н-ЯМР, представленные в таблицах (см. ниже), были зарегистрированы с использованием спектрометра 300 МГц (Brucker AVANCE-300) и представлены в 5-величинах. Если это не оговорено особо, то в качестве растворителя для ЯМР использовали CDCl3, а в качестве внутреннего стандарта использовали тетраметилсилан. Препаративный пример 1. 5-(3-Фтор-4-метоксифенил)-1-(4-метилсульфанилфенил)-3-трифтор-метил-1Н-пиразол (соединение № 14) Стадия 1. Получение ^трет-бутоксикарбонил-^(4-метилсульфанил)фенилгидразина. Смесь 4-метилсульфанилиодбензола (10 г), трет-бутилкарбазата (5,2 г), карбоната цезия (18,2 - 21 - 008303 г), иодида меди (80 мг) и 1,10-фенантролина (576 мг) в ДМФ (30 мл) перемешивали при 90°С в течение 18 ч в атмосфере азота. Реакционную смесь хроматографировали на силикагеле с использованием в качестве элюента 5% этилацетата в петролейном эфире и получали 6,2 г продукта в виде густой жидкости. Стадия 2. Получение 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфанилфенил)-3-трифторме-тил-1Н-пиразола. Смесь 1-(3-фтор-4-метоксифенил)-4,4,4-трифторбутан-1,3-диона (1,0 г) и N-трет-бутокси-карбонил-М-(4-метилтио)фенилгидразина (0,9 г) (полученного как описано выше в стадии 1) в смеси этанола-НС1 (25 мл, 12%) нагревали при температуре флегмообразования (с обратным холодильником) в течение 24 ч. Растворитель выпаривали при пониженном давлении. К остатку добавляли воду (50 мл) и экстрагировали диэтиловым эфиром (3х50 мл). Органический экстракт промывали водой (2х 50 мл), насыщенным раствором соли (50 мл), сушили над сульфатом натрия и выпаривали при пониженном давлении. Полученный продукт хроматографировали на силикагеле с использованием в качестве элюента 2% этилацетата в петролейном эфире и получали 820 мг продукта в виде густой жидкости. Аналогичным образом, в соответствии с вышеописанной методикой были получены нижеследующие соединения, представленные в табл. 1. Таблица 1 Мол.масса Выход(%) тт П тт П 1/__- - _ -____~> ro т-"______/ О- \ _-1 л гзы.х.ид \ -о 1 -ot ХН: 2,49 (ЗН, с), 6,7 (1Н, с) , 7,0 (2Н, т, J=8,7 Гц), 7,2 (6Н, м). CF3 Мол.масса=368,5 Выход (%) =62 ХН: 2,5 (ЗН, с), 6,7 (1Н, с), 7,15 (2Н, д, J=8,5 Гц), 7,2 (4Н, м), 7,3 (2Н, д, J=8,5 Гц). CF3 H3C Мол.масса=34 8 Выход(%)=50 XH: 2,3 (ЗН, с), 2,48 (ЗН, с), 6,7 (1Н, с), 7,1 (4Н, м) , 7,13 (ЗН, м), 7,3 (1Н, м). CF3 H3co Мол.масса=364 Выход(%)=67 ХН: 2,4 (ЗН, с), 3,8 (ЗН, с), 6,67 (1Н, с), 6,8 (2Н, д, J=8,8 Гц), 7,1 (2Н, д, J=8,8 Гц), 7,2 (4Н, м). CF3 л-РЮ Мол.масса=392 Выход(%)=4 6 ХН: 1,0 (ЗН, т, J=5,7 Гц), 1,8 (2Н, м) , 2,4 (ЗН, с), 3,9 (2H, т, J=6,5 Гц), 6,6 (1Н, с), 6,8 (2Н, д, J=6,7 Гц), 7,1 (2H, д, J=6,6 Гц), 7,2 (4Н, д, J=2,3 Гц). - 22 - 008303 CF3 Мол.масса=378 Выход(%)=82 ХН: 1,4 (ЗН, т, J=6,9 Гц), 2,4 (ЗН, с), 4,0 (2Н, кв, J=6,9 Гц), 6,6 (1Н, с), 6,8 (2Н, д, J=8,7 Гц), 7,1 (2Н, д, J=8,7 Гц), 7,2 (4Н, м). CF3 Мол,масса=392 Выход(%)=69 ХН: 1,3 (6Н, д, J=6,0 Гц), 2,48 (ЗН, с), 4,5 (1Н, м) , 6,6 (1Н, с), 6,8 (2Н, д, J=6,6 Гц), 7,1 (2Н, д, J=8,7 Гц), 7,2 (4Н, м) . и il Т_1 I'ivjJl . ivicn_^a - 0 и и , и п. " " / о_ \ - с л ХН: 2,5 (ЗН, с), 6,7 (1Н, с) , 7,1 (2Н, м) , 7,2 (ЗН, м) , 7,3 (2Н, дд, J=6,8 и 2,2 Гц). CF3 'XT' Мол.масса=370 Выход(%)=88 1П: 2,5 (ЗН, с), 6,7 (1Н, с), 6,9-7,25 (7Н, комплекс). CF3 F ' Мол.масса=366 Выход(%)=53 XH: 2,2 (ЗН, с), 2,4 (ЗН, с), 6,7 (1Н, с), 6,9 (2Н, д, J=7,4 Гц), 7,1 (1Н, д, J=7,2 Гц), 7,2 (4Н, м). CF3 "XX H3co Мол.масса=3 7 8 Выход(%)=58 ХН: 1,57 (ЗН, с), 2,49 (ЗН, с), 3,9 (ЗН, с), 6,7 (1Н, с), 6,8 (1Н, д, J=8,7 Гц), 6,9 (1Н, дд, J=2,l и 8,7 Гц), 7,2 (4Н, м), 7,3 (1Н, д, J=2,l Гц). CF3 H3CO Мол.масса=398,5 Выход(%)=57 ХН: 2,49 (ЗН, с), 3,9 (ЗН, с), 6,7 (1Н, с), 6,8 (1Н, д, J=8,7 Гц), 6,9-7,0 (1Н, дд, J-2,4 и 8,7 Гц), 7,2 (4Н, м), 7,3 (1Н, д, J=2,4 Гц). - 23 - 008303 CF3 H3CO Мол.масса=443 Выход(%)=55 ХН: 2,49 (ЗН, с), 3,9 (ЗН, с), 6,7 (1H, с), 6,8 (1H, д, J=7,8 Гц), 7,0 (1Н, дд, J=2,l и 8,5 Гц), 7,2 (4Н, м), 7,5 (1Н, д, J=2,6 Гц). CF3 HjCO Мол.масса=382 Выход(%)=56,5 ХН: 2,49 (ЗН, с), 3,9 (ЗН, с), 6,7 (1Н, с), 6,8-6,9 (ЗН, м), 7,2 (4Н, м). CF3 H3C Мол.масса=37 8 Выход(%)=50,3 АН: 2,2 (ЗН, с), 2,48 (ЗН, с), 3,6 (ЗН, с), 6,6 (1Н, с), 6,7 (2Н, м), 7,0 (1Н, д, J=7,5 Гц), 7,2 (4Н, м). CF3 Мол.масса=382 Выход(%)=74 ХН: 2,8 (ЗН, с), 3,8 (ЗН, с), 6,7 (1Н, с), 6,8 (2Н, дд, J=8,8 и 2,14 Гц), 6,9 (2Н, дд, J=10,4 и 2,01 Гц), 7,15 (2Н, дд, J=8,85 и 2,1 Гц), 1,4 (1Н, т, J=8,0 Гц). CF3 HjCO Мол.масса=382 Выход(%)=66 *Н: 2,4 (ЗН, с), 3,8 (ЗН, с), 6,67 (1Н, с), 6,8 (2Н, д, J=8,8 Гц), 7,1 (2Н, м), 7,17 (ЗН, м). CF3 Мол,масса=334 Выход(%)=59 2H: 2,48 (ЗН, с), 6,7 (1Н, с), 7,23 (4Н, м), 7,3 (5Н, м) . CH3 HjCO Мол.масса=310 Выход(%)=42,6 ХН: 2,23 (ЗН, с), 2,46 (ЗН, с), 3,74 (ЗН, с), 6,3 (1Н, с), 6,9 (2Н, д, J=8,8 Гц), 7,1 (4Н, м) , 7,25 (2Н, д, J=8,67 Гц). - 24 - 008303 CF3 Мол.масса=37 9 Выход(%)=77 ХН: 2,5 (ЗН, с), 6,8 (1Н, с), 7,2 (4Н, м) , 7,4 (2Н, д, J=8,9 Гц), 8,2 (2Н, д, J=8,9 Гц). CF3 Мол.масса=364 Выход(%)=71 1Н: 2,48 (ЗН, с), 3,7 (ЗН, с), 6,7-6,8 (ЗН, м) , 6,9 (1Н, м) , 7,3 (5Н, м). CF3 HjCO J Мол.масса=400 Выход(%)=73, 6 ХН: 2,5 (ЗН, с), 4,0 (ЗН, с), 6,7 (1Н, с), 6,79 (2Н, д, J=8,6 Гц), 7,24 (4Н, м). CF3 HjCO Мол.масса=380 Выход(%)=98,5 ХН: 2,5 (ЗН, с), 3,9 (ЗН, с), 5,7 (1Н, с, -ОН), 6,4-6,8 (4Н, м), 7,1-7,2 (4Н, м). COOH НзСО Мол.масса=340 Выход(%)=90 ХН: 2,49 (ЗН, с), 3,82 (ЗН, с), 6,8 (2Н, д, J=8,76 Гц), 7,0 (1Н, с), 7,1 (2Н, д, J=8,"/6 Гц), 7,26 (4Н, м) . сн2он HjCO Мол.масса=32 6 Выход(%)=85, 5 ХН: 2,0 (1Н, т, ОН), 2,48 (ЗН, с), 3,8 (ЗН, с), 4,8 (2Н, м), 6,4 (1Н, с), 6,8 (2Н, дд, J=8,8 и 3,5 Гц), 7,1 (2Н, д, J=8,7 Гц), 7,14-7,3 (4Н, м). CF3 Мол.масса=з94 Выход(%)=53 ХН: 2,48 (ЗН, с), 3,98 (2Н, м) , 4,0 (2Н, м) , 6,68 (1 Н, с), 6,88 (2Н, д, J=8,85 Гц), 7,1 (2Н, д , J=8, 9 Гц), 7,2 (4Н, м) . - 25 - 008303 CF3 Мол.масса=335 Выход(%)=25,9 ХН: 2,55 (ЗН, с), 7,18 (1Н, с), 1,3 (2Н, дд, J=6,7 и 2,1 Гц), 7,4 (2Н, д, J=8,6 Гц), 7,7 <2Н, дд, J=4,5 и 1,5 Гц), 8,7 (2Н, дд, J=4,6 и 1,5 Гц). CF3 Мол.масса=335 Выход(%)=61, 3 ХН: 2,54 (ЗН, с), 6,8 (1Н, с), 7,2 (4Н, м) , 7,4 (1Н, м) , 8,2 (1Н, м), 8,5 (1Н, д, J=2,0 Гц), 9,0 (1Н, д, J=l,5 Гц). CF3 Мол.масса=335 Выход(%)=27, 8 ХН: 2,54 (ЗН, с), 7,3 (1Н, дд, J=6,0 и 1,0 Гц), 7,35 (2Н, д, J=8,6 Гц), 7,48 (ЗН, м), 7,7 (1Н, м) , 8,0 (1Н, д, J=7,9 Гц), 8,6 (1Н, м) . CF3 Мол.масса=34 0 Выход(%)=45 2H: 2,54 (ЗН, с), 6,7 (1Н, с), 6,8 (1Н, дд, J=3,57 и 1,05 Гц), 6,9 (1Н, дд, J=5,0 и 3,6 Гц), 7,28 (4Н, м), 7,33 (1Н, дд, J=5,0 и 1,0 Гц). Препаративный пример 2. 5-(3 -Фтор-4-метоксифенил)- 1-(4-метилсульфинилфенил)-3-трифторметил-1 Н-пиразол (соединение № 44) HjC н3сц -CF3 К раствору 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфанилфенил)-3-трифторметил-1Н-пиразола (соединения № 14) (790 мг) в хлороформе (25 мл) при -40°С одной порцией добавляли м-хлорпербензойную кислоту (55-75%, 464 мг), и смесь перемешивали при той же температуре в течение одного часа. Реакционную смесь разбавляли хлороформом (50 мл), промывали насыщенным раствором водного бикарбоната натрия (30 мл) и водой (2 х 30 мл), а затем сушили над хлоридом кальция и упаривали при пониженном давлении. Полученный продукт хроматографировали на си-ликагеле с использованием в качестве элюента смеси этилацетат:петролейный эфир, 7:3, и получали 600 мг продукта в виде густой жидкости. Аналогичным образом, в соответствии с вышеописанной методикой были получены нижеследующие соединения, представленные в табл. 2: - 26 - 008303 Таблица 2 О X, Мол.масса Выход(%) CF3 Мол.масса=368 Выход(%)=59 XH: 2,7 (ЗН, с), 6,7 (1H, с), 7,0 (2Н, т, J=8,7 Гц), 7,2 (2Н, м), 7,4 (2H, д, J=8,7 Гц), 7,6 (2Н, д, J=8,7 Гц) CF3 Мел,масса=384,5 Выход(%)=53 2,7 (ЗН, с), 6,7 (1Н, с), 7,1 (2Н, д, J=8,5 Гц), 7,3 (2Н, д, J=8,5 Гц), 7,4 (2Н, д, J=6,4 Гц), 7,6 (2Н, д, J=8,6 Гц). CF3 Мол.масса=364 Выход(%)=70 ХН: 2,3 (ЗН, с), 2,7 (ЗН, с), 6,7 (1Н, с), 7,11 (2Н, д, J=8,l Гц), 7,16 (2Н, д, J=8,l Гц), 7,49 (2Н, д, J=8,5 Гц), 7,6 (2Н, д, J=8,5 Гц). *¦* А г> т-1 ur3 ¦К Я_________"i П /*\ Lyl ШЛиД { Ъ ) ^DJ 1Е: 2,7 (ЗН, с), 3,8 (ЗН, с), 6,7 (1Н, с), 6,8 (2Н, д, J=8,7 Гц), 7,1 (2Н, д, J=8,7 Гц), 7,5 (2Н, д, J=8,5 Гц), 7,6 (2Н, д, J=8,9 Гц). - 27 - 008303 CF3 Мол.масса=408 Выход(%)=87 ХН: 1,0 (ЗН, т, J=7,4 Гц), 1,8 (2Н, м) , 2,7 (ЗН, с), 3,9 (2Н, т, J=6,5 Гц), 6,7 (1Н, с), 6,8 (2Н, д, J=6,7 Гц), 7,1 (2Н, д, J=6,7 Гц), 7,4 (2Н, д, J=6,6 Гц). CF3 Мол.масса=394 Выход(%)=84 ХН: 1,4 (ЗН, т, J=6,9 Гц), 2,7 (ЗН, с), 4,0 (2Н, кв, J=6,9 Гц), 6,7 (1Н, с), 6,8 (2Н, д, J=8,8 Гц), 7,1 (2Н, д, J=8,8 Гц), 7,5 (2Н, д, J=8,6 Гц), 7,6 (2Н, д, J=8,6 Гц). CF3 Мол.масса=408 Выход(%)=68 ХН: 1,3 (6Н, д, J=6,l Гц), 2,7 (ЗН, с), 4,5 (1Н, м) , 6,7 (1Н, с), 6,8 (2Н, д, J=8,9 Гц), 7,1 (2Н, д, J=9,0 Гц), 7,5 (2Н, д, J=8,7 Гц), 7,6 (2Н, д, J=8,9 Гц). CF3 Мол.масса=402,5 Выход(%)=64 'Н: 2,7 (ЗН, с), 6,7 (1 Н, с), 7,1 (2Н, м) , 7,3 (1Н, дд, J=8,9 и 2,1 Гц), 7,5 (2Н, д, J=8,67 Гц), 7,7 (2Н, д, J=8,7 Гц). CF3 Мол.масса=386 Выход(%)=65 ХН: 2,7 (ЗН, с), 6,78 (1Н, с), 7,1 (ЗН, м) , 7,5 (2Н, д, J=8,6 Гц), 7,7 (2Н, д, J=8,3 Гц). CF3 Мол.масса=382 Выход(%)=65 ХН: 2,2 (ЗН, с), 2,7 (ЗН, с), 6,7 (1Н, с), 6,9 (2Н, м) , 7,1 (1Н, м), 7,4 (2Н, д, J=8,7 Гц), 7,6 (2Н, д, J=8,6 Гц). - 28 - 008303 CF3 НзСО Мол.масса=394 Выход(%)=78 ХН: 2,1 (ЗН, с), 2,7 (ЗН, с), 3,8 (ЗН, с), 6,7 (1Н, с), 6,73 (1Н, д, J=8,3 Гц), 6,9 (1Н, дд, J=2,1 и 8,1 Гц), 7,0 (1Н, д, J=2,4 Гц), 7,5 (2Н, д, J=8,5 Гц), 7,6 (2Н, д, J=8,3 Гц). CF3 cxx H3CO Мол.масса=414,5 Выход(%)=80, 5 XH: 2,7 (ЗН, с), 3,9 (ЗН, с), 6,7 (1Н, с), 6,8 (1Н, д, J=8,5 Гц), 7,0 (1Н, дд, J=2,l и 8,4 Гц), 7,3 (1Н, д, J=2,4 Гц), 7,5 (2Н, д, J=8,5 Гц), 7,6 (2Н, д, J=8,5 Гц). CF3 H3CO Мол.масса=459 Выход(%)=55 ХН: 2,7 (ЗН, с), 3,9 (ЗН, с), 6,7 (1Н, с), 6,8 (1Н, д, J=8,5 Гц), 7,0 (1Н, дд, J=2,l и 8,5 Гц), 7,4-7,5 (ЗН, м), 7,6 (2Н, д, J=8,5 Гц). CF3 H3CO Мол.масса=398 Выход(%)=73 ХН: 2,7 (ЗН, с), 3,9 (ЗН, с), 6,7 (1Н, с), 6,9 (ЗН, м) , 7,4 (2Н, д, J=8,5 Гц), 7,6 (2Н, д, J=8,5 Гц). CF3 H3C Мол.масса=394 Выход(%)=71 ХН: 2,2 (ЗН, с), 2,7 (ЗН, с), 3,6 (ЗН, с), 6,6 (1Н, д, J=l,2 Гц), 6,6-6,7 (1Н, дд, J=l,4 и 7,6 Гц), 6,7 (1Н, с), 7,0-7,1 (1Н, д, J=7,6 Гц), 7,5 (2Н, д, J=8,6 Гц), 7,6 (2Н, д, J=8,6 Гц). CF3 H3C0 Мол.масса=398 Выход(%)=51 ХН: 2,7 (ЗН, с), 3,8 (ЗН, с), 6,7 (1Н, с), 6,8 (2Н, д, J=8,8 Гц), 7,1 (2Н, д, J=8,8 Гц), 7,4 (2Н, м) , 7,6 (1Н, м) . - 29 - 008303 CF3 Н3СО Мол.масса=398 Выход(%)=77 XH: 2,8 (ЗН, с), 3,8 (ЗН, с), 6,7 (1Н, с), 6,9 (2Н, д, J=8,8 Гц), 7,1 (2Н, д, J=8,8 Гц), 7,2 (2Н, м), 7,8 (1Н, т, J=7,8 Гц). CF3 Мол.масса=350 Выход(%)=36 ХН: 2,7 (ЗН, с), 6,7 (1Н, с), 7,2 (2Н, д, J=8,5 Гц), 7,4 (ЗН, м), 7,5 (2Н, д, J=8,5 Гц), 7,6 (2Н, д, J=8,5 Гц). СНз Мол.масса=32 6 Выход(%)=80 ХН: 2,37 (ЗН, с), 2,7 (ЗН, с), 3,8 (ЗН, с), 6,27 (1Н, с), 6,8 (2Н, д, J=8,8 Гц), 7,1 (2Н, д, J=8,8 Гц), 7,46 (2Н, д, J=8,6 Гц), 7,6 (2Н, д, J=8,6 Гц). CF3 Мол.масса=395 Выход(%)=82 ХН: 2,8 (ЗН, с), 6,9 (1Н, с), 7,2-7,4 (4Н, м) , 7,7 (2Н, д, J=8,5 Гц), 8,25 (2Н, д, J=8,8 Гц). СР3 МЪл.масса=380 Выход(%)=68 ХН: 2,7 (ЗН, с), 3,7 (ЗН, с), 6,8 (ЗН, м) , 6,9 (1Н, м) , 7,3 (1Н, м), 7,5 (2Н, д, J=8,5 Гц), 7,7 (2Н, д, J=8,5 Гц). СРз Fxx HjCO J Мол.масса=416 Выход(%)=49 2,7 (ЗН, с), 4,0 (ЗН, с), 6,79 (ЗН, м) , 7,5 (2Н, д, J=8,64 Гц), 7,7 (2Н, д, J=8,6 Гц). CF3 "XX HjCO Мол,масса=396 Выход(%)=83 ХН: 2,7 (ЗН, с), 3,9 (ЗН, с), 5,7 (1Н, с), 6,7 (2Н, м) , 6,8 (2Н, м) , 7,5 (2Н, д, J=8,6 Гц), 7,67 (2Н, д, J=8,6 Гц). - 30 - 008303 соон HjCO Мол.масса=356 Выход(%)=63 lH: 2,7 (ЗН, с), 3,8 (ЗН, с), 6,8 (2Н, д, J=8,4 Гц), 6,9 (1Н, с), 7,16 (2Н, д, J=8,34 Гц), 7,5 (2Н, д, J=8,3 Гц), 7,65 (2Н, д, J=8,3 Гц). сн2он HjCO Мол.масса=342 Выход(%)=80 ХН: 2,7 (ЗН, с), 3,8 (ЗН, с), 4,79 (2Н, с), 6,5 (1Н, с), 6,87 (2Н, д, J=8,7 Гц), 7,16 (2Н, д, J=8,7 Гц), 7 47 (2Н, д, J=8,5 Гц), 7,6 (2Н, д, J=8,5 Гц). CF3 Мол.масса=410 Выход(%)=70 АН: 2,74 (ЗН, с), 3,98 (2Н, м) , 4,1 (2Н, дд, J=5,4 и 4,0 Гц), 6,7 (1Н, с), 6,9 (2Н, дд, J=8,8 и 2,0 Гц), 7,1 (2Н, дд, J=8,8 и 2,0 Гц), 7,5 (2Н, дд, J=8,9 и 2,1 Гц), 7,6 (2Н, дд, J=6,6 и 1,9 Гц). CF3 Мол.масса=351 Выход(%)=25,9 ХН: 2,89 (ЗН, с), 7,66 (1Н, с), 7,84 (2Н, д, J=8,55 Гц), 7,9 (4Н, м), 8,6 (2Н, д, J=5,7 Гц). CF3 Мол.масса=351 Выход(%)=61, 3 ХН: 2,8 (ЗН, с), 7,1 (1Н, с), 7,4 (1Н, м) , 7,75 (2Н, д, J=8,58 Гц), 7,8 (2Н, д, J=8,64 Гц), 8,1 (1Н, м), 8,6 (1Н, дд, J=4,74 и 1,2 Гц), 9,0 (1Н, д, J=l,53 Гц). CF3 Мол.масса=351 Выход(%)=27,8 ХН: 2,8 (ЗН, с), 7,3 (1Н, дд, J=9,0 и 1,2 Гц), 7,54 (1Н, с), 7,8 (5Н, м) , 8,0 (1Н, д, J=8,0 Гц), 8,67 (1Н, д, J=4,5 Гц). CF3 Мол.масса=356 Выход(%)=54 XH: 2,76 (ЗН, с), 6,8 (1Н, с), 6,9 (1Н, дд, J=3,7 и 1,05 Гц), 7,0 (1Н, дд, J=5,0 и 3,6 Гц), 7,4 (1Н, дд, J=5,l и 1,1 Гц), 7,6 (2Н, дд, J=8,5 и 1,9 Гц), 7,7 (2Н, дд, J=8, 5 и 1,9 Гц). - 31 - 008303 Препаративный пример 3. 5-(3-Фтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразол (соединение № 74) h3cvnh °Т1 н3с.0Л^ К раствору 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфинилфенил)-3-трифторметил-1Н-пира-зола (соединения № 44) (570 мг) в хлороформе (25 мл) при 0°С добавляли азид натрия (186 мг), а затем концентрированную серную кислоту (0,14 мл), и смесь перемешивали при 40°С в течение 18 ч. Затем четыре раза через каждые два часа добавляли такое же количество азида натрия и серной кислоты, которое было добавлено перед этим, и перемешивали еще 4 ч при 40°С. Реакционную смесь охлаждали до 20°С, разбавляли хлороформом (50 мл), промывали насыщенным раствором водного бикарбоната натрия (2х50 мл) и водой (50 мл), а затем сушили над хлоридом кальция и упаривали при пониженном давлении, в результате чего получали продукт (500 мг) в виде густой жидкости. Аналогичным образом, в соответствии с вышеописанной методикой были получены соединения, представленные в табл. 3. Таблица 3 Мол.масса Выход(%) CF3 Мол.масса=383 Выход(%)=36 1Н/ CD3OD: 3,8 (ЗН, с), 6,9 (1Н, с), 7,0 (2Н, т, J=8,7 Гц), 7,2 (2Н, м), 7,6 (2Н, д, J=8,9 Гц), 8,1 (2Н, д, J=8,9 Гц). CF3 Мел.масса=399,5 Выход(%)=72 ХН, CD3OD: 3,8 (ЗН, с), 7,0 (1Н, с), 7,3 (2Н, д, J=8,7 Гц), 7,4 (2Н, д, J=8,6 Гц), 7,7 (2Н, д, J=8,9 Гц), 8,2 (2Н, д, J=9,0 Гц) . CF3 Мол.масса=37 9 Выход(%)=71 XH: 2,3 (ЗН, С), 3,1 (ЗН, С), 6,7 (1Н, с), 7,1 (2Н, Д, J=8,l Гц), 7,18 (2Н, д, J=8,l Гц), 7,5 (2Н, д, J=8,5 Гц), 7,9 (2Н, д, J=8,5 Гц) . CF3 Мол.масса=395 Выход(%)=51 ХН, CD3OD: 3,8 (ЗН, с), 3,9 (ЗН, с), 6,9 (1Н, с), 6,9 (2Н, д, J=8,7 Гц), 7,2 (2Н, д, J=9,0 Гц), 7,7 (2Н, д, J=9,0 Гц), 8,2 (2Н, д, J=9,l Гц). CF3 Мол.масса=423 Выход(%)=33 1Н, ДМСО-сЗб: 1,0 (ЗН, т, J=7,4 Гц), 1,8 (2Н, м) , 3,8 (ЗН, с), 3,9 (2Н, т, J=6,4 Гц), 6,9 (2Н, д, J=8,7 Гц), 6,9 (1Н, с), 7,2 (2Н, д, J=8,7 Гц), 7,7 (2Н, д, J=8,8 Гц), 8,19 (2Н, д, J=8,8 Гц). - 32 - 008303 CF3 Мол,масса=4 09 Выход(%)=22 ХН, CD3OD: 1,2 (ЗН, т, J=6,9 Гц), 3,7 (ЗН, с), 3,9 (2Н, кв, J=6,9 Гц), 6,8 (1Н, с), 6,8 (2Н, д, J=8,8 Гц), 7,1 (2Н, д, J=8,8 Гц), 7,6 (2Н, д, J=8,9 Гц), 8,1 (2Н, д, J=8,9 Гц). CF3 Мол.масса=381 Выход(%)=66 ХН, CD3OD: 3,8 (ЗН, с), 6,7 (2Н, д, J=8,6 Гц), 6,8 (1Н, с), 7,1 (2Н, д, J=8,6 Гц), 7,7 (2Н, д, J=8, 9 Гц), 8,2 (2Н, д, J=8,9 Гц). CF3 Мол.масса=417,5 Выход(%)=95 1Е, CD3OD: 3,89 (ЗН, с), 7,0 (1Н, с), 7,3 (2Н, д, J=7,7 Гц), 7,5 (1Н, д, J=6,9 Гц), 7,8 (2Н, д, J=8,9 Гц), 8,2 (2Н, м) . CF3 Мол.масса=4 01 Выход(%)=96 ХН, CD3OD: 3,9 (ЗН, с), 7,0 (1Н, с), 7,2 (1Н, м), 7,3 (2Н, м), 7,8 (2Н, д, J=8,8 Гц), 8,2 (2Н, д, J=8,8 Гц). CF3 H,cFxr Мол.масса=397 Выход(%)=47 ХН, CD3OD: 2,2 (ЗН, с), 3,7 (ЗН, с), 6,9 (1Н, с), 7,1 (2Н, м), 7,3 (1Н, д, J=7,2 Гц), 7,7 (2Н, д, J=8,9 Гц), 8,2 (2Н, д, J=8,9 Гц). CF3 H,0ir H3C0' ^ Мол.масса=409 Выход(%)=41 XH, CD3OD: 2,1 (ЗН, с), 3,3 (ЗН, с), 3,8 (ЗН, с), 6,9 (1Н, д, J=8,5 Гц), 7,0 (1Н, дд, J=2,l и 8,5 Гц), 7,1 (1Н, с), 7,2 (1Н, д, J=l,52 Гц), 7,6 (2Н, Д, J=8,6 Гц), 8,0 (2Н, д, J=8,7 Гц). - 33 - 008303 CF3 H3CO Мол.масса=4 2 9,5 Выход(%)=34,5 ХН, CD3OD: 3,8 (ЗН, с), 3,9 (ЗН, с), 6,9 (1Н, с), 7,0-7,1 (1Н, д, J=8,6 Гц), 7,2 (1Н, дд, J=2,l и 8,2 Гц), 7,3 (1Н, д, J=2,l Гц), 7,7 (2Н, д, J=8,9 Гц), 8,2 (2Н, д, J=8,9 Гц). CF3 H3C0 ^ Мол.масса=47 4 Выход(%)=56 1Н, CD3OD: 3,9 (ЗН, с), 3,92 (ЗН, с), 6,9 (1Н, с), 7,0 (1Н, д, J=8,5 Гц), 7,2-7,3 (1Н, дд J=2,l и 8,5 Гц), 7,5 (1Н, д, J=2,l Гц), 7,8 (2Н, д, J=8, 9 Гц), 8,2 (2Н, д, J=8, 9 Гц). CF3 НзСО ^ Мол.масса=413 Выход(%)=74 "Н, CD3OD: 3,89 (ЗН, с), 3,9 (ЗН, с), 6,9 (1Н, с), 7,1 (ЗН, м), 7,7 (2Н, д, J=8,8 Гц), 8,2 (2Н, д, J=8,5 Гц). CF3 Мол.масса=409 Выход(%)=40 *H: 2,2 (ЗН, с), 2,7 (ЗН, с), 3,6 (ЗН, с), 6,6 (1Н, д, J=l,2 Гц), 6,6-6,7 (1Н, дд, J=l,4 и 7,6 Гц), 6,7 (1Н, с), 7,0-7,1 (1Н, д, J=7,6 Гц), 7,5 (2Н, д, J=8,6 Гц), 7,6 (2Н, д, J=8, 6 Гц). CF3 H3C0 Мол.масса=413 Выход(%)=94 ХН: 3,1 (ЗН, с), 3,8 (ЗН, с), 6,7 (1Н, с), 6,8 (2Н, дд, J=2,0 и 8,8 Гц), 7,1 (2Н, дд, J=2,0 и 8,8 Гц), 7,7 (2Н, м) , 7,9 (1Н, м) . CF3 Мол.масса=413 Выход(%)=25 'Н: 3,2 (ЗН, с), 3,8 (ЗН, с}, 6,7 (1Н, с), 6,9 (2Н, д, J=8,8 Гц), 7,1 (ЗН, м) , 7,3 (1Н, дд, J=l,9 и 10,4 Гц), 7,9 (1Н, т, J=8,4 Гц). - 34 - 008303 CF3 Мол.масса=365 Выход(%)=32 XH, CD3OD: 3,8 (ЗН, с), 7,0 (1Н, с), 7,3-7,4 (5Н, м) , 7,7 (2Н, д, J=8,7 Гц), 8,1 (2Н, д, J=8,8 Гц). СНз Мол.масса=341 Выход(%)=93 ХН, CD3OD: 2,35 (ЗН, с), 3,8 (ЗН, с), 3,89 (ЗН, с), 6,4 (1Н, с), 6,9 (2Н, д, J=8,8 Гц), 7,2 (2Н, д, J=8,8 Гц), 7,7 (2Н, д, J=8,9 Гц), 8,1 (2Н, д, J=8,9 Гц). CF3 02N Мол.масса=410 Выход(%)=92 ХН, CD3OD: 3,9 (ЗН, с), 7,2 (1Н, с), 7,6 (2Н, д, J=8,9 Гц), 7,8 (2Н, д, J=8,9 Гц), 8,2 (4Н, м). CF3 Мол.масса=395 Выход(%)=84 ХН, CD3OD: 3,7 (ЗН, с), 3,9 (ЗН, с), 6,9 (2Н, м) , 7,0 (2Н, м), 7,3 (1Н, т, J=7,9 Гц), 7,8 (2Н, д, J=8,9 Гц), 8,2 (2Н, д, J=8, 9 Гц) . CF3 HjCO f Мол.масса=431 Выход(%)=90 ХН, CD3OD: 3,9 (ЗН, с), 4,0 (ЗН, с), 7,02 (1Н, с), 7,06 (2Н, д, J=2,7 Гц), 7,8 (2Н, д, J=8,9 Гц), 8,2 (2Н, д, J=8,9 Гц). CF3 myy H3C0 Мол.масса=411 Выход(%)=4 6 ХН, CD3OD: 3,86 (ЗН, с), 3,91 (ЗН, с), 6,7 (1Н, д, J=2,07 Гц), 6,8 (1Н, дд, J=8,25 и 2,07 Гц), 6,9 (2Н, м) , 7,8 (2Н, д, J=8,85 Гц), 8,2 (2Н, д, J=8,85 Гц). COOH HjCO Мол.масса=371 Выход(%)=56 ХН, ДМСО-616: 3,09 (ЗН, с), 3,75 (ЗН, с), 6,9 (2Н, д, J=8,7 Гц), 7,0 (1Н, с), 7,2 (2Н, д, J=8,7 Гц), 7,5 (2Н, д, J=8,5 Гц), 7,9 (2Н, д, J=8,5 Гц). - 35 - 008303 Н3СО Мол.масса=357 Выход(%)=46 1Н, CD3OD: 3,8 (ЗН, с), 3,9 (ЗН, с), 4,67 (2Н, с), 6,6 (1Н, с), 6,95 (2Н, д, J=8,8 Гц), 7,23 (2Н, д, J=8,8 Гц), 7,7 (2Н, д, J=8,99 Гц), 8,17 (2Н, д, J=8,99 Гц). CH20S03H Н3СО Мол.масса=4 37 Выход(%)=28 ХН, ДМСО-с1б: 3,77 (ЗН, с), 3,85 (ЗН, с), 4,87 (2Н, с), 6,6 (1Н, с), 6,98 (2Н, д, J=8,7 Гц), 7,2 (2H, д, J=8,7 Гц), 7,65 (2H, д, J=8,8 Гц), 8,1 (2Н, д, J=8,8 Гц). CF3 HQ^ Мол.масса=425 Выход(%)=25 1,99 (1Н, т, ОН), 2,73 (1Н, шир. , NH) , 3,1 (ЗН, с), 4,0 (2Н, м), 4,1 (2Н, м), 6,7 (1Н, с), 6,9 (2Н, дд, J=8,7 и 2,1 Гц), 7,15 (2Н, дд, J=8,8 и 2,1 Гц), 7,5 (2Н, дд, CF3 Кол.масса=366 Выход(%)=7 8,3 ХН: 3,18 (ЗН, с), 7,27 (1Н, с), 7,75 (2Н, дд, J=4,5 и 1,6 Гц), 7,8 (2Н, д, J=8,5 Гц), 8,2 (2Н, д, J=8,7 Гц), 8,7 (2Н, дд, J=4,5 и 1,5 Гц). CF3 Мол,масса=366 Выход(%)=86,5 XH: 3,18 (ЗН, с), 7,23 (1Н, с), 7,4 (1Н, м) , 7,8 (2Н, д, J=8,61 Гц), 8,1 (ЗН, м) , 8,6 (1Н, д, J=4,7 Гц), 9,0 (1н, с) . Н Н CF Мол.масса=366 Выход(%)=88,8 1Н: 3,1 (ЗН, с), 7,3 (1Н, м) , 7,5 (1Н, с), 7,7-7,8 (ЗН, м) , 8,0 (1Н, д, J=7,9 Гц), 8,2 (2Н, д, J=8,64 Гц), 8,69 (1Н, д, J=4,68 Гц). CF3 Мол.масса=423 Выход(%)=82 XH: 1,3 (6Н, д, J=6,0 Гц), 3,1 (ЗН, с), 4,6 (1Н, м) , 6,7 (1Н, с), 6,85 (2Н, д, J=8,6 Гц), 7,1 (2Н, д, J=8, 67 Гц), 7,5 (2Н, д, J=8,52 Гц), 8,0 (2Н, д, J=8,55 Гц). CF3 Мол.масса=371 Выход(%)=14 гН, CD3OD: 3,8 (ЗН, с), 7,1 (ЗН, м) , 7,6 (1Н, дд, J=4,8 и 1,4 Гц), 7,8 (2Н, д, J=8,7 Гц), 8,2 (2Н, д, J=8,7 Гц). - 36 - 008303 Препаративный пример 4. 5-Хлор-3-(4-метилсульфанилфенил)-[2,3']бипиридинил (соединение № 93). H3C-S Смесь 3-[2-(4-метилсульфанилфенил)ацетил]пиридина (0,9 г), 2-хлормалондиальдегида (0,98 г) и ацетата аммония (1,85 г) нагревали до 130°С в течение 16 ч, и образовавшуюся уксусную кислоту отгоняли. Реакционную смесь охлаждали, подщелачивали водным карбонатом натрия, экстрагировали дихлорметаном (2х100 мл) и сушили над безводным сульфатом натрия. Объединенный органический слой нагревали с активированным углем, фильтровали и упаривали при пониженном давлении. Неочищенный продукт хроматографировали на силикагеле с использованием в качестве элюента 10-50% этилацетата в петролейном эфире, в результате чего получали 280 мг продукта в виде темно-желтого твердого вещества. Аналогичным образом, в соответствии с вышеописанной методикой были получены соединения, представленные в табл. 4. Таблица 4 № соединения Мол. масса Выход (%) Мол.масса=312,5 Выход(%)=24,21 LR: 2,48 (ЗН, с), 7,06-7,08 (2Н, д, J=8,4 Гц), 7,15-7,18 (2Н, д, J=8,4 Гц), 7,20-7,25 (1Н, м), 7,67-7,69 (1Н, м), 7,73-7,74 (1Н, д, J=2,3 Гц), 8,50-8,52 (1Н, дд, J=3,2 и 4,8 Гц), 8,57 (1Н, д, J=l,64 Гц), 8,6 (1Н, д, J=2,35 Гц). Мол.масса=326,5 Выход(%)=26,24 ХН: 2,48 (ЗН, с), 2,53 (ЗН, с), 7,05-7,09 (ЗН, м), 7,19-7,16 (2Н, д, J=6,39 Гц), 7,59-7,55 (1Н, д, J=8,04 Гц), 7,71-7,70 (1Н, д, J=2,34 Гц), 8,45-8,44 (1Н, д, J=2,25 Гц), 8,64-8, 63 (1Н, д, J=2,37 Гц). Сульфиды, полученные в соответствии с методикой, описанной в препаративном примере 4, превращали в соответствующие сульфоксиды как описано выше в препаративном примере 2. - 37 - 008303 Таблица 5 № соединения Мол. масса Выход (%) Мол.масса=328,5 Выход(%)=44,16 ХН: 2,76 (ЗН, с), 7,28-7,30 (1Н, д, J=4,95 Гц), 7,34-7,37 (2Н, д, J=8,3 Гц), 7,6-1-7,64 (2Н, д, J=8,3 Гц), 7, 73-7,76 (1Н, д, 8 Гц), 7,78-7,79 (1Н, д, J=2,34 Гц), 8,54 (2Н, с), 8,72-8,73 (1Н, д, :г=2,3 Гц). Мол.масса=342,5 Выход(%)=47 гК: 2,54 (ЗН, с), 2,76 (ЗН, с), 7,06-7,08 (1Н, д, J=8 Гц), 7,34-7,37 (2Н, д, J=8,37 Гц), 7,54-7,57 (1Н, дд, J=2,3 и 8 Гц), 7,6-7,63 (2Н, д, J=6,4 Гц), 7,7 (1Н, д, J=2,34 Гц), 8,4 (1Н, д, J=2,3 Гц), 8,7 (1Н, д, J=2,3 Гц). Сульфоксиды, полученные в соответствии с методикой, описанной в препаративном примере 5, превращали в соответствующие сульфоксимины как описано выше в препаративном примере 3. Таблица 6 № соединения Мол. масса Выход (%) Мол.масса=3 43,5 Выход(%)=44 ХН: 2,75 (ЗН, с), 7,22-7,24 (1Н, м), 7,33-7,36 (2Н, д, J=8,2 Гц), 7,60-7,63 (2Н, д, J=8,2 Гц), 7,67-7,7 (1Н, д, J=8 Гц), 7,77-7,78 (1Н, д, J=2,3 Гц), 8,52-8,54 (2Н, с), 8,72 (1Н, д, J=2,3 Гц). - 38 - 008303 Мол.масса=357,5 Выход(%)=7 9 ХН: 2,54 (ЗН, с), 3,14 (ЗН, с), 7,10-7,13 (1Н, д, J=8,04 Гц) , 7,36-7,39 (2Н д, J=8 Гц), 7,607,64 (1Н, дд, J=2,3 и 8,04 Гц), 7,7 (1Н, д, J=2,3 Гц), 7, 96-7, 98 (2Н, д, J=8,5 Гц), 8,3 (1Н, д, J=2 Гц), 8,7 (1Н, д, J=2,4 Гц). Сульфиды общей формулы, представленной ниже, были получены в соответствии с процедурами, хорошо известными специалистам (например, как описано в WO 0181332). H,C'S' R3 Y О Сульфиды общей формулы, представленной выше, превращали в соответствующие сульфоксиды как описано в препаративном примере 2. Таблица 7 Соединение № Мол.масса Выход(%) Мол.масса=385 Выход(%)=41,1 ХН: 2,9 (ЗН, с), 5,2 (2Н, с), 7,05 (1Н, дд, J=l,5 и 10 Гц), 7,2 (1Н, дд, J=2 и 8,3 Гц), 7,3 (1Н, д, J=l,5 и 8,1 Гц), 7,4 (1Н, д, J=8,3 Гц), 7,5 (1Н, д, J=8,4 Гц), 7,9 (1Н, т, J=7,6 Гц). - 39 - 008303 100 Мол.масса=350, 5 Выход(%)=70 *H: 2,9 (ЗН, с), 5,2 (2H, с),7,05 (1Н, дд, J=l,5 и 10 Гц), 7,3-7,4 (5Н, м), 7,8 (1Н, т, J=7,5 Гц). 101 Мол.масса=316 Выход(%)=33,3 *H: 2,85 (ЗН, с), 5,2 (2Н, с), 7,05 (1Н, дд, J=l,5 и 10 Гц), 7,34-7, 37 (1Н, дд, J=l,5 и 8,1 Гц), 7,38-7,8 (5Н, м), 7,83-7,89 (1Н, т, J=7,7 Гц). 102 Мол.масса=352 Выход(%)=57,4 ХН: 2,87 (ЗН, с), 5,2 (2Н, с), 7,03-7, 07 (1Н, дд, J=l,5 и 10 Гц), 7,16-7,3 (ЗН, м), 7,34-7,37 (1Н, дд, J=l,5 и 8,1 Гц), 7,9 (1Н, т, J=7,6 Гц). 103 Н3СО Мол.масса=37 6 Выход(%)=66 ^Н: 2,Ь5 (ЗН, с), 3,Ь0 (ЗН, с), 3,У (ЗН, с), 5,15 (2Н, с), 6, 86-6,89 (1Н, д, J=8,2 Гц), 6,96-7,0 (2Н, м) , 7,09-7,14 (1Н, дд, J=l,5 и 10,3 Гц), 7,4 (1Н, дд, J=l,5 и 8,07 Гц), 7,86-7,91 (1Н, т, J=7,6 Гц). 104 HjCo'"4"^ Мол,масса=346 Выход(%)=71, 5 ХН: 2,86 (ЗН, с), 3,84 (ЗН, с), 5,14 (2Н, с), 6,91-6,95 (2Н, дд, J=2 и 6,87 Гц), 7,08-7,12 (1Н, дд, J=l,4 и 10,3 Гц), 7,36-7,39 (ЗН, м), 7,84-7,89 (1Н, т, J=7,6 Гц). 105 Н3С Мол.масса=330 Выход(%)=35,4 ХН: 2,39 (ЗН, с), 2,85 (ЗН, с), 5,15 (2Н, с), 7,07-7,1 (1Н, дд, J=l,5 и 10,35 Гц), 7,2-7,32 (4Н, м) , 7, 34-7,38 (1Н, дд, J=l,5 и 8,1 Гц), 7,84-7,89 (1Н, т, J=7,6 Гц). - 40 - 008303 Сульфоксиды, представленные в табл. 7, превращали в соответствующие сульфоксимины как описано выше в препаративном примере 3. Таблица 8 Соединение № Мол.масса Выход(%) 106 Мол.масса=400 Выход(%)=77 ^ 3,-3 (ЗН, с), 5,18 (2Н, с), 7,15-7,27 (ЗН, м) , 7,47-7,5 (1Н, д, J=8,3 Гц), 7,58 (1Н, д, J=2 Гц), 7,97-8,02 (1Н, т, J=7,6 Гц). 107 Мол.масса=3 65,5 Выход(%)=77 ХН: 3,3 (ЗН, с), 5,17 (2Н, с), 7,15-7,19 (1Н, дд, J=l,56 И 10,32 Гц), 7,24 (1Н, д, J=l,6 Гц), 7,327,42 (4Н, м), 7,95-8,0 (1Н, т, J=7,8 Гц). 108 Мол.масса=331 Выход(%)=47 1Н, flMCO-d6: 3,30 (ЗН, с), 5,39 (2Н, с), 7,32-7,36 (ЗН, м), 7,42-7,5 (4Н, м), 7,83-7,88 (1Н, т, J=7,9 Гц). 109 Мол.масса=367 Выход(%)=67 ХН: 3,3 (ЗН, с), 5,17 (2Н, с), 7,15-7,34 (5Н, м) , 7,97-8,02 (1Н, т, J=7,7 Гц). 110 Мол.масса=391 Выход(%)=30 - 41 - 008303 XH: 3,3 (ЗН, с), 3,8 (ЗН, с), 3,9 (ЗН, с), 5,15 (2Н, с), 6,85-6, 88 (1Н, д, J=8,3 Гц), 6,93-6,96 (1Н, д, J=2 и 8,3 Гц), 7,0 (1Н, д, J=l,5 Гц), 7,20-7,24 (1Н, дд, J=l,5 и 8,1 Гц), 7,29-7,32 (1Н, дд, J=l,5 и 8,1 Гц), 7,93-7,98 (1Н, т, J=7,8 Гц). 111 Мол. масса=3 61 Выход(%)=4 8 гЯ: 3,3 (ЗН, с), 3,85 (ЗН, с), 5,14 (2Н, с), 6,926,95 (2Н, д, J=6,78 Гц), 7,18-7,22 (1Н, дд, J=l,5 и 10,56 Гц), 7,27-7,30 (1Н, дд, 1,59 и 8,25 Гц), 7,35-7,38 (2Н, д, J=6,8 Гц), 7, 92-7,98 (1Н, т, J=7,8 Гц). 112 Н3С Мол.масса=345 Выход(%)=69 гК: 2,39 (ЗН, с), 3,28 (ЗН, с) , 5,15 (2Н, с), 7,17-7,13 (6Н, м), 7,91-7,97 (1Н, т, J=7,8 Гц). Препаративный пример 5. 3-(3-Фторфенил)-4-(4-метилсульфанил)-3Н-тиазол-2-он (соединение № 113) H3CS Стадия 1. Получение этил(3-фторфенил)тиокарбамата. Раствор 3-фторанилина (4 г) и бис(этокситиокарбанил)сульфида (7,56 г) в 50 мл EtOH перемешивали при комнатной температуре в течение 24 ч. Растворитель выпаривали и остаток растирали с пентаном с получением 4,0 г продукта в виде светло-кремового твердого вещества. Стадия 2. Получение 3-(3-фторфенил)-4-гидрокси-4-(4-метилсульфанилфенил)тиазолидин-2- она. Смесь этил(3-фторфенил)тиокарбамата (1 г) (полученного на стадии 1) и 2-бром-1-(4-метил-сульфанилфенил)этанона (1,4 г) в 20 мл ТТФ нагревали при температуре флегмообразования (с обратным холодильником) в течение 8 ч. Слабо растворимое вещество фильтровали, а затем растворитель выпаривали и остаток растворяли в дихлорметане. Органический раствор сушили над сульфатом натрия, упаривали и остаток кристаллизовали из эфира с получением 0,8 г продукта в виде светло-желтого твердого вещества. Стадия 3. Получение 3-(3-фторфенил)-4-(4-метилсульфанил)-3Н-тиазол-2-она. К раствору 3-(3-фторфенил)-4-гидрокси-4-(4-метилсульфанилфенил)тиазолидин-2-она (1 г) (полученного на стадии 2) в этаноле (50 мл) добавляли 0,5 мл концентрированной НС1 и нагревали при температуре флегмообразования (с обратным холодильником) в течение 5 ч. Реакционную смесь охлаждали до 25°С. Осажденное твердое вещество фильтровали, промывали этанолом и сушили с получением 0,8 г продукта в виде светло-желтого твердого вещества. Аналогичным образом, в соответствии с вышеописанной методикой были получены соединения, представленные в табл. 9. - 42 - 008303 Таблица 9 № соединения Мол. масса Выход (%) 113 Мол.масса=317 Выход(%)=84 XH: 2,45 (ЗН, с), 6,18 (1H, с), 6,89-7,09 (6H, комплекс), 7,28-7,31 (2Н, м). 114 Мол.масса=368 Выход(%)=84 ХН: 2,46 (ЗН, с), 6,18 (1Н, с), 6,88-6,92 (1Н, дд, J=2,43 Гц и 8,5 Гц), 6, 96-6,99 (2Н, д, J=8,4 Гц), 7,09-7,12 (2Н, д, J=7,5 Гц), 7,35 (1Н, д, J=2,4 Гц), 7,37-7,40 (1Н, д, J=8,6 Гц). Сульфиды, полученные как описано выше, превращали в соответствующие сульфоксиды в соответствии с методикой, описанной в препаративном примере 2. Таблица 10 Соединение № Мол.масса Выход(%) 115* Мол.масса=368 Выход(%)=64, 5 ХН: 2,74 (ЗН, с), 6,9-7,0 (1Н, д, J=8,6 и 2,5 Гц), 7,1 (1Н, с), 7,2 (2Н, д, J=8,5 Гц), 7,4 (1Н, д, 5=2,5 Гц), 7,4 (1Н, д, J=8,6 Гц), 7,6 (2Н, д, J=8,5 Гц). 116* Мол.масса=37 8 Выход(%)=73 гЯ: 2,74 (ЗН, с), 7,0 (2Н, д, J=8,7 Гц), 7,09 (1Н, с), 7,2 (2Н, д, J=8,4 Гц), 7,5 (2Н, д, J=8,7 Гц), 7,6 (2Н, д, J=8,4 Гц). 117* Мол.масса=299 Выход(%)=28 XH: 2,7 (ЗН, с), 7,1 (1Н, с) , 7,2 (4Н, м) , 7,4 (ЗН, м), 7,5 (2Н, д, J=8,5 Гц). - 43 - 008303 118* Мол.масса=317 Выход(%)=53 XH: 2,7 (ЗН, с), 7,2 (ЗН, м), 7,27 (2Н, д, J=8,3 Гц), 7,3-7,4 (2Н, м), 7,6 (2Н, д, J=8,4 Гц). ¦1 1 П + -L-L Z? " "Л_________ООО т-> . ~ - , о. \ _п с оылид \ 'о ) — 1 \) XH: 2,7 (ЗН, с), 6,3 (1Н, с) , 6,4-6,9 (2Н, м) , 7,0-7,08 (1Н, м) , 7,23-7,36 (ЗН, м) , 7,5 (2Н, д, J=8,2 Гц). 120* Мол.масса=384 Выход(%)=88 XH: 2,72 (ЗН, с), 6,3 (1Н, с) , 6,9 (1Н, дд, J=2,4 и 8,5 Гц), 7,2 (2Н, д, J=8,3 Гц), 7,3 (1Н, д, J=2,4 Гц), 7,4 (1Н, д, J=8,5 Гц), 7,5 (2Н, д, J=8,3 Гц). Соответствующие сульфиды получали методами, известными специалистам. Препаративный пример 6. 4-(4-Метилсульфоксиминилфенил)-3-(3,4-дихлорфенил)-3Н-окса-зол-2-он (соединение № 121). HN4 Р% К перемешиваемому раствору 4-(4-метилсульфинилфенил)-3-(3,4-дихлорфенил)-3Н-оксазол-2-она (соединения № 115) (1,1 г) в 20 мл дихлорметана добавляли О-мезитиленсульфо-нилгидроксиламин (1,12 г) при 25°С и перемешивали 12 ч. Реакционную смесь подщелачивали 2н. раствором NaOH до рН 11, перемешивали в течение 30 мин и экстрагировали дихлорметаном (3х100 мл). Органический экстракт сушили над безводным сульфатом натрия и упаривали при пониженном давлении. Полученный неочищенный продукт хроматографировали с использованием в качестве элюента 20-60% этилацетата в петролейном эфире, в результате чего получали 670 мг чистого продукта в виде смолы. Аналогичным образом, в соответствии с вышеописанной методикой были получены соединения, представленные в табл. 11. Таблица 11 - 44 - 008303 Соединение № Мол.масса Выход(%) 121 Мол.масса=383 Выход(%)=32 1Н/ CD3OD: 3,6 (ЗН, с), 7,0-7,1 (1Н, д, J=2,4 и 8,6 Гц), 7,4-7,5 (4Н, м) , 7,59 (1Н, с), 8,0 (2Н, д, J=8,7 Гц). 122 Мол,масса=393 Выход(%)=57,7 XH: 3,1 (ЗН, с), 7,0 (2Н, д, J=6,7 Гц), 7,09 (1Н, с), 7,2 (2Н, д, J=6,2 Гц), 7,5 (2Н, д, J=8,7 Гц), 7,9 (2Н, д, J=8,4 Гц). 123 Мол.масса=314 Выход (%)=47 ХН, CDCl3+flMCO-d6: 3,2 (ЗН, с), 7,2 (2Н, д, J=8,l Гц), 7,3 (2Н, д, J=9,0 Гц), 7,4 (ЗН, м), 7,8 (2Н, д, J=8,5 Гц), 8,1 (1Н, с). 124 Мол.масса=332 Выход(%)=53 XH: 3,08 (ЗН, с), 7,1 (ЗН, м), 7,2 (2Н, д, J=8,49 Гц), 7,3-7,4 (2Н, м), 7,9 (2Н, д, J=8,5 Гц). 125 'ГУ Мол.масса=34 8 Выход(%)=60 ХН, CD3OD: 3,8 (ЗН, с) , 6,8 (1Н, с), 7,0 (1Н, д, J=8,0 Гц), 7,09-7,16 (2Н, м) , 7,3-7,4 (1Н, дд, J=6,3 и 8,0 Гц), 7,6 (2Н, д, J=8,6 Гц), 8,0 (2Н, д, J=8,6 Гц). 126 Мол.масса=399 Выход(%)=61 ХН, ДМСО-de: 3,5 (ЗН, с), 6,9 (1Н, с), 7,2 (1Н, дд, J=2,4 и 8,5 Гц), 7,5 (2Н, д, J=8,5 Гц), 7,6 (1Н, д, J=8,5 Гц), 7,7 (1Н, д, J=2,4 Гц), 7,9 (2Н, д, J=8,4 Гц). - 45 - 008303 Препаративный пример 7. 3-(3,4-Дихлорфенил)-4-[4-(К-хлорацетил)метилсульфоксиминил-фенил]-ЗН-оксазол-2-он (соединение № 128). н3с К раствору 3-(3,4-дихлорфенил)-4-[4-метилсульфоксиминилфенил]-3Н-оксазол-2-она (соединения № 119) (100 мг) и триэтиламина (0,18 мл) в сухом ТГФ (5 мл) добавляли хлорацетилхлорид (59 мг) при 0°С. Реакционную смесь оставляли для нагревания до 25°С и перемешивали в течение 2 ч. Реакцию гасили водой, и смесь экстрагировали дихлорметаном (3х10 мл). Органический экстракт промывали водой, а затем насыщенным раствором соли, после чего сушили над хлоридом кальция и упаривали при пониженном давлении. Неочищенный продукт очищали на силикагеле с использованием в качестве элюента 50% этилацетата в петролейном эфире, в результате чего получали 70 мг продукта в виде желтого твердого вещества. Аналогичным образом, в соответствии с вышеописанной методикой были получены соединения, представленные в табл. 12. Таблица 12 Соединение № Мол.масса Выход(%) 127 "XX Мол.масса=424 Выход(%)=69 XH: 2,1 (ЗН, с), 3,3 (ЗН, с), 6,9 (1Н, Д, J=2,4 и 8,5 Гц), 7,1 (1Н, с), 7,3 (2Н, д, J=8,5 Гц), 7,4 (1Н, д, J=2,5 Гц), 7,4 (1Н, д, J=8,5 Гц), 7,9 (2Н, д, J=8,5 Гц). 128 Мол.масса=4 60 Выход(%)=50 3,3 (ЗН, с), 4,1 (2Н, с), 6,9 (1Н, дд, J=2,5 и 8,5 Гц), 7,1 (1Н, с), 7,3 (2Н, д, J=8,6 Гц), 7,4 (1Н, д, J=2,4 Гц), 7,4 (1Н, д, J=8,5 Гц), 7,9 (2Н, д, J=8, 67 Гц) . 129 -S-СНз О Мол.масса=4 61 Выход(%)=66 гЯ: 3,1 (ЗН, С), 3,4 (ЗН, с), 6,9 (1Н, дд, J=2,5 и 8,6 Гц), 7,1 (1Н, с), 7,3 (2Н, д, J=8,5 Гц), 7,4 (1Н, д, J=2,5 Гц), 7,4 (1Н, д, J=8,5 Гц), 7,9 (2Н, д, J=8,5 Гц). 130 О j-v о - Мол.масса=537 Выход(%)=53 1Н: 2,4 (ЗН, с), 3,4 (ЗН, с), 6,9 (1Н, дд, J=2,5 и 8,6 Гц), 7,1 (1Н, с), 7,2-7,3 (4Н, м), 7,4 (1Н, д, J=2,4 Гц), 7,4 (1Н, д, J=8,6 Гц), 7,8 (2Н, д, J=8,3 Гц), 7,9 (2Н, д, J=8,6 Гц). - 46 - 008303 Препаративный пример 8. 3-(4-Метоксифенил)-4-(4-метилсульфанил)-5-метилизоксазол (соединение № 138). Стадия 1. Получение 3-(4-метоксифенил)-4-(4-метилсульфанил)-5-метил-4,5-дигидроизокса-зол-5-ола К перемешиваемому раствору оксима 1-(4-метоксифенил)-2-(4-метилсульфанилфенил) этанона (4,5 г) в сухом ТГФ (30 мл) в течение 30 мин при -70°С добавляли раствор н-бутиллития (1,3 М, 30,7 мл) в гексане. Реакционную смесь нагревали до 20°С в течение 2 ч. К этой смеси добавляли этил-ацетат (2,1 мл), и реакционную смесь перемешивали при той же температуре в течение 30 мин. Затем реакционную смесь гасили холодной водой (100 мл) и экстрагировали этилацетатом (3х100 мл). Органический экстракт промывали водой (100 мл) и насыщенным раствором соли (100 мл), а затем сушили над сульфатом натрия и упаривали при пониженном давлении. Неочищенный продукт хроматографировали на силикагеле с использованием в качестве элюента 10% этилацетата в петролейном эфире, и получали 4,1 г чистого продукта в виде светло-желтого твердого вещества. Стадия 2. Получение 3-(4-метоксифенил)-4-(4-метилсульфанил)-5-метилизоксазола. Раствор 3-(4-метоксифенил)-4-(4-метилсульфанил)-5-метил-4,5-дигидроизоксазол-5-ола (2,1 г) и PTSA (пара-толуолсульфоновой кислоты) (100 мг) в бензоле (20 мл) нагревали при температуре флегмообразования (с обратным холодильником) в течение 30 мин. Реакционную смесь охлаждали до 25°С, разбавляли 50 мл бензола и промывали водой (50 мл), а затем насыщенным раствором соли (50 мл). Органический экстракт сушили над сульфатом натрия и упаривали при пониженном давлении с получением 1,7 г продукта в виде густой жидкости. Препаративный пример 9. 5-Хлор-4-(4-метилсульфанилфенил)-3-фенилизоксазол (соединение № 136). Стадия 1. Получение 5-гидрокси-4-(4-метилсульфанилфенил)-3-фенилизоксазола. К перемешиваемому раствору оксима 1-фенил-2-(4-метилсульфанилфенил)этанона (2,0 г) в сухом ТГФ (20 мл) в течение 30 мин при -70°С добавляли раствор н-бутиллития (0,98 М, 25 мл) в гек-сане. Реакционную смесь нагревали до 20°С в течение 2 ч. К этой смеси добавляли твердый CO2 (25 г) и реакционную смесь перемешивали при той же температуре в течение 30 мин. Затем реакционную смесь гасили холодной 1н. НС1 (20 мл) и экстрагировали этилацетатом (3х50 мл). Органический экстракт промывали водой (100 мл); насыщенным раствором соли (100 мл), сушили над сульфатом натрия и упаривали при пониженном давлении. Неочищенный продукт хроматографировали на си-ликагеле с использованием в качестве элюента 10% этилацетата в петролейном эфире и получали 1,2 г чистого продукта в виде густой жидкости. Стадия 2.: Получение 5-хлор-4-(4-метилсульфанилфенил)-3-фенилизоксазола. К смеси 5-гидрокси-4-(4-метилсульфанилфенил)-3-фенилизоксазола (соединения, полученного в стадии 1) (0,6 г) и триэтиламина (0,43 мл) добавляли, перемешивая, POCl3 (10 мл), и реакционную смесь нагревали до 70°С в течение 4 ч. Растворители выпаривали и неочищенный продукт хромато-графировали на силикагеле с использованием петролейного эфира в качестве элюента, в результате чего получали 310 мг продукта в виде светло-желтого твердого вещества. Аналогичным образом, в соответствии с методикой, описанной в препаративном примере 8, были получены соединения, представленные в нижеследующей таблице. 008303 Таблица 13 Соединение № Мол.масса Выход(%) 131 Мол.масса=295 Выход(%)=44 1Н: 1,3 (ЗН, т, J=7,6 ГЦ), 2,7 (ЗН, с) , 2,8 (2Н, кв, J=7,6 Гц), 7,2-7,6 (9Н, комплекс). 132 -СН2ОСН3 Мол.масса=311 Выход(%)=60 XH: 2,5 (ЗН, с), 3,4 (ЗН, с), 4,5 (2Н, с), 7,1-7,2 (4Н, м), 7,3 (ЗН, м), 7,4 (2Н, м). 133 -СНз Мол.масса=2 99 Выход(%)=35 XH: 2,4 (ЗН, с), 2,7 (ЗН, с), 7,0 (2Н, т, J=8,7 Гц), 7,3 (4Н, м), 7,6 (2Н, д, J=8,4 Гц). 134 -СНз Мол.масса=315,5 Выход(%)=85 XH: 2,4 (ЗН, с), 2,7 (ЗН, с), 7,2-7,3 (6Н, и), 7,6 (2Н, д, J=8,2 Гц). 135 -^СНз Мол.масса=2 95 Выход(%)=23 1Н: 1,2 (ЗН, т, J=7,5 Гц), 2,6 (2Н, кв, J=7,5 Гц), 2,8 (ЗН, с), 7,3 (ЗН, м), 7,4 (4Н, м), 7,7 (2Н, д, J=8, 4 Гц). 136 -С1 Мол.масса=301, 5 Выход(%)=4 9 XH: 2,7 (ЗН, с), 7,2-7,4 (7Н, комплекс), 7,6 (2Н, д, J=8,3 Гц) . 137 -СНз Мол.масса=281 Выход (%) =94 2,45 (ЗН, с), 2,5 (ЗН, с), 7,1 (2Н, д, J=8,44 Гц), 7,2 (2Н, д, J=8,44 Гц), 7,3 (ЗН, м), 7,4 (2Н, м) . 138 -СН3 Мол.масса=311 Выход(%)=85 ХН: 2,4 (ЗН, с), 2,5 (ЗН, с), 3,8 (ЗН, с), 6,8 (2Н, дд, J=6,8 и 2,0 Гц), 7,1 (2Н, дд, J=6,5 и 1,9 Гц), 7,2 (2Н, дд, J=6,57 и 1,9 Гц), 7,3 (2Н, дд, J=6,8 и 2,0 Гц). - 48 - 008303 Сульфиды, представленные в табл. 13, превращали в соответствующие сульфоксиды в соответствии с методикой, описанной в препаративном примере 2. Таблица 14 Ц р Соединение № Мол.масса Выход(%) 139 Мол.масса=311 Выход(%)=67 ХН: 1,3 (ЗН, т, J=7,6 Гц), 2,7 (ЗН, с), 2,8 (2Н, кв, J=7,6 Гц), 7,2-7,6 (9Н, комплекс). 140 -СН2ОСН3 Мол,масса=327 Выход(%)=72 141 -СНз Мол.масса=315 Выход(%)=87 XH: 2,4 (ЗН, с), 2,7 (ЗН, с), 7,0 (2Н, т, J=8,7 Гц), 7,3 (4Н, м), 7,6 (2Н, д, J=8,4 Гц). 142 -СНз Мол.масса=3 31,5 Выход(%)=7 9 ХН: 2,4 (ЗН, с), 2,7 (ЗН, с), 7,2-7,3 (6Н7 м) , 7,6 (2Н, д, J=8,2 Гц). 143 ^сн3 Мол.масса=311 Выход(%)=71 XH: 1,2 (ЗН, т, J=7,5 Гц), 2,6 (2Н, кв, J=7,5 Гц), 2,8 (ЗН, с), 7,3 (ЗН, м), 7,4 (4Н, м), 7,7 (2Н, д, J=8, 4 Гц) . 144 -С1 Кол.масса=317,5 Выход(%)=51 ХН: 2,7 (ЗН, с), 7,2-7,4 (7Н, комплекс), 7,6 (2Н, Д, 8,3 Гц). 145 -СНз Мол.масса=2 97 Выход(%)=72 XH: 2,5 (ЗН, с), 2,8 (ЗН, с), 7,3-7,4 (7Н, м), 7,6 (2Н, д, J=8,5 Гц). 146 н3С.0ХХ -СН3 Мол,масса=327 Выход(%)=78 XH: 2,5 (ЗН, с), 2,8 (ЗН, с), 3,8 (ЗН, с), 6,8 (2Н, дд, J=6,82 и 2,02 Гц), 7,3 (4Н, м), 7,6 (2Н, д, J=8,3 Гц). - 49 - 008303 Сульфоксиды, представленные в табл. 14, превращали в соответствующие сульфоксимины в соответствии с методикой, описанной в препаративном примере 3. Таблица 15 Соединение № Мол.масса Выход(%) 147 ^СН3 Мол.масса=326 Выход(%)=71 ХН, ДМСО-de: 1,3 (ЗН, т, J=7,6 Гц), 2,8 (2Н, кв, J=7,6 Гц), 3,79 (ЗН, с), 7,4 (5Н, м) , 7,6 (2Н, д, J=8,5 Гц), 8,1 (2Н, д, J=8,5 Гц). 148 -СН2ОСНз Мол.масса=342 Выход(%)=26 ХН, ДМСО-ds: 3,3 (ЗН, с), 3,4 (ЗН, с), 4,5 (2Н, с), 7,4 (5Н, м), 7,5 (2Н, д, J=8,4 Гц), 8,0 (2Н, д, J=8,4 Гц). 149 -СН3 Мол.масса=330 Выход(%)=41 *H: 2,4 (ЗН, с), 2,7 (ЗН, с), 7,0 (2Н, т, J=8,7 Гц), 7,3 (4Н, м) , 7,6 (2Н, д, J=8,4 Гц). 150 СГ ^ -СНз Мол.масса=346, 5 Выход(%)=86 1Е, flMCO-d6: 3,4 (ЗН, с), 3,5 (ЗН, с), 7,3 (2Н, д, J=8,5 Гц), 7,4 (2Н, д, J=8,5 Гц), 7,5 (2Н, д, J=8,4 Гц), 8,0 (2Н, д, J=8,7 Гц). 151 ^СН3 Мол.масса=32 6 Выход(%)=63 *Н, ДМСО-ds: 1,1 (ЗН, т, J=7,5 Гц), 2,6 (2Н, кв, J=7,5 Гц), 3,6 (ЗН, с), 7,4 (5Н, м) , 7,7 (2Н, д, J=8,4 Гц), 8,1 (2Н, д, J=8,4 Гц). 152 -С1 Мол.масса=332,5 Выход(%)=57 ХН, ДМСО-de: 3,3 (ЗН, с), 7,3-7,4 (5Н, м) , 7,5 (2Н, д, J=8,4 Гц), 8,0 (2Н, д, J=8,4 Гц). 153 -СНз Мол,масса=312 Выход(%)=87 XH: 2,5 (ЗН, с), 3,2 (ЗН, с), 7,3-7,4 (7Н, м) , 7,6 (2Н, дд, J=6,7 и 1,8 Гц). - 50 - 008303 154 -СН3 Мол.масса=342 Выход(%)=30,2 ХН: 2,5 (ЗН, с), 3,1 (ЗН, с), 3,8 (ЗН, с), 6,8 (2Н, д, J=8,8 Гц), 7,3 (4Н, м) , 8,0 (2Н, д, J=8,3 Гц). Препаративный пример 10. 5-(4-Метилсульфоксиминилфенил)-1-фенил-3-ттшфторметил-3Н-пиразол (соединение № 155) H3CNP CF, N-N Стадия 1. Получение 5-(4-метилсульфанилфенил)-1-фенил-3-трифторметил-3Н-пиразола. Раствор 4,4,4-трифтор-(4-метилсульфанилфенил)бутан-1,3-диона (3,0 г) и гидрохлорида фе-нилгидразина (1,18 г) в этаноле (20 мл) нагревали при температуре флегмообразования (с обратным холодильником) в течение 7 ч. Растворитель выпаривали и остаток хроматографировали на силика-геле с использованием в качестве элюента 20% этилацетата в петролейном эфире, в результате чего получали 2,25 г продукта (выход = 83%, молекулярная масса = 334) в виде смолы. 1Н-ЯМР: 2,4 (3Н, с), 6,7 (1Н, с), 7,12 (2Н, дд, J=6,3 и 2,3 Гц), 7,15 (2Н, дд, J=6,3 и 2,2 Гц), 7,3 (5Н, м). Стадия 2. Получение 5-(4-метилсульфинилфенил)-1-фенил-3-трифторметил-1Н-пиразола. Указанное в заголовке соединение (1,3 г, выход = 60%, молекулярная масса = 350) получали из 5-(4-метилсульфанилфенил)-1-фенил-3-трифторметил-1Н-пиразола (2,1 г) (полученного в вышеописанной стадии 1) в соответствии с методикой, описанной в препаративном примере 2. 1Н-ЯМР: 2,7 (3Н, с), 6,8 (1Н, с), 7,3 (2Н, дд, J=6,2 и 2,0 Гц), 7,4 (5Н, м), 7,6 (2Н, дд, J=8,2 и 1,6 Гц). Стадия 3. Получение 5-(4-метилсульфоксиминилфенил)-1-фенил-3-трифторметил-1Н-пиразола (соединения № 155). Указанное в заголовке соединение (310 мг, выход = 45%, молекулярная масса = 365) получали из 5-(4-метилсульфинилфенил)-1-фенил-3-трифторметил-1 Н-пиразола (600 мг) (полученного в вышеописанной стадии 2) в соответствии с методикой, описанной в препаративном примере 3. 1Н-ЯМР, CD3OD: 3,8 (3Н, с), 7,17 (1Н, с), 7,3 (2Н, м), 7,4 (3Н, м), 7,7 (2Н, дд, J=8,7 и 1,8 Гц), 8,1 (2Н, дд, J=8,7 и 1,8 Гц). Препаративный пример 11. Гидрохлоридная соль 5-(3-фтор-4-метоксифенил)-1-(4-метил-сульфоксиминилфенил)-3-трифторметил-1Н-пиразол (соединение № 167) Н3сч ,NH.HCI 0 XI К 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразолу (соединению № 74) (500 мг) добавляли метаноловый раствор НС1 (10 мл, 15%) и перемешивали при 25-30°С в течение 0,5 ч. Растворитель выпаривали при пониженном давлении, и остаточное масло перемешивали с диизопропиловым эфиром с получением продукта (440 мг) в виде не совсем белого твердого вещества. Препаративный пример 12. Бисульфатная соль 5-(3-метокси-4-метилфенил)-1-(4-метилсуль-фоксиминилфенил)-3-трифторметил-1Н-пиразола (соединения № 168). H3C^NH.H2S04 - 51 - 008303 К 5-(3 -метокси-4-метилфенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пира-золу (соединению № 75) (120 мг) добавляли охлажденный раствор ацетона (10 мл), содержащий серную кислоту (28 мг), и смесь перемешивали при 0°С в течение 30 мин. Растворитель выпаривали в потоке азота, к остаток перемешивали с диизопропиловым эфиром с получением продукта (75 мг) в виде не совсем белого твердого вещества. Аналогичным образом, соединения, представленные в табл. 16, были получены в соответствии с методикой, описанной в препаративных примерах 11, 12. Таблица 16 Соединение № Свободное основание № Полученная соль Температура плавления (°C) 156 НС1 182 157 НС1 200 158 НС1 171 159 НС1 178 160 НС1 163 161 H2so4 135 162 H2so4 195 163 НС1 150 164 НС1 170 165 НС1 178 166 НС1 170 167 НС1 168 168 H2S04 192 169 НС1 170 НС1 163 171 H2S04 141 172 H2S04 181 173 H2S04 165 174 H2S04 174 175 H2S04 199 176 H2S04 214 177 H2S04 115 178 HC1 168 179 121 HC1 178 - 52 - 008303 180 123 НС1 184 181 124 HC1 170 182 125 HC1 120 183 126 HC1 176 184 147 HC1 166 185 148 HC1 171 186 149 HC1 169 187 151 HC1 169 188 152 HC1 158 189 153 HC1 168 190 155 HC1 153 * Температуры плавления являются некоррелированными и могут варьировать в пределах ±4°С. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I), где G представляет собой группы А, В, С, D, Е или F, описанные ниже: D Е F где R1 представляет собой водород, ацильную, галогенацильную группу; R2 представляет собой (^-С^алкил; X1, X2, Х3, Х4 могут быть одинаковыми или различными и представляют собой водород или галоген; и если G представляет собой гетероцикл "D", то по меньшей мере одна из групп, определенных как X1, X2, Х3, Х4, не является водородом; R3 выбран из замещенных или незамещенных арильных или гетероарильных групп, где заместители арильных групп выбраны из галогена, нитро, гидроксила, (C1-C3)алкила, (^-^^люкси, гидрокси (C1-C3)алкокси, а заместители гетероарильных групп выбраны из (C1-C3)алкильных групп; R4 выбран из атома водорода, атома галогена, карбокси, прямой или разветвленной (C1-С3)алкильной, гидрокси(C1-C3)алкильной, алкокси (C1-C3)алкильной, галоген(C1-C3)алкильной и фенильной групп, и R5 представляет собой водород; Y представляет собой О; W представляет собой О или S; его таутомеры, фармацевтически приемлемые соли и сольваты. 2. Соединение по п.1, где указанными фармацевтически приемлемыми солями являются соли винной кислоты, миндальной кислоты, фумаровой кислоты, яблочной кислоты, молочной кислоты, малеиновой кислоты, салициловой кислоты, лимонной кислоты, аскорбиновой кислоты, бензол-сульфоновой кислоты, п-толуолсульфоновой кислоты, гидроксинафтойной кислоты, метансульфо-новой кислоты, уксусной кислоты, бензойной кислоты, янтарной кислоты, пальмитиновой кислоты, хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты и азотной кислоты. 3. Фармацевтическая композиция, содержащая соединения по п.1 или их фармацевтически приемлемые соли или сольваты и фармацевтически приемлемый носитель, разбавитель, наполнитель. 4. Фармацевтическая композиция по п.3 в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. - 53 - 008303 5. Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение по п.2 или его сольват и фармацевтически приемлемый носитель, разбавитель, наполнитель. 6. Фармацевтическая композиция по п.5, содержащая соединение по п.2 и изготовленная в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 7. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли. 8. Способ по п.7, где указанное соединение вводят перорально, интраназально, парентерально, местно, чрескожно или ректально. 9. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.2. 10. Способ по п.9, где указанное соединение вводят перорально, интраназально, парентерально, местно, чрескожно или ректально. 11. Соединение по п.1, выбранное из 5-(4-фторфенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-хлорфенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метилфенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-н-пропоксифенил)-3-трифторметил-1Н-пиразола; 5-(4-этоксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-гидроксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-хлор-4-фторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3,4-дифторфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-фтор-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(4-метокси-3-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-хлор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-бром-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-фтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3-метокси-4-метилфенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(2-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразола; 1-(3-фтор-4-метилсульфоксиминилфенил)-5-(4-метоксифенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-фенил-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-( 1-нафтил)-3-трифторметил-1Н-пиразола; 5-(4-метоксифенил)-3 -метил-1 -(4-метилсульфоксиминилфенил)-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-нитрофенил)-3-трифторметил-1Н-пиразола; 5-(3-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3,5-дифтор-4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-(3 -гидрокси-4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-3-трифторметил-1Н- пиразола; 5-(4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-1Н-пиразол-3 -карбоновой кислоты; 3-(гидроксиметил)-5-(4-метоксифенил)-1-(4-метилсульфоксиминилфенил)-1Н-пиразола; 5-(4-метоксифенил)-1 -(4-метилсульфоксиминилфенил)-1Н-пиразол-3 -илметилгидросульфата; 5-{4-(2-гидроксиэтокси)фенил}-1-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(4-пиридил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(3-пиридил)-3-трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(2-пиридил)-3-трифторметил-1Н-пиразола; 5-(4-изопропоксифенил)-1 -(4-метилсульфоксиминилфенил)-3 -трифторметил-1Н-пиразола; 1-(4-метилсульфоксиминилфенил)-5-(2-тиофенил)-3-трифторметил-1Н-пиразола; 5-(4-метилсульфоксиминилфенил)-1-фенил-3-трифторметил-1 Н-пиразола; 1-(4-метоксифенил)-5-(4-метилсульфоксиминилфенил)-3-трифторметил-1Н-пиразола; 5-этил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 5-метоксиметил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 3-(4-фторфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-(4-хлорфенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-этил-4-(4-метилсульфоксиминилфенил)-5-фенилизоксазола; 5-хлор-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; - 54 - 008303 5-метил-4-(4-метилсульфоксиминилфенил)-3-фенилизоксазола; 3-(4-метоксифенил)-5-метил-4-(4-метилсульфоксиминилфенил)изоксазола; 3-(3,4-дихлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-хлорфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-фенил-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(3,4-дифторфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(3,4-диметоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-метоксифенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 3-(4-метилфенил)-4-(3-фтор-4-метилсульфоксиминилфенил)-5Н-фуран-2-она; 5-хлор-3-(4-метилсульфоксиминилфенил)-6'-метил [2,3'] бипиридинила; 5-хлор-3-(4-метилсульфоксиминилфенил)- [2,3'] бипиридинила; 3-(3-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-она; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-(4-метилсульфоксиминилфенил)-3Н-тиазол-2-она; 3-(2-фторфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 3- (4-бромфенил)-4-(4-метилсульфоксиминилфенил)-3Н-оксазол-2-она; 4- (4-метилсульфоксиминилфенил)-3-фенил-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(К-хлорацетил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(К-ацетил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(К-метилсульфонил)метилсульфоксиминилфенил]-3Н-оксазол-2-она; 3-(3,4-дихлорфенил)-4-[4-(К-(4-метилфенил)сульфонил}метилсульфоксиминилфенил]-3Н-оксазол-2-она. 12. Соединение по п.11, где указанными фармацевтически приемлемыми солями являются соли винной кислоты, миндальной кислоты, фумаровой кислоты, яблочной кислоты, молочной кислоты, малеиновой кислоты, салициловой кислоты, лимонной кислоты, аскорбиновой кислоты, бензол-сульфоновой кислоты, п-толуолсульфоновой кислоты, гидроксинафтойной кислоты, метансульфо-новой кислоты, уксусной кислоты, бензойной кислоты, янтарной кислоты, пальмитиновой кислоты, хлористо-водородной кислоты, бромисто-водородной кислоты, серной кислоты и азотной кислоты. 13. Фармацевтическая композиция, содержащая соединение по п.11 или 12 или его сольват и фармацевтически приемлемый носитель, разбавитель, наполнитель. 14. Фармацевтическая композиция по п.13 в форме таблетки, капсулы, порошка, гранул, сиропа, раствора или суспензии. 15. Способ лечения воспаления или ассоциированного с воспалением расстройства у индивидуума, где указанный способ включает лечение индивидуума, страдающего указанным расстройством или восприимчивого к указанному расстройству, путем введения указанному индивидууму терапевтически эффективного количества соединения по п.11-12 или его фармацевтически приемлемой соли. 16. Применение соединения по пп.1-2 и 11-12 для лечения воспалений и ассоциированных с воспалением заболеваний. 17. Способ получения соединений формулы (I) G представляет собой группы А, В, С, D, Е или F, описанные ниже: С = 008303 Хь X2, Х3, Х4 могут быть одинаковыми или различными и представляют собой водород или галоген; и если G представляет собой гетероцикл D, то по меньшей мере одна из групп, определенных как Х\, Х2, Х3, Х4, не является водородом; R3 выбран из замещенных или незамещенных арильных или гетероарильных групп, где заместители арильных групп выбраны из галогена, нитро, гидроксила, (С1-С3)алкила, (СгС3)алкокси, гидрокси(СгС3)алкокси, а заместители гетероарильных групп выбраны из (С1-С3)алкильн^1х групп; R4 выбран из атома водорода, атома галогена, карбокси, прямой или разветвленной (С1-С3)ал-кильной, гидрокси(С1-С3)алкильной, алкокси(С1-С3)алкильной, галоген(С1-С3)алкильной и фениль-ной групп, и R5 представляет собой водород; Y представляет собой О; W представляет собой О или S; и где указанный способ предусматривает окисление соединения формулы (Р) с получением соединения формулы (Q), которое подвергают иминированию подходящими реагентами и получают соединение формулы (I), которое может быть затем, если это необходимо, превращено в его фармацевтически приемлемые соли. Х2 Й X;, R'NN4//0X2 R/SX^XX1 °кисление. R2'sXjX*1 иминирование- R/Sx!XXl Х4 ^ Х4 Х4 (р) (Q) U) 18. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой R3 Y Y а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия галогенкетона формулы (II) с соединением формулы (III) с получением меркапто-соединения формулы (P) + X -^ Л (P) 19. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой а все остальные символы являются такими, как они были определены выше, включающий превращение оксима формулы (VII) в меркапто-соединение формулы (Р) (VD) (Р) 20. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой - 56 - 008303 XN-N а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия гидразина формулы (XI) с 1,3-дикетоном формулы (XII) с получением меркапто-соединения формулы (Р) х/у^Гтг к/у^ъ хЛА Х4 Вое ЕЦ 3 1 (XI) (ХН) (р) 21. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой -R4 а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия соединения формулы (XVII) с соединением формулы (XVIII) с получением меркапто-соединения формулы (Р) Х2 Х2 R2~S\Z^s_-X, 9 R2-Sv^L^X, (XVII) (XVDI) (Р) 22. Способ получения соединения общей формулы (Р) указанного в п.17, где G представляет собой N-N F а все остальные символы являются такими, как они были определены выше, включающий проведение реакции взаимодействия соединения формулы (XXI) с соединением формулы (XXII) с получением меркапто-соединения формулы (Р) HN-MH2 x2^f^f^G (ХХП) R2-sX|AX4 (P) ^^) Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6 - 57 - 
|