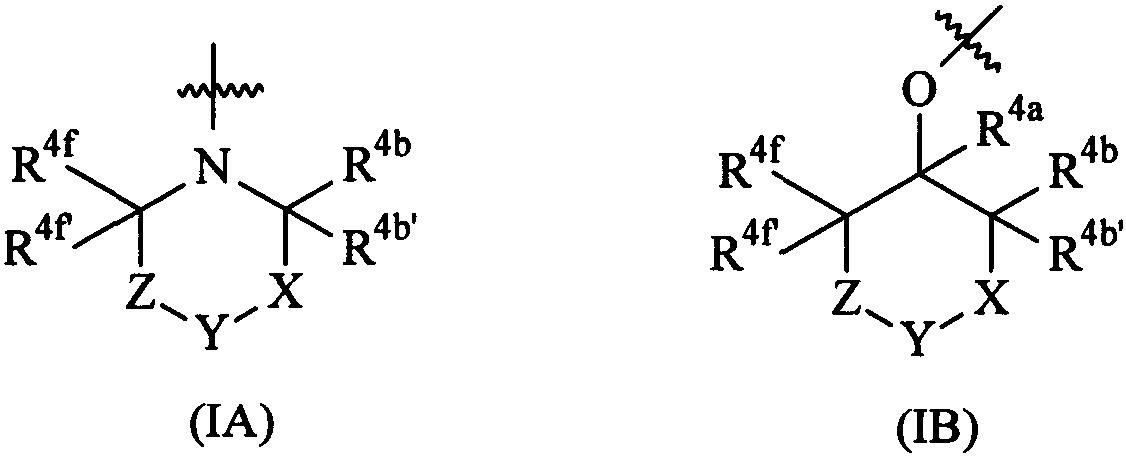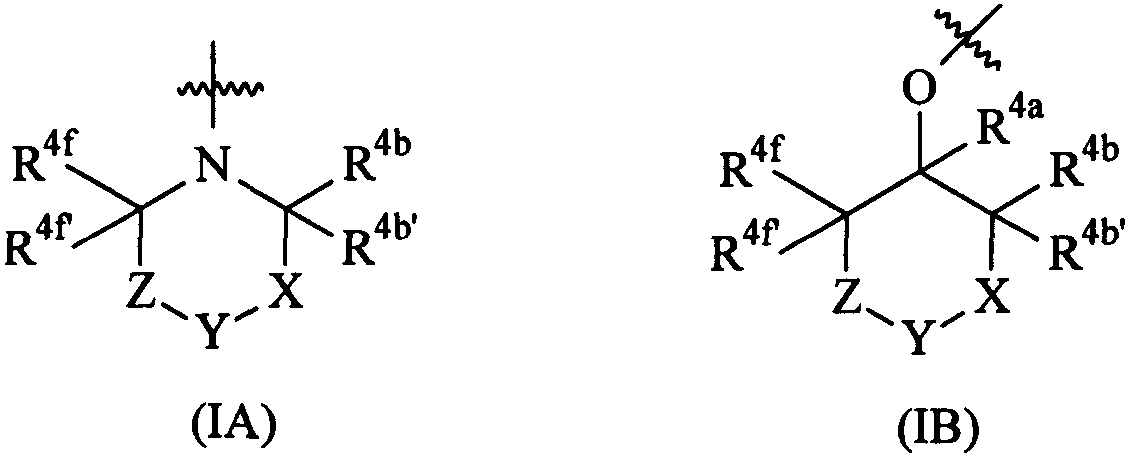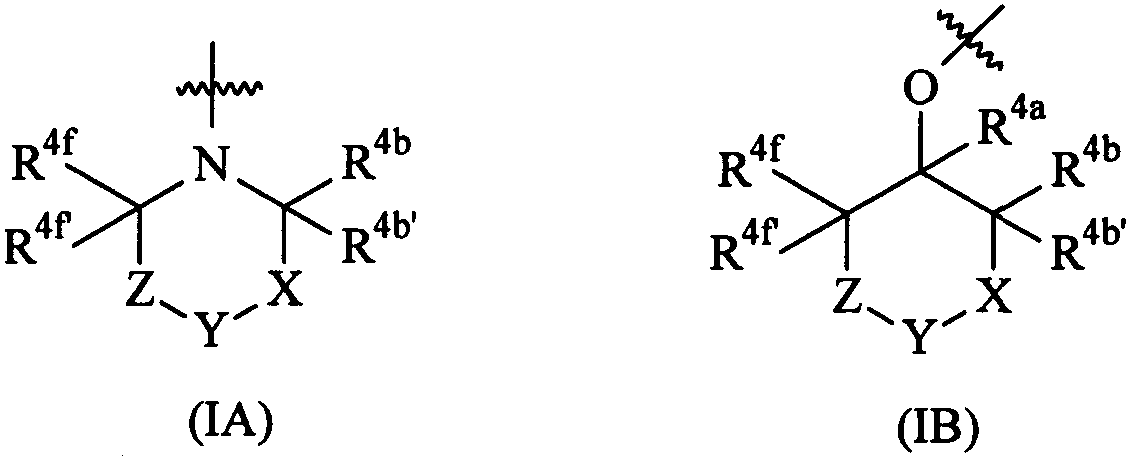|
Патентная документация ЕАПВ |
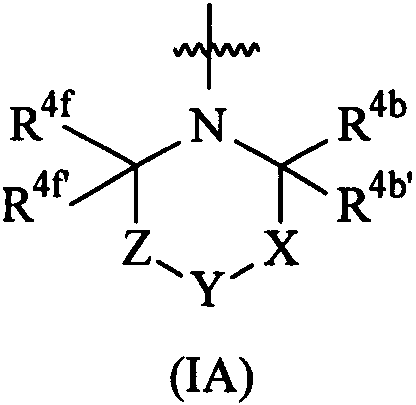
|
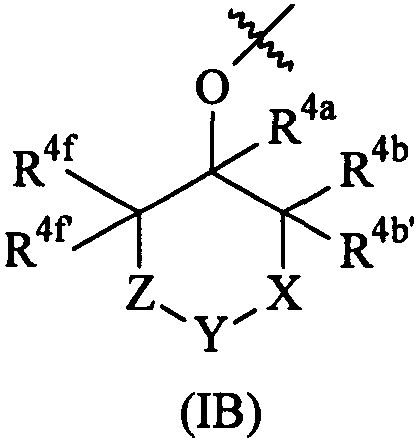
||
| Запрос: | ea000008176b*\id |
|
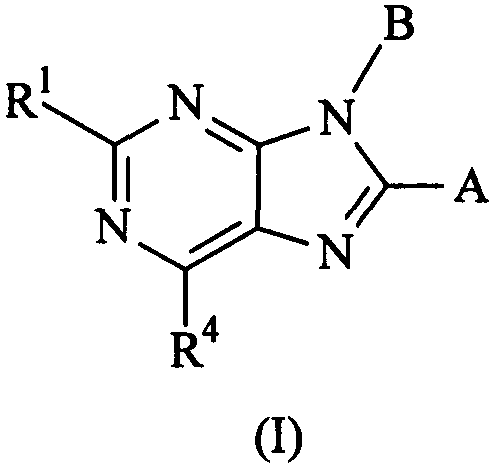
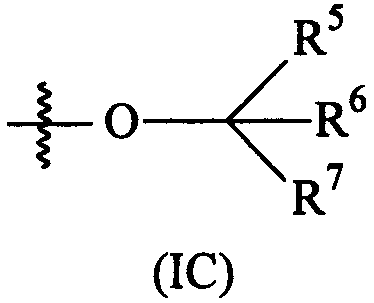
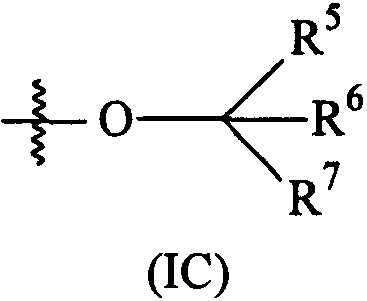
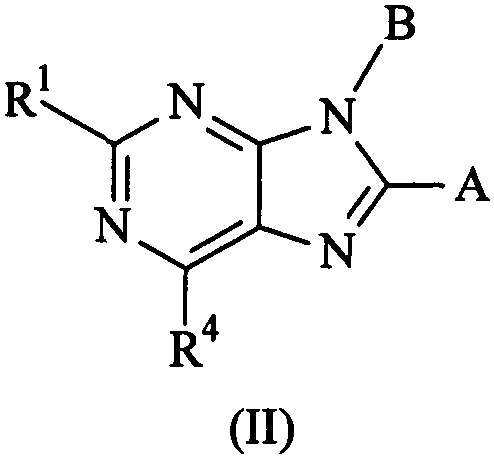
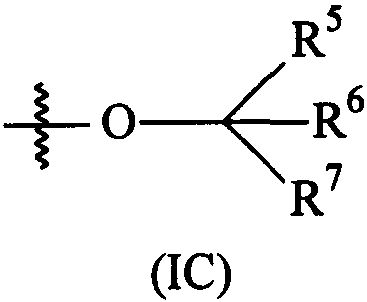
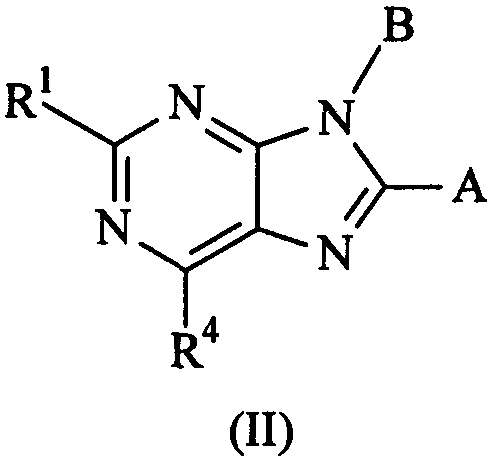
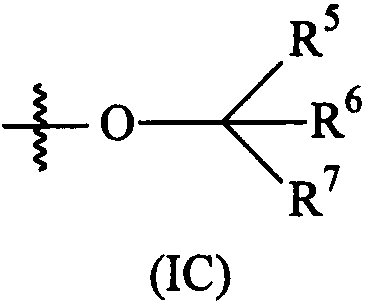
Термины запроса в документе Реферат 1. Соединение формулы (I) где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси; R 4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB) где R 4a представляет собой водород или (С 1 -С 3 )алкил; R 4b и R 4b' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4b , либо R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NC(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)-, -C(=N-OH)- или -C(R 4d )(R 4d' )-, где R 4d и R 4d' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-С(О)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, HO-NH-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; и R 4f и R 4f' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4f , либо R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; при условии, что когда R 4 представляет собой группу формулы (IA), тогда (а) по меньшей мере один из R 4b , R 4b' , R 4c , R 4c' , R 4d , R 4d' , R 4d" , R 4e , R 4e' , R 4f и R 4f' является иным, чем водород, (С 1 -С 4 )алкил или галогенозамещенный (С 1 -С 4 )алкил; и (б) Y не представляет собой кислород, серу или -NH-, когда X и Z представляют собой связь, -СН 2 - или -СН 2 СН 2 -, и R 4b , R 4b' , R 4f и R 4f' представляют собой водород; или (2) группу, имеющую формулу (IС) где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (C 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 5 и R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 2. Соединение по п.1, где R 4 представляет собой группу, имеющую формулу (IA) где R 4b и R 4b' , каждый независимо, представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4b или R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик, и R 4c' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 Н-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, и R 4d' представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик, и R 4е' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NH-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик, и R 4f и R 4f' , каждый независимо, представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4f или R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 3. Соединение по п.1, где R 4 представляет собой группу формулы (IB) где R 4a такой, как определено в п.1; R 4b представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, R 4b' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4b или R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик, и R 4c' представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d представляет собой водород, циано, гидрокси, амино, Н 2 NC(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-О-С(О)-, (С 1 -С 4 )алкил-NH-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, и R 4d' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы; Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик, и R 4e' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; R 4f представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена; и R 4f' представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4f или R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 4. Соединение по пп.1, 2 или 3, где X представляет собой -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, H 2 NC(O)-, возможно замещенный (С 1 -С 6 )алкил, (C 1 -С 4 )алкил-NH-С(O)- или ((C 1 -C 4 )алкил) 2 N-C(O)-, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонила, (С 1 -С 3 )алкиламиносульфонила, ди(С 1 -С 3 )алкиламиносульфонила, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, H 2 NC(O)-, возможно замещенный (С 1 -С 6 )алкил, (С 1 -С 4 )алкил-NН-С(O)- или ((C 1 -C 4 )алкил) 2 N-C(O)-, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 5. Соединение по пп.1, 2 или 3, где Y представляет собой -C(R 4d )(R 4d' )-, где R 4d представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, R 4d' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 6. Соединение по п.5, где R 4b , R 4b' , R 4f и R 4f' , все представляют собой водород; и R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо или указанное лактамовое кольцо возможно содержит дополнительный гетероатом, выбранный из кислорода, азота или серы; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 7. Соединение по п.1, где R 4 представляет собой группу, имеющую формулу (IС), где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (С 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 5 и R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 8. Соединение по любому из пп.1-7, где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С 1 -С 4 )алкокси, (С 1 -С 4 )алкила, галогенозамещенного (С 1 -С 4 )алкила и циано; его фармацевтически приемлемая соль или сольват или гидрат указанного соединения или указанной соли. 9. Соединение по п.1, выбранное из группы, состоящей из 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиридин-2-илпиперазин-1-ил)-9Н-пурина; 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиримидин-2-илпиперазин-1-ил)-9Н-пурина; 4-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-2-карбоновой кислоты метиламида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-этиламиноазетидин-3-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-изопропиламиноазетидин-3-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-2-метил-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-кар-боновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-пирролидин-1-илпиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амида; 4-амино-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-карбоновой кислоты амида; 1-{1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ил}этанона; {3-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1 a ,5 a ,6 a )азабицикло[3,1,0]гекс-6-ил}диметиламина; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-(4-фторфенил)пиперидин-4-ола; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ола; 4-бензил-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-ола; 8-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4-она; 8-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4-она; 9-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-метил-4-окса-1,9-диазаспиро[5,5]ундекан-2-она; 6-(1-бензилпирролидин-3-илокси)-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина; 9-(4-хлорфенил)-6-(1-циклогексилазетидин-3-илокси)-8-(2,4-дихлорфенил)-9Н-пурина; 6-трет-бутокси-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина; и 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-изопропокси-9Н-пурина; их фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли. 10. Соединение, представляющее собой 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амид или его фармацевтически приемлемую соль. 11. Соединение по п.10, где фармацевтически приемлемая соль выбрана из солей гидрохлорид, мезилат и безилат. 12. Фармацевтическая композиция, содержащая (1) соединение по любому из пп.1-11, фармацевтически приемлемую соль указанного соединения или сольват или гидрат указанного соединения или указанной соли; и (2) фармацевтически приемлемый эксципиент, разбавитель или носитель. 13. Фармацевтическая композиция по п.12, дополнительно содержащая по меньшей мере один дополнительный фармацевтический агент, выбранный из частичного агониста никотинового рецептора, антагониста опиоида, допаминергического агента, агента против ADHD или агента против ожирения. 14. Соединение формулы (1c/d) где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С 1 -С 4 )алкокси, (С 1 -С 4 )алкила, галогенозамещенного (С 1 -С 4 )алкила и циано; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкок-си; и R 4 представляет собой гидрокси или галогено. 15. Соединение формулы (1b) где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С 1 -С 4 )алкокси, (С 1 -С 4 )алкила, галогенозамещенного (С 1 -С 4 )алкила и циано; и R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси. 16. Способ лечения заболевания, состояния или расстройства, которое модулируется антагонистом каннабиноидного рецептора, у животных, включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (II) где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси; R 4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), где R 4a представляет собой водород или (С 1 -С 3 )алкил; R 4b и R 4b' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4b , либо R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )цикло-алкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d и R 4d' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )цик-лоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; и R 4f и R 4f' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(N)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4f , либо R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; или (2) группу, имеющую формулу (IС), где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (С 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 5 и R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; (3) аминогруппу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из (С 1 -С 8 )алкила, фенил(С 1 -С 4 )алкила, частично или полностью насыщенного (С 3 -С 8 )циклоалкила, гидрокси(С 1 -С 6 )алкила, (С 1 -С 3 )алкокси(С 1 -С 6 )алкила, гетероарил(С 1 -С 3 )алкила и частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; или (4) (С 1 -С 6 )алкильную группу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из гидрокси, (С 1 -С 6 )алкокси, амино, (С 1 -С 6 )алкиламино, ди((С 1 -С 6 )алкил)амино, (С 1 -С 3 )алкилсульфонила, (С 1 -С 3 )алкилсульфамида, ди((С 1 -С 3 )алкил)сульфамила, ацилокси, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного циклоалкила; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли. 17. Применение соединения формулы (II) в производстве лекарства для лечения заболевания, состояния или расстройства, которое модулируется антагонистом каннабиноидного рецептора, где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси; R 4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), где R 4a представляет собой водород или (С 1 -С 3 )алкил; R 4b и R 4b' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4b , либо R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NC(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d и R 4d' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 Н-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; и R 4f и R 4f' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 Н-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4f , либо R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; или (2) группу, имеющую формулу (IС), где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (С 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; (3) аминогруппу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из (С 1 -С 8 )алкила, фенил(С 1 -С 4 )алкила, частично или полностью насыщенного (С 3 -С 8 )циклоалкила, гидрокси(С 1 -С 6 )алкила, (С 1 -С 3 )алкокси(С 1 -С 6 )алкила, гетероарил(С 1 -С 3 )алкила и частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; или (4) (С 1 -С 6 )алкильную группу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из гидрокси, (С 1 -С 6 )алкокси, амино, (С 1 -С 6 )алкиламино, ди((С 1 -С 6 )алкил)амино, (C 1 -С 3 )алкилсульфонила, (С 1 -С 3 )алкилсульфамила, ди((С 1 -С 3 )алкил)сульфамила, ацилокси, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного циклоалкила; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемой соли. или сольвата, или гидрата указанного соединения или указанной соли.
Полный текст патента (57) Реферат / Формула: где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси; R 4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB) где R 4a представляет собой водород или (С 1 -С 3 )алкил; R 4b и R 4b' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4b , либо R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NC(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)-, -C(=N-OH)- или -C(R 4d )(R 4d' )-, где R 4d и R 4d' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-С(О)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, HO-NH-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; и R 4f и R 4f' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4f , либо R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; при условии, что когда R 4 представляет собой группу формулы (IA), тогда (а) по меньшей мере один из R 4b , R 4b' , R 4c , R 4c' , R 4d , R 4d' , R 4d" , R 4e , R 4e' , R 4f и R 4f' является иным, чем водород, (С 1 -С 4 )алкил или галогенозамещенный (С 1 -С 4 )алкил; и (б) Y не представляет собой кислород, серу или -NH-, когда X и Z представляют собой связь, -СН 2 - или -СН 2 СН 2 -, и R 4b , R 4b' , R 4f и R 4f' представляют собой водород; или (2) группу, имеющую формулу (IС) где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (C 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 5 и R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 2. Соединение по п.1, где R 4 представляет собой группу, имеющую формулу (IA) где R 4b и R 4b' , каждый независимо, представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4b или R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик, и R 4c' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 Н-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, и R 4d' представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик, и R 4е' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NH-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик, и R 4f и R 4f' , каждый независимо, представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4f или R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 3. Соединение по п.1, где R 4 представляет собой группу формулы (IB) где R 4a такой, как определено в п.1; R 4b представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, R 4b' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4b или R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик, и R 4c' представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d представляет собой водород, циано, гидрокси, амино, Н 2 NC(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-О-С(О)-, (С 1 -С 4 )алкил-NH-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, и R 4d' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы; Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (C 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик, и R 4e' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; R 4f представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена; и R 4f' представляет собой водород, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4f или R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 4. Соединение по пп.1, 2 или 3, где X представляет собой -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, H 2 NC(O)-, возможно замещенный (С 1 -С 6 )алкил, (C 1 -С 4 )алкил-NH-С(O)- или ((C 1 -C 4 )алкил) 2 N-C(O)-, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонила, (С 1 -С 3 )алкиламиносульфонила, ди(С 1 -С 3 )алкиламиносульфонила, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, H 2 NC(O)-, возможно замещенный (С 1 -С 6 )алкил, (С 1 -С 4 )алкил-NН-С(O)- или ((C 1 -C 4 )алкил) 2 N-C(O)-, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 5. Соединение по пп.1, 2 или 3, где Y представляет собой -C(R 4d )(R 4d' )-, где R 4d представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, R 4d' представляет собой водород, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 6. Соединение по п.5, где R 4b , R 4b' , R 4f и R 4f' , все представляют собой водород; и R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо или указанное лактамовое кольцо возможно содержит дополнительный гетероатом, выбранный из кислорода, азота или серы; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 7. Соединение по п.1, где R 4 представляет собой группу, имеющую формулу (IС), где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (С 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 5 и R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 8. Соединение по любому из пп.1-7, где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С 1 -С 4 )алкокси, (С 1 -С 4 )алкила, галогенозамещенного (С 1 -С 4 )алкила и циано; его фармацевтически приемлемая соль или сольват или гидрат указанного соединения или указанной соли. 9. Соединение по п.1, выбранное из группы, состоящей из 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиридин-2-илпиперазин-1-ил)-9Н-пурина; 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиримидин-2-илпиперазин-1-ил)-9Н-пурина; 4-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-2-карбоновой кислоты метиламида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-этиламиноазетидин-3-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-изопропиламиноазетидин-3-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-2-метил-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-кар-боновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-пирролидин-1-илпиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амида; 4-амино-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-карбоновой кислоты амида; 1-{1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ил}этанона; {3-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1 a ,5 a ,6 a )азабицикло[3,1,0]гекс-6-ил}диметиламина; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-(4-фторфенил)пиперидин-4-ола; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ола; 4-бензил-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-ола; 8-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4-она; 8-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4-она; 9-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-метил-4-окса-1,9-диазаспиро[5,5]ундекан-2-она; 6-(1-бензилпирролидин-3-илокси)-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина; 9-(4-хлорфенил)-6-(1-циклогексилазетидин-3-илокси)-8-(2,4-дихлорфенил)-9Н-пурина; 6-трет-бутокси-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина; и 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-изопропокси-9Н-пурина; их фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли. 10. Соединение, представляющее собой 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амид или его фармацевтически приемлемую соль. 11. Соединение по п.10, где фармацевтически приемлемая соль выбрана из солей гидрохлорид, мезилат и безилат. 12. Фармацевтическая композиция, содержащая (1) соединение по любому из пп.1-11, фармацевтически приемлемую соль указанного соединения или сольват или гидрат указанного соединения или указанной соли; и (2) фармацевтически приемлемый эксципиент, разбавитель или носитель. 13. Фармацевтическая композиция по п.12, дополнительно содержащая по меньшей мере один дополнительный фармацевтический агент, выбранный из частичного агониста никотинового рецептора, антагониста опиоида, допаминергического агента, агента против ADHD или агента против ожирения. 14. Соединение формулы (1c/d) где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С 1 -С 4 )алкокси, (С 1 -С 4 )алкила, галогенозамещенного (С 1 -С 4 )алкила и циано; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкок-си; и R 4 представляет собой гидрокси или галогено. 15. Соединение формулы (1b) где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С 1 -С 4 )алкокси, (С 1 -С 4 )алкила, галогенозамещенного (С 1 -С 4 )алкила и циано; и R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси. 16. Способ лечения заболевания, состояния или расстройства, которое модулируется антагонистом каннабиноидного рецептора, у животных, включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (II) где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси; R 4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), где R 4a представляет собой водород или (С 1 -С 3 )алкил; R 4b и R 4b' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4b , либо R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )цикло-алкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d и R 4d' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-С(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )цик-лоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; и R 4f и R 4f' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 N-С(N)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4f , либо R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; или (2) группу, имеющую формулу (IС), где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (С 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 5 и R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; (3) аминогруппу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из (С 1 -С 8 )алкила, фенил(С 1 -С 4 )алкила, частично или полностью насыщенного (С 3 -С 8 )циклоалкила, гидрокси(С 1 -С 6 )алкила, (С 1 -С 3 )алкокси(С 1 -С 6 )алкила, гетероарил(С 1 -С 3 )алкила и частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; или (4) (С 1 -С 6 )алкильную группу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из гидрокси, (С 1 -С 6 )алкокси, амино, (С 1 -С 6 )алкиламино, ди((С 1 -С 6 )алкил)амино, (С 1 -С 3 )алкилсульфонила, (С 1 -С 3 )алкилсульфамида, ди((С 1 -С 3 )алкил)сульфамила, ацилокси, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного циклоалкила; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли. 17. Применение соединения формулы (II) в производстве лекарства для лечения заболевания, состояния или расстройства, которое модулируется антагонистом каннабиноидного рецептора, где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R 1 представляет собой водород, (С 1 -С 4 )алкил, галогенозамещенный (С 1 -С 4 )алкил или (С 1 -С 4 )алкокси; R 4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), где R 4a представляет собой водород или (С 1 -С 3 )алкил; R 4b и R 4b' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((C 1 -C 4 )алкил) 2 N-C(O)-, (С 1 -С 6 )алкиламино-, ((С 1 -С 4 )алкил) 2 амино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4b , либо R 4b' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН 2 СН 2 - или -C(R 4c )(R 4c' )-, где R 4c и R 4c' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NC(О)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (C 1 -C 4 )алкил-NH-C(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4c , либо R 4c' , взятый вместе с R 4e , R 4e' , R 4f или R 4f' , образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R 4d )(R 4d' )-, где R 4d и R 4d' , каждый независимо, представляет собой водород, циано, гидрокси, амино, Н 2 NС(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 Н-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R 4d и R 4d' , взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR 4d" -, где R 4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 3 -С 6 )циклоалкила, (С 1 -С 3 )алкилсульфонил-, (С 1 -С 3 )алкиламиносульфонил-, ди(С 1 -С 3 )алкиламиносульфонил-, ацила, (С 1 -С 6 )алкил-O-С(O)-, фенила и гетероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН 2 СН 2 - или -C(R 4e )(R 4e' )-, где R 4e и R 4e' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NН-С(O)-, ((C 1 -С 4 )алкил) 2 N-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4e , либо R 4e' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; и R 4f и R 4f' , каждый независимо, представляет собой водород, циано, гидрокси, амино, H 2 NC(O)- или химическую группировку, выбранную из группы, состоящей из (С 1 -С 6 )алкила, (С 1 -С 6 )алкокси, ацилокси, ацила, (С 1 -С 3 )алкил-O-С(O)-, (С 1 -С 4 )алкил-NH-C(O)-, ((С 1 -С 4 )алкил) 2 Н-С(O)-, (С 1 -С 6 )алкиламино-, ди(С 1 -С 4 )алкиламино-, (С 3 -С 6 )циклоалкиламино-, ациламино-, фенил(С 1 -С 4 )алкиламино-, гетероарил(С 1 -С 4 )алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R 4f , либо R 4f' , взятый вместе с R 4b , R 4b' , R 4c или R 4c' , образует связь, метиленовый мостик или этиленовый мостик; или (2) группу, имеющую формулу (IС), где R 5 и R 6 , каждый независимо, представляет собой водород или (С 1 -С 4 )алкил, и R 7 представляет собой (С 1 -С 4 )алкил-, галогенозамещенный (С 1 -С 4 )алкил-, (С 1 -С 4 )алкокси(С 1 -С 4 )алкил-, (С 1 -С 4 )алкиламино(С 1 -С 4 )алкил-, ди(С 1 -С 4 )алкиламино(С 1 -С 4 )алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R 5 и R 6 или R 7 , взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; (3) аминогруппу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из (С 1 -С 8 )алкила, фенил(С 1 -С 4 )алкила, частично или полностью насыщенного (С 3 -С 8 )циклоалкила, гидрокси(С 1 -С 6 )алкила, (С 1 -С 3 )алкокси(С 1 -С 6 )алкила, гетероарил(С 1 -С 3 )алкила и частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; или (4) (С 1 -С 6 )алкильную группу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из гидрокси, (С 1 -С 6 )алкокси, амино, (С 1 -С 6 )алкиламино, ди((С 1 -С 6 )алкил)амино, (C 1 -С 3 )алкилсульфонила, (С 1 -С 3 )алкилсульфамила, ди((С 1 -С 3 )алкил)сульфамила, ацилокси, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного циклоалкила; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемой соли. или сольвата, или гидрата указанного соединения или указанной соли.
008176 Область изобретения Настоящее изобретение относится к пуриновым соединениям и промежуточным соединениям, полезным в синтезе пуриновых соединений. Пуриновые соединения полезны в качестве лигандов каннаби-ноидных рецепторов, в частности в качестве антагонистов СВ-1 рецепторов. В результате, настоящее изобретение также относится к применению пуриновых соединений в лечении заболеваний, состояний и расстройств, которые модулируются лигандами каннабиноидных рецепторов, включая фармацевтические композиции для такого применения. Предшествующий уровень техники Ожирение вызывает большую озабоченность здравоохранения из-за его широкой распространенности и связанным с ним риском для здоровья. Как правило, ожирение и избыточный вес определяют по индексу массы тела (BMI), который коррелирует с общей тучностью организма и дает оценку относительного риска заболевания. BMI рассчитывают как массу в килограммах, деленную на рост в метрах в квадрате (кг/м2). Избыточный вес обычно определяют, когда BMI составляет 25-29,9 кг/м2, а ожирение обычно определяют, когда BMI составляет 30 кг/м2 (см., например, National Heart, Lung, and Blood Institute, Clinical Guidelines on the Identification, Evaluation, and Treatment of Overweight and Obesity in Adults (Национальный институт сердца, легких и крови, Клиническое руководство по идентификации, оценке и лечению избыточного веса и ожирения у взрослых), The Evidence Report, Washington, DC: U.S. Department of Health and Human Services, NIH publication no. 98-4083 (1998)). Рост случаев ожирения вызывает беспокойство из-за чрезмерного риска для здоровья, связанного с ожирением, включая ишемическую болезнь сердца, инсульты, гипертензию, сахарный диабет 2 типа, дислипидемию, приступы апноэ во сне, остеоартрит, заболевание желчного пузыря, депрессию и некоторые формы рака (например, рака эндометрия, молочной железы, предстательной железы и толстой кишки). Негативные в отношении здоровья последствия ожирения делают его второй лидирующей причиной предотвратимой смерти в Соединенный Штатах и оказывают значительное экономическое и психосоциальное воздействие на общество (см. McGinnis M., Foege W.H., "Actual Causes of Death in the United States", JAMA, 270, 2207-12 (1993)). В настоящее время ожирение признано хроническим заболеванием, которое требует лечения с целью понижения связанного с ним риска для здоровья. Несмотря на то, что уменьшение массы представляет собой важный результат лечения, одна из главных задач лечения ожирения заключается в улучшении сердечно-сосудистых и метаболических показателей с целью снижения связанных с ожирением заболеваемости и смертности. Было показано, что уменьшение массы тела на 5-10% может значительно улучшить метаболические показатели, такие как содержание глюкозы в крови, кровяное давление и концентрация липидов. Поэтому считается, что преднамеренное уменьшение массы тела на 5-10% может понизить заболеваемость и смертность. Доступные в настоящее время отпускаемые по рецепту лекарственные средства для лечения ожирения, как правило, снижают массу путем стимулирования насыщения или уменьшения всасывания пищевых жиров. Насыщение достигается путем увеличения синаптических уровней норэпинефрина, серотонина или их обоих. Например, стимулирование серотониновых рецепторов подтипов 1B, 1D и 2С и 1- и 2-адренерги-ческих рецепторов уменьшает всасывание пищи посредством регулирования насыщения (см. Bray G.A., "The New Era of Drug Treatment. Pharmacologic Treatment of Obesity: Symposium Overview", Obes. Res., 3 (suppl. 4), 415s-7s (1995)). Адренергические агенты (например, диэтилпропион, бензфетамин, фендимет-разин, мазиндол и фентермин) действуют путем модулирования норэпинефриновых и допаминовых рецепторов центральной нервной системы посредством стимулирования высвобождения катехоламина. Более ранние адренергические лекарства для снижения массы (например, амфетамин, метамфетамин и фенметразин), которые в значительной степени затрагивают пути метаболизма допамина, более не рекомендуются из-за риска привыкания к ним. Фенфлурамин и дексфенфлурамин, оба серотонинергических агента, которые применялись для регулирования аппетита, более не допускаются для использования. Совсем недавно антагонисты/обратные агонисты каннабиноидных СВ1 рецепторов были предложены в качестве потенциальных средств, подавляющих аппетит (см., например, Аните, М., et al., "Selective Inhibition of Sucrose and Ethanol Intake by SR141716, an Antagonist of Central Cannabinoid (CB1) Receptors", Psychopharmacol., 132, 104-106 (1997); Colombo, G., et al., "Appetite Suppression and Weight Loss after the Cannabinoid Antagonist SR141716", Life Sci., 63, PL113-PL117 (1998); Simiand, J., et al., "SR141716, a CB1 Cannabinoid Receptor Antagonist, Selectively Reduces Sweet Food Intake in Marmose", Behav. Pharmacol., 9, 179-181 (1998); и Chaperon, F., et al., "Involvement of Central Cannabinoid (CB1) Receptors in the Establishment of Place Conditioning in Rats", Psvchopharmacology, 135, 324-332 (1998). Обзор модуляторов каннабиноидных рецепторов СВ1 и СВ2 см. в Pertwee, R.G., "Cannabinoid Receptor Ligands: Clinical and Neu-ropharmacological Considerations, Relevant to Future Drug Discovery and Development", Exp. Opin. Invest. Drugs, 9(7), 1553-1571 (2000)). Несмотря на то, что исследования ведутся постоянно, потребность в более эффективном и безопасном терапевтическом лечении для уменьшения или предупреждения прироста массы все еще существует. Помимо ожирения существует также неудовлетворенная потребность в лечении злоупотребления алкоголем. В Соединенных Штатах алкоголизм поражает приблизительно 10,9 млн мужчин и 4,4 млн - 1 - 008176 женщин. Приблизительно 100000 несчастных случаев со смертельным исходом в год связаны со злоупотреблением алкоголем или алкогольной зависимостью. Риск для здоровья, связанный с алкоголизмом, включает ухудшение двигательного контроля и принятия решения, рак, болезнь печени, врожденные дефекты, болезнь сердца, взаимодействия лекарство/лекарство, панкреатит и межличностные проблемы. При проведении исследований было высказано предположение, что эндогенный каннабиноидный тонус играет критическую роль в регулировании поглощения этанола. Было показано, что эндогенный СВ1-ре-цепторный антагонист SR-141716A блокирует произвольное всасывание этанола у крыс и мышей. См. Ar-none, M., et al., "Selective Inhibition of Sucrose and Ethanol Intake by SR141716, an Antagonist of Central Cannabinoid (CB1) Receptors", Psychopharmacol., 132, 104-106 (1997). См. также обзор в Hungund, B.L. and B.S. Basavarajappa", Are Anadamide and Cannabinoid Receptors involved in Ethanol Tolerance? A Review of the Evidence", Alcohol & Alcoholism, 35(2), 126-133, 2000. Существующие в настоящее время терапии злоупотребления алкоголем или алкогольной зависимости в большинстве случаев страдают от несоблюдения режима лечения или потенциальной гепатоток-сичности. Следовательно, существует высокая неудовлетворенная потребность в более эффективном лечении злоупотребления алкоголем/алкогольной зависимости. Сущность изобретения Согласно настоящему изобретению предложены соединения формулы (I), действующие как лиган- ды каннабиноидных рецепторов (в частности, антагонисты СВ1 рецепторов), / -N )-А (I) где А представляет собой возможно замещенный арил или возможно замещенный гетероарил (предпочтительно А представляет собой замещенный фенил, более предпочтительно фенил, замещенный заместителями в количестве от одного до трех, независимо выбранными из группы, состоящей из галогено (предпочтительно хлоро или фторо), (С1-С4)алкокси, (С1-С4)алкила, галогенозамещенного (С1-С4)алкила (предпочтительно фторзамещенного алкила) и циано, наиболее предпочтительно А представляет собой 2-хлорфенил, 2-фторфенил, 2,4-дихлорфенил, 2-фтор-4-хлорфенил, 2-хлор-4-фторфенил или 2,4-дифторфенил); В представляет собой возможно замещенный арил или возможно замещенный гетероарил (предпочтительно В представляет собой замещенный фенил, более предпочтительно фенил, замещенный заместителями в количестве от одного до трех, независимо выбранными из группы, состоящей из галогено (предпочтительно хлоро или фторо), (С1-С4)алкокси, (С1-С4)алкила, галогенозамещенного (С1-С4)алкила (предпочтительно фторзамещенного алкила) и циано, наиболее предпочтительно В представляет собой 4-хлорфенил или 4-фторфенил); R1 представляет собой водород, (С1-С4)алкил, галогенозамещенный (С1-С4)алкил или (С1-С4)алкокси (предпочтительно R1 представляет собой водород, метил, этил, галогенозамещенный метил или этил или (С1-С4)алкокси; более предпочтительно R1 представляет собой водород, метил, этил, фторзамещенный метил или этил или (С1-С4)алкокси; наиболее предпочтительно R1 представляет собой водород, метил или фторзамещенный метил); R4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), RVv4b R4^CR4b (IA) (IB) где R4a представляет собой водород или (С1-С3)алкил; R4b и R4b', каждый независимо представляет собой водород, циано, гидрокси, амино, ЩМС^)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-O-С(O)-, (СгС^алкил-М!-^)-, ((СгС^алкил^-С^)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)ал-киламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или либо R4b, либо R4b', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c и R4c', каждый независимо пред - 2 - 008176 ставляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (^-С^алкокси, ацилокси, ацила, (С1-Сз)алкил-O-С(O)-, (С1-С4)ал-кил-NН-С(O)-, ((C1-С4)алкил)2N-С(O)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкил-амино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или либо R4c, либо R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)-, -C(=N-OH)- или -C(R4d)(R4d')-, где R4d и R4d', каждый независимо представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (^-С^алкила, (С1-С6)алкокси, ацилокси, ацила, (С^С^алкил-О-С^)-, (С1-С4)алкил-NН-С(О)-, ((С1-С4)алкил)2N-С(O)-, HO-NH-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4d и R4', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где данное гетероциклическое кольцо, данное лактоновое кольцо и данное лактамовое кольцо возможно замещены и данное лактоновое кольцо и данное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d"-, где R4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3) алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-O-С(O)-, арила и гетероари-ла, где данная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e и R4e', каждый независимо представляет собой водород, циано, гидрокси, амино, Н^С(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-O-С(O)-, (С1-С4)алкил-МН-С^)-, ((C1-С4)алкил)2N-С(O)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-член-ного карбоциклического кольца, где данная группировка возможно замещена, или либо R4e, либо R4e', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; и R4f и R4f, каждый независимо представляет собой водород, циано, гидрокси, амино, Н^С(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (Q-C^raui-NH-QO)-, ((С1-С4)алкил)2N-С(O)-, (С1-С6))алкиламино-, ди (С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4) алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или либо R4f, либо R4f', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; при условии, что, когда R4 представляет собой группу формулы (IA), тогда (а) по меньшей мере один из R4b, R4b', R4c, R4c', R4d, R4d', R4d", R4e, R4e', R4f и R4f является иным, чем водород, (С1-С4)алкил или галогенозамещенный (С1-С4)алкил; и (б) Y не представляет собой кислород, серу или -NH-, когда X и Z представляют собой связь, -СН2- или -СН2СН2- и R4b, R4b', R4f и R4f' представляют собой водород; или (2) группу, имеющую формулу (1С), (1С) где R5 и R6, каждый независимо представляет собой водород или (С1-С4)алкил и R7 представляет собой (С1-С4)алкил-, галогенозамещенный (С1-С4)алкил-, (С1-С4)алкокси(С1-С4)алкил-, (С1-С4)ал-киламино(С1-С4)алкил-, ди(С1-С4)алкиламино(С1-С4)алкил- или частично либо полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R5 и R6 или R5 и R7, взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или 4-6-членный частично или полностью насыщенный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где данный лактон, данный лактам и данный гетеро-цикл возможно замещены; их фармацевтически приемлемые соли, пролекарства данных соединений или данных солей или - 3 - 008176 сольваты или гидраты данных соединений, данных солей или данных пролекарств. Предпочтительным соединением по настоящему изобретению является соединение формулы (I), где R4 представляет собой группу формулы (IA). Предпочтительно R4b и R4b, каждый независимо представляет собой водород, Н2ЖХО)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-О-С(О)-, (С1-С4)алкил-NН-С(0)-, ((Q-Q^raufhN-QO)-, арила, гете-роарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4b или R4b', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6) алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NH-С(0)-, ((C1-C4)алкил)2N-C(O)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)ал-киламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4c, взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик, и R4c' представляет собой водород, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(О)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоцик-лического кольца, где данная группировка возможно замещена, или R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R4d)(R4d')-, где R4d представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С1-С4)ал-rauibN-QO)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил (С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоцикличе-ского кольца, где данная группировка возможно замещена, и R4d представляет собой водород, ЩЧС(О)-или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-О-С(О)-, (С1-С4)алкил-NН-С(0)-, ((C1-C4)алкил)2N-C(0)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоцик-лического кольца, где данная группировка возможно замещена, или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где данное гетероциклическое кольцо, данное лактоновое кольцо и данное лактамовое кольцо возможно замещены и данное лактоновое кольцо и данное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d"-, где R4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3) алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-0-С(0)-, арила и гетероарила, где данная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6) алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, (C1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)ал-киламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4e, взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик, и R4e' представляет собой водород, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (^-С^алкила, ацила, (С1-С3)алкил-О-С(О)-, (С1-С4)алкил-NH-C(0)-, ((С1-С4)алкил)2N-С(О)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоцик-лического кольца, где данная группировка возможно замещена, или R4e, взятый вместе с R4b, R4b, R(: или Rс, образует связь, метиленовый мостик или этиленовый мостик; и R4f и R4f, каждый независимо представляет собой водород, Н2ЖС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-О-С(О)-, (^-^^^№N1^(0)-, ((С1-С4)алкил)2N-С(0)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетеро-цикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4f или R4f', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; его фармацевтически приемлемая соль, пролекарство данного соединения или данной соли или сольват или гидрат данного соединения, данной соли или данного пролекарства. Предпочтительно R4b представляет собой водород, возможно замещенный (C1 -С3)алкил или, взятый - 4 - 008176 вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; R4b' представляет собой водород, возможно замещенный (С1-С3)алкил или, взятый вместе с R4e, R4e, R4f или R4f, образует связь, метиленовый мостик или этиленовый мостик; R4f представляет собой водород, возможно замещенный (С1-С3)алкил или, взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; R4f' представляет собой водород, возможно замещенный (С1-С3)алкил или, взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; и еще более предпочтительно R4b, R4b', R4f и R4f', все представляют собой водород. Когда Y представляет собой -NR4d -, тогда R4d предпочтительно представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонила, (Q-С^алкиламиносульфонила, ди(С1-С3)алкиламиносульфонила, ацила, (С1-С6)ал-кил-О-С(О)-, арила и гетероарила, где данная группировка возможно замещена (более предпочтительно R4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С3)алкилсульфонила, (С1-С3)алкиламиносульфонила, ди(С1-С3)алкиламиносульфонила, ацила, (С1-С6)ал-кил-О-С(О)- и гетероарила, где данная группировка возможно замещена (предпочтительно (С1-С3)алкилсульфонил, (С1-С3)алкиламиносульфонил, ди(С1-С3)алкиламиносульфонил, ацил и (С1-С6)алкил-0-С(0)- возможно замещены атомами фтора в количестве от 1 до 3 и данный гетероарил возможно замещен заместителями в количестве от 1 до 2, независимо выбранными из группы, состоящей из хлоро, фторо, (С1-С3)алкокси, (С1-С3)алкила и фторзамещенного (С1-С3)алкила)); X представляет собой -C(R4c)(R4c')-, где R4c и R4c', каждый независимо представляет собой водород, Н^С^)-, возможно замещенный (С1-С6)алкил, (C1-С4)алкил-NH-С(0)- или ((С1-С4)алкил)2N-С(0)-, или либо R4c, либо R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; и Z представляет собой -C(R4e)(R4e')-, где R4e и R4e', каждый независимо представляет собой водород, H2NC(0)-, возможно замещенный (С1-С6)алкил, (С1-С4)алкил-NН-С(0)- или ((С1-С4)алкил)2N-С(0)-, или либо R4e, либо R4e, взятый вместе с R4b, R4b, R4с или R4(:, образует связь, метиленовый мостик или этиленовый мостик. Когда Y представляет собой -C(R4d)(R4d')-, тогда R4d представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (^-^^^№N1-^0)-, ((C1-C4)алкил)2N-C(0)-, (С1-С6)алкиламино-, ((C1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена (предпочтительно R4d представляет собой амино, (С1-С6)алкиламино, ди(С1-С4)алкиламино, (С3-С6)циклоалкиламино, ациламино, арил(С1-С4)алкиламино- или гетероарил(С1-С4)алкиламино; более предпочтительно R4d представляет собой амино, (С1-С6)алкиламино, ди(С1-С4)ал-киламино, (С3-С6)циклоалкиламино), и R4d представляет собой водород, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NH-С(0)-, ((С^С^алкил)^-С(0)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена (предпочтительно R4d' представляет собой (С1-С6)алкил, Н2NС(0)-, (С1-С4)алкил-NН-С(0)-, или ((^-^^^^N^(0)-, или арил; более предпочтительно R4d' представляет собой H2NC(0)-, (Q-Оал-кил-NH-C(0)- или |((Cl-C4)алкил)2N-C(0)-), или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, 5-6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где данное гетероциклическое кольцо, данное лактоновое кольцо и данное лактамовое кольцо возможно замещены и данное лактоновое кольцо и данное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы; X представляет собой связь или -C(R4c)(R4c')-, где R4c и R4c', каждый независимо представляет собой водород; и Z представляет собой связь или -C(R4e)(R4e')-, где R4e и R4e', каждый независимо представляет собой водород. 4d 4d' Другим гфедпочтительньгм воплощением является соединение, где Y представляет собой -C(R4d)(R4d)-, R4b, R4b', R4f и R4f', все представляют собой водород; R4d представляет собой водород, гидрокси, амино или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (С1-С6)алкиламино- и ди(С1-С4)алкиламино-, где данная группировка возможно замещена (предпочтительно R4d представляет собой водород, гидрокси, амино или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкокси, ацила, (С1-С6)алкиламино- и ди(С1-С4) алкиламино-); и R4d' представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, арила и гетероарила, где данная группировка возможно замещена (предпочтительно R4d' представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила и арила, где данная группировка возможно замещена). В этом воплощении X пред - 5 - 008176 почтительно представляет собой -C(R4c)(R4c')-, где R4c и R4c', каждый независимо представляет собой водород или возможно замещенный (С1-С6)алкил, или либо R4c, либо R4c, взятый вместе с R4e или R4i!, образует связь, метиленовый мостик или этиленовый мостик (предпочтительно R4c и R4c', каждый независимо представляет собой водород, или либо R4c, либо R4c', взятый вместе с R4e или R4e', образует связь); и Z предпочтительно представляет собой -C(R4e)(R4e')-, где R4e и R4e', каждый независимо представляет собой водород или возможно замещенный (С1-С6)алкил, или либо R4e, либо R4e', взятый вместе с R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик (предпочтительно R4e и R4e', каждый независимо представляет собой водород, или либо R4e, либо R4e', взятый вместе с R4c или R4c', образует связь). Еще одним другим ггоедпочтительныгм воплощением является соединение, где Y представляет собой -C(R4d)(R4d')-, R4b, R4b', R4f и R4f', все представляют собой водород; R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, 5-6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где данное гетероциклическое кольцо, данное лактоновое кольцо и данное лактамовое кольцо возможно замещены и данное лактоновое кольцо или данное лактамовое кольцо возможно содержит дополнительный гетероатом, выбранный из кислорода, азота или серы (предпочтительно R4d и R4d', взятые вместе, образуют 5-6-членное лактамовое кольцо, где данное лактамовое кольцо возможно замещено и возможно содержит дополнительный гетероатом, выбранный из азота или кислорода). В этом воплощении X предпочтительно представляет собой связь, -СН2СН2- или -C(R4c)(R4(:)-, где R4(: и R4(:, каждый независимо представляет собой водород или возможно замещенный (С1-С6)алкил, или либо R4c, либо R4c, взятый вместе с R4e или Rе, образует связь, метиленовый мостик или этиленовый мостик (более предпочтительно X представляет собой связь или -C(R4c)(R4c')-, где R4c и R4c', каждый представляет собой водород); и Z предпочтительно представляет собой связь, -СН2СН2-или -C(R4e)(R4e')-, где R4i! и R4i!, каждый независимо представляет собой водород или возможно замещенный (С1-С6)алкил, или либо R4e, либо R4e', взятый вместе с R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик (более предпочтительно Z представляет собой связь или -C(R4e)(R4e')-, где R4e и R4e', каждый представляет собой водород). Другим предпочтительным соединением по настоящему изобретению является соединение формулы (I), где R4 представляет собой группу формулы (IB), где R4a такой, как определено выше, R4b представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (С1-С4)ал-кил-NН-С(О)-, ((С1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкил-амино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, R4b представляет собой водород, Н2NС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4b или R4b', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6) алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (С1-С4)алкил-NН-С(0)-, ((C1-C4)алкил)2N-C(0)-, (C1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)ал-киламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4c, взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик, и R4c' представляет собой водород, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (^-С^алкила, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NH-С(0)-, ((С1-С4)алкил)2N-С(О)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоцик-лического кольца, где данная группировка возможно замещена, или R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик (предпочтительно X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c и R4c', каждый независимо представляет собой водород или (С1-С6)алкил); Y представляет собой кислород, серу, -С(О)- или -C(R4d)(R4d')-, где R4d представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (C1-C4)алкил-NH-C(0)-, ((С1-С4) алкил)2N-С(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил (С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, и R4d представляет собой водород, Н2ЖС(0)- или - 6 - 008176 химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-О-С(О)-, ^-^^^№N3-^0)-, ((С1-С4)алкил)2N-С(0)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклическо-го кольца, где данная группировка возможно замещена, или R4d и R4d, взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где данное гетероциклическое кольцо, данное лактоновое кольцо и данное лактамовое кольцо возможно замещены и данное лактоновое кольцо и данное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d -, где R4d представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3) алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-0-С(0)-, арила и гетероарила, где данная группировка возможно замещена (предпочтительно, Y представляет собой -NR4d -, где R4d представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)ал-кила, (С3-C6)циклоалкила, (С1-C3)алкилсульфонил-, (С1-С3)алкиламиносульфонил-, ди(С1-С3)алкиламино-сульфонил-, ацила, (С1-С6)алкил-О-С(О)-, арила и гетероарила, где данная группировка возможно замещена); Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6) алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (С1-С4)алкил-NH-С(0)-, ((C1-C4)алкил)2N-C(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)ал-киламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4e, взятый вместе с R4b, R4b, R4c или R4c, образует связь, метиленовый мостик или этиленовый мостик, и R4e представляет собой водород, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (^-^^^№N1^(0)-, ((C1-C4)алкил)2N-С(О)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоцикли-ческого кольца, где данная группировка возможно замещена, или R4e, взятый вместе с R4b, R4b, R(: или R(:, образует связь, метиленовый мостик или этиленовый мостик (предпочтительно Z представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c и R4c', каждый независимо представляет собой водород или (С1-С6)алкил); R4f представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (^-С^алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((C1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)цик-лоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена; и R4f представляет собой водород, Н2NС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4f или R4f, взятый вместе с R4b, R4b, R4c или R4c, образует связь, метиленовый мостик или этиленовый мостик; его фармацевтически приемлемая соль, пролекарство данного соединения или данной соли или сольват или гидрат данного соединения, данной соли или данного пролекарства. Еще одним предпочтительным соединением по настоящему изобретению является соединение формулы (I), где R4 представляет собой группу формулы (ГС), где R5 и R6, каждый независимо представляет собой водород или (С1-С4)алкил, и R7 представляет собой (С1-С4)алкил-, галогенозшещенный (С1-С4)алкил-, (C1-С4)алкокси(С1-С4)алкил-, (С1-С4)алкиламино(С1-С4)алкил-, ди(С1-С4)алкиламино(С1-С4)алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетеро-атомов, независимо выбранных из кислорода, серы или азота, или R5 и R6 или R5 и R7, взятые вместе, образуют 5-6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-член-ный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где данный лактон, данный лактам и данный гетероцикл возможно замещены; его фармацевтически приемлемая соль, пролекарство данного соединения или данной соли либо сольват или гидрат данного соединения, данной соли или данного пролекарства. Предпочтительно R5 и R6, каждый независимо представляет собой водород или (С1-С4)алкил и R7 представляет собой (С1-С4)алкил. Предпочтительные соединения по настоящему изобретению включают: 1-[9-(4-хлорфенил)-8-(2-хлор-фенил)-9Н-пурин-6-ил]-3-этиламиноазетидин-3-карбоновой кислоты амид; 1-[9-(4-хлорфенил)-8-(2-хлор-фенил)-9Н-пурин-6-ил]-3-изопропиламиноазетидин-3-карбоновой кислоты амид; 1-{1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ил}этанон; {3-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1а,5а,6а)азабицикло[3,1,0]гекс-6-ил}диметиламин; 6-(1-бензилпирролидин-3-илокси)-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин; 9-(4-хлорфенил)-6-(1-циклогексилазетидин-3-илокси)-8 - 7 - 008176 (2,4-дихлорфенил)-9Н-пурин; 6-трет-бутокси-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин; 9-(4-хлор-фенил)-8-(2,4-дихлорфенил)-6-изопропокси-9Н-пурин; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пу-рин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-2-метил-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-пирролидин-1-ил-пиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлор-фенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлор-фенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амид; 4-ами-но-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-карбоновой кислоты амид; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амид; 8-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4-он; 9-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-метил-4-окса-1,9-диазаспиро[5,5]ундекан-2-он; 8-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4-он; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-(4-фторфенил)пиперидин-4-ол; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ол; 4-бензил-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-ол; 4-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-2-карбо-новой кислоты метиламид; 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиридин-2-ил-пиперазин-1-ил)-9Н-пурин; и 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиримидин-2-ил-пиперазин-1-ил)-9Н-пурин; их фармацевтически приемлемые соли или сольваты или гидраты данных соединений или данных солей. Предпочтительные фармацевтически приемлемые соли включают соли гидрохлорид, мезилат и безилат. В некоторых случаях предпочтительно свободное основание. Термин "свободное основание" относится к аминогруппе, имеющей неподеленную электронную пару. Другое воплощение настоящего изобретения охватывает промежуточные соединения (1c/d) и (1b), используемые в синтезе соединений по настоящему изобретению, (lc/d) где А и В каждый независимо представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С1-С4)алкокси, (С1-С4)алкила, галогенозамещенного (С1-С4)алкила и циано; R1 представляет собой водород, (С1-С4)алкил, галогенозамещенный (С1-С4)алкил или (С1-С4)алкокси; и R4 представляет собой гидрокси или галогено; и (lb) где А и В, каждый независимо представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С1-С4)алкокси, (С1-С4)алкила, га-логенозамещенного (С1-С4)алкила и циано; и R1 представляет собой водород, (С1-С4)алкил, галогенозамещенный (С1-С4)алкил или (С1-С4)алкокси. Предпочтительно А и В, каждый независимо представляет собой фенил, замещенный заместителями в количестве от 1 до 2, независимо выбранными из группы, состоящей из хлоро, фторо, (С1-С4)алкокси, (С1-С4)алкила, галогенозамещенного (С1-С4)алкила и циано. Более предпочтительно А представляет собой 2-хлорфенил, 2-фторфенил, 2,4-дихлорфенил, 2-фтор-4-хлорфенил, 2-хлор-4-фторфенил или 2,4-ди-фторфенил; и В представляет собой 4-хлорфенил или 4-фторфенил. Еще одно воплощение настоящего изобретения охватывает фармацевтическую композицию, содержащую (1) соединение по настоящему изобретению и (2) фармацевтически приемлемый эксципиент, разбавитель или носитель. Предпочтительно данная композиция содержит терапевтически эффективное количество соединения по настоящему изобретению. Данная композиция также может содержать по меньшей мере один дополнительный фармацевтический агент (описанный в данном описании). Предпочтительные агенты включают частичные агонисты никотиновых рецепторов, опиоидные антагонисты (например, налтрексон и налмефен), дофаминергические агенты (например, апоморфин), агенты против - 8 - 008176 синдрома дефицита внимания/гиперактивности (ADHD) (например, Ritalin(tm), Strattera(tm), Concerta(tm) и Adderall(tm)) и агенты против ожирения (описанные в данном описании ниже). Еще одно воплощение настоящего изобретения охватывает способ лечения заболевания, состояния или расстройства, модулируемого антагонистом каннабиноидных рецепторов (в частности, СВ1 рецептора), у животных, включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (II) (или его фармацевтической композиции), R (И) где А представляет собой возможно замещенный арил или возможно замещенный гетероарил; В представляет собой возможно замещенный арил или возможно замещенный гетероарил; R1 представляет собой водород, (СгС4)алкил, галогенозамещенный (СгС4)алкил или (СгС4)алкокси; R4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), R4a R4\ ^ ^R4b R4' X R4b R4f-T l44b' R4f> 1 hR4b' (IA) (IB) где R4a представляет собой водород или (С1-С3)алкил; R4b и R4b, каждый независимо представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (СгС3)алкил-О-С(О)-, (Сl-С4)алкил-NH-C(O)-, ((Сl-С4)алкил)2N-С(O)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)ал-киламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или либо R4b, либо R4b', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c)-, где R4c и R4c, каждый независимо представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-O-С(O)-, (СгС^алкил-МН-С^)-, ((C1-С4)алкил)2N-С(O)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоцик-лического кольца, где данная группировка возможно замещена, или либо R4c, либо R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R4d)(R4d')-, где R4d и R4d', каждый независимо представляет собой водород, циано, гидрокси, амино, ЩМС^)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (^-С^алишси, ацилокси, ацила, (С1-С3)алкил-O-С(O)-, (С1-С4)алкил-NH-С(O)-, ((C1-С4)алкил)2N-С(O)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоал-киламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где данное гетероциклическое кольцо, данное лактоновое кольцо и данное лактамовое кольцо возможно замещены и данное лактоновое кольцо и данное лактамовое кольцо возможно содержат дополнительный гетероатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d"-, где R4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3) алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-О-С(О)-, арила и гетеро-арила, где данная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e и R4e', каждый независимо представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (Q-С^алкокси, ацилокси, ацила, (С1-С3)алкил-O-С(O)-, (С1-С4)ал - 9 - 008176 кил-ЫН-С(О)-, ((C1-С4)алкил)2N-С(O)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкил-амино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или либо R4e, либо R4e, взятый вместе с R4b, R4b, R4c или R4c, образует связь, метиленовый мостик или этиленовый мостик; и R4f и R4f, каждый независимо представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (Сl-С4)алкил-NH-C(O)-, ((С1-С4)алкил)2Ы-С(0)-, (С1-Сб)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, арил(С1-С4)алкиламино-, гетероарил(С1-С4)ал-киламино-, арила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где данная группировка возможно замещена, или либо R4f, либо R4f, взятый вместе с R4b, R4b, R4c или R4c, образует связь, метиленовый мостик или этиленовый мостик; или (2) группу, имеющую формулу (1С), 4-0-^-R6 V (1С) где R5 и R6 , каждый независимо представляет собой водород или (С1-С4)алкил и R7 представляет собой (С1-С4)алкил-, галогенозамещенный (С1-С4)алкил-, (С1-С4)алкокси(С1-С4)алкил-, (С1-С4)алкил-амино(С1-С4)алкил-, ди(С1-С4)алкиламино(С1-С4)алкил- или частично либо полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R5 и R6 или R5 и R7, взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично либо полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где данный лактон, данный лактам и данный гете-роцикл возможно замещены; (3) аминогруппу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из (С1-С8)алкила, арил(С1-С4)алкила, частично или полностью насыщенного (С3-С8)циклоалкила, гидрокси(С1-С6)алкила, (С1-С3)алкокси(С1-С6)алкила, гетероарил(С1-С3)алкила и частично или полностью насыщенного гетероцикла; или (4) (С1-С6)алкильную группу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из гидрокси, (С1-С6)алкокси, амино, (С1-С6)алкиламино, ди((С1-С6)ал-кил)амино, (С1-С3)алкилсульфонила, (С1-С3)алкилсульфамила, ди((С1-С3)алкил)сульфамила, ацилокси, частично или полностью насыщенного гетероцикла и частично или полностью насыщенного циклоалкила; его фармацевтически приемлемой соли, пролекарства данного соединения или данной соли или сольвата или гидрата данного соединения, данной соли или данного пролекарства. Заболевания, состояния и/или расстройства, модулируемые антагонистами каннабиноидных рецепторов, включают расстройства приема пищи (например, расстройство, представляющее собой резкое увеличение приема пищи, анорексию и булимию), похудание или регулирование массы (например, снижение потребления калорий или пищи и/или подавление аппетита), ожирение, депрессию, атипичную депрессию, биполярные расстройства, психозы, шизофрению, поведенческие пристрастия, подавление связанного с поощрением поведения (например, условно-рефлекторное избегание места, такое как подавление условно-рефлекторного предпочтения места, побуждающего к употреблению кокаина или морфина), злоупотребление веществами, расстройства привыкания, импульсивность, алкоголизм (например злоупотребление алкоголем, пристрастие к алкоголю и/или алкогольная зависимость, включая лечение в целях отказа от приема алкоголя, стремления к сокращению приема алкоголя и предупреждения рецидивов), злоупотребление табаком (например, пристрастие к курению, прекращение курения и/или зависимость от него, включая лечение в целях стремления к сокращению табакокурения и предупреждения рецидивов), деменцию (в том числе потерю памяти, болезнь Альцгеймера, старческую де-менцию, сосудистую деменцию, умеренное ухудшение когнитивной способности, возрастное ухуждше-ние когнитивной способности и умеренное нейрокогнитивное расстройство), половую дисфункцию у мужчин (например, эректильную дисфункцию), судорожные расстройства, эпилепсию, расстройства желудочно-кишечного тракта (например, дисфункцию желудочно-кишечной моторики и кишечной про-пульсии), синдром дефицита внимания/гиперактивности (ADHD), болезнь Паркинсона и диабет типа II. В предпочтительном воплощении данный способ используют в лечении ожирения, ADHD, алкоголизма и/или злоупотребления табаком. Соединения по изобретению можно вводить в комбинации с другими фармацевтическими агентами. Предпочтительные фармацевтические агенты включают частичные агонисты никотиновых рецепто - 10 - 008176 ров, опиоидные антагонисты (например, налтрексон (в том числе депо налтрексона), антабус и налме-фен), дофаминергические агенты (например, апоморфин), агенты против ADHD (например, метилфени-дата гидрохлорид (например, Ritalin(tm) и Concerta(tm)), атомоксетин (например, Strattera(tm)) и амфетамины (например, Adderall(tm))) и агенты против ожирения, такие как ингибиторы аро-В/МТР, агонисты MCR-4, агонисты ССК-А, ингибиторы обратного захвата моноаминов, симпатомиметические агенты, агонисты Р3-адренергических рецепторов, агонисты дофаминовых рецепторов, аналоги рецепторов меланоцитсти-мулирующего гормона, агонисты 5-НТ2с рецепторов, антагонисты рецепторов меланинконцентрирую-щего гормона, лептин, аналоги лептина, агонисты лептинового рецептора, антагонисты галанинового рецептора, ингибиторы липазы, агонисты бомбезинового рецептора, антагонисты рецепторов нейропеп-тида-Y, тиромиметические агенты, дегидроэпиандростерон или его аналоги, антагонисты глюкокортико-идного рецептора, антагонисты орексинового рецептора, агонисты рецепторов глюкагонподобного пеп-тида-1, цилиарные нейротрофические факторы, агонисты агутисвязанного белка человека, антагонисты рецепторов грелина, антагонисты или обратные агонисты рецепторов гистамина 3 и агонисты рецепторов нейромедина U и тому подобное. Комбинированную терапию можно назначать с введением (а) единой фармацевтической композиции, содержащей соединение по настоящему изобретению, по меньшей мере один дополнительный фармацевтический агент, описанный здесь, и фармацевтически приемлемый эксципиент, разбавитель или носитель; или (б) двух отдельных фармацевтических композиций, содержащих (1) первую композицию, содержащую соединение по настоящему изобретению и фармацевтически приемлемый эксципиент, разбавитель или носитель, и (2) вторую композицию, содержащую по меньшей мере один дополнительный фармацевтический агент, описанный здесь, и фармацевтически приемлемый эксципиент, разбавитель или носитель. Эти фармацевтические композиции можно вводить одновременно или последовательно и в любом порядке. Еще один аспект настоящего изобретению включает фармацевтический набор для использования пользователем для лечения заболеваний, состояний или расстройств, модулируемых антагонистами кан-набиноидных рецепторов, у животного. Этот набор включает в себя: а) подходящую лекарственную форму, содержащую соединение по настоящему изобретению; и б) инструкции, в которых описан способ применения этой лекарственной формы для лечения заболеваний, состояний или расстройств, модулируемых антагонистами каннабиноидных рецепторов (в частности, СВ1 рецептора). Другое воплощение включает фармацевтический набор, включающий в себя: а) первую лекарственную форму, содержащую (1) соединение по настоящему изобретению и (2) фармацевтически приемлемый носитель, эксципиент или разбавитель; б) вторую лекарственную форму, содержащую (1) дополнительный фармацевтический агент, описанный здесь, и (2) фармацевтически приемлемый носитель, эксципиент или разбавитель; и в) контейнер. Определения Используемый здесь термин "алкил" относится к углеводородному радикалу общей формулы CnH2n+1. Алкановый радикал может быть прямым или разветвленным. Например, термин " (С1-С6)алкил" относится к одновалентной прямой или разветвленной алифатической группе, содержащей от 1 до 6 атомов углерода (например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, неопентил, 3,3-диметилпропил, гексил, 2-метил-пентил и тому подобное). Подобным образом, алкильная часть (то есть алкильная группировка) алкокси-, ацильной (например, алканоильной), алкиламино-, диалкиламино- и алкилтиогруппы имеет то же определение, которое приведено выше. Если указано "возможно замещенный", то алкановый радикал или алкильная группировка могут быть незамещенными или замещенными одним или более чем одним заместителем (в общем случае, заместителями в количестве от одного до трех, за исключением случая га-логеновых заместителей, таких как перхлоро или перфторалкилов), независимо выбранными из группы заместителей, перечисленных ниже в определении термина "замещенный". "Галогенозамещенный алкил" относится к алкильной группе, замещенной одним или более чем одним атомом галогена (например, фторметил, дифторметил, трифторметил, перфторэтил и тому подобное). В случае, когда они замещены, алкановые радикалы или алкильные группировки предпочтительно замещены заместителями фторо в количестве от одного до трех или одним или двумя заместителями, независимо выбранными из (С1-С3) алкила, (С3-С6)циклоалкила, (С2-С3)алкенила, арила, гетероарила, 3-6-членного гетероцикла, хлоро, циа-но, гидрокси, (С1-С3)алкокси, арилокси, амино, (С1-С6)алкиламино, ди(С1-С4)алкиламино, аминокарбок-силата (то есть (Q-^^raui-O-C^-NH-), гидрокси(С2-С3)алкиламино или кето (окси), и более предпочтительно группами фторо в количестве от одного до трех или одним заместителем, выбранным из (С1-С3) алкила, (С3-С6)циклоалкила, (С6)арила, 6-членного гетероарила, 3-6-членного гетероцикла, (С1-С3)алкок-си, (С1-С4)алкиламино или ди(С1-С2)алкиламино. Термин "частично или полностью насыщенное карбоциклическое кольцо" (также обозначаемый "частично или полностью насыщенный циклоалкил") относится к неароматическим кольцам, которые либо частично, либо полностью гидрированы и могут существовать в виде единичного кольца, бицикли-ческого кольца или спирального кольца. Если не оговорено особо, карбоциклическое кольцо в общем случае представляет собой 3-8-членное кольцо (предпочтительно 3-6-членное кольцо). Например, час - 11 - 008176 тично или полностью насыщенные карбоциклические кольца (или циклоалкил) включают такие группы, как циклопропил, циклопентил, циклобутил, циклобутенил, циклопентил, циклопентенил, циклопента-диенил, циклогексил, циклогексенил, циклогексадиенил, норборнил (бицикло[2,2,1]гептил), норборне-нил, бицикло[2,2,2]октил и тому подобное. Если указано "возможно замещенный", то частично насыщенная или полностью насыщенная циклоалкильная группа может быть незамещенной или замещенной одним или более чем одним заместителем (обычно от одного до трех заместителей), независимо выбранным из группы заместителей, перечисленных ниже в определении термина "замещенный". Замещенное карбоциклическое кольцо также включает группы, где это карбоциклическое кольцо конденсировано с фенильным кольцом (например, инданил). Карбоциклическая группа может быть присоединена к хими-ческому(ой) объекту или группировке по любому одному из атомов углерода в пределах карбоцикличе-ской кольцевой системы. В случае, когда она замещена, карбоциклическая группа предпочтительно замещена одним или двумя заместителями, независимо выбранными из (С1-С3)алкила, (С2-С3)алкенила, (С1-С6)алкилиденила, арила, гетероарила, 3-6-членного гетероцикла, хлоро, фторо, циано, гидрокси, (С1-С3)алкокси, арилокси, амино, (С1-С6)алкиламино, ди-(С1-С4)алкиламино, аминокарбоксилата (то есть (С1-С3)алкил-0-С(0)-Мг1-), гидрокси(С2-С3)алкиламино или кето (окси), и более предпочтительно одним или двумя заместителями, независимо выбранными из (С1-С2)алкила, 3-6-членного гетероцикла, фторо, (С1-С3)алкокси, (С1-С4)алкиламино или ди(С1-С2)алкиламино. Подобным образом, любая циклоалкильная часть группы (то есть циклоалкилалкил, циклоалкиламино и т.д.) имеет то же самое определение, которое приведено выше. Термин "частично насыщенное или полностью насыщенное гетероциклическое кольцо" (к которому также относится "частично насыщенный или полностью насыщенный гетероцикл") относится к неароматическим кольцам, которые либо частично, либо полностью гидрированы и могут существовать в виде единичного кольца, бициклического кольца или спиро кольца. Если не оговорено особо, гетероциклическое кольцо в общем случае представляет собой 3-6-членное кольцо, содержащее от 1 до 3 гетеро-атомов (предпочтительно 1 или 2 гетероатома), независимо выбранных из серы, кислорода или азота. Частично насыщенные или полностью насыщенные гетероциклические кольца включают такие группы, как эпокси, азиридинил, тетрагидрофуранил, дигидрофуранил, дигидропиридинил, пирролидинил, N-ме-тилпирролидинил, имидазолидинил, имидазолинил, пиперидинил, пиперазинил, пиразолидинил, 2Н-пи-ранил, 4Н-пиранил, 2Н-хроменил, оксазинил, морфолино, тиоморфолино, тетрагидротиенил, тетрагидро-тиенил 1,1-диоксид и тому подобное. Если указано "возможно замещенный", то частично насыщенная или полностью насыщенная гетероциклическая группа может быть незамещенной или замещенной одним или более чем одним заместителем (обычно от одного до трех заместителей), независимо выбранным из группы заместителей, перечисленных ниже в определении термина "замещенный". Замещенное гетероциклическое кольцо включает группы, в которых гетероциклическое кольцо конденсировано с арильным или гетероарильным кольцом (например, 2,3-дигидробензофуранил, 2,3-дигидроиндолил, 2,3-дигидробензтиофенил, 2,3-дигидробензтиазолил и т.д.). Будучи замещенной, гетероциклическая группа предпочтительно замещена одним или двумя заместителями, независимо выбранными из (С1-С3)алкила, (С3-С6)циклоалкила, (С2-С4)алкенила, арила, гетероарила, 3-6-членного гетероцикла, хлоро, фторо, циа-но, гидрокси, (С1-С3)алкокси, арилокси, амино, (С1-С6)алкиламино, ди(С1-С3)алкиламино, аминокарбок-силата (то есть (С1-С3)алкил-O-С(O)-NH-) или кето (окси), и более предпочтительно одним или двумя заместителями, независимо выбранными из (С1-С3)алкила, (С3-С6)циклоалкила, (С6)арила, 6-членного гетероарила, 3-6-членного гетероцикла или фторо. Гетероциклическая группа может быть присоединена к химическому(ой) объекту или группировке по любому одному из кольцевых атомов в пределах гетероциклической кольцевой системы. Подобным образом, любая гетероциклическая часть группы (то есть гетероциклзамещенный алкил, гетероциклический карбонил и т.д.) имеет то же самое определение, которое приведено выше. Термин "арил" или "ароматическое карбоциклическое кольцо" относится к ароматическим группировкам, имеющим единичную (например, фенил) или конденсированную кольцевую систему (например, нафталин, антрацен, фенантрен и т.д.). Типичной арильной группой является 6-10-членное ароматическое карбоциклическое кольцо(а). Если указано "возможно замещенный", то арильные группы могут быть незамещенными или замещенными одним или более чем одним заместителем (предпочтительно не более трех заместителей), независимо выбранным из группы заместителей, приведенных ниже в определении термина "замещенный". Замещенные арильные группы включают цепь из ароматических группировок (например, бифенил, терфенил, фенилнафталил и т. д.). Будучи замещенными, ароматические группировки предпочтительно замещены одним или двумя заместителями, независимо выбранными из (С1-С4)алкила, (С2-С3)алкенила, арила, гетероарила, 3-6-членного гетероцикла, бромо, хлоро, фторо, иодо, циано, гидрокси, (С1-С4)алкокси, арилокси, амино, (С1-С6)алкиламино, ди(С1-С3)алкиламино или амино-карбоксилата (то есть (С^С^алкил-О-С^^МН-), и более предпочтительно одним или двумя заместителями, независимо выбранными из (С1-С4)алкила, хлоро, фторо, циано, гидрокси или (С1-С4)алкокси. Арильная группа может быть присоединена к химическому(ой) объекту или группировке по любому одному из атомов углерода в пределах ароматической кольцевой системы. Подобным образом, арильная часть (то есть ароматическая группировка) ароила или ароилокси (то есть (арил)-С(О)-О-) имеет то же - 12 - 008176 самое определение, которое приведено выше. Термин "гетероарил" или "гетероароматическое кольцо" относится к ароматическим группировкам, содержащим по меньшей мере один гетероатом (например, кислород, серу, азот или их комбинацию) в пределах 5-10-членной ароматической кольцевой системы (например, пирролил, пиридил, пиразолил, индолил, индазолил, тиенил, фуранил, бензофуранил, оксазолил, имидазолил, тетразолил, триазинил, пиримидил, пиразинил, тиазолил, пуринил, бензимидазолил, хинолинил, изохинолинил, бензтиофенил, бензоксазолил и т. д). Гетероароматическая группировка может состоять из единичной или конденсированной кольцевой системы. Типичное единичное гетероарильное кольцо представляет собой 5-6-членное кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и типичная конденсированная гетероарильная кольцевая система представляет собой 9-10-членную кольцевую систему, содержащую от 1 до 4 гетероатомов, независимо выбранных из кислорода, серы и азота. Если указанно "возможно замещенный", то гетероарильные группы могут быть незамещенными или замещенными одним или более чем одним заместителем (предпочтительно не более трех заместителей), независимо выбранным из группы заместителей, приведенных ниже в определении термина "замещенный". Будучи замещенными, гетероароматические группировки предпочтительно замещены одним или двумя заместителями, независимо выбранными из (С1-С4)алкила, (С2-С3)алкенила, арила, гетероарила, 3-6-член-ного гетероцикла, бромо, хлоро, фторо, иодо, циано, гидрокси, (С1-С4)алкокси, арилокси, амино, (С1-С6) алкиламино, ди(С1-С3)алкиламино или аминокарбоксилата (то есть (С1-С3)алкил-O-С(O)-NН-), и более предпочтительно одним или двумя заместителями, независимо выбранными из (С1-С4)алкила, хлоро, фторо, циано, гидрокси, (С1-С4)алкокси, (С1-С4)алкиламино и ди(С1-С2)алкиламино. Гетероарильная группа может быть присоединена к химическому(ой) объекту или группировке по любому одному из атомов в пределах ароматической кольцевой системы (то есть имидазол-1-ил, имидазол-2-ил, имидазол-4-ил, имидазол-5-ил, пирид-2-ил, пирид-3-ил, пирид-4-ил, пирид-5-ил или пирид-6-ил). Подобным образом, гетероарильная часть (то есть гетероароматическая группировка) гетероароила (то есть (гетероарил)-С(О)-О-) имеет то же самое определение, которое приведено выше. Термин "ацил" относится к алкилу, частично насыщенному или полностью насыщенному циклоал-килу, частично насыщенному или полностью насыщенному гетероциклу, арилу и гетероарилу, замещенному карбонильными группами. Например, ацильные группы включают такие группы, как (С1-С6)алка-ноил (например, формил, ацетил, пропионил, бутирил, валерил, капроил, трет-бутилацетил и т.д.), (С3-С6)циклоалкилкарбонил (например, циклопропилкарбонил, циклобутилкарбонил, циклопентилкарбонил, циклогексилкарбонил и т.д.), гетероциклический карбонил (например, пирролидинилкарбонил, пирро-лид-2-он-5-карбонил, пиперидинилкарбонил, пиперазинилкарбонил, тетрагидрофуранилкарбонил и т.д.), ароил (например, бензоил) и гетероароил (например, тиофенил-2-карбонил, тиофенил-3-карбонил, фура-нил-2-карбонил, фуранил-3-карбонил, 1Н-пирролил-2-карбонил, 1Н-пирролил-3-карбонил, бензо[Ь]тио-фенил-2-карбонил и т. д.). Кроме того, алкильная, циклоалкильная, гетероциклическая, арильная и гете-роарильная части ацильной группы могут представлять собой любую одну из групп, указанных выше в соответствующих определениях. Если указано "возможно замещенный", то ацильная группа может быть незамещенной или замещенной одним или более чем одним заместителем (обычно от одного до трех заместителей), независимо выбранным из группы заместителей, приведенных ниже в определении термина "замещенный", или алкильная, циклоалкильная, гетероциклическая, арильная и гетероарильная части ацильной группы могут быть замещены, как описано выше в предпочтительном и более предпочтительном списке заместителей, соответственно. Термин "замещенный" конкретно допускает и предусматривает один или более чем один заместитель из числа общепринятых в данной области техники. Впрочем, специалистам в данной области техники обычно понятно, что данные заместители следует выбирать так, чтобы они не оказывали неблагоприятного воздействия на фармакологические характеристики соединения или неблагоприятного влияния при использовании лекарства. Подходящие заместители для любой из групп, определенных выше, включают (С1-С6)алкил, (С3-С7)циклоалкил, (С2-С6)алкенил, (С1-С6)алкилиденил, арил, гетероарил, 3-6-членный гетероцикл, галогено (например, хлоро, бромо, иодо и фторо), циано, гидрокси, (С1-С6)алкокси, арилок-си, сульфгидрил (меркапто), (C1-С6)алкилтио, арилтио, амино, моно- или ди(С1-С4)алкиламино, четвертичные соли аммония, амино(С1-С6)алкокси, аминокарбоксилат (то есть (С1-С6)алкил-О-С(О)-№Н-), гид-рокси(С2-С6)алкиламино, амино(С1-С6)алкилтио, цианоамино, нитро, (С1-С6)карбамил, кето (окси), ацил, (С1-С6)алкил-СО2-, гликолил, глицил, гидразино, гуанил, сульфамил, сульфонил, сульфинил, тио(С1-С6)алкил-С(О)-, тио(С1-С6)алкил-СО2- и их комбинации. В случае замещенных комбинаций, таких как "замещенный арил(С1-С6)алкил", может быть замещена либо арильная, либо алкильная группа или и арильная, и алкильная группы могут быть замещены одним или более чем одним заместителем (обычно от одного до трех заместителей, за исключением случая пергалогенозамещения). Арил- или гетероарил-замещенная карбоциклическая или гетероциклическая группа может представлять собой конденсированное кольцо (например, инданил, дигидробензофуранил, дигидроиндолил и т.д.). Термин "галогено" относится к группе хлоро, бромо, фторо или иодо. Термин "сольват" относится к молекулярному комплексу соединения, представленного формулой (I) или (II) (включая пролекарства и их фармацевтически приемлемые соли), с одной или более чем од- 13 008176 ной молекулой растворителя. Молекулы таких растворителей представляют собой молекулы растворителей, обычно используемых в фармацевтической области, которые известны как безвредные для реципиента, например вода, этанол и тому подобное. Термин "гидрат" относится к комплексу, в котором молекула растворителя представляет собой воду. Фраза "фармацевтически приемлемый" указывает на то, что данные вещество или композиция должны быть совместимы с точки зрения химии и/или токсикологии с другими ингредиентами, входящими в состав препарата, и/или млекопитающим, которого лечат им. Термин "защитная группа" или "Pg" относится к заместителю, обычно используемому для блокировки или защиты конкретной функциональной группы при взаимодействии других функциональных групп соединения. Например, "аминозащитная группа" представляет собой присоединенный к аминогруппе заместитель, который блокирует или защищает функциональную аминогруппу в этом соединении. Подходящие аминозащитные группы включают ацетил, трифторацетил, трет-бутоксикарбонил (ВОС), бензилоксикарбонил (CBz) и 9-флуоренилметиленоксикарбонил (Fmoc). Аналогично, термин "гидрокси-защитная группа" относится к заместителю гидроксигруппы, который блокирует или защищает функциональную гидроксигруппу. Подходящие защитные группы включают ацетил и силил. Термин "карбокси-защитная группа" относится к заместителю карбоксигруппы, который блокирует или защищает функциональную карбоксигруппу. Обычно используемые карбоксизащитные группы включают -СН2СН2SО2Рh, цианоэтил, 2-(триметилсилил)этил, 2-(триметилсилил)этоксиметил, 2-(П-ТОЛУОЛСУЛЬФОНИЛ)ЭТИЛ, 2-(n-нитрофенилсульфенил)этил, 2-(дифенилфосфино)этил, нитроэтил и тому подобное. Общее описание защитных групп и их использования см. в Т.\?. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 1991. Фраза "терапевтически эффективное количество" означает количество соединения по настоящему изобретению, которое (1) лечит или предупреждает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства или (3) предупреждает или задерживает начало одного или более симптомов конкретного заболевания, состояния или расстройства, описанного здесь. Термин "животное" относится к людям (мужского или женского пола), домашним животным (например, собакам, кошкам и лошадям), животным-источникам продовольствия, животным зоопарков, морским животным, птицам и другим подобным видам животных. Термин "пригодные в пищу животные" относятся к животным-источникам продовольствия, таким как крупный рогатый скот, свиньи, овцы и домашняя птица. Термины "лечение", "лечить" или "терапия" включают как превентивное, то есть профилактическое, так и паллиативное лечение. Термин "модулируемый каннабиноидным рецептором" или "модулирование каннабиноидного рецептора" относится к активации или инактивации каннабиноидного рецептора. Например, лиганд может действовать как агонист, частичный агонист, обратный агонист, антагонист или частичный антагонист. Термин "антагонист" включает как полные антагонисты, так и частичные антагонисты, а также обратные агонисты. Термин "СВ-1 рецептор" относится к связанному с G-белком каннабиноидному рецептору типа 1. Термин "соединения по настоящему изобретению" (если конкретно не указано иное) относится к соединениям формулы (I) и формулы (II), их пролекарствам, фармацевтически приемлемым солям данных соединений и/или пролекарств и гидратам или сольватам данных соединений, солей и/или проле-карств, а также ко всем стереоизомерам (включая диастереоизомеры и энантиомеры), таутомерам и соединениям, меченным изотопом. Если особо не оговорено, термин "соединения по настоящему изобретению" не включает в себя промежуточные соединения (1c/d) или (1b). Подробное описание Соединения по настоящему изобретению могут быть синтезированы с использованием путей синтеза, которые включают способы, аналогичные хорошо известным в области химии, в частности в свете содержащегося здесь описания. Как правило, исходные вещества доступны из коммерческих источников, таких как Aldrich Chemicals (Milwaukee, WI), или легко могут быть получены способами, хорошо известными специалистам в данной области техники (например, их получают способами, описанными в Louis F. Fieser and Mary Fieser, Reagents for Organic Synthesis, v. 1-19, Wiley, New York (1967-1999 ed.) или Beilsteins Handbuch der organischen Chemie, 4, Aufl. ed. Springer-Verlag, Berlin, включая приложения (доступные также через онлайн базу данных Beilstein). В иллюстративных целях изображенные ниже реакционные схемы демонстрируют возможные пути синтеза соединений по настоящему изобретению, в том числе ключевых промежуточных соединений. Более подробное описание отдельных реакционных стадий см. в приведенном ниже разделе "Примеры". Для специалистов в данной области техники очевидно, что для синтеза соединений по настоящему изобретению (в том числе промежуточных соединений по изобретению) могут быть использованы и другие пути синтеза. Несмотря на то, что конкретные исходные вещества и реагенты описаны на схемах и обсуждены ниже, их легко можно заменить другими исходными веществами и реагентами для обеспечения получения разнообразных производных и/или реакционных условий. К тому же многие из соединений, - 14 - 008176 полученных описанными ниже способами, могут быть дополнительно модифицированы в свете данного описания с использованием традиционной химии, которую хорошо знают специалисты в данной области техники. При получении соединений по настоящему изобретению может потребоваться защита функциональных групп (например, первичного или вторичного амина) в промежуточных соединениях. Необходимость в такой защите будет варьировать в зависимости от природы функциональной группы и условий способов получения. Подходящие аминозащитные группы (NH-Pg) включают ацетил, трифторацетил, трет-бутоксикарбонил (ВОС), бензилоксикарбонил (CBz) и 9-флуоренилметиленоксикарбонил (Fmoc). Необходимость в такой защите легко определяется специалистом в данной области техники. Общее описание защитных групп и их использования см. в LW. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 1991. Соединения формулы (I) и (II) могут быть получены с использованием общепринятых методик, описанных R.J. Chorvat и др. в J. Med. Chem., 42, 833-848 (1999) и представленных ниже на схеме I. Схема I (I) или (II) Промежуточное соединение 1(a) может быть получено путем взаимодействия желаемого аминосое-динения (B-NH2, где В такой, как определено выше) с 4,6-дихлор-5-аминопиримидином (доступным от Sigma-Aldrich, St. Louis, МО) в водной соляной кислоте в условиях дефлегмации (A. Miyashita и др. в Chem.Pharm. Bull., 46, 390-399 (1998)) или этоксиэтаноле при повышенной температуре. Подходящие аминосоединения (B-NH2) включают такие соединения, где В представляет собой арил (например, анилин) или замещенный арил (например, 2-хлоранилин, 2-фторанилин, 2,4-дихлоранилин, 2-фтор-4-хлор-анилин, 2-хлор-4-фторанилин, 2,4-дифторанилин и другие замещенные ариламины). В качестве исходного вещества для тех соединений формулы (I) или (II), в которых R1 является иным, чем водород, могут быть использованы другие имеющиеся в продаже производные 4,6-дихлор-5-аминопиримидина (например, 2-метил-4,6-дихлор-5-аминопиримидин и 2-этил-4,6-дихлор-5-аминопиримидин). Для ознакомления с представленными в литературе характерными путями синтеза 4,6-дихлор-5-аминопиримидиновых производных смотри: A. Albert и др. в J. Chem. Soc., 3832 (1954) и W.E. Hymans в J. Heterocycl. Chem., 13,1141 (1976). Промежуточное соединение 1(a) затем может быть ацилировано с использованием традиционной химии, которую хорошо знают специалисты в данной области техники. Например, промежуточное соединение 1(a) может быть подвергнуто взаимодействию с желаемым ароил- или гетероароилхлоридом в основном растворителе (например, пиридине) до образования промежуточного соединения 1(b). Альтернативно, промежуточное соединение 1(a) может быть подвергнуто взаимодействию с желаемым ароил-или гетероароилхлоридом в реакционно-инертном растворителе (например, тетрагидрофуране, метилен-хлориде, ^^диметилацетамиде). Добавление подходящего основания (например, триэтиламина, диизо-пропилэтиламина) может способствовать протеканию реакции. Подходящие ароилхлориды включают бензоилхлорид, о-хлорбензоилхлорид, о-фторбензоилхлорид, n-хлорбензоилхлорид, n-фторбензоилхло - 15 - 008176 рид, 2,4-дихлорбензоилхлорид, 2,4-дифторбензоилхлорид и тому подобное. Промежуточное соединение 1(b) затем может быть циклизовано до 6-хлорпуринового промежуточного соединения 1(c) путем обработки агентом конденсации с использованием методик и условий, аналогичных описанным в патенте США № 4728644, который включен в данное описание посредством ссылки. В предпочтительном способе промежуточное соединение 1(b) может быть подвергнуто кипячению с обратным холодильником в слабой кислоте (например, уксусной кислоте) или серной кислоте в соответствующем растворителе (например, изопропиловом спирте, толуоле) до образования гидроксипу-ринового промежуточного соединения 1(d) с последующим кипячением с обратным холодильником в оксихлориде фосфора, толуоле в присутствии оксихлорида фосфора и триэтиламина или 2,6-лутидине в оксихлориде фосфора с получением промежуточного соединения 1(c). В другом предпочтительном способе соединение 1(b) может быть прямо превращено в соединение 1(c) путем кипячения с обратным холодильником в оксихлориде фосфора, причем для способствования конденсации могут быть добавлены соответствующий сорастворитель (например, толуол) и/или основание (например, пиридин, триэтила-мин). В конце может быть введена группа R4 замещением хлорида на пуриновом кольце по положению 6. Для соединений формулы (I) и (II), где R4 представляет собой аминогруппу, в общем случае промежуточное соединение 1(c) перемешивают с желаемым амином (например, замещенным или незамещенным арил(С1-С4)алкиламином, замещенным или незамещенным 2-анданиламином, замещенным или незамещенным циклогексиламином, замещенным или незамещенным циклопентиламином, замещенным или незамещенным норбораниламином, гидрокси(С1-С6)алкиламином, замещенным или незамещенным гетероариламином, гетероарил(С1-С3)алкиламином и замещенным или незамещенным 5-6-членным гетероциклическим амином (то есть амином формулы (1а), определенным выше)). Данный амин может действовать как растворитель, или может быть добавлен растворитель (например, этанол, метиленхлорид и т.д.) для способствования солюбилизации реагентов и/или для создания среды, имеющей соответствующую температуру дефлегмации для доведения замещения до конца. Для ускорения процесса реакционная смесь может быть нагрета. К тому же для того, чтобы погасить кислоту, образовавшуюся в данном процессе, может быть использовано подходящее основание, такое как триэтиламин. Подходящие амино-соединения либо могут быть приобретены коммерчески, либо легко могут быть получены по стандартным методикам, хорошо известным специалистам в данной области техники. Упомянутые выше соединения формулы (I), где R4 представляет собой первичный или вторичный амин, могут быть алкилированы, сульфированы и/или ацилированы с получением дополнительных производных (например, алкиламинов, диалкиламинов, сульфонамидов, амидов, карбаматов, мочевин и т.д.) по стандартным методикам, хорошо известным специалистам в данной области техники. Упомянутые выше соединения формулы (I), где R4 представляет собой аминокислоту, могут быть получены, как описано A.M. Shalaby и др. в J. Chem. Res., 134-135 (1998). Эти вещества затем могут быть превращены в амиды и сложные эфиры с использованием стандартных методик, хорошо известных специалистам в данной области техники. Многочисленные аминосоединения формулы (IA) доступны из коммерческих источников, или их получают известными способами, легко доступыми для специалистов в данной области техники. Приведенные в качестве примера способы получения аминосоединений формулы (IA) проиллюстрированы ниже в примерах. Получение 4-аминопиперидин-4-карбоксамидных групп формулы (IA) и 4-амино-4-циано-пиперидиновых групп формулы (IA) и их бензилзащищенных предшественников описано P.A.J. Janssen в патенте США № 3161644, С. van de Westeringh и др. в J. Med. Chem., 7, 619-623 (1964) и К.А. Metwally и др. в J. Med. Chem., 41, 5084-5093 (1998), где упомянутые выше 4-аминогруппы представляют собой незамещенное, монозамещенное, дизамещенное гетероциклическое кольцо или его часть. Родственные бицик-лические производные описаны K. Frohlich и др. в Tetrahedron, 54, 13115-13128 (1998) и содержащихся там ссылках. Спирозамещенные пиперидины формулы (IA) описаны P.A.J. Janssen в патенте США № 3155670, К.А. Metwally и др. в J. Med. Chem., 41, 5084-5093 (1998), Т. Toda и др. в Bull. Chem. Soc. Japan. 44, 34453450 (1971) и W. Brandau и S. Samnick в WO 9522544. Получение 3-аминоазетидин-3-карбоксамида описано А.Р. Kozikowski и А.Н. Fauq в Synlett, 783-784 (1991). Получение предпочтительных 4-алкиламино-пиперидин-4-карбоксамидных групп формулы (IA) представлено ниже на схеме II. Схема II ^ О Ш(алкил) Ш(алкил) JJ -J> - XV" 2(a) 2(b) 2(c) Сначала защищают аминогруппу 4-пиперидинона с получением промежуточного соединения 2(a). Пригодной защитной группой является бензил. 4-Пиперидинон и его производные могут быть приобретены коммерческим путем у различных источников (например, Interchem Corporation, Paramus, NJ и Sigma-Aldrich Co., St. Louis, МО). Затем пиперидинон 2(a) подвергают взаимодействию с желаемым ал-киламином и цианидом калия в смеси растворителей водная HCl/этанол при приблизительно 0-30°С. - 16 - 008176 Цианогруппу превращают в соответствующий амид с использованием кислоты и воды. Защитную группу затем удаляют традиционными способами для использованной конкретной защитной группы. Например, бензилзащитная группа может быть удалена путем гидрирования в присутствии Pd/C. Для соединений формулы (I) и (II), где R4 представляет собой аминоалкильную, алкиламиноалкиль-ную или диалкиламиноалкильную группу, хлор в промежуточном соединении 1(c) может быть сначала замещен цианогруппой (например, путем обработки тетрабутиламмонийцианидом в присутствии 1,4-диазабицикло[2,2,2]октана (DABCO) в апротонном растворителе (например, ацетонитриле) при комнатной температуре). См., например, Hocek et al. Collect. Czech. Chem. Commun., 60, 1386 (1995). Цианогруппа затем может быть восстановлена до алкиламина с использованием стандартных методов восстановления, хорошо известных специалистам в данной области техники (например, путем обработки DIBAL или водородом в присутствии Pd/C). Аминогруппа затем может быть алкилирована с использованием стандартных методик восстановительного алкилирования. В общем, шиффово основание образуется в результате взаимодействия амина с желаемым кетоном или альдегидом в полярном растворителе при температуре от приблизительно 10 до приблизительно 140°С в течение от приблизительно 2 до приблизительно 24 ч в присутствии молекулярных сит 3 А. Обычно к кетону или альдегиду добавляют эквивалентное количество или незначительный избыток аминосоединения. Подходящие полярные растворители включают метиленхло-рид, 1,2-дихлорэтан, диметилсульфоксид, диметилформамид, спирты (например, метанол или этанол) или их смеси. Предпочтительным растворителем является метанол. Затем в том же самом реакционном сосуде имин может быть восстановлен до вторичного амина в присутствии восстанавливающего агента при температуре от приблизительно 0 до приблизительно 10°С и далее нагрет до температуры от приблизительно 20 до приблизительно 40°С в течение приблизительно от 30 мин до приблизительно 2 ч. Подходящие восстанавливающие агенты включают комплекс пиридинборан и боргидриды металлов, такие как боргидрид натрия, триацетоксиборгидрид натрия и цианоборгидрид натрия. Подходящие альдегиды или кетоны включают параформальдегид, ацетальдегид, ацетон, бензальдегид и тому подобное. Альтернативно, аминоалкильная группа может быть введена с использованием способов, описанных Hocek и др. в Tetrahedron, 53(6), 2291-2302 (1997). 6-Хлорпуриновое промежуточное соединение 1(c) превращают в 6-ацетилпуриновое соединение путем взаимодействия промежуточного соединения 1(c) с (1-этоксивинил)три-н-бутилоловом в условиях Pd(PPh3)4-кaтaлизa с последующим гидролизом с использованием смеси ацетона и водного НС1 (или смеси DMF/водн. НС1) при температуре дефлегмации с получением ацетилированного пурина. Ацетильную группу затем без труда превращают в амин или замещенный амин путем восстановительного аминирования, способа, хорошо известного специалистам в данной области техники. Во взятой в качестве примера методике используется соль желаемого амина (например, хлорид аммония, хлорид метиламмония, хлорид аллиламмония, хлорид циклопропиламмо-ния, хлорид циклогексиламмония, хлорид диметиламмония, хлорид бензиламмония и т.д.) и восстанавливающий агент (например, NaBH4, NаВН3СN или триацетоксиборгидрид) в полярном растворителе при комнатной температуре. См. Abdel-Magid, et al., J. Org. Chem.. 61, 3849-3862 (1996) для большого разнообразия альдегидов, кетонов и аминов, которые могут быть использованы либо в восстановительном ал-килировании 6-аминопурина, либо восстановительном аминировании 6-ацетилпурина. Для тех соединений формулы (I) и (II), где R4 представляет собой незамещенную или замещенную алкоксигруппу, промежуточное соединение 1(c) может быть обработано желаемым спиртом в присутствии основания (например, трет-бутоксида калия) и апротонного растворителя (например, THF). Подходящие спирты могут быть либо приобретены коммерческим путем, либо легко могут быть получены с использованием стандартных методик, хорошо известных специалистам в данной области техники. Альтернативно, соединения формулы (I) или (II), где R4 представляет собой гидрокси- или алкокси-замещенную алкильную группу, могут быть получены путем замещения хлоргруппы в промежуточном соединении 1(с) желаемым электрофилом с использованием методик, описанных Sugimoto и др. в Tetrahedron Letters, 40, 2139-2140 (1999). 6-Хлорпуриновое промежуточное соединение 1(c) подвергают взаимодействию с н-бутантеллуролатом лития (продукт взаимодействия теллура с н-бутиллитием) в апротонном растворителе (например, THF) при -78°С с последующим добавлением желаемого электрофила (например, ацетальдегида, бензальдегида, ацетона, метилэтилкетона и т.д.), а затем нагревают до комнатной температуры до образования желаемого гидроксиалкильного производного. Альтернативно, гидрокси-производное может быть образовано с использованием методик, описанных Leonard и др. в J. Org. Chem., 44(25), 4612-4616 (1979). 6-Хлорпуриновое промежуточное соединение 1(c) обрабатывают н-бутилли-тием до образования карбаниона при -78°С с последующим взаимодействием с желаемым электрофилом (например, кетоном или ацетальдегидом) до образования гидроксиалкильного производного. Еще в одном подходе 6-ароилпуриновое соединение может быть получено с использованием методик, описанных Miyashita и др. в Chem. Pharm. Bull., 46(30), 390-399 (1998). Ароильная группа затем может быть восстановлена до соответствующего вторичного спирта путем обработки восстанавливающим агентом, таким как алюмогидрид лития. Третичный спирт может быть получен при обработке алкилме-таллическим реагентом, таким как алкильный реагент Гриньяра, в подходящем растворителе (например, тетрагидрофуране, диэтиловом эфире). И, наконец, амин можно ввести путем восстановительного ами-нирования (см. выше). - 17 - 008176 В приведенных выше примерах полученная гидроксиалкильная группа затем может быть подвергнута алкилированию или ацетилированию до образования желаемого алкокси или ацилата (например, (алкил)-С(0)-0-, (арил)-С(0)-0-, (гетероарил)-С(0)-0- и т.д.) по стандартным методикам, хорошо известным специалистам в данной области техники. Альтернативно, гидроксигруппа может быть подвергнута конденсации с другими группировками с получением ряда заместителей (например, сульфамила, сульфонила и т.д.). Аминоалкильную группу можно модифицировать подобным образом с получением амидов, сульфонамидов и т. д. Группа R4 может быть присоединена к пиримидиновой группировке либо после (как описано выше), либо до циклизации пурина. Представленная ниже схема III иллюстрирует введение группы R4 до циклизации пурина. Схема III (I) или (II) Хлоргруппа промежуточного пиримидинового соединения 1(a) может быть замещена желаемым нуклеофилом (например, аминосоединением, спиртом и т. д.) с образованием промежуточного соединения 3(a). Промежуточное соединение 3(a) затем может быть подвергнуто конденсации с арил- или гете-роарилкарбоновой кислотой или производным (например, хлорангидридом кислот, сложным эфиром и т.д.) с получением пуринового соединения (I). Циклизация может быть проведена с использованием методик, описанных Young и др. в J. Med. Chem., 33, 2073-2080 (1990). Например, промежуточное соединение 3(a) нагревают с бензойной кислотой в присутствии полифосфорной кислоты (РРА) до температуры от приблизительно 150 до приблизительно 170°С в течение приблизительно 1 ч. Альтернативно, желаемый пурин (I) может быть получен после того, как этот диамин и арилкарбоновую кислоту нагревают до температуры приблизительно 100°С в присутствии дегидратирующего агента (например, пропанфосфо-новой кислоты циклического ангидрида) в соответствующем растворителе (например, диоксане). Группа В может быть прямо присоединена к пуриновой группировке, как иллюстрируется на приведенной ниже cхеме IV. Схема IV 1(c) 4(c) Промежуточное соединение 4(a) может быть сначала ацилировано хлорангидридом кислоты. Подходящие хлорангидриды кислот (А-СОС!) включают такие соединения, где А представляет собой арил - 18 - 008176 (например, бензоилхлорид), замещенный арил (например, 2-хлорбензоилхлорид, 4-хлорбензоилхлорид и другие замещенные хлорангидриды ариловых кислот), гетероарил или замещенный гетероарил. Соединение 4(b) может быть превращено в промежуточное соединение 4(c) с использованием дегидратирующих агентов, подобных РОС13, по методикам, описанным Н.С. Koppel в J. 0rg. Chem., 23, 1457 (1958) и в J. Chem. Soc, Perkin Trans. I, 879 (1984). Группа В, где В представляет собой арил, замещенный арил, ге-тероарил или замещенный гетероарил, затем может быть введена с использованием реагентов, подобных R1-B(0H)2, R1-Br или R1-I, и катализаторов на основе Pd (см. Y. Wan и др. в Synthesis, 1597-1600 (2002) и содержащиеся там ссылки) или катализаторов на основе меди(П), таких как ацетат меди или бромид меди (см. S. Ding и др. в Tetrahedron Lett., 42, 8751-8755 (2001), A. Klapars et al. J. Am. Chem. Soc., 123, 7727-7729 (2001) и содержащиеся там ссылки). SNAr реакция также может быть полезна для введения электрон-дефицитных гетероциклов (см. М. Medebielle в New. J. Chem., 19, 349 (1995)). Для выделения соединений по настоящему изобретению, а также различных промежуточных соединений, имеющих отношение к ним, могут быть использованы традиционные способы и/или методики разделения и очистки, известные специалисту в данной области техники. Такие методики очевидны специалисту в данной области техники и могут включать, например, все типы хроматографии (жидкостную хроматографию высокого давления (ЖХВД), колоночную хроматографию с использованием общепринятых адсорбентов, таких как силикагель, и тонкослойную хроматографию (ТСХ)), перекристаллизацию и методики дифференциальной (то есть жидкость-жидкость) экстракции. Соединения по настоящему изобретению могут быть выделены и использованы сами по себе или в форме своих фармацевтически приемлемых солей, сольватов и/или гидратов. Термин "соли" относится к неорганическим и органическим солям соединения по настоящему изобретению, которые могут быть введены в молекулу посредством ионной связи или в виде комплекса. Эти соли могут быть получены in situ в процессе окончательного выделения и очистки соединения или путем отдельного взаимодействия соединения или пролекарства с подходящей органической или неорганической кислотой или основанием и выделения образовавшейся таким образом соли. Типичные соли включают соли гидробромид, гидрохлорид, гидроиодид, сульфат, бисульфат, нитрат, ацетат, трифторацетат, оксалат, безилат, пальмитиат, памоат, малонат, стеарат, лаурат, малат, борат, бензоат, лактат, фосфат, гексафторфосфат, бензолсульфо-нат, тозилат, формиат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат, мезилат, глюкогептонат, лактобионат и лаурилсульфонат и тому подобное. Предпочтительными солями соединений по настоящему изобретению являются соли мезилат, безилат и гидрохлорид. Эти соли могут включать катионы щелочных и щелочно-земельных металлов, таких как натрий, литий, калий, кальций, магний и тому подобное, а также нетоксичные катионы аммония, четвертичного аммония и аминов, включая аммоний, тетра-метиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, этиламин и тому подобное, но ими не ограничиваются. См., например Berge, et al., J. Pharm. Sci., 66, 1-19 (1977). Термин "пролекарство" означает соединение, которое in vivo подвергается трансформации с образованием соединения формулы (I) или фармацевтически приемлемой соли, гидрата или сольвата этого соединения. Эта трансформация может протекать по различным механизмам, например посредством гидролиза в крови. Обсуждение использования пролекарств приведено в Т. Higuchi and W. Stella, "Prodrugs as Novel Delivery Systems", Vol. 14 of the A.C.S. Symposium Series и в Bioreversible Carriers in Drag Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987. Например, если соединение по настоящему изобретению содержит карбоново-кислотную функциональную группу, то пролекарство может включать сложный эфир, образованный замещением атома водорода кислотной группы такой группой, как (С1-С8)алкил, (С2-С12)алканоилоксиметил, 1-(алканоилокси) этил, имеющий от 4 до 9 атомов углерода, 1-метил-1-(алканоилокси)этил, имеющий от 5 до 10 атомов углерода, алкоксикарбонилоксиметил, имеющий от 3 до 6 атомов углерода, 1-(алкоксикарбонилокси)этил, имеющий от 4 до 7 атомов углерода, 1-метил-1-(алкоксикарбонилокси)этил, имеющий от 5 до 8 атомов углерода, ^(алкоксикарбонил)аминометил, имеющий от 3 до 9 атомов углерода, 1-(№(алкоксикарбонил) амино)этил, имеющий от 4 до 10 атомов углерода, 3-фталидил, 4-кротонолактонил, гамма-бутиролактон-4-ил, ди-^^^-С^алкиламино^-С^алкил (как, например, в-диметиламиноэтил), карбамоил(С1-С2)алкил, ^^ди^-С^алкилкарбамоил^-С^алкил и пиперидино-, пирролидино- или морфолино(С1-С2)алкил. Подобным образом, если соединение по настоящему изобретению содержит спиртовую функциональную группу, то пролекарство может быть образовано замещением атома водорода спиртовой группы такой группой, как (С1-С6)алканоилоксиметил, 1-((С1-С6)алканоилокси)этил, 1-метил-1-((С1-С6)алканоил-окси)этил, (С1-С6)алкоксикарбонилоксиметил, ^(С^С^алкоксикарбониламинометил, сукциноил, (С1-С6)алканоил, а-амино(С1-С4)алканоил, арилацил и а-аминоацил или а-аминоацил-а-аминоацил, где каждая а-аминоацильная группа независимо выбрана из L-аминокислот природного происхождения, Р(0)(ОН)2, Р(0)(0(С1-С6)алкил)2 или гликозил (радикал, образованный в результате удаления гидро-ксильной группы полуацетальной формы углевода). Если соединение по настоящему изобретению содержит функциональную аминогруппу, пролекарство может быть образовано замещением атома водорода в аминогруппе такой группой, как R-карбонил, R0-карбонил, NRR'-карбонил, где R и R', каждый независимо представляет собой (С1-С10)алкил, (С3- - 19 - 008176 С7)циклоалкил, бензил, или R-карбонил представляет собой природный а-аминоацил или (природный а-аминоацил)-(природный а-аминоацил), -C(0H)C(0)0Y', где Y' представляет собой Н, (С1-С6)алкил или бензил, -C(0Y0)Y1, где Y0 представляет собой (С1-С4)алкил и Y1 представляет собой (С1-С6)алкил, кар-бокси(С1-С6)алкил, амино(С1-С4)алкил или моно-N- либо ди-^^^-С^алкиламиноалкил, -С(Y2)Y3, где Y2 представляет собой Н или метил и Y3 представляет собой моно-N- или ди-^^^-С^алкиламино, морфолино, пиперидин-1-ил или пирролидин-1-ил. Соединения по настоящему изобретению (в том числе промежуточные соединения по изобретению) могут содержать асимметрические или хиральные центры, поэтому эти соединения и промежуточные соединения могут существовать в разных стереоизомерных формах (например, энантиомеры и диасте-реоизомеры). Это означает, что все стереоизомерные формы промежуточных соединений и соединений по настоящему изобретению, а также их смеси, включая рацемические смеси, составляют часть настоящего изобретения. Кроме того, настоящее изобретение охватывает все геометрические изомеры и позиционные изомеры. Например, если промежуточное соединение или соединение по настоящему изобретению содержит двойную связь или конденсированное кольцо, то как цис-, так и транс-форма, а также их смеси входят в объем изобретения. Диастереомерные смеси могут быть разделены на их индивидуальные диастереоизомеры на основе их физико-химических различий способами, хорошо известными специалистам в данной области техники, например хроматографией и/или фракционной кристаллизацией. Энантиомеры могут быть разделены путем превращения энантиомерной смеси в диастереомерную смесь в результате взаимодействия с подходящим оптически активным соединением (например, хиральным вспомогательным веществом, таким как хиральный спирт или хлорангидрид Мошера (Mosher)), разделения диастереоизомеров и превращения (например, гидролизом) индивидуальных диастереоизомеров в соответствующие чистые энантиоме-ры. Кроме того, некоторые соединения по настоящему изобретению могут представлять собой атропизо-меры (например, замещенные биарилы) и рассматриваются как часть данного изобретения. Энантиомеры также могут быть разделены с использованием хиральной ЖХВД колонки. Соединения по настоящему изобретению могут существовать в несольватированной форме, а также в сольватированной форме с фармацевтически приемлемыми растворителями, такими как вода, этанол и тому подобное, и это означает, что изобретение охватывает как сольватированные, так и несольватиро-ванные формы. Возможно также, что промежуточные соединения и соединения по настоящему изобретению могут существовать в разных таутомерных формах, и все такие формы входят в объем данного изобретения. Термин "таутомер" или "таутомерная форма" относится к структурным изомерам разной энергии, взаи-мопревращаемым через низкий энергетический барьер. Например, протонные таутомеры (также известные как прототропные таутомеры) включают взаимопревращения посредством миграции протона, например кето-енольную и имин-енаминную изомеризации. Конкретным примером протонного таутомера является имидазольная группировка, в которой водород может мигрировать между кольцевыми атомами азота. Валентные таутомеры включают взаимопревращения посредством перестройки некоторых электронов связи. Настоящее изобретение также охватывает соединения по настоящему изобретению (включая промежуточные соединения), меченные изотопом, которые идентичны перечисленным в данном описании соединениям, если не считать, что один или более атомов заменены атомами, имеющими атомную массу или массовое число, отличную(ое) от атомной массы или массового числа, обычно обнаруживаемых в природе. Примеры изотопов, которые могут быть инкорпорированы в промежуточные соединения или соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, иода и хлора, такие как 2Н, 3Н, 11С, 13С, 14С, 13N, 15N, 150, 170, 180, 31P, 32P, 35S, 18F, 123I, 125I и 36d соответственно. Некоторые меченные изотопом соединения по настоящему изобретению (например, меченные 3Н и 14С) полезны в анализах распределения соединения и/или субстрата в тканях. Тритиированные (то есть 3Н) и меченные изотопом углерод-14 (то есть 14С) соединения особенно предпочтительны благодаря легкости их получения и детектирования. Замещение более тяжелыми изотопами, такими как дейтерий (то есть 2Н), также может давать некоторые терапевтические преимущества, обусловленные повышенной метаболической стабильностью (например, увеличенный in vivo период полувыведения или снижение дозировки), и поэтому может быть предпочтительным в некоторых обстоятельствах. Позитрониспус-кающие изотопы, такие как 15О, 13N, 11С и 18F, полезны для исследований методом позитронной эмиссионной томографии (PET) для изучения заселенности субстрата рецепторами. В общем случае, меченные изотопом соединения по настоящему изобретению могут быть получены по следующим методикам, аналогичным описанным ниже на схемах и/или в примерах, с заменой не меченного изотопом реагента меченным реагентом. Соединения по настоящему изобретению полезны для лечения заболеваний, состояний или расстройств, модулируемых лигандами каннабиноидных рецепторов (например, антагонистами СВ-1 рецепторов), поэтому еще одним воплощением настоящего изобретения является фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по настоящему изобретению и - 20 - 008176 фармацевтически приемлемый эксципиент, разбавитель или носитель. Типичный препарат готовят путем смешивания соединения по настоящему изобретению и носителя, разбавителя или эксципиента. Подходящие носители, разбавители и эксципиенты хорошо известны специалистам в данной области техники и включают такие вещества, как углеводы, воски, растворимые и/или набухаемые в воде полимеры, гидрофильные или гидрофобные вещества, желатин, масла, растворители, воду и им подобное. Выбор конкретного носителя, разбавителя или эксципиента будет зависеть от средства и назначения, по которому соединение по настоящему изобретению будет применяться. Как правило, растворители выбирают из растворителей, признанных специалистами в данной области безвредными (GRAS) для введения млекопитающему. Как правило, безвредными растворителями являются нетоксичные водные растворители, такие как вода и другие нетоксичные растворители, которые растворимы в воде или смешиваются с водой. Подходящие водные растворители включают воду, этанол, про-пиленгликоль, полиэтиленгликоли (например, PEG400, PEG300) и т.д. и их смеси. Препараты могут также включать в себя одно или более из следующих: буферы, стабилизирующие агенты, поверхностно-активные вещества, увлажняющие агенты, смазывающие агенты, эмульгаторы, суспендирующие агенты, консерванты, антиоксиданты, агенты, делающие препарат непрозрачным, глиданты, технологические добавки, красители, подсластители, отдушки, корригенты и другие известные добавки для обеспечения наилучшей презентации лекарственного средства (то есть соединения по настоящему изобретению или фармацевтической композиции на его основе) или содействия производству фармацевтического продукта (то есть лекарства). Препараты могут быть приготовлены с использованием традиционных методик растворения и смешивания. Например, лекарственную субстанцию (то есть соединение по настоящему изобретению или стабилизированную форму соединения (например, комплекс с производным циклодекстрина или другим известным агентом комплексообразования)) растворяют в подходящем растворителе в присутствии одного или более эксципиентов, описанных выше. Соединение по настоящему изобретению обычно вводят в состав фармацевтических лекарственных форм, обеспечивающих легко контролируемую дозировку лекарственного средства и дающий лучший продукт, с которым легко обращаться. Фармацевтическая композиция (или препарат) для применения может быть упакована различными способами в зависимости от способа, используемого для введения данного лекарства. В общем случае, изделие для распространения включает контейнер с размещенным в нем фармацевтическим препаратом в соответствующей форме. Подходящие контейнеры хорошо известны специалистам в данной области и включают такие материалы, как бутылки (пластиковые и стеклянные), саше, ампулы, пластиковые пакеты, металлические цилиндрические сосуды и тому подобное. Контейнер также может включать в себя блок, предохраняющий от неумелого обращения, для предупреждения неосторожного доступа к содержимому упаковки. Кроме того, контейнер снабжен этикеткой с описанием содержимого контейнера. Этикетка также может содержать соответствующие предостережения. Согласно настоящему изобретению предложен также способ лечения заболеваний, состояний и/или расстройств, модулируемых антагонистами каннабиноидных рецепторов, у животного, включающий введение животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по настоящему изобретению или фармацевтической композиции, содержащей эффективное количество соединения по настоящему изобретению и фармацевтически приемлемый эксципиент, разбавитель или носитель. В частности, данный способ полезен для лечения заболеваний, состояний и/или расстройств, модулируемых антагонистами каннабиноидных рецепторов (в частности, СВ1 рецептора). Проведенные ранее исследования показали, что антагонисты каннабиноидных рецепторов модулируют следующие заболевания, состояния и/или расстройства: расстройства приема пищи (например, расстройство, представляющее собой резкое увеличение приема пищи, анорексию и булимию), похудание или регулирование массы (например, снижение потребления калорий или пищи и/или подавление аппетита), ожирение, депрессию, атипичную депрессию, биполярные расстройства, психозы, шизофрению, поведенческие пристрастия, подавление связанного с поощрением поведения (например, условно-рефлекторное избегание места, такое как подавление условно-рефлекторного предпочтения места, побуждающего к употреблению кокаина или морфина), злоупотребление веществами, расстройства привыкания, импульсивность, алкоголизм (например, злоупотребление алкоголем, пристрастие к алкоголю и/или алкогольная зависимость, включая лечение в целях отказа от приема алкоголя, стремления к сокращению приема алкоголя и предупреждения рецидивов), злоупотребление табаком (например, пристрастие к курению, прекращение курения и/или зависимость от него, включая лечение в целях стремления к сокращению табакокурения и предупреждения рецидивов), деменцию (в том числе потерю памяти, болезнь Альцгеймера, старческую деменцию, сосудистую деменцию, умеренное ухудшение когнитивной способности, возрастное ухудшение когнитивной способности и умеренное нейрокогнитивное расстройство), половую дисфункцию у мужчин (например, эректильную дисфункцию), судорожные расстройства, эпилепсию, расстройства желудочно-кишечного тракта (например, дисфункцию желудочно-кишечной моторики и кишечной пропульсии), синдром дефицита внимания/гиперактивности (ADHD), болезнь Паркинсона и диабет типа II. Соответственно, описанные здесь соединения по настоящему изобретению полезны в лечении за - 21 - 008176 болеваний, состояний или расстройств, которые модулируются антагонистами каннабиноидных рецепторов. Таким образом, соединения по настоящему изобретению (в том числе композиции и способы, в которых они используются), могут быть полезны в производстве лекарства для описанных здесь терапе-тических применений. Другие заболевания, состояния и/или расстройства, в отношении которых антагонисты каннабино-идных рецепторов могут быть эффективны, включают: предменструальный синдром или синдром поздней фазы созревания желтого тела, мигрени, паническое расстройство, тревогу, посттравматический синдром, социальную фобию, когнитивную недостаточность у неслабоумных индивидуумов, не вызывающую нарушение памяти умеренную когнитивную недостаточность, послеоперационное ухудшение когнитивной способности, расстройства, ассоциированные с импульсивным поведением (такие как разрушительные поведенческие расстройства (например, тревога/депрессия, перестройка исполнительной функции, тиковые расстройства, нарушение манеры поведения и/или оппозиционное вызывающее поведение), расстройства зрелой личности (например, пограничное расстройство личности и антисоциальное расстройство личности), заболевания, ассоциированные с импульсивным поведением (например, злоупотребление веществами, парафилия и членовредительство) и расстройства импульсивного конроля (например, перемежающееся взрывное расстройство, клептомания, пиромания, патологическая склонность к азартным играм и трихотиломания)), обсессивно-компульсивное расстройство, синдром хронической усталости, сексуальную дисфункцию у мужчин (например, преждевременную эякуляцию), сексуальную дисфункцию у женщин, расстройства сна (например, апноэ во сне), аутизм, мутизм, нейродегенеративные двигательные расстройства, повреждение спинного мозга, повреждение центральной нервной системы (например, травма), удар, нейродегенеративные заболевания или токсические или инфекционные заболевания ЦНС (например, энцефалит или менингит), сердечно-сосудистые расстройства (например, тромбоз) и диабет. Соединения по настоящему изобретению можно вводить пациенту в дозировке в пределах от приблизительно 0,7 до приблизительно 7000 мг в сутки. Для взрослого человека, имеющего массу тела приблизительно 70 кг, дозировка в пределах от приблизительно 0,01 до приблизительно 100 мг на килограмм массы тела обычно бывает достаточной. Однако некоторая вариабельность в общем диапазоне дозировок может понадобиться в зависимости от возраста и массы подвергаемого лечению субъекта, планируемого способа введения, конкретного вводимого соединения и т.п. Определение диапазонов дозировок и оптимальных дозировок для конкретного пациента находится в пределах компетенции специалиста в данной области, располагающего настоящим описанием. Кроме того, необходимо отметить, что соединения по настоящему изобретению могут быть использованы в форме препаратов длительного высвобождения, регулируемого высвобождения и задержанного высвобождения, и такие формы также хорошо известны специалисту в данной области. Соединения по данному изобретению также могут быть использованы совместно с другими фармацевтическими агентами для лечения описанных здесь заболеваний, состояний и/или расстройств. Поэтому предложены также способы лечения, включающие введение соединений по настоящему изобретению в комбинации с другими фармацевтическими агентами. Подходящие фармацевтические агенты, которые могут быть использованы в комбинации с соединениями по настоящему изобретению, включают средства против ожирения, такие как ингибиторы секреции аполипопротеина-В/микросомального белка-переносчика триглицеридов (аро-В/МТР), агонисты рецептора меланокортина-4 (MCR-4), агонисты холеци-стокинина-А (ССК-А), ингибиторы обратного захвата моноаминов (такие как сибутрамин), симпатоми-метические агенты, агонисты р3-адренергических рецепторов, агонисты допаминовых рецепторов (такие как бромокриптин), аналоги рецепторов меланоцитстимулирующего гормона, агонисты 5-НТ2с рецептора, антагонисты меланинконцентрирующего гормона, лептин (ob-белок), аналоги лептина, агонисты леп-тинового рецептора, антагонисты галанинового рецептора, ингибиторы липазы (такие как тетрагидро-липстатин, то есть орлистат), аноректические агенты (такие как агонисты бомбезина), антагонисты рецепторов нейропептида-Y, тиромиметические агенты, дегидроэпиандростерон или его аналог, агонисты или антагонисты глюкокортикоидного рецептора, антагонисты орексинового рецептора, агонисты рецепторов глюкагоноподобного пептида-1, цилиарные нейротрофические факторы (такие как Axokine(tm), поставляемый Regeneron Pharmaceuticals, Inc., Tarrytown, NY и Procter & Gamble Company, Cincinnati, ОН), ингибиторы агутисвязанного белка (AGRP) человека, антагонисты грелинового рецептора, антагонисты или обратные агонисты рецепторов гистамина 3, агонисты рецепторов нейромедина U и тому подобное. Другие средства против ожирения, включая предпочтительные агенты, приведенные в данном описании ниже, хорошо известны или очевидны в свете настоящего описания специалисту в данной области. Особенно предпочтительны средства против ожирения, выбранные из группы, состоящей из орли-стата, сибутрамина, бромокриптина, эфедрина, лептина и псевдоэфедрина. Предпочтительно соединения по настоящему изобретению и комбинированные терапии назначают в сочетании с физическими упражнениями и целесообразной диетой. Репрезентативные агенты против ожирения для использования в комбинациях, фармацевтических композициях и способах по изобретению могут быть получены способами, известными специалисту в данной области. Например, сибутрамин может быть получен, как описано в патенте США № 4929629; бромокриптин может быть получен, как описано в патентах США №№ 3752814 и 3752888; и орлистат - 22 - 008176 может быть получен, как описано в патентах США №№ 5274143, 5420305, 5540917 и 5643874. Все приведенные выше патенты США включены в данное описание посредством ссылки. Другие подходящие фармацевтические агенты, которые можно вводить в комбинации с соединениями по настоящему изобретению, включают агенты, предназначенные для лечения злоупотребления табаком (например, частичные агонисты никотиновых рецепторов, бупропиона гипохлорид (также известный под торговым названием Zyban(tm)) и никотиновые заместительные терапии), агенты для лечения эректильной дисфункции (например, допаминергические агенты, такие как апоморфин), агенты против ADHD (например, Ritalin(tm), Strattera(tm), Concerta(tm) и Adderall(tm)) и агенты для лечения алкоголизма, такие как опиоидные антагонисты (например, налтрексон (также известный под торговым названием ReVia(tm)) и налмефен), дисульфирам (также известный под торговым названием Antabuse(tm)) и акампро-сат (также известный под торговым названием Campral(tm))). Кроме того, также можно совместно вводить агенты для снижения симптомов алкогольной абстиненции, такие как бензодиазепины, бета-блокаторы, клонидин, карбамазепин, прегабалин и габапентин (Neurontin(tm)). Лечение алкоголизма предпочтительно назначают в комбинации с поведенческой терапией, включая такие компоненты, как мотивационная активирующая терапия, когнитивная поведенческая терапия и направление в группы самопомощи, включая общество анонимных алкоголиков (АА). Другие фармацевтические агенты, которые могут быть полезны, включают гипотензивные агенты; антидепрессанты (например, флуоксетина гидрохлорид (Prozac(tm))); агенты, улучшающие когнитивную способность (например, донепезил гидрохлорид (Aircept(tm)) и другие ингибиторы ацетилхолинэстеразы); нейропротекторные агенты (например, мемантин); антипсихотические лекарства (например, зипразидон (Geodon(tm)), рисперидон (Risperdal(tm)) и оланзапин (Zyprexa(tm))); инсулин и аналоги инсулина (например, LysPro-инсулин), GLP-1 (7-37) (инсулинотропин) и GLP-1 (7-36)-NH2; сульфонилмочевины и их аналоги: хлорпропамид, глибенкламид, толбутамид, толазамид, ацетогексамид, Glypizide(r), глимепирид, репагли-нид, меглитинид; бигуаниды: метформин, фенформин, буформин; а2-антагонисты и имидазолины: мида-глизол, изаглидол, дериглидол, идазоксан, эфароксан, флупароксан; другие средства, усиливающие секрецию инсулина: линоглирид, А-4166; глитазоны: сиглитазон, Actos(r) (пиоглитазон), энглитазон, трогли-тазон, дарглитазон, Avandia(r) (BRL49653); ингибиторы окисления жирных кислот: кломоксир, этомоксир; ингибиторы а-глюкозидазы: акарбозу, миглитол, эмиглитат, воглибозу, MDL-25637, камиглибозу, MDL-73945; в-агонисты: BRL 35135, BRL 37344, R0 16-8714, ICI D7114, CL 316243; ингибиторы фосфодиэсте-разы: L-386398; снижающие содержание липидов агенты: бенфлуорекс, фенфлурамин; ванадатные и ванадиевые комплексы (например, Naglivan(r)) и пероксованадиевые комплексы; амилиновые антагонисты; глюкагоновые антагонисты; ингибиторы глюконеогенеза; аналоги соматостатина; антилиполитические агенты: никотиновую кислоту, аципимокс, WAG 994, прамлинтид (Symlin(tm)), AC 2993, натеглинид, ингибиторы альдозоредуктазы (например, зополрестат), ингибиторы гликогенфосфорилазы, ингибиторы сорбитолдегидрогеназы, ингибиторы натрий-водородного ионообменника типа 1 (NHE-1) и/или ингибиторы биосинтеза холестерина или ингибиторы абсорбции холестерина, в частности ингибитор HMG-CoA-редуктазы, или ингибитор HMG-CoA-синтазы, либо ингибитор экспрессии гена HMG-CoA-редуктазы или -синтазы, ингибитор СЕТР, усиливающее экскрецию желчных кислот вещество, фибрат, ингибитор АСАТ, ингибитор скваленсинтетазы, антиоксидант или ниацин. Соединения по настоящему изобретению также можно вводить в комбинации с соединением природного происхождения, снижающим уровни холестерина в плазме. Такие соединения природного происхождения обычно называются нутрицевтическими и включают, например, экстракт чеснока, растительные экстракты Hoodia и ниацин. Дозировка дополнительного фармацевтического агента, как правило, зависит от ряда факторов, включая состояние здоровья подвергаемого лечению субъекта, продолжительность желаемого лечения, характер и вид параллельной терапии, если она проводится, периодичность лечения и характер желательного эффекта. В общем случае, диапазон дозировки дополнительного фармацевтического агента составляет от приблизительно 0,001 до приблизительно 100 мг на кг массы тела субъекта в сутки, предпочтительно от приблизительно 0,1 до приблизительно 10 мг на кг массы тела субъекта в сутки. Однако некоторая вариабельность общего диапазона дозировки может также понадобиться в зависимости от возраста и массы подвергаемого лечению субъекта, планируемого пути введения, конкретного вводимого агента против ожирения и т. п. Определение диапазонов дозировки и оптимальных дозировок для конкретного пациента также находится в пределах компетенции специалиста в данной области, располагающего настоящим описанием. В соответствии со способами по данному изобретению соединение по настоящему изобретению или комбинацию соединения по настоящему изобретению и по меньшей мере одного дополнительного фармацевтического агента вводят нуждающемуся в таком лечении субъекту предпочтительно в форме фармацевтической композиции. В аспекте данного изобретения, касающемся комбинации, соединение по настоящему изобретению и по меньшей мере один другой фармацевтический агент (например, агент против ожирения, частичный агонист никотинового рецептора, агент против ADHD, допаминергический агент или опиоидный антагонист) могут быть введены либо по отдельности, либо вместе в составе фармацевтической композиции, содержащей обоих. Обычно предпочтительно, чтобы такое введение было - 23 - 008176 пероральным. Однако если подвергаемый лечению субъект не способен проглатывать или пероральное введение не может быть осуществлено по иным причинам или нежелательно, подходящим может быть парентеральное или трансдермальное введение. В соответствии со способами по данному изобретению, когда комбинацию соединения по настоящему изобретению и по меньшей мере одного другого фармацевтического агента вводят совместно, такое введение может быть последовательным по времени или одновременным, причем одновременное введение обычно является предпочтительным. При последовательном введении соединение по настоящему изобретению и дополнительный фармацевтический агент можно вводить в любом порядке. В общем случае, предпочтительно, чтобы такое введение было пероральным. Особенно предпочтительно, чтобы такое введение было пероральным и одновременным. Когда соединение по настоящему изобретению и дополнительный фармацевтический агент вводят последовательно, то введение каждого может осуществляться одним способом или разными способами. В соответствии со способами по данному изобретению соединение по настоящему изобретению или комбинацию соединения по настоящему изобретению и по меньшей мере одного дополнительного фармацевтического агента (упоминаемую в данном описании как "комбинация") предпочтительно вводят в форме фармацевтической композиции. Соответственно, соединение по настоящему изобретению или комбинацию можно вводить пациенту по отдельности или совместно в любой традиционной перораль-ной, ректальной, трансдермальной, парентеральной (например, внутривенной, внутримышечной или подкожной), интрацистернальной, интравагинальной, интраперитонеальной, интравезикальной, местной (например, в форме порошка, мази или капель) или трансбуккальной или назальной лекарственной форме. Как правило, композиции, пригодные для парентеральной инъекции, включают фармацевтически приемлемые стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии и стерильные порошки для разведения в стерильных инъекционных растворах или дисперсиях. Примеры подходящих водных и неводных носителей или разбавителей (включая растворители и наполнители) включают воду, этанол, полиолы (пропиленгликоль, полиэтиленгликоль, глицерин и тому подобное), подходящие их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры, такие как этилолеат. Надлежащую текучесть можно поддерживать, например, используя покрытия, такие как лецитин, сохраняя требуемый размер частиц в случае дисперсии или используя поверхностно-активные вещества. Эти композиции также могут содержать эксципиенты, такие как консервирующие, увлажняющие, эмульгирующие и диспергирующие агенты. Предохранение от загрязнения микроорганизмами данных композиций может быть выполнено с использованием различных антибактериальных и противогрибковых агентов, например парабенов, хлорбутанола, фенола, сорбиновой кислоты и им подобных. Также может быть желательно включение в состав изотонических агентов, например сахаров, хлорида натрия и им подобных. Пролонгированное всасывание инъецируемых фармацевтических композиций может быть осуществлено с использованием агентов, способных задерживать всасывание, например моностеарата алюминия и желатина. Твердые лекарственные формы для перорального введения включают капсулы, таблетки, порошки и гранулы. В таких твердых лекарственных формах соединение по настоящему изобретению или комбинацию смешивают с по меньшей мере одним обычным инертным фармацевтическим эксципиентом (или носителем), таким как цитрат натрия, или дизамещенный фосфат кальция, или (а) наполнители или сухие разбавители (например, крахмалы, лактоза, сахароза, маннит, кремниевая кислота и тому подобное); (б) связующие (например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза, аравийская камедь и тому подобное); (в) увлажнители (например, глицерин и тому подобное); (г) разрыхлители (например, агар-агар, карбонат кальция, картофельный крахмал или крахмал из тапиоки, аль-гиновая кислота, некоторые сложные силикаты, карбонат натрия и тому подобное); (д) замедлители растворения (например, парафин и тому подобное); (е) ускорители всасывания (например, четвертичные аммониевые соединения и тому подобное); (ж) смачивающие агенты (например, цетиловый спирт, моно-стеарат глицерина и тому подобное); (з) адсорбенты (например, каолин, бентонит и тому подобное); и/или (и) смазывающие вещества (например, тальк, стеарат кальция, стеарат магния, твердые полиэти-ленгликоли, лаурилсульфат натрия и тому подобное). В случае капсул и таблеток лекарственные формы могут также содержать буферные агенты. Твердые композиции подобного типа могут быть использованы также в качестве наполнителей в мягких или твердых желатиновых капсулах с использованием таких эксципиентов, как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей и тому подобного. Твердые лекарственные формы, такие как таблетки, драже, капсулы и гранулы, могут быть приготовлены с покрытиями и оболочками, такими как энтеросолюбильные и другие покрытия, хорошо известные в данной области. Они также могут содержать заглушающие агенты и могут также быть такого состава, что они высвобождают соединение по настоящему изобретению и/или дополнительный фармацевтический агент с задержкой. Примерами герметиков, которые могут быть использованы, являются полимерные вещества и воски. Лекарственное средство может быть также в микроинкапсулированной форме, если подходит, с одним или более чем одним из упомянутых выше эксципиентов. - 24 - 008176 Жидкие лекарственные формы для перорального введения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к соединению по настоящему изобретению или комбинации жидкая лекарственная форма может содержать инертные разбавители, обычно используемые в данной области, такие как вода или другие растворители, солюбилизирующие агенты и эмульгаторы, например этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (например, хлопковое масло, арахисовое масло, кукурузное масло, оливковое масло, касторовое масло, кунжутное масло и тому подобное), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот и сорбитана или смеси этих веществ и тому подобное. Кроме таких инертных разбавителей композиция также может включать в себя такие эксципиенты, как увлажняющие агенты, эмульгирующие и суспендирующие агенты, подсластители, корригенты и отдушки. Суспензии, в дополнение к соединению по настоящему изобретению или комбинации, могут также содержать суспендирующие агенты, например этоксилированные изостеариловые спирты, эфиры поли-оксиэтиленсорбита и сорбитана, микрокристаллическую целлюлозу, метагидроксид алюминия, бентонит, агар-агар и трагакант или смеси этих веществ и тому подобное. Композиции для ректального или вагинального введения предпочтительно включают суппозитории, которые могут быть приготовлены смешиванием соединения по настоящему изобретению или комбинации с подходящими, не вызывающими разражения эксципиентами или носителями, такими как масло какао, полиэтиленгликоль или суппозиторный воск, который является твердым при обычной комнатной температуре, но жидким при температуре тела и поэтому плавится в прямой кишке или вагинальной полости, тем самым высвобождая активный(ые) компонент(ы). Лекарственные формы для местного введения соединений по настоящему изобретению и комбинаций соединений по настоящему изобретению с агентами против ожирения могут представлять собой мази, порошки, спреи и ингалируемые средства. Лекарственные средства смешивают в стерильных условиях с фармацевтически приемлемым носителем и любыми консервантами, буферами или пропеллентами, которые могут потребоваться. Офтальмические препараты, глазные мази, порошки и растворы входят в объем настоящего изобретения. В следующих ниже абзацах описаны типичные препараты, дозировки и т.д., полезные для живот-ных-не людей. Введение соединений по настоящему изобретению и комбинаций соединений по настоящему изобретению с агентами против ожирения может быть осуществлено перорально или неперорально (например, инъекцией). Количество соединения по настоящему изобретению или комбинации соединения по настоящему изобретению с агентом против ожирения вводят таким образом, чтобы была получена эффективная доза. В общем случае суточная доза, вводимая перорально животному, находится между приблизительно 0,01 и приблизительно 1000 мг/кг массы тела, предпочтительно между приблизительно 0,01 и приблизительно 300 мг/кг массы тела. Удобно доставлять соединение по настоящему изобретению (или комбинацию) в питьевой воде с тем, чтобы терапевтическая дозировка данного соединения проглатывалась с суточным запасом воды. Соединение может быть прямо отмерено в питьевую воду, предпочтительно в форме жидкого, водорастворимого концентрата (такого, как водный раствор водорастворимой соли). Удобно добавлять соединение по настоящему изобретению (или комбинацию) также непосредственно в корм, само по себе или в форме кормовой добавки для животных, называемой также премиксом или концентратом. Для введения агента в корм чаще всего используют премикс или концентрат соединения в носителе. Подходящие носители являются жидкими или твердыми, по желанию, такие как вода, различные виды муки, такие как мука из люцерны, соевая мука, мука из семян хлопка, мука из семян льна, мука из кукурузных початков и зерновая мука, меласса, мочевина, костная мука и минеральные смеси, такие как смеси, обычно используемые в качестве корма для домашней птицы. Особенно эффективным носителем является соответствующий животный корм сам, то есть небольшая порция такого корма. Носитель способствует равномерному распределению соединения в конечном корме, с которым смешивают премикс. Предпочтительно соединение тщательно перемешивают в премиксе и, соответственно, в корме. Для этого соединение может быть диспергировано или растворено в подходящем масляном разбавителе, таком как соевое масло, кукурузное масло, хлопковое масло и тому подобное, либо в летучем органическом растворителе, а затем смешано с носителем. Должно быть понятно, что доля соединения в концентрате может меняться в широких пределах, так как количество соединения в готовом корме можно регулировать путем смешивания соответствующей части премикса с кормом для получения желаемого содержания соединения. Крепкие концентраты могут быть смешаны производителем кормов с белковым носителем, таким как соевая мука и другие виды муки, которые описаны выше, для получения концентрированных добавок, которые подходят непосредственно для кормления животных. В таких случаях животным разрешается потреблять обычный корм. Альтерантивно, такие концентрированные добавки можно добавлять непосредственно в корм для получения сбалансированного с питательной точки зрения готового корма, содержащего терапевтически эффективное количество соединения по настоящему изобретению. Эти - 25 - 008176 смеси тщательно перемешивают для обеспечения гомогенности с использованием стандартных процедур, например в смесителе с двойным кожухом. Если добавку используют для поливки корма, то это также помогает обеспечить однородность распределения соединения по всей поверхности корма. Питьевую воду и корм, эффективные для увеличения отложения постного мяса и для улучшения соотношения постное мясо/жир, обычно готовят путем смешивания соединения по настоящему изобретению с достаточным количеством животного корма для обеспечения содержания данного соединения в корме или воде от приблизительно 10-3 до приблизительно 500 млн-1 долей. Предпочтительный лечебный корм для свиней, крупного рогатого скота, овец и коз в общем случае содержит от приблизительно 1 до приблизительно 400 г соединения по настоящему изобретению (или комбинации) на тонну корма, причем оптимальное количество для этих животных обычно составляет от приблизительно 50 до приблизительно 300 г на тонну корма. Предпочтительные корма для домашней птицы и домашних животных обычно содержат от приблизительно 1 до приблизительно 400 г и предпочтительно приблизительно от 10 до приблизительно 400 г соединения по настоящему изобретению (или комбинации) на тонну корма. Для парентерального введения животным соединение по настоящему изобретению (или комбинация) может быть приготовлено в форме пасты или гранулы и введено в виде имплантата, обычно под кожу головы или уха животного, у которого пытаются увеличить отложение постного мяса и улучшить соотношение постное мясо/жир. В общем случае парентеральное введение включает инъекцию достаточного количества соединения по настоящему изобретению (или комбинации) для доставки животному от приблизительно 0,01 до приблизительно 20 мг/кг/сутки массы тела лекарственного средства. Предпочтительная дозировка лекарственного средства для домашней птицы, свиней, крупного рогатого скота, овец, коз и домашних животных находится в пределах от приблизительно 0,05 до приблизительно 10 мг/кг/сутки массы тела. Препараты в виде пасты могут быть приготовлены путем диспергирования лекарственного средства в фармацевтически приемлемом масле, таком как арахисовое масло, кунжутное масло, кукурузное масло и тому подобное. Гранулы, содержащие эффективное количество соединения по настоящему изобретению, фармацевтической композиции или комбинации, могут быть приготовлены путем смешивания соединения по настоящему изобретению или комбинации с разбавителем, таким как карбовоск, карнаубский воск и тому подобное, а для улучшения процесса гранулирования может быть добавлено смазывающее вещество, такое как стеарат магния или кальция. Само собой разумеется, что для достижения желаемого уровня дозы, который обеспечит желательное увеличение отложения постного мяса и улучшение соотношения постное мясо/жир, животному может быть введена более чем одна гранула. Более того, обнаружено, что имплантаты также можно периодически вводить во время лечения животного, чтобы поддержать надлежащий уровень лекарственного средства в организме животного. Настоящее изобретение имеет несколько ветеринарных преимуществ. Для владельца домашнего животного или ветеринара, которые желают увеличить постность домашних животных и/или избавить их от нежелательного жира, согласно настоящему изобретению предложен способ, с помощью которого этого можно достичь. Для птицеводов, животноводов и свиноводов результатом использования способа по настоящему изобретению являются животные с небольшим содержанием жира, которые продаются по более высоким отпускным ценам. Воплощения настоящего изобретения иллюстрируются приведенными ниже примерами. Следует иметь в виду, однако, что воплощения данного изобретения не ограничены конкретными подробностями этих примеров, так как в свете настоящего описания специалисту в данной области техники станут известны или очевидны другие их варианты. Примеры Если не оговорено особо, исходные вещества получены из коммерческих источников, таких как Aldrich Chemicals Co. (Milwaukee, WI), Lancaster Synthesis, Inc. (Windham, NH), Acros 0rganics (Fairlawn, NJ), Maybridge Chemical Company, Ltd. (Cornwall, England), Tyger Scientific (Princeton, NJ) и AstraZeneca Pharmaceuticals (London, England). Общие экспериментальные методики ЯМР спектры регистрировали на Varian Unity(tm) 400 или 500 (доступен от Varian Inc., Palo Alto, CA) при комнатной температуре при 400 и 500 МГц 1Н соответственно. Химические сдвиги выражены в миллионных долях (8) относительно резидуального растворителя в качестве внутреннего контроля. Формы пиков обозначены следующим образом: s, синглет; d, дублет; t, триплет; q, квартет; m, мультиплет; br s, широкий синглет; v br s, очень широкий синглет; br m, широкий мультиплет; 2s, два синглета. В некоторых случаях даны только репрхарактерные пики 1Н ЯМР. Масс-спектры (MS) регистрировали прямым анализом потоков с использованием химической ионизации при атмосферном давлении (APCI) в режимах сканирования положительных и отрицательных ионов. Для проведения экспериментов использовали масс-спектрометр Waters APCI/MS, модель ZMD, осна - 26 - 008176 щенный жидкостной системой управления Gilson 215. Масс-спектрометрический анализ также осуществляли методом градиентной ОФ-ЖХВД (обращен-но-фазовая жидкостная хроматография высокого давления) для хроматографического разделения. Моле-кулярно-массовую идентификацию фиксировали при электрораспылительной ионизации (ESI) в режимах сканирования положительных и отрицательных ионов. Для проведения экспериментов использовали масс-спектрометр Waters/Micromass ESI/MS, модель ZMD или LCZ, оснащенный жидкостной системой управления Gilson 215 и HP 1100 DAD. Если указана интенсивность хлор- или бромсодержащих ионов, то наблюдалось ожидаемое соотношение интенсивностей (приблизительно 3:1 для 35С1/37С1-содержащих ионов и 1:1 для ^Вт^^-содержа-щих ионов), и приводится только более низкая ионная масса. MS пики приведены для всех примеров. Оптические вращения определяли на поляриметре PerkinElmer(tm) 241 (доступном от PerkinElmer Inc., Wellesley, MA) с использованием натриевой D линии (Х=589 нм) при указанной температуре, и они приводятся следующим образом: [ос]гзтемп, концентрация (с=г/100 мл) и растворитель. Колоночную хроматографию проводили с использованием либо силикагеля Baker(tm) (40 мкм; J.T. Baker, Phillipsburg; NJ), либо силикагеля 50 (ЕМ Sciences(tm), Gibbstown, NJ) в стеклянных колонках или в колонках Biotage(tm) (ISC, Inc., Shelton, CT) при низком давлении азота. Круговую хроматографию проводили с использованием Chromatotron(tm) (Harrison Research). Получение ключевых промежуточных соединений Получение промежуточного 6-хлор-№-(4-хлорфенил)пиримидин-4,5-диамина (I-(lA-l)a). N С1 Н I NH2 И1А-Па 5-Амино-4,6-дихлорпиримидин (5,00 г; 29 ммоль) и 4-хлоранилин (4,71 г; 36 ммоль) суспендировали в 80 мл Н2О и 12 мл этанола. Добавляли концентрированную НС1 (1,2 мл; 14,5 ммоль) при комнатной температуре, а затем нагревали реакционную смесь до 82°С. После перемешивания в течение 19 ч реакционную смесь охлаждали до комнатной температуры и перемешивали в течение 60 ч. Осадок собирали на воронке из пористого стекла и промывали водой, а затем гексанами. После сушки под вакуумом получили Г(1А-1)а в виде не совсем белого твердого вещества (7,38 г; 98%): +ESI MS (М+1) 255,3; 1Н ЯМР (400 МГц, CD3OD): 5 7,87 (s, 1H), 7,66 (d, J=8,7 Гц, 2H), 7,30 (d, J=8,7 Гц, 2Н). Получение промежуточного 2,4-дихлор-N-[4-хлор-6-(4-хлорфениламино)пиримидин-5-ил]бензамида (I-(lA-l)b). ci. 1-(1А-ПЬ 6-Хлор-№-(4-хлорфенил)пиримидин-4,5-диамин Г(1А-1)а (34 г; 134 ммоль) в пиридине (150 мл) охлаждали до 0°С и к нему добавляли 2,4-дихлорбензоилхлорид (25 мл; 178 ммоль). Реакционную смесь оставляли нагреваться до температуры окружающей среды в течение ночи. Твердый осадок собирали вакуумной фильтрацией и сушили под высоким вакуумом с получением указанного в заголовке соединения А-1)Ь в виде бесцветного твердого вещества (14 г; 25%). Пиридиновый раствор концентрировали при пониженном давлении и затем растирали с метанолом (500 мл) с получением дополнительного количества вещества (35 г; 60%): +ESI MS (M+1) 427,4; 1Н ЯМР (400 МГц, DMSO-d6): 5 10,08 (s, 1H), 9,16 (s, 1H), 8,38 (s, 1H), 7,97 (d, J=8,7 Гц, 1H), 7,75 (d, J=2,0 Гц, 2H), 7,64-7,60 (m, 3H), 7,40 (d, J=8,7 Гц, 2Н). Получение промежуточного 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ола (I-(lA-l)c). 1-0 А-Пс Суспензию 2,4-дихлор-N-[4-хлор-6-(4-хлорфениламино)пиримидин-5-ил]бензамида А-1)Ь (48 г; 0,11 моль) в уксусной кислоте (1 л) нагревали до температуры дефлегмации в течение 7 ч. Реакционную - 27 - 008176 смесь охлаждали до 0°С, продукт (бесцветные игольчатые кристаллы) собирали вакуумной фильтрацией и твердое вещество промывали дополнительным количеством уксусной кислоты, этилацетатом и затем эфиром. Продукт сушили в течение ночи под высоким вакуумом с получением указанного в заголовке соединения Ь(1А-1)с (32 г; 73%) в виде бесцветного ворсистого твердого вещества. Маточный раствор концентрировали при пониженном давлении и твердое вещество кристаллизовали из метанола с получением дополнительного количества вещества (16 г) в виде бесцветного твердого вещества: т. пл. 314-315°С; +ESI MS (М+1) 391,3; 1Н ЯМР (400 МГц, CD3OD): 5 8,06 (s, 1H), 7,61 (d, J=8,3 Гц, 1H), 7,52 (d, J=2,1 Гц, 1H), 7,48-7,41 (m, 3H), 7,31 (d, J=8,7 Гц, 2Н). Получение промежуточного 6-хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина (I-(lA-l)d). H1A-I)d 9-(4-Хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ол Ь(1А-1)с (6,5 г; 17 ммоль) нагревали до температуры дефлегмации в РОС13 (3 мл) в течение ночи. Реакционную смесь концентрировали при пониженном давлении и остаток растворяли в хлороформе и выливали на лед. Органический слой разделяли и промывали насыщенным водным NaHCO3. Органические слои объединяли, сушили (Na2SO4), фильтровали и концентрировали при пониженном давлении. Остаток переносили в смесь 1:1 метиленхлорид/ди-этиловый эфир (200 мл) и затем фильтровали для удаления остаточного исходного вещества. Концентрирование органического слоя дало указанное в заголовке соединение I-(1A-1)d в виде желтой пены (5,8 г; 85%): +ESI MS (М+1) 411,4; 1Н ЯМР (400 МГц, DMSO-d6): 5 8,83 (s, 1H), 7,79-7,75 (m, 2H), 7,63-7,58 (m, 1H), 7,56 (d, J=8,7 Гц, 2Н), 7,42 (d, J=6,7 Гц, 2Н). Получение промежуточного 2-хлор-Ы-[4-хлор-6-(4-хлорфениламино)пиримидин-5-ил]бензамида (1-(4А-7)а). N С1 Н т о 1-(4А-7Ь 6-Хлор-Ш-(4-хлорфенил)пиримидин-4,5-диамин Ь(1А-1)а (1,00 г; 3,92 ммоль) растворяли в 6 мл ^^диметилацетамида, получая прозрачный коричневый раствор. После охлаждения до 5°С добавляли за 1 мин неразбавленный 2-хлорбензоилхлорид (0,80 г; 4,34 ммоль). Раствор нагревали до комнатной температуры и перемешивали в течение 4 ч. Добавление воды (15 мл) приводило к выпадению из раствора белого осадка. Смесь перемешивали в течение еще 30 мин при комнатной температуре, после чего осадок собирали вакуумной фильтрацией, промывая Н2О, а затем гексанами. Твердое вещество затем сушили под вакуумом с получением Ь(4А-7)а в виде бесцветного твердого вещества (1,27 г; 82%): +APCI MS (М+1) 393,1; 1H ЯМР (400 МГц, DMSO-d6): 5 10,02 (s, 1Н), 9,11 (s, 1H), 8,40 (s, 1H), 7,93 (dd, J=7,4, 1,6 Гц, 1 Н), 7,66-7,40 (m, 7H). Получение промежуточного 9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ола (I-(4A-7)b). 1-(4А-1)Ъ К суспензии 2-хлор-N-[4-хлор-6-(4-хлорфениламино)пиримидин-5-ил]бензамида Ь(4А-7)а (1,00 г; 2,54 ммоль) в изопропаноле (20 мл) добавляли неразбавленную H2SO4 (410 мкл; 7,4 ммоль) при комнатной температуре. Реакционную смесь кипятили с обратным холодильником в течение 8 ч, после чего охлаждали до комнатной температуры и перемешивали в течение 16 ч. К этому гетерогенному раствору добавляли 20 мл воды для стимуляции осаждения продукта. После перемешивания в течение 1 дополнительного часа при комнатной температуре твердое вещество собирали на воронке из пористого стекла, промывая водой, а затем гексанами. Продукт затем сушили при пониженном давлении с получением Ь(4А-7)Ь в виде бесцветного твердого вещества (0,72 г; 80%): 1Н ЯМР (400 МГц, DMSO-d6): 5 12,57 (s, 1Н), 8,08 (d, J=4,1 Гц, 1H), 7,66 (dd, J=7,4, 1,2 Гц, 1H), 7,51-7,41 (m, 5H), 7,33-7,29 (m, 2H). - 28 - 008176 Получение промежуточного 6-хлор-9-(4-хлорфенил)-8-(2-хлорфенил)9Н-пурина (1-(4А-7)с). И4А-7)с 9-(4-Хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ол I-(4А-7)b (2,49 г; 6,97 ммоль) суспендировали в 50 мл толуола. Добавляли триэтиламин (1,07 мл; 7,68 ммоль) с последующим добавлением РОС13 (720 мкл; 7,72 ммоль) при комнатной температуре. Реакционную смесь нагревали до температуры дефлегмации и перемешивали в течение 23 ч с получением прозрачного оранжевого раствора. После охлаждения реакционной смеси до комнатной температуры ее концентрировали при пониженном давлении, разбавляли изопропанолом (50 мл) и затем концентрировали при пониженном давлении до тех пор, пока из раствора не выпадало значительное количество осадка. Концентрированную суспензию охлаждали в ледяной бане и перемешивали в течение 2 ч. Осадок собирали на воронке из пористого стекла и промывали холодным изопропанолом, что позволило получить после сушки в вакууме Ь(4А-7)с в виде не совсем белого твердого вещества (2,13 г; 82%): +ESI MS (M+1) 375,1; 1Н ЯМР (400 МГц, DMSO-d6): 5 8,84 (s, 1H), 7,76 (dd, J=7,46, 1,2 Гц, 1Н), 7,58-7,40 (m, 7H). Получение промежуточного 6-хлор-К4-(4-хлорфенил)-2-метилпиримидин-4,5-диамина (1-(7А-80)а). 1-(7А-80)а 4,6-Дихлор-2-метилпиримидин-5-иламин (100 мг; 0,56 ммоль) и 4-хлорфениламин (86 мг; 0,68 ммоль) объединяли в Н2О (1,5 мл) и смеси 10:1 этанол/НС1 (0,24 мл) и нагревали до температуры дефлегмации в течение 6 ч. Реакционную смесь охлаждали и к ней добавляли Н2О. Продукт собирали фильтрованием и сушили в высоком вакууме с получением целевого соединения Ц7А-80)а в виде твердого вещества рыжевато-коричневого цвета (173 мг), которое переносят на следующую стадию неочищенным: +ESI MS (M+1) 269,2. Получение промежуточного N-[4-хлор-6-(4-хлорфениламино)-2-метилпиримидин-5-ил]-2-фторбензамида (1-(7А-80)Ь). Н7А-80)Ь 2-Фторбензоилхлорид (93 мкл; 0,78 ммоль) добавляли к 6-хлор-Ш-(4-хлорфенил)-2-метилпирими-дин-4,5-диамину Ь(7А-80)а (173 мг) и пиридину (1 мл) и перемешивали при комнатной температуре в течение 7 ч. Реакция не завершилась к этому времени, поэтому к реакционной смеси дополнительно добавляли 1,5 экв. 2-фторбензоилхлорида и перемешивание продолжали в течение ночи при комнатной температуре. Реакционную смесь экстрагировали из насыщенного раствора №НСО3 в этилацетат. Органические слои объединяли, сушили (Na2SO4), фильтровали и концентрировали досуха сполучением целевого неочищенного продукта Ь(7А-80)Ь (0,25 г): +ESI MS (M+1) 391,2. Получение промежуточного 6-хлор-9-(4-хлорфенил)-8-(2-фторфенил)-2-метил-9Н-пурина (1-(7А-80)с). 1-(7А-80)с Раствор N- [4-хлор-6-(4-хлорфениламино)-2-метилпиримидин-5-ил]-2-фторбензамида Ь(7А-80)Ь (0,25 г) в диоксане (6 мл) обрабатывали 50% циклическим ангидридом пропанфосфорной кислоты - 29 - 008176 (РРАА) в этилацетате (0,6 мл) и нагревали до температуры дефлегмации в течение ночи. Было определено, что продукт представлял собой смесь целевого продукта и оксисоединения (замещение атома хлора). Поэтому реакционную смесь концентрировали при пониженном давлении и нагревали в течение ночи при температуре дефлегмации с РОС13 (6 мл). Реакционную смесь концентрировали досуха, разбавляли этилацетатом и выливали на лед. Далее добавляли насыщенный раствор №НСО3 и эту смесь перемешивали. Органический слой отделяли, промывали рассолом, сушили (Na2SO4), фильтровали и концентрировали досуха. Неочищенный продукт очищали на пластине препаративной ТСХ, используя смесь 5% ме-танола/метиленхлорид в качестве растворителя, с получением целевого соединения Ь(7А-80)с (88 мг; 42% от 4,6-дихлор-2-изопропилпиримидин-5-иламина) в виде твердого вещества: +ESI MS (М+1) 373,2; 1Н ЯМР (400 МГц, CDCI3): 5 7,80-6,90 (m, 8Н), 2,76 (s, 3Н). Получение промежуточного 1-бензил-4-этиламинопиперидин-4-карбонитрила (I-(7A-80)d). HN' CN И7А-80М К раствору 4-№бензилпиперидона (5,69 г; 29,5 ммоль) в этаноле (4,2 мл), охлажденному в ледяной бане, добавляли этиламина гидрохлорид (2,69 г; 32,3 ммоль) в воде (3 мл), поддерживая внутреннюю температуру реакционной смеси ниже 10°С. Раствор KCN (2,04 г; 31,3 ммоль) в воде (7 мл) добавляли к реакционному раствору за 10 мин, поддерживая внутреннюю температуру ниже 10°С. Реакционную смесь затем нагревали до комнатной температуры и перемешивали 18 ч. К реакционной смеси добавляли изопропанол (10 мл) с получением двух отдельных слоев: нижнего бесцветного водного слоя и расположенного выше органического слоя оранжевого цвета. Органический слой отделяли и перемешивали с водой (30 мл) в течение 30 мин. Органический слой отделяли (теперь органический слой оранжевого цвета был внизу) и оранжевое масло разбавляли СН2С12 (30 мл). Органический слой промывали рассолом, сушили (Na2SO4), фильтровали и концентрировали в вакууме с получением Ь(7А-80^ в виде оранжевого масла (6,05 г; 84%): +APCI MS (M+1) 244,2; 1Н ЯМР (400 МГц, CD2C12): 5 7,32 (d, J=4,1 Гц, 4Н), 7,29-7,23 (m, 1Н), 3,54 (s, 2H), 2,81-2,76 (m, 2H), 2,75 (q, J=7,1 Гц, 2H), 2,35-2,29 (m, 2H), 2,01-1,98 (m, 2H), 1,74-1,68 (m, 2H), 1,14 (t, J=7,1 Гц, 3Н). Получение промежуточного 1-бензил-4-этиламинопиперидин-4-карбоновой кислоты амида (1-(7А-80)е). HN' NH2 И7А-80)е Раствор 1-бензил-4-этиламинопиперидин-4-карбонитрила I-(7A-80)d (0,58 г; 2,38 ммоль) в метилен-хлориде (2 мл), охлажденный в ледяной бане, обрабатывали H2SO4 (1,8 мл; 33 ммоль) по каплям, поддерживая внутреннюю температуру ниже 20°С. Реакционную смесь затем нагревали до комнатной температуры и перемешивали в течение 19 ч. После прекращения перемешивания густой бледно-оранжевый H2SO4 нижний слой отделяли, охлаждали в ледяной бане и затем осторожно гасили концентрированным NH4OH, поддерживая внутреннюю температуру ниже 55°С. Водный слой экстрагировали метиленхлори-дом (2х10 мл), объединенные органические слои промывали рассолом (20 мл), сушили (Na2SO4) и затем концентрировали в вакууме с получением Ь(7А-80)е в виде бледно-оранжевого масла, которое при стоянии отверждается до твердого вещества персикового цвета (0,54 г; 87%): +APCI MS (M+1) 262,2; 1Н ЯМР (400 МГц, CD2C12): 5 7,34-7,30 (m, 4H), 7,29-7,21 (m, 1Н), 7,16 (br s, 1H), 3,48 (s, 2H), 2,71-2,68 (m, 2H), 2,47 (q, J=7,0 Гц, 2Н), 2,17-2,02 (m, 4H), 1,62-1,58 (m, 2H), 1,41 (br s, 1H), 1,09 (t, J=7,0 Гц, 3Н). Получение промежуточного 4-этиламинопиперидин-4-карбоновой кислоты амида (I-(7A-80)f). NH2 I-r7A-80)f К раствору 1-бензил-4-этиламинопиперидин-4-карбоновой кислоты амида Ь(7А-80)е (7,39 г; 28,3 ммоль) в метаноле (100 мл) добавляли 20% Pd(OH)2 на угле (50% воды; 1,48 г). Смесь помещали на шейкер Parr(r) и восстанавливали (50 фунт/кв.дюйм (344,75 кПа) Н2) при комнатной температуре в течение ночи. Смесь фильтровали через слой Ce1ite(r) и затем концентрировали до бесцветного твердого вещества (4,84 г; количественно): +APCI MS (М+1) 172,2; 1Н ЯМР (400 МГц, CD2C12): 5 2,89 (ddd, J=12,9, 8,7, 3,3 Гц, 2Н), 2,75 (ddd, J=12,9, 6,6, 3,7 Гц, 2Н), 2,45 (q, J=7,2 Гц, 2Н), 1,95 (ddd, J=13,7, 8,3, 3,7 Гц, 2Н), 1,55 (ddd, J=13,7, 6,6, 3,3 Гц, 2Н), 1,08 (t, J=7,1 Гц, 3Н). Получение промежуточного 4-хлор-№ [4-хлор-6-(4-хлорфениламино)пиримидин-5-ил]-2-фторбензамида (Ц7А-91)а). - 30 - 008176 Н7А-9Па 6-Хлор-Ж-(4-хлорфенил)пиримидин-4,5-диамин 1-(1А-1)а (6,6 г; 26 ммоль) в пиридине (30 мл) охлаждали до 0°С и к нему добавляли 4-хлор-2-фторбензоилхлорид (5 г; 26 ммоль). Реакционную смесь затем оставляли нагреваться до температуры окружающей среды в течение ночи. Гетерогенную реакционную смесь разбавляли этанолом (50 мл) и полученное твердое вещество собирали фильтрованием. Твердые вещества суспендировали в толуоле, который затем удаляли при пониженном давлении для удаления остаточного этанола. Твердое вещество суспендировали в диэтиловом эфире и затем собирали фильтрованием с получением 1-(7А-91)а (8,3 г; 78%): +APCI MS (М+1) 409,0; 1Н ЯМР (400 МГц, CD3OD): 5 10,60 (s, 1Н), 10,10 (s, 1H), 9,19 (s, 1H), 8,74 (t, J=8,1 Гц, 1H), 8,46-8,40 (m, 3H), 8,28 (dd, J=8,7, 2,1 Гц, 1Н), 8,20 (d, J=8,7 Гц, 2H). Получение промежуточного 6-хлор-8-(4-хлор-2-фторфенил)-9-(4-хлорфенил)-9Н-пурина (I-(7A-91)b). I-(7A-91)b Суспензию 4-хлор-К-[4-хлор-6-(4-хлорфениламино)пиримидин-5-ил]-2-фторбензамида Ь(7А-91)а (8,3 г; 20 ммоль) в РОС13 (100 мл) нагревали до температуры дефлегмации. Светло-коричневая реакционная смесь становилась гомогенной через 2 ч. После кипячения с обратным холодильником в течение 3 ч реакционную смесь охлаждали и концентрировали при пониженном давлении с получением вязкого масла. Остаток разбавляли этилацетатом и выливали в смесь лед/водный бикарбонат натрия. Органический слой отделяли, промывали рассолом, сушили (Na2SO4) и концентрировали. Кристаллизация из диэтило-вого эфира привела к получению продукта Ь(7А-91)Ь (5,8 г; 73%) в виде не совсем белого твердого вещества: +ESI MS (М+1) 393,0; 1Н ЯМР (400 МГц, DMSO-d6): 5 8,81 (s, 1H), 7,72 (t, J=8,1 Гц, 1H), 7,607,55 (m, 3H), 7,50-7,42 (m, 3H). Получение промежуточного 1-бензгидрил-З-изопропиламиноазетидин-З-карбонитрила (1-(7А-106)а). H7A-106te К раствору 1-бензгидрилазетидин-3-она (3,20 г; 13,5 ммоль) в этаноле (100 мл), охлажденому в ледяной бане, добавляли изопропиламин (1,26 мл; 14,8 ммоль) с последующим добавлением по каплям концентрированного водного НС1 (1,23 мл; 14,8 ммоль). После перемешивания в течение 15 мин к реакционной смеси добавляли раствор NaCN (0,727 г; 14,8 ммоль) в воде (30 мл) за 7 мин. Реакционную смесь затем нагревали до комнатной температуры и перемешивали в течение ночи. После концентрирования реакционной смеси в вакууме до половины объема проводили экстракцию из насыщенного водного бикарбоната натрия этилацетатом. Объединенные органические слои промывали рассолом, сушили (Na2SO4), фильтровали и концентрировали в вакууме с получением масла (3,17 г), которое представляло собой смесь 2:1 цианогидрина и кетона, что было установлено по данным 1Н ЯМР и LCMS. Раствор остатка в метаноле (17 мл) обрабатывали изопропиламином (2,3 мл; 27 ммоль) и затем уксусной кислотой (1,6 мл; 27 ммоль) при комнатной температуре. После перемешивания в течение 30 мин добавляли твердый NaCN (330 мг; 6,7 ммоль) и эту смесь нагревали до температуры дефлегмации в течение ночи. Реакционную смесь концентрировали в вакууме и затем экстрагировали из насыщенного водного бикарбоната натрия этилацетатом. Объединенные органические слои промывали рассолом, сушили (Na2SO4), фильтровали и концентрировали в вакууме с получением I-(7A-106)a в виде темной пены (3,41 г; 83%): +APCI MS (M+1) 306,4; 1H ЯМР (400 МГц, CD2Q2): 5 7,45-7,42 (m, 4Н), 7,31-7,18 (m, 6Н), 4,42 (s, 1H), - 31 - 008176 3,68 (d, J=8,3 Гц, 2Н), 3,11 (септуплет, J=6,2 Гц, 1Н), 3,07 (d, J=8,3 Гц, 2H), 1,01 (d, J=6,2 Гц, 6Н). Получение промежуточного 1-бензгидрил-3-изопропиламиноазетидин-3-карбоновой кислоты амида (1-(7А-106)Ь). ША-Юб^Ь Раствор 1-бензгидрил-3-изопропиламиноазетидин-3-карбонитрила (1-(7А-106)а; 3,40 г; 11,1 ммоль) в метиленхлориде (25 мл), охлажденный в ледяной бане, обрабатывали H2SO4 (5,95 мл; 111 ммоль) по каплям. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешиваться в течение ночи, после чего ее охлаждали в ледяной бане и затем осторожно гасили концентрированным NH4OH до рН 11. Смесь экстрагировали метиленхлоридом, объединенные органические слои сушили (Na2SO4) и затем концентрировали в вакууме с получением неочищенной пены (3,3 г), которую затем очищали на колонке Biotage(tm) Flash 40M, используя смесь 0-2% метанола в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения Г(7А-106)Ь (2,32 г; 64%) в виде твердого вещества коричневого цвета: +ESI MS (М+1) 324,4; 1Н ЯМР (400 МГц, CD3OD): 5 7,40 (d, J=7,5 Гц, 4Н), 7,24 (t, J=7,5 Гц, 4Н), 7,15 (t, J=7,1 Гц, 2Н), 4,46 (s, 1H), 3,53 (d, J=8,7 Гц, 2Н), 3,06 (d, J=8,7 Гц, 2Н), 2,90 (септуплет, J=6,4 Гц, 1H), 0,97 (d, J=6,6 Гц, 6Н). Получение промежуточного 3-изопропиламиноазетидин-3-карбоновой кислоты амида, гидрохло-ридной соли (I-(7A-106)c). NH2 HN. " 0 -2HC1 I-(7A-106)c К раствору 1-бензгидрил-3-изопропиламиноазетидин-3-карбоновой кислоты амида (Т-(7А-106)Ь; 2,28 г; 7,05 ммоль) в метаноле (100 мл) добавляли 1М НС1 в эфире (14,8 мл; 14,8 ммоль) и затем воду (10 мл). После добавления 20% Pd(OH)2 на угле (60% воды; 1,43 г) смесь помещали на шейкер Parr(r) и затем восстанавливали (50 фунт/кв. дюйм (344,75 кПа) Н2) при комнатной температуре в течение ночи. Смесь фильтровали через слой Celite(r) и затем концентрировали в вакууме. Остаток затем концентрировали в вакууме из толуола (2Х), ацетонитрила (2Х) и затем метанола с получением Г(7А-106)с (1,59 г; 98%) в виде твердого вещества рыжевато-коричневого цвета: +APCI MS (М+1) 158,1; 1 Н ЯМР (400 МГц, CD3OD): 5 4,71 (d, J=13,3 Гц, 2Н), 4,60 (d, J=13,3 Гц, 2Н), 3,49 (септуплет, J=6,6 Гц, 1Н), 1,34 (d, J=6,6 Гц, 6Н). Получение промежуточного 1-бензгидрил-З-бензиламиноазетидин-З-карбонитрила (1-(13А-9)а). 1-ПЗА-9)а К раствору 1-бензгидрилазетидин-3-она (3,3 г; 14 ммоль) в метаноле (35 мл) добавляли бензиламин (1,6 мл; 15 ммоль) и затем уксусную кислоту (0,88 мл; 15 ммоль) при комнатной температуре. После перемешивания в течение 45 мин порциями добавляли твердый NaCN (0,76 г; 15 ммоль) за 2 мин и эту смесь нагревали до температуры дефлегмации в течение ночи. Реакционную смесь, которая теперь содержала осадок, охлаждали и затем перемешивали при комнатной температуре. Твердое вещество собирали вакуумной фильтрацией, промывали небольшим объемом холодного метанола и затем сушили в вакууме с получением Г-(13А-9)а в виде твердого вещества (3,56 г; 72%): +APCI MS (М+1) 354,4; 1Н ЯМР (400 МГц, CD3OD): 5 7,40 (d, J=7,5 Гц, 4Н), 7,35 (d, J=7,5 Гц, 2Н), 7,31-7,20 (m, 7Н), 7,16 (t, J=7,3 Гц, 2Н), 4,44 (s, 1H), 3,76 (s, 2H), 3,48 (d, J=8,3 Гц, 2H), 3,05 (d, J=8,3 Гц, 2Н). Получение промежуточного 1-бензгидрил-3-бензиламиноазетидин-3-карбоновой кислоты амида (!-(13А-9)Ь). - 32 - 008176 1-ПЗА-9)Ь Раствор 1-бензгидрил-3-бензиламиноазетидин-3-карбонитрила 1-(13А-9)а (3,45 г; 9,76 ммоль) в метиленхлориде (55 мл), охлажденный в ледяной бане, обрабатывали H2SO4 (8,1 мл; 0,15 моль) по каплям. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешиваться в течение ночи, после чего ее охлаждали в ледяной бане и затем осторожно гасили концентрированным NH4OH до рН 10. Смесь экстрагировали метиленхлоридом, а затем объединенные органические слои промывали рассолом, сушили (Na2SO4) и концентрировали в вакууме до получения твердого вещества коричневого цвета. Растирание этого вещества со смесью гексаны/диэтиловый эфир привело к получению твердого вещества светло-рыжего цвета, которое собирали выкуумной фильтрацией, промывали дополнительно гексанами и сушили в вакууме с получением Ц^А^ (3,34 г; 92%): +ESI MS (M+1) 372,4; 1Н ЯМР (400 МГц, CD3OD): 5 7,41 (d, J=7,5 Гц, 4Н), 7,35 (d, J=7,5 Гц, 2Н), 7,31-7,22 (m, 7Н), 7,16 (t, J=7,7 Гц, 2Н), 4,50 (s, 1Н), 3,60 (s, 2Н), 3,48 (d, J=8,3 Гц, 2Н), 3,16 (d, J=8,3 Гц, 2H). Получение промежуточного 1-бензгидрил-3-(бензилэтиламино)азетидин-3-карбоновой кислоты амида, гидрохлоридной соли (1-(13А-9)с). ЬПЗА-^с Суспензию 1-бензгидрил-3-бензиламиноазетидин-3-карбоновой кислоты амида Ь^А^^ (3,06 г; 8,24 ммоль) в метаноле (80 мл), охлажденную в ледяной бане, обрабатывали уксусной кислотой (2,4 мл; 41 ммоль), ацетатом натрия (6,8 г; 82 ммоль) и ацетальдегидом (1,8 мл; 41 ммоль). После перемешивания в течение 10 мин порциями добавляли NaCNBH3 (6,24 мг; 9,9 ммоль). После перемешивания в течение 45 мин смесь оставляли нагреваться до комнатной температуры и перемешиваться в течение ночи. Реакционную смесь концентрировали в вакууме и остаток затем экстрагировали из насыщенного водного бикарбоната натрия этилацетатом, объединенные органические слои промывали рассолом, сушили (MgSO4) и затем концентрировали в вакууме с получением неочищенного продукта (3,8 г): +APCI MS (М+1) 400,5; 1H ЯМР (400 МГц, CD2Q2): 5 7,41-7,37 (m, 6H), 7,29-7,22 (m, 6H), 7,20-7,12 (m, 3Н), 4,44 (s, 1H), 3,74 (s, 2H), 3,47 (d, J=8,3 Гц, 2Н), 3,12 (d, J=8,3 Гц, 2Н), 2,56 (q, J=7,2 Гц, 2Н), 0,85 (t, J=7,1 Гц, 3Н). Для очистки раствор свободного основания в метаноле (75 мл) обрабатывали 1М НС1 в диэтиловом эфире (21 мл) по каплям в течение 5 мин. После перемешивания в течение 20 мин смесь концентрировали при пониженном давлении с последующим концентрированием из дополнительного количества метанола (2Х) и затем этанола. Остаток затем суспендировали и перемешивали в изопропаноле (3 мл), одновременно добавляя диэтиловый эфир (50 мл). Затем после перемешивания в течение 45 мин выделяли твердые вещества вакуумной фильтрацией, промывали эфиром и сушили в вакууме с получением Ь(13А-9)с (4,4 г; количественный выход): +APCI MS (М+1) 400,5; 1Н ЯМР (400 МГц, CD3OD): 5 7,55-7,25 (br m, 15H), 5,76 (br s, 1H), 4,21 (br s, 4H), 3,93 (v br s, 2H), 1,02 (br s, 3H). Получение промежуточного l-бензгидрил-З-этиламиноазетидин-З-карбонитрила (I-(13A-9)d). HN^ H13A-9M К смеси 1-бензгидрилазетидин-3-она (9,5 г; 40 ммоль) в метаноле (30 мл) добавляли этиламин гидрохлорид (4,2 г; 52 ммоль) и затем уксусную кислоту (3,0 мл; 52 ммоль) при комнатной температуре. После перемешивания в течение 15 мин добавляли твердый KCN (3,4 г; 52 ммоль) и гомогенную смесь - 33 - 008176 нагревали при 60°С в течение ночи. Реакционную смесь охлаждали и затем концентрировали в вакууме. Остаток затем экстрагировали из насыщенного водного бикарбоната натрия этилацетатом, объединенные органические слои промывали рассолом, сушили (MgSO4) и затем концентрировали в вакууме с получением I-(13A-9)d в виде бесцветного твердого вещества (11,7 г; количественно): +ES MS (М+1) 292,2; 1Н ЯМР (400 МГц, CD3OD): 5 7,42 (d, J=7,5 Гц, 4Н), 7,26 (t, J=7,5 Гц, 4Н), 7,17 (t, J=7,3 Гц, 2Н), 4,47 (s, 1H), 3,54 (d, J=8,3 Гц, 2Н), 3,25 (d, J=8,3 Гц, 2Н), 2,61 (s, J=7,2 Гц, 2Н), 1,11 (t, J=7,3 Гц, 3Н). Получение промежуточного 1 -бензгидрил-З-этиламиноазетидин-З-карбоновой кислоты амида (1-(13А-9)е). H13A-9te Интенсивно перемешиваемый раствор 1-бензгидрил-3-этиламиноазетидин-3-карбонитрила (I-(13A-9)d; 11,7 г; 40 ммоль) в метиленхлориде (150 мл), охлажденный в ледяной бане, обрабатывали H2SO4 (22 мл; 0,4 моль) по каплям. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешиваться в течение ночи, после чего ее охлаждали в ледяной бане и затем осторожно гасили концентрированным NH4OH до рН 11. Не совсем белые твердые вещества, которые образовались в процессе гашения, собирали вакуумной фильтрацией. Водную смесь затем экстрагировали метиленхлоридом, объединенные органические слои промывали рассолом, сушили (Na2SO4) и затем концентрировали в вакууме с получением дополнительного количества твердых веществ. Объединенные твердые вещества перемешивали в течение 1 ч в этилацетате (150 мл) и затем собирали вакуумной фильтрацией с получением Ь(13А-9)е (9,2 г; 74%) в виде твердого вещества: +ES MS (M+1) 310,2; 1Н ЯМР (400 МГц, CD3OD): 5 7,41 (d, J=7,1 Гц, 4Н), 7,25 (t, J=7,5 Гц, 4Н), 7,16 (t, J=7,5 Гц, 2Н), 4,49 (s, 1H), 3,44 (d, J=8,3 Гц, 2Н), 3,11 (d, J=8,3 Гц, 2Н), 2,47 (q, J=7,1 Гц, 2H), 1,10 (t, J=7,3 Гц, 3Н). Получение промежуточного 3-этиламиноазетидин-3-карбоновой кислоты амида, гидрохлоридной соли (I-(13A-9)f). HN^ NH2 HN. 0 -2НС1 H13A-9)f К раствору 1-бензгидрил-3-(бензилэтиламино)азетидин-3-карбоновой кислоты амида, гидрохлоридной соли (Ц13А-9)с; 0,66 г; 1,4 ммоль) в метаноле (25 мл) добавляли 20% Pd(OH)2 на угле (30% воды; 0,13 г). Смесь помещали в шейкер Parr(r) и затем восстанавливали (45 фунт/кв.дюйм (310,275 кПа) Н2) при комнатной температуре в течение ночи. Смесь разбавляли метанолом (200 мл), фильтровали через 0,45 мкм фильтровальный диск и затем концентрировали до твердого вещества. Остаток растирали с ди-этиловым эфиром, собирали вакуумной фильтрацией, промывали эфиром и затем сушили в вакууме с получением I-(13A-9)f (298 мг; 98%): +APCI MS (M+1) 144,1; 1Н ЯМР (400 МГц, CD2Cl2): 5 4,56 (s, 4H), 3,00 (q, J=12 Гц, 2Н), 1,36 (t, J=7,1 Гц, 3Н). Альтернативно, к раствору 1-бензгидрил-3-этиламиноазетидин-3-карбоновой кислоты амида (I-2A-1g; 9,2 г; 30 ммоль) в метаноле (150 мл) при 0°С добавляли 1М НС1 в эфире (75 мл; 75 ммоль). Смесь концентрировали в вакууме до 2/3 объема для удаления эфира и затем добавляли метанол, чтобы довести объем реакционной смеси до 150 мл. Это повторяли 2 раза. После добавления 20% Pd(OH)2 на угле (50% воды; 2,3 г) смесь помещали в шейкер Parr(r) и затем восстанавливали (45 фунт/кв.дюйм (310,275 кПа) Н2) при комнатной температуре в течение ночи. Смесь разбавляли метанолом (350 мл), фильтровали через Celite(r), промывая дополнительным количеством метанола. Метанольные фракции фильтровали через 0,45 мкм фильтровальный диск и затем концентрировали при пониженном давлении с получением твердого остатка, который растирали с диэтиловым эфиром, собирали вакуумной фильтрацией, промывали эфиром и затем сушили в вакууме с получением I-(13A-9)f (6,3 г; 91%) в виде твердого вещества рыжевато-коричневого цвета. Получение промежуточного 1-[9-(4-хлорфенил)-8-(2,4-дггхлорфенил)-9Н-пурин-6-ил]этанона (1-(15А-1)а). Н15А-1)а Раствор 6-хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина !-(1А-Щ (202 мг; 0,49 ммоль) и - 34 - 008176 тетракис(трифенилфосфин)палладия(0) (60 мг; 0,049 ммоль) в диметилформамиде (1,5 мл) дегазировали и к нему добавляли трибутил-(1-этоксивинил)станнан (250 мкл; 0,74 ммоль). Реакционную смесь нагревали до 100°С до полного завершения реакции по данным ТСХ. К реакционной смеси добавляли раствор 2:1 Н2О/конц. НС1 (1,5 мл), и нагревание продолжали в течение 1 ч. Реакционную смесь разбавляли этилацетатом и промывали водой. Органические слои объединяли, сушили (^^O^, фильтровали и концентрировали досуха. Неочищенное вещество очищали на пластине препаративной ТСХ, используя смесь 30% этилацетата/гексаны в качестве растворителя, с получением целевого продукта I-(15A-1)a (50 мг; 25%): +ESI MS (М+1) 417,3; 1Н ЯМР (400 МГц, CDCl3): 5 9,11 (s, 1H), 7,58 (d, J=8,7 Гц, 1H), 7,43-7,30 (m, 4H), 7,21 (d, J=8,7 Гц, 2H), 2,92 (s, 3H). Получение промежуточного 9-(4-хлорфенил)-8-(2,4-дихлорфенил-9Н-пурин-6-карбонигрила (I-(16A-l)a). " ^ CN I-(16A-l)a 6-Хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин I-(1А-1)d (200 мг; 0,49 ммоль) растворяли в ацетонитриле (5 мл) и перемешивали при 0°С. Цианид тетрабутиламмония (236 мг; 0,98 ммоль) и 1,4-диазабицикло[2,2,2]октан (173 мг; 1,5 ммоль) добавляли в реакционную смесь и перемешивание продолжали при 0°С в течение 3 ч. Реакционную смесь концентрировали при пониженном давлении и затем очищали флэш-хроматографией, используя смесь 30% этилацетата/гексаны в качестве элюента, с получением целевого продукта Ь(16А-1)а (215 мг; колич.): +ESI MS (М+1) 400,2; 1Н ЯМР (400 МГц, CDCI3): 5 9.09 (s, 1H), 7,57 (d, J=8,7 Гц, 1H), 7,45-7,39 (m, 4H), 7,21 (d, J=8,7 Гц, 2Н). Получение промежуточного С-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]метиламина (I-(16A-l)b). И16А-ПЬ 9-(4-Хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-карбонитрил Ь(16А-1)а (110 мг; 0,27 ммоль) растворяли в метиленхлориде (0,9 мл) и этот раствор охлаждали до -78°С. В реакционную смесь добавляли по каплям диизобутилалюминий гидрид (1 М в метиленхлориде; 590 мкл; 0,59 ммоль) и перемешивание продолжали при -78°С до тех пор, пока по данным ТСХ не было установлено отсутствие исходного вещества. К смеси добавляли метанол (100 мкл) для гашения реакции и охлаждающую баню удаляли. Реакционную смесь экстрагировали этилацетатом из 1М НС1. Органический слой реэкстрагировали 1М НС1 и водные слои объединяли. Затем водные слои доводили до основного рН гидроксидом натрия и экстрагировали этилацетатом. Органические слои объединяли, сушили (№^О4), фильтровали и упаривали досуха с получением целевого соединения !-(16А-1)Ь: +ESI MS (M+1) 404,4; 1Н ЯМР (400 МГц, CD3OD): 5 8,92 (s, 1Н), 7,69 (d, J=8,3 Гц, 1H), 7,57 (d, J=1,7 Гц, 1H), 7,53-7,43 (m, 3H), 7,36 (d, J=8,3 Гц, 2H), 4,40 (s, 2H). Получение промежуточного К4-(4-хлорфенил)-6-пирролидин-1-ил-пиримидин-4,5-диамина (I-(17A-l)a). Н17А-Па 6-Хлор-N4-(4-хлорфенил)пиримидин-4,5-диамин I-(1А-1)а (114 мг; 0,45 ммоль) и пирролидин (1 мл; избыток) объединяли и нагревали с перемешиванием при 100°С в течение 2 ч. Реакционную смесь разбавляли насыщенным раствором №НСО3 и экстрагировали этилацетатом. Органические слои объединяли, сушили (Na2SO4), фильтровали и упаривали досуха с получением целевого соединения !-(17А-1)а (131 мг; количественно) в виде твердого вещества оранжево-коричневого цвета: +ESI MS (M+1) 290,3; 1 Н ЯМР (500 МГц, CD3OD): 5 7,85 (s, 1H), 7,45 (d, J=8,8 Гц, 2Н), 7,26 (d, J=8,8 Гц, 2H), 3,63 (m, 4H), 1,96 (m, 4H). Получение промежуточного 2-бензгидрил-5-бензил-2,5,7-триазаспиро[3,4]окт-6-ен-8-она (!-(29А-6)а). - 35 - 008176 Н29А-6)а ^^Диметилформамида диметилацеталь (16 мл; 121 ммоль) объединяли с 1-бензгидрил-3-бензил-аминоазетидин-3-карбоновой кислоты амидом (I-(13A-9)b; 3,03 г; 8,16 ммоль) и нагревали до температуры дефлегмации. Через 4 ч суспензию охлаждали и экстрагировали из насыщенного водного №НСО3 этилацетатом. Объединенные экстракты сушили (Na2SO4) и концентрировали в вакууме до неочищенного твердого вещества (3,50 г). Очистка остатка на колонке Biotage(tm) Flash 40М с использованием 0-3% метанола в метиленхлориде в качестве элюента дала Г(29А-6)а в виде желтоватого твердого вещества (1,92 г; 62%): +ES MS (M+1) 382,3; 1Н ЯМР (400 МГц, CD3OD): 5 8,66 (s, 1H), 7,59 (d, J=7,1 Гц, 2Н), 7,497,11 (m, 13H), 5,12 (s, 2H), 4,44 (s, 1H), 3,31 (d, J=9,6 Гц, 2Н), 3,20 (d, J=9,6 Гц, 2Н). Получение промежуточного 2,5,7-триазаспиро[3,4]октан-8-она, гидрохлоридной соли (1-(29А-6)Ь). HN-д NH HN- _ •НС1 Н29А-6)Ь К раствору 2-бензгидрил-5-бензил-2,5,7-триазаспиро[3,4]окт-6-ен-8-она (Ц29А-6)а; 1,83 г; 4,80 ммоль) в смеси метанол/метиленхлорид добавляли избыток 1М НС1 в диэтиловом эфире (10 мл). После перемешивания в течение 10 мин растворитель удаляли в вакууме и полученную гидрохлоридную соль растворяли в метаноле (50 мл). После добавления 20% Pd(OH)2 на угле (50% воды; 1,1 г) смесь помещали в шейкер Parr(r) и затем восстанавливали (50 фунт/кв. дюйм (344,75 кПа) Н2) при комнатной температуре в течение 22 ч. Реакционную смесь фильтровали через 0,45 мкм диск и затем концентрировали в вакууме с получением смолистого твердого вещества. Это вещество растирали с метанолом с получением Г^А^^ (450 мг; 47%) в виде твердого вещества рыжевато-коричневого цвета: +APCI MS (M+1) 127,9; 1Н ЯМР (400 МГц, CD3OD): 5 4,51 (s, 2H), 4,41-4,33 (m, 4H). Получение промежуточного 1-бензгидрил-З-метиламиноазетидин-З-карбонитрила (1-(29А-7)а). 1-(29А-7)а К раствору 1-бензгидрилазетидин-3-она (2,13 г; 8,98 ммоль) в метаноле (17 мл) добавляли метиламина гидрохлорид (1,21 г; 18,0 ммоль) и затем уксусную кислоту (1,03 мл; 18,0 ммоль) при комнатной температуре. После перемешивания в течение 5 мин добавляли твердый KCN (1,17 г; 18,0 ммоль) и эту смесь нагревали до 60°С в течение 19 ч. Реакционную смесь охлаждали, твердый продукт собирали вакуумной фильтрацией, промывали метанолом и затем сушили в вакууме с получением Г(29А-7)а в виде бесцветного твердого вещества (2,50 г; количественный выход): +ES MS (М+1) 278,3; 1 Н ЯМР (400 МГц, CD2CI2): 5 7,43 (d, J=7,5 Гц, 4Н), 7,29 (t, J=7,5 Гц, 4Н), 7,23 (t, J=7,3 Гц, 2Н), 4,45 (s, 1H), 3,55 (d, J=7,5 Гц, 2Н), 3,15 (d, J=7,1 Гц, 2H), 2,40 (s, 3H). Получение промежуточного 1-бензгидрил-З-метиламиноазетидин-З-карбоновой кислоты амида (I-(29A-7)b). \-(29А-ЪЪ Интенсивно перемешиваемый раствор 1-бензгидрил-3-метиламиноазетидин-3-карбонитрила (I-(29A-7)а; 2,10 г; 7,57 ммоль) в метиленхлориде (25 мл), охлажденный в ледяной бане, обрабатывали H2SO4 (4,0 мл; 76 ммоль) по каплям. Реакционную смесь оставляли нагреваться до комнатной температуры и перемешиваться в течение ночи, после чего ее охлаждали в ледяной бане и затем осторожно гасили концентри - 36 - 008176 рованным NH4OH до рН 11. Смесь экстрагировали метиленхлоридом, объединенные органические слои сушили (Na2SO4) и затем концентрировали в вакууме с получением 1-(29А-7)Ь (1,2 г; 54%) в виде не совсем белого твердого вещества: +ES MS (M+1) 296,3; 1Н ЯМР (400 МГц, CD3OD): 5 7,41 (d, J=7,5 Гц, 4Н), 7,25 (t, J=7,5 Гц, 4Н), 7,16 (t, J=7,1 Гц, 2H), 4,48 (s, 1H), 3,41 (d, J=8,7 Гц, 2Н), 3,09 (d, J=8,7 Гц, 2Н), 2,24 (s, 3H). Получение промежуточного 2-бензгидрил-5-метил-2,5,7-триазаспиро[3,4]окт-6-ен-8-она (I-(29A-7)c). I-(29A-7te ^^Диметилформамида диметилацеталь (1,1 мл; 8,3 ммоль) объединяли с 1-бензгидрил-3-метил-аминоазетидин-3-карбоновой кислоты амидом (1-(29А-7)Ь; 153 мг; 0,52 ммоль) и нагревали до температуры дефлегмации. Через 3 ч суспензию охлаждали и экстрагировали из насыщенного водного №НСО3 этилацетатом. Объединенные экстракты сушили (Na2SO4) и концентрировали в вакууме с получением 1-(29А-7)с в виде твердого вещества (152 мг; 96%): +ES MS (M+1) 306,3; 1Н ЯМР (400 МГц, CD3OD): 5 8,42 (s, 1H), 7,47 (d, J=7,5 Гц, 4Н), 7,27 (t, J=7,5 Гц, 4Н), 7,17 (t, J=7,5 Гц, 2H), 4,57 (s, 1H), 3,58 (s, 3H), 3,55 (d, J=10,0 Гц, 2Н), 3,34 (d, J=10,0 Гц, 2Н). Получение промежуточного 5-метил-2,5,7-триазаспиро[3,4]октан-8-она, гидрохлоридной соли (I-(29A-7)d). HN- 6 -НС] И29А-7М К раствору 2-бензгидрил-5-метил-2,5,7-триазаспиро[3,4]окт-6-ен-8-она (!-(29А-7)с; 189 мг; 0,619 ммоль) в метаноле (30 мл) добавляли 1М НС1 в диэтиловом эфире (1,3 мл). После добавления 20% Pd(OH)2 на угле (50% воды; 95 мг) смесь помещали в шейкер Parr(r) и затем восстанавливали (50 фунт/кв. дюйм (344,75 кПа) Н2) при комнатной температуре в течение 5 ч. Реакционную смесь фильтровали через 0,45 мкм диск и затем концентрировали в вакууме с получением твердого вещества. Растирание из диэтилового эфира дало I-(29A-7)d (124 мг; 94%) в виде не совсем белого твердого вещества: +APCI MS (M+1) 142,0; 1Н ЯМР (400 МГц, CD3OD): 5 4,38 (d, J=12,0 Гц, 2Н), 4,17 (s, 2Н), 4,13 (d, J=12,5 Гц, 2Н), 2,71 (s, 3Н). Пример 1. Получение 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-изопропокси-9H-пурина (1 A-1). 1А-1 Натрий (7 мг; 0,3 ммоль) растворяли в изопропаноле (1 мл) и к нему добавляли 6-хлор-9-(4-хлор-фенил)-8-(2,4-дихлорфенил)-9Н-пурин 1-(1А-1^ (30 мг; 0,07 ммоль). После перемешивания при комнатной температуре в течение ночи реакционную смесь упаривали досуха и экстрагировали в этилацетат из насыщенного водного раствора №НСО3. Органические слои объединяли, сушили (№2SO4), фильтровали и концентрировали досуха. Неочищенный остаток очищали на пластине препаративной ТСХ, используя смесь 4% метанола/метиленхлорид в качестве растворителя, с получением указанного в заголовке соединения 1А-1. Раствор этого вещества в метиленхлориде обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением гидрохло-ридной соли соединения 1А-1 (8 мг; 26%): +ESI MS (М+1) 433,4; 1Н ЯМР (400 МГц, CD3OD): 5 8,50 (s, 1H), 7,64 (d, J=8,3 Гц, 1H), 7,55 (d, J=1,7 Гц, 1Н), 7,49-7,45 (3H), 7,34 (d, J=9,1 Гц, 2Н), 5,73 (септуплет, J=6,2 Гц, 1Н), 1,48 (d, J=6,2 Гц, 6Н). Соединения, перечисленные ниже в табл. 1, были получены по методикам, аналогичным описанным выше для синтеза соединения 1 А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области способов или получены аналогично описанным выше способам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. - 37 - 008176 Таблица 1 Пример -OR MS (М+Н) + 1А-2 2,4-дихлорфенил -ОМе 405,4 1А-3 2,4-дихлорфенил -OEt 419,6 1А-4 2,4-дихлорфенил -О-н-Рг 433,4 1А-5 2,4-дихлорфенил -О-н-Ви 447,0 Пример 2. Получение 6-трет-бутокси-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина (2А-1). 2А-1 6-Хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин I-(1A-1)d, трет-бутоксид калия (20 мг; 0,15 ммоль) и тетрагидрофуран (1 мл) объединяли и перемешивали в течение ночи при температуре окружающей среды. Реакционную смесь концентрировали досуха и остаток экстрагировали в этилацетат из насыщенного водного раствора NaHCO3. Органические слои объединяли, сушили (Na2SO4), фильтровали и упаривали досуха. Неочищенный продукт очищали хроматографией на пластине препаративной ТСХ, используя смесь 4% метанола/метиленхлорид в качестве растворителя, с получением указанного в заголовке соединения 2А-1 в виде желтого масла: +ESI MS (М+1) 447,5; 1Н ЯМР (400 МГц, CD3OD): 5 8,48 (s, 1H), 7,64 (d, J=8,3 Гц, 1H), 7,55 (d, J=2,1 Гц, 1H), 7,49-7,44 (m, 3H), 7,34 (d, J=9,1 Гц, 2H), 1,77 (s, 9H). Пример 3. Получение 6-(1-бензгидрилазетидин-3-илокси)-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина (ЗА-1). ЗАЛ К раствору 6-хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина I-(L\-1)d (30 мг; 0,073 ммоль) и 1-бензгидрилазетидин-3-ола (53 мг; 0,22 ммоль) в тетрагидрофуране (1 мл) добавляли трет-бутоксид калия (24 мг; 0,22 ммоль). Объединенные реагенты перемешивали в течение ночи при температуре окружающей среды. Реакционную смесь концентрировали досуха и остаток экстрагировали в этилацетат из насыщенного раствора NaHCO3. Органические слои объединяли, сушили (Na2SO4), фильтровали и упаривали досуха. Неочищенный продукт очищали хроматографией на пластине препаративной ТСХ, используя смесь 4% метанола/метиленхлорид в качестве растворителя, с получением указанного в заголовке соединения 3А-1 в виде желтого масла. Раствор этого вещества в метиленхлориде обрабатывали избытком 1 н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением гидрохлоридной соли соединения 3А-1 (14 мг; 31%): +ESI MS (М+1) 612,2; 1Н ЯМР (400 МГц, CD3OD): 5 8,51 (s, 1H), 7,65-7,30 (m, 17H), 5,85-5,77 (br m, 2H), 4,75-4,60 (br m, 2H), 4,55-4,30 (br m, 2H). Соединения, перечисленные ниже в табл. 2, были получены по методикам, аналогичным описанным выше для синтеза соединения 3А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области способов или получены аналогично описанным выше способам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. - 38 - 008176 Таблица 2 Пример № -OR MS (M+H)+ ЗА-2 2,4-дихлорфенил 488,4 ЗА-3 2,4-дихлорфенил M64 Me Me 544,4 ЗА-4 2,4-дихлорфенил 502,4 ЗА-5 2,4-дихлорфенил 488,4 ЗА-6 2,4-дихлорфенил 488,4 ЗА-7 2,4-дихлорфенил 474,0 ЗА-8 2,4-дихлорфенил 550,2 ЗА-9 2,4-дихлорфенил 502,4 ЗА-10 2,4-дихлорфенил 528,0 ЗА-11 2,4-дихлорфенил 514,8 Пример 4. Получение 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(тетрагидрофуран-2-илметокси)-9Н-пурина (4А-1). 4А-1 9-(4-Хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ол 1-(1А-1)с (100 мг; 0,255 ммоль), 2-бромметил- - 39 - 008176 тетрагидрофуран (42 мг; 0,255 ммоль) и карбонат цезия (83 мг; 0,26 ммоль) объединяли в диметилфор-мамиде (5 мл) и нагревали до 100°С в течение ночи. Реакционную смесь разбавляли этилацетатом и промывали рассолом. Органический слой сушили (Na2SO4), фильтровали и упаривали досуха. Неочищенное вещество очищали на пластине препаративной ТСХ, используя смесь 75% этилацетата/гексаны в качестве элюента, с получением указанного в заголовке соединения 4А-1 (20 мг; 16%); 1Н ЯМР (400 МГц, CD3OD): 5 8,52 (s, 1H), 7,64 (d, J=8,3 Гц, 1H), 7,49 (d, J=2,1 Гц, 1H), 7,50-7,44 (m, 3H), 7,34 (d, J=8,7 Гц, 2Н), 4,68 (d, J=5,0 Гц, 2H), 4,39 (m, 1H), 3,91 (m, 1H), 3,79 (m, 1H), 2,20-1,83 (m, 4H). Раствор этого вещества в метиленхлориде обрабатывали 4М HCl/диоксан, упаривали досуха, затем дополнительно сушили в высоком вакууме с получением гидрохлоридной соли соединения 4А-1: +APCI MS (M+1) 475,2. Соединения, перечисленные ниже в табл. 3, были получены по методикам, аналогичным описанным выше для синтеза соединения 4А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 3 Пример № -OR MS (M+H) + 4А-2 2,4-дихлорфенил 475,1 4А-3 2,4-дихлорфенил 449,1 4А-4 2,4-дихлорфени л 477,2 4А-5 2,4-дихлорфенил 489,2 4А-6 2,4-дихлорфенил ОМе V-O'^^^OMe 493,2 4А-7 2-хлорфенил -OEt 385,2 4А-8 2-хлорфенил -ОМе 371,2 4А-9 2-хлорфенил 439,2 Пример 5. Получение 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(2,2,2-трифторэтокси)-9Н-пурина (5А-1). 5А-1 трет-Бутоксид калия (1М в THF; 0,73 мл; 0,73 ммоль) и 2,2,2-трифторэтанол (2 мл) перемешивали при комнатной температуре и к этой смеси добавляли 6-хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин Г(1А-1^ (100 мг; 0,24 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 суток, затем гасили Н2О и разбавляли хлороформом. Органический слой промывали рассолом, сушили (Na2SO4), фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали препаративной ТСХ, используя смесь 20% этилацетата/гексаны в качестве элюента, с получением указанного в заголовке соединения 5А-1 (20 мг; 17%): +APCI MS (М+1) 473,1; 1Н ЯМР (400 МГц, - 40 - 008176 CD3OD): 5 8,58 (s, 1Н), 7,64 (d, 1H), 7,57 (d, 1H), 7,50-7,41 (m, 3H), 7,36 (d, 2H), 5,23 (q, 2H). Пример 6. Получение 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]циклогексиламина (6A-1). 6A-1 6-Хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин I-(1A-1)d (30 мг; 0,07 ммоль) и циклогексил-амин (0,3 мл) объединяли в этаноле (0,5 мл) и нагревали при 60°С в течение 30 мин. Реакционную смесь концентрировали под струей N2 и затем экстрагировали в этилацетат из насыщенного раствора NaHCO3. Органические слои объединяли, сушили (Na2SO4), фильтровали, упаривали досуха и затем очищали препаративной ТСХ, используя смесь 25% этилацетата/гексаны в качестве элюента, с получением указанного в заголовке соединения 6А-1. Раствор этого вещества в метиленхлориде обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением гидрохлоридной соли соединения 6А-1 (9,8 мг; 57%) в виде твердого вещества: +ESI MS (М+1) 472,6; 1Н ЯМР (500 МГц, CD3OD): 5 8,40 (s, 1H), 7,66-7,60 (m, 2H), 7,38-7,35 (m, 3Н), 7,53-7,50 (d, J=8,8 Гц, 2H), 3,90 (br m, 1H), 2,12 (br d, J=11,9 Гц, 2Н), 1,94 (br d, J=13,0 Гц, 2H), 1,78 (br d, J=14,5 Гц, 1H), 1,62-1,23 (m, 5H). Соединения, перечисленные ниже в табл. 4, были получены по методикам, аналогичным описанным выше для синтеза соединения 6А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 4 Пример -NRR' MS (М+Н) + 6А-2 2,4-дихлорфенил 458,5 6А-3 2,4-дихлорфенил 460,5 6А-4 2,4-дихлорфенил 446,5 6А-5 2,4-дихлорфенил 446,5 6А-6 2,4-дихлорфенил 473,6 Пример 7. Получение 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]пиперидин-4-карбо-новой кислоты этилового эфира (7А-1). 7А-1 - 41 - 008176 6-Хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин I-(1A-1)d (30 мг; 0,07 ммоль), пиперидин-4-карбоновой кислоты этиловый эфир (34 мг; 0,22 ммоль) и триэтиламин (20 мкл; 0,29 ммоль) объединяли в этаноле (1 мл) и нагревали при 70°С в течение 2 ч. Реакционную смесь концентрировали под струей N2 и затем экстрагировали в этилацетат из насыщенного раствора NaHCO3. Органические слои объединяли, сушили (№^О4), фильтровали, упаривали досуха и затем очищали препаративной ТСХ, используя 4% метанол в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения 7A-1. Раствор вещества в метиленхлориде обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали и упаривали досуха с получением гидрохлоридной соли соединения 7А-1 (24 мг; 65%) в виде твердого вещества: +ESI MS (М+1) 530,1; 1Н ЯМР (400 МГц, CD3OD): 5 8,35 (s, 2Н), 7,60 (d, J=8,3 Гц, 1Н), 7,56 (d, J=2,1 Гц, 1H), 7,50-7,45 (m, 3H), 7,34 (d, J=8,7 Гц, 2H), 4,15 (q, J=7,1 Гц, 2H), 3,68 (v br s, 2H), 2,85 (m, 1H), 2,16 (m, 2H), 1,89 (m, 2H), 1,25 (t, J=7,1 Гц, 3Н). Соединения, перечисленные ниже в табл. 5, были получены по методикам, аналогичным описанным выше для синтеза соединения 7А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 5 Пример № -NRR' MS (М+Н)+ 7А-2 2,4-дихлорфенил 462,0 7А-3 2,4-дихлорфенил 457,1 7А-4 2,4-дихлорфенил 502,5 7А-5 2,4-дихлорфенил О OEt 530,4 7А-6 2,4-дихлорфенил 484,4 7А-7 2,4-дихлорфенил н о 490,8 7А-8 2,4-дихлорфенил 432,0 7А-9 2,4-дихлорфенил н о 462,0 7А-10 2,4-дихлорфенил н о 504,8 - 42 - 008176 7А-11 2,4-дихлорфенил 460,0 7А-12 2,4-дихлорфенил 446,0 7А-13 2,4-дихлорфенил 515,2 7А-14 2,4-дихлорфенил 444,0 7А-15 2,4-дихлорфенил 444,6 7А-16 2,4-дихлорфенил 460,0 7А-17 2,4-дихлорфенил 474,4 7А-18 2,4-дихлорфенил 430,0 7А-19 2,4-дихлорфенил СК^ОМе 504,4 7А-20 2,4-дихлорфенил Н О 476,0 7А-21 2,4-дихлорфенил 446,0 7А-22 2,4-дихлорфенил 488,8 7А-23 2,4-дихлорфенил 472,4 7А-24 2,4-дихлорфенил н о 461,5 7А-25 2,4-дихлорфенил 474,4 7А-26 2,4-дихлорфенил Н 1^,0 517,2 7А-27 2,4-дихлорфенил 503,2 7А-28 2,4-дихлорфенил 517,2 - 43 - 008176 7А-29 2,4-дихлорфенил 489,6 7А-30 2,4-дихлорфенил 487,2 7А-31 2,4-дихлорфенил 475,2 7А-32 2,4-дихлорфенил 513,2 7А-33 2,4-дихлорфенил 517,2 7А-34 2,4-дихлорфенил 503,2 7А-35 2,4-дихлорфенил н " "Н 499,6 7А-36 2,4-дихлорфенил 499,2 7А-37 2,4-дихлорфенил 487,2 7А-38 2,4-дихлорфенил 485,2 7А-39 2,4-дихлорфенил 549,2 7А-40 2,4-дихлорфенил 537,2 7А-41 2,4-дихлорфенил 536,4 7А-42 2,4-дихлорфенил 487,2 7А-43 2,4-дихлорфенил 461,9 7А-44 2,4-дихлорфенил 503,2 7А-45 2,4-дихлорфенил 515,2 - 44 - 008176 7А-46 2,4-дихлорфенил 487,2 7А-47 2,4-дихлорфенил 487,2 -Ч Me Me/ 7А-48 2,4-дихлорфенил 501,2 7А-49 2,4-дихлорфенил Me r^NvMe 515,2 7А-50 2,4-дихлорфенил 501,2 7А-51 2,4-дихлорфенил ¦T-N Me Me 475,2 7А-52 2,4-дихлорфенил 549,2 7А-53 2,4-дихлорфенил 527,1 7А-54 2,4-дихлорфенил 487,4 7А-55 2,4-дихлорфенил 487,5 "VMe Me/ 7А-56 2,4-дихлорфенил 494,0 7А-57 2,4-дихлорфенил 506,4 7А-58 2,4-дихлорфенил 486,4 7А-59 2,4-дихлорфенил Me Me 508,0 7А-60 2,4-дихлорфенил 480,9 - 45 - 008176 7А-61 2,4-дихлорфенил 512,4 7А-62 2,4-дихлорфенил 500,4 7А-63 2,4-дихлорфенил 566,0 7А-64 2,4-дихлорфенил 470,0 7А-65 2,4-дихлорфенил 512,4 7А-66 2,4-дихлорфенил 506,4 7А-67 2,4-дихлорфенил 473,6 7А-68 2,4-дихлорфенил 509,5 7А-69 2,4-дихлорфенил 495,9 7А-70 2,4-дихлорфенил 481,2 7А-71 2,4-дихлорфенил 481,9 7А-72 2,4-дихлорфенил 495,1 7А-73 2,4-дихлорфенил 481,2 7А-74 2,4-дихлорфенил 523,2 7А-75 2,4-дихлорфенил 495,3 7А-76 2,4-дихлорфенил 535,2 - 46 - 008176 7А-77 2,4-дихлорфенил 535,2 7А-78 2,4-дихлорфенил 507,6 7А-79 2,4-дихлорфенил 495,9 7А-80 2-фторфенил -СНз "ОС 508,3 7А-81 2,4-дихлорфенил CAN-H 530,1 7А-82 2,4-дихлорфенил 544,1 7А-83 2,4-дихлорфенил 558,1 7А-84 2-фторфенил н чн 480,2 7А-85 2-фторфенил н н 494,2 7А-86 2-фторфенил н чн 508,2 7А-87 2-хлорфенил 496,1 7А-88 2-хлорфенил 510,2 - 47 - 008176 7А-89 2-хлорфенил 524,2 7А-90 2-хлорфенил H-N 536,2 7А-91 4-хлор-2- фторфенил 514,1 7А-92 4-хлор-2-фторфенил O^N-H 528,1 7А-93 4-хлор-2-фторфенил 542,1 7А-94 2,4-дихлорфенил 544,2 7А-95 2-фторфенил 494,1 7А-96 2-хлорфенил 438,1 7А-97 2,4-дихлорфенил 0 H 570,1 7А-98 2,4-дихлорфенил 584,1 7А-99 4-хлор-2-фторфенил 542,2 7А-100 4-хлор-2-фторфенил 554,2 - 48 - 008176 7А-101 4-хлор-2-фторфенил 568,3 7А-102 2,4-дихлорфенил 598,2 7А-103 2-фторфенил 548,3 7А-104 4-хлор-2-фторфенил н~Ч° 582,2 7А-105 4-хлор-2-фторфенил уОч н~Ч° 528,2 7А-106 2-хлорфенил I 0 н 496,1 7А-107 2-хлорфенил нЧ° 572,2 7А-108 2-хлорфенил Ч?" 482,2 7А-109 2-фторфенил -СН3 н~Ч° 522,3 Пример 8. Получение промежуточного 4-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пипера-зин-1,3-дикарбоновой кислоты 1-трет-бутилового эфира 3-этилового эфира (1-(8А-1)а). 6-Хлор-9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин 1-(4А-7)с (103 мг; 0,27 ммоль), пиперазин-1,3-дикар-боновой кислоты 1-трет-бутиловый эфир 3-этиловый эфир (Chiu, С.К.-F. and Griffith, DA., ЕР 1004583 А2; 156 мг; 0,60 ммоль) и триэтиламин (95 мкл, 0,68 ммоль) объединяли в этаноле (1,5 мл) и нагревали при 60°С до полного завершения реакции по данным ТСХ (3 суток). Реакционную смесь концентрировали при пониженном давлении и затем очищали на колонке Biotage(tm) Flash 12M, используя 20-30% этилацетат в гек-санах в качестве элюента, что позволило получить указанное в заголовке соединение Т-(8А-1)а (78 мг; 48%): +ESI MS (M+1) 597,3; 1Н ЯМР (400 МГц, CD3OD): 5 8,298 (br s, 1Н), 7,57 (br s, 1H), 7,48-7,25 (m, 7H), 5,60 (v - 49 - 008176 br s, 1H), 4.67 (d, J=13,7 Гц, 1H), 4,23-4,05 (br m, 3H), 3,43-3,00 (br m, 2H), 1,46 (s, 9H), 1,22 (t, J=7,1 Гц, 3H). Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-2-карбоновой кислоты этилового эфира, гидрохлоридной соли (8А-1). 8А-1 4-[9-(4-Хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-1,3-дикарбоновой кислоты трет-бу-тиловый эфир Г^А-^ растворяли в 4М НС1 в диоксане (0,5 мл). Через 30 мин ставшую теперь гетерогенной реакционную смесь концентрировали при пониженном давлении и затем растирали с эфиром с получением указанного в заголовке соединениия 8А-1 (38 мг; количественный выход): +ESI MS (М+1) 497,2; 1Н ЯМР (400 МГц, CD3OD): 5 8,43 (s, 1H), 7,58 (d, J=7,5 Гц, 1H), 7,51-7,30 (m, 7H), 4,35-4,15 (m, 2H), 4,06 (d, J=13,3 Гц, 1H), 3,73-3,47 (m, 5H), 3,40-3,30 (m, 1H), 1,23 (t, J=7,1 Гц, 3Н). Соединения, перечисленные ниже в табл. 6, были получены по методикам, аналогичным описанным выше для синтеза соединения 8А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 6 Пример -NRR' MS (M+H)+ 8А-2 2,4-дихлорфенил 473,3 8А-3 2,4-дихлорфенил 471,2 8А-4 2,4-дихлорфенил 485,3 8А-5 2,4-дихлорфенил 459,3 8А-6 2,4-дихлорфенил ^N"^\^N"Me 447,3 Пример 9. Получение {3-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1а,5а,6а)азаби-цикло[3,1,0]гекс-6-ил } диметиламина (9А-1). 9А-1 - 50 - 008176 3-[9-(4-Хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1а,5а,6а)азабицикло[3,1,0]гекс-6-иламин гидрохлорид 14А-5 (20 мг; 0,039 ммоль), параформальдегид (40 мг), метанол (0,75 мл) и уксусную кислоту (13 мкл; 0,22 ммоль) объединяли и перемешивали при комнатной температуре в течение 30 мин. После этого добавляли цианоборгидрид натрия (5 мг; 0,074 ммоль) и эту реакционную смесь перемешивали в течение 4 суток при комнатной температуре. Реакционную смесь разбавляли насыщенным раствором NaHCO3 и экстрагировали этилацетатом. Органические слои объединяли, сушили (Na2SO4), фильтровали и упаривали досуха. Неочищенный продукт очищали на пластине препаративной ТСХ, используя смесь 7:3:0,1 гексаны/диэтиламин/метанол в качестве растворителя, с получением указанного в заголовке соединения 9А-1. Раствор этого вещества в метиленхлориде обрабатывали избытком 1н НС1 в диэтило-вом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением гид-рохлоридной соли соединения 9А-1: +ESI MS (M+1) 499,2. Получение {3-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1а,3а,6р)азабицикло[3,1,0] гекс-6-ил}диметиламина (9А-2). 9А-2 {3-[9-(4-Хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1а,5а,6р)азабицикло[3,1,0]гекс-6-ил} диметиламин получали, используя методики, аналогичные описанным выше для синтеза соединения 9А-1. Соединение превращали в соответствующую гидрохлоридную соль для тестирования: +ESI MS (M+1) 499,2. Пример 10. Получение 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-1-4-изопропилами-нопиперидин-4-карбоновой кислоты амида (10А-1). 10А-1 6-Хлор-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин Ь(1А-1^ (300 мг; 0,58 ммоль) и 4-изопро-пиламинопиперидин-4-карбоновой кислоты амид (101 мг; 0,548 ммоль) суспендировали в смеси эта-нол/метиленхлорид (3 мл/1 мл). К этой суспезии добавляли триэтиламин (0,16 мл; 1,1 ммоль) и смесь нагревали до 60°С до тех пор, пока по данным ТСХ не определяли, что реакция прошла до конца (3 ч). Реакционную смесь распределяли между насыщенным раствором №НСО3 и метиленхлоридом. Органический слой сушили (N2SO4), фильтровали и концентрировали досуха. Чистое свободное основание выделяли хроматографией на силикагеле, используя смесь 2-4% метанола/метиленхлорид в качестве градиентного элюента, с получением указанного в заголовке соединения 10А-1. Раствор этого вещества в ме-тиленхлориде обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением гидрохлоридной соли соединения 10А-1 в виде твердого вещества рыжевато-коричневого цвета (115 мг; 38%): +ESI MS (M+1) 558,2; 1Н ЯМР (400 МГц, CD3OD): 5 8,40 (s, 1H), 7,60 (d, J=8,3 Гц, 1Н), 7,56 (d, J=2,1 Гц, 1H), 7,51-7,44 (m, 3H), 7,33 (d, J=8,7 Гц, 2H), 5,20 (v br m, 2H), 3,87 (br m, 2H), 3,59 (септуплет, J=6,6 Гц, 1Н), 2,68 (br d, J=13,7 Гц, 2Н), 2,16 (ddd, J=14,5, 10,4, 4,1 Гц, 2H), 1,39 (d, J=6,6 Гц, 6Н). Пример 11. Получение 9-(4-хлорфенил)-8-(2-фторфенил)-2-метил-6-(4-метилпиперазин-1-ил)-9Н-пурина (11A-1). 11A-1 Раствор 1-метилпиперазина (200 мкл) в этаноле (0,8 мл) добавляли к 6-хлор-9-(4-хлорфенил)-8-(2-фторфенил)-2-метил-9Н-пурину I-(11A-1)c (24 мг; 0,06 ммоль) и помещали на 60°С на шейкер на 30 мин. Реакционную смесь наносили прямо на пластину препаративной ТСХ для очистки, используя смесь 10% - 51 - 008176 метанола/этилацетат в качестве растворителя, с получением целевого указанного в заголовке соединения 11А-1: +ESI MS (М+1) 465. Раствор этого вещества в смеси метиленхлорид/метанол обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире сполучением гидрохлоридной соли соединения 11А-1 (35 мг; количественный выход): +ESI MS (М+1) 437,2; 1Н ЯМР (400 МГц, CD3OD): 5 7,70-7,25 (br m, 7Н), 7,09 (t, J=9,1 Гц, 1H), 5,80 (br s, 2H), 3,74 (br s, 4H), 3,36 (br s, 2H), 2,99 (s, 3H), 2,64 (s, 3H). Соединения, перечисленные ниже в табл. 8, были получены по методикам, аналогичным описанным выше для синтеза соединения 11А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 8 Пример № -NRR' MS (М+Н) + 11А-2 2-хлорфенил Me Me Н Н но 499,1 11А-3 2-фторфенил -СН2С(СН3)з 493,4 11А-4 2-фторфенил -СН(СНз)2 465,3 11А-5 2-фторфенил -СН2СН2СН3 436,3 11А-6 2-фторфенил -СН(СН3)2 436,3 11А-7 2-фторфенил -СН2С(СН3)з 464,3 11А-8 2-фторфенил -СНз 408,2 Пример 12. Получение 9-(4-хлорфенил)-8-(2-фторфенил)-6-(4-метилпиперазин-1 -ил)-9Н-пурина (12А-1). 12А-1 Смесь 6-хлор-9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурина (полученного аналогично Ц7А-80)с; 25 мг; 0,07 ммоль) и 1-метилпиперазина (200 мкл) в этаноле (1 мл) перемешивали в течение ночи при комнатной температуре. Выпавшее в осадок указанное в заголовке соединение 12А-1 собирали фильтрованием и промывали эфиром (15 мг; 51%): +ESI MS (М+1) 410; 1Н ЯМР (400 МГц, CD2Cl2): 5 8,27 (s, 1H), 7,63 (td, J=7,3, 1,7 Гц, 1H), 7,45 (m, 1H), 7,38 (d, J=8,7 Гц, 2Н), 7,26 (t, J=7,5 Гц, 1Н), 7,22 (d, J=8,7 Гц, 2H), 7,01 (t, J=8,9 Гц, 1H), 4,34 (br m, 4H), 2,52 (t, J=5,0 Гц, 4Н), 2,30 (s, 3Н). Раствор этого вещества в смеси метиленхлорид/метанол обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире, с получением гидрохлоридной соли соединения 12А-1. - 52 - 008176 Соединения, перечисленные ниже в табл. 9, были получены по методикам, аналогичным описанным выше для синтеза соединения 12А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 9 Пример № -NRR' MS (М+Н)+ 12А-2 2-фторфенил 410,2 12А-3 2-фторфенил 408,1 12А-4 2-хлорфенил 426,1 12А-5 2-хлорфенил 439,1 12А-6 2-хлорфенил 424,1 12А-7 2-хлорфенил нет 443,1 12А-8 2-хлорфенил k/0H 443,1 Пример 13. Получение 8-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-три-азаспиро[4,5]декан-4-она (13А-1). 13А-1 Смесь 6-хлор-9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурина 1-(4А-7)с (19 мг; 0,052 ммоль), 1-изопро-пил-1,3,8-триазаспиро[4,5]декан-4-она (Janssen, P.A.J., патент США 3238216; 20 мг; 0,10 ммоль) и три-этиламина (11 мкл) в этаноле (1 мл) перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении и затем очищали на колонке Biotage(tm) Flash 12S, используя смесь 3% метанола в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения 13А-1 (25 мг): +ESI MS (M+1) 536,3; 1Н ЯМР (400 МГц, CD3OD): 5 8,22 (s, 1Н), 7,59 (d, J=7,5 Гц, 1H), 7,46-7,35 (m, 5H), 7,29 (d, J=8,7 Гц, 2H), 4,27 (s, 2H), 4,25 (v br s, 4H), 3,15 (септуплет, J=6,6 Гц, 1 Н), 2,00-1,83 (m, 4H), 1,07 (d, J=6,6 Гц, 6Н). Раствор этого вещества в смеси метиленхло-рид/метанол обрабатывали избытком 1н HCl в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением гидрохлоридной соли соединения 13А-1 (23 мг; 77%): 1Н ЯМР (400 МГц, CD3OD) 5 8,43 (s, 1Н), 7,61 (d, J=7,5 Гц, 1Н), 7,53-7,40 (т, 5Н), 7,35 (d, J=8,7 Гц, 2Н), 4,20 (v br s), 3,94 (септуплет, J=6,6 Гц, 1Н), 2,45 (m, 4H), 1,41 (d, J=6,6 Гц, 6Н). Соединения, перечисленные ниже в табл. 10, были получены по методикам, аналогичным описан- 53 008176 ным выше для синтеза соединения 13А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 10 Пример № -NRR' MS (М+Н)+ 13А-2 2-фторфенил H-N \ 508,3 13А-3 2-фторфенил H-N \ 534,3 13А-4 2-фторфенил w н 520,3 13А-5 2-хлорфенил Н" н 524,3 13А-6 2-хлорфенил 550,3 13А-7 2-хлорфенил H'NH 564,2 13А-8 2-хлорфенил 497,1 13А-9 2-хлорфенил 482,4 13А-10 2-хлорфенил N- 1 -ОН ^0 455,3 - 54 - 008176 Пример 14. Получение промежуточного {3-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-3-(1а,5а,6а)азабицикло[3,1,0]гекс-6-ил}карбаминовой кислоты трет-бутилового эфира (1-(14А-1)а). 6-Хлор-9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин 1-(4А-7)с (83 мг; 0,22 ммоль), (3-(1ос,5ос,6р)азаби-цикло[3,1,0]гекс-6-ил)карбаминовой кислоты трет-бутиловый эфир (полученный по методике, описанной в Brighty, Katherine E., патент США № 5164402; 87 мг; 0,44 ммоль) и триэтиламин (46 мкл; 0,33 ммоль) объединяли в этаноле (1 мл) и перемешивали в течение ночи. Реакционную смесь концентрировали при пониженном давлении и затем очищали на колонке Biotage(tm) Flash 12S, используя 3% метанол в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения Е(14А-1)а (117 мг; 99%): +APCI MS (М+1) 537,4; 1Н ЯМР (400 МГц, CD3OD): 5 8,19 (s, 1Н), 7,59 (d, J=7,5 Гц, 1H), 7,50-7,35 (m, 5H), 7,27 (d, J=8,7 Гц, 2H), 4,75 (br s, 1H), 4,20 (br s, 1H), 4,03 (br s, 1H), 3,75 (br s, 1H), 2,24 (s, 1H), 1,89 (br s, 2H), 1,42 (s, 9H). Получение 3-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-3-(1а,5а,6а)-азабицикло[3,1,0]гекс-6-иламина гидрохлоридной соли (14А-1). счул- 14А-1 {3-[9-(4-Хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-3-(1а,5а,6а)азабицикло[3,1,0]гекс-6-ил}кар-баминовой кислоты трет-бутиловый эфир Е(14А-1)а растворяли в метаноле (1 мл) и к этой смеси добавляли 4М НС1 в диоксане (1 мл). Реакционную смесь перемешивали 5 ч и затем концентрировали и растирали в эфире с получением указанного в заголовке соединения 14А-1 (112 мг; количественный выход): +ESI MS (М+1) 437,1; 1Н ЯМР (400 МГц, CD3OD): 5 8,39 (s, 1Н), 7,60 (d, J=7,5 Гц, 1H), 7,55-7,40 (m, 5H), 7,32 (d, J=8,7 Гц, 2H), 2,66 (s, 1H), 2,37 (br s, 2H). Соединения, перечисленные ниже в табл. 11, были получены по методикам, аналогичным описанным выше для синтеза соединения 14А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 11 .......NH2 Пример № -NRR' MS (М+Н) + 14A-2 2-хлорфенил \-j--^"*N Н Н 437,1 14A-3 2-фторфенил *-......N н н 421,1 14A-4 2-фторфенил \-p-^N н н 421,1 14A-5 2,4-дихлорфенил ^-'N н н 471,3 - 55 - 008176 Пример 15. Получение {1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]этил}изопропиламина (15А-1). 15А-1 Раствор 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]этанона 1-(15А-1)а (16 мг; 0,038 ммоль) и изопропиламина (6,5 мкл; 0,076 ммоль) в метиленхлориде (0,3 мл) перемешивали при комнатной температуре и к нему добавляли изопропоксид титана(ГУ) (34 мкл; 0,114 ммоль). Реакционную смесь перемешивали в течение 3 ч и затем добавляли метанол (0,5 мл) с последующим добавлением боргидрида натрия (5 мг). Когда по данным LC/MS реакция завершилась, реакционную смесь очищали на пластине препаративной ТСХ, используя смесь 10% метанола/метиленхлорид с 1% гидроксида аммония в качестве растворителя, с получением указанного в заголовке соединения 15А-1. Раствор этого вещества в метиленхлориде обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением соль гидрохлорида соединения 15А-1 (5,9 мг): +ESI MS (M+1) 460,5; 1Н ЯМР (500 МГц, CD3OD): 5 9,08 (s, 1Н), 7,77 (d, J=8,3 Гц, 1H), 7,64 (s, 1H), 7,59-7,48 (m, 3H), 7,41 (d, J=8,8 Гц, 2Н), 5,38 (q, J=6,2 Гц, 1Н), 3,45 (септуплет, J=6,5 Гц, 1Н), 1,84 (d, J=6,7 Гц, 3H), 1,43 (d, J=6,7 Гц, 3Н), 1,41 (d, J=6,2 Гц, 3Н). Получение 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(1 -пиперидин- 1-илэтил)-9Н-пурина (15А-2). 15А-2 9-(4-Хлорфенил)-8-(2,4-дихлорфенил)-6-(1-пиперидин-1-илэтил)-9Н-пурин получали по методикам, аналогичным описанным выше для синтеза соединения 15А-1. Соединение превращали в соответствующую гидрохлоридную соль для тестирования: +ESI MS (M+1) 486,5. Пример 16. Получение [9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-илметил]циклогексил-амина (16А-1). 16A-1 С-[9-(4-Хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]метиламин !-(16А-1)Ь (19 мг; 0,047 ммоль) растворяли в метаноле (1 мл) и к нему добавляли циклогексанон (1 каплю) и уксусную кислоту (1 каплю). Реакционную смесь перемешивали при комнатной температуре в течение 0,5 ч, затем добавляли циано-боргидрид натрия (5 мг) и перемешивание продолжали до тех пор, пока реакция не завершалась полностью (2 ч). Реакционную смесь концентрировали, остаток разбавляли насыщенным раствором NaHCO3 и экстрагировали в этилацетат. Органические слои объединяли, сушили (Na2SO4), фильтровали, и 5% метанол в этилацетате в качестве растворителя дал указанное в заголовке соединение 16А-1. Остаток растворяли в метиленхлориде и обрабатывали 2М HCl/эфир до образования целевой НС1 соли. Для осаждения продукта к реакционной смеси добавляли эфир. Избыток эфира декантировали и кристаллы высушивали досуха в высоком вакууме с получением гидрохлоридной соли соединения 16А-1 (6,8 мг; 30%): +ESI MS (M+1) 486,6; 1Н ЯМР (500 МГц, CD3OD): 5 9,07 (s, 1H), 7,71 (d, J=8,8 Гц, 1H), 7,64 (d, J=2,1 Гц, 1Н), 7,56 (dd, J=8,8, 2,1 Гц, 1Н), 7,52 (d, J=8,8 Гц, 2H), 7,40 (d, J=8,8 Гц, 2H), 4,94 (s, 2H), 3,35 (m 1H), 2,28 (br d, J=12,4 Гц, 2Н), 1,96 (brd, J=13,5 Гц, 2H), 1,78 (brd, J=13,0 Гц, 1H), 1,60-1,20 (m, 5H). Соединения, перечисленные ниже в табл. 13, были получены по методикам, аналогичным описанным выше для синтеза соединения 16А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного ос - 56 - 008176 нования, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 13 Пример № -NRR' MS (М+Н) + 16А-2 446,5 16А-3 488,5 16А-4 474,6 16А-5 460,5 Пример 17. Получение 9-(4-хлорфенил)-8-(2-хлорфенил)-6-пирролидин-1-ил-9Н-пурина (17А-1). 17А-1 ^-4-(4-Хлорфенил)-6-пирролидин-1-ил-пиримидин-4,5-диамин 1-(17А-1)а (25 мг; 0,086 ммоль) и 2-хлорбензойной кислоты этиловый эфир (31 мг; 0,17 ммоль) объединяли в полифосфорной кислоте (1 мл) и нагревали до 150°С до завершения реакции (2 ч). Реакционную смесь разбавляли водой, подщелачивали 6М раствором NaOH и затем экстрагировали метиленхлоридом. Органические слои объединяли, сушили (Na2SO4), фильтровали и концентрировали досуха. Неочищенное вещество очищали препаративной ТСХ, 2 раза пропуская 20% этилацетат в метиленхлориде в качестве растворителя, с получением указанного в заголовке соединения 17А-1 (11 мг; 32%): +ESI MS (М+1) 410,5; 1Н ЯМР (500 МГц, CDCl3): 5 8,44 (s, 1H), 7,51 (dd, J=7,8, 2,1 Гц, 1H), 7,42-7,33 (m, 5H), 7,21 (d, J=8,8 Гц, 2H), 4,30 (br s, 2H), 3,88 (br s, 2H), 2,15-2,00 (br m, 4H). Раствор этого вещества в метиленхлориде обрабатывали избытком 1н НС1 в диэтиловом эфире, перемешивали, упаривали досуха и затем растирали в диэтиловом эфире с получением соли гидрохлорида соединения 17А-1 (12 мг; количественно): +ESI MS (M+1) 410,5. Соединения, перечисленные ниже в табл. 14, были получены по методикам, аналогичным описанным выше для синтеза соединения 17А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше сособам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 14 Пример № MS (М+Н) + 17А-2 3-хлорфенил 410,5 17А-3 4-хлорфенил 410,5 - 57 - 008176 Пример 18. Получение 9-(4-хлорфенил)-8-(2-фторфенил)-6-пирролидин-1-ил-9Н-пурина (18А-1). 18А-1 2-Фторбензойную кислоту (22 мг; 0,15 ммоль) и К4-(4-хлорфенил)-6-пирролидин-1-ил-пиримидин-4,5-диамин 1-(17А-1)а (30 мг; 0,10 ммоль) растворяли в диоксане (0,7 мл) и 50% пропанфосфорной кислоты циклическом ангидриде в этилацетате (0,3 мл). Полученную смесь встряхивали при 95°С в течение 48 ч. Реакционную смесь охлаждали и разбавляли до объема 1,8 мл водой для очистки. Очистку неочищенной смеси завершали обращенно-фазовой препаративной ЖХВД Gilson 215 c Hewlett Packard Series 1100MSD и G1315A DAD с использованием колонки Luna 5 мкм С8(2) 250x21,2 мм Phenomenex. Использованный градиентный элюент 0,1% муравьиная кислота в воде (А) и ацетонитрил (В) с трифторуксус-ной кислотой в качестве буфера был: 0,04 мин - 80% А, 20% В; 20 мин - 20% А, 80% В; 25 мин - 100% В. Фракции с целевым соединением объединяли и упаривали досуха с получением указанного в заголовке соединения 18А-1. Остаток растворяли в метаноле (1,5 мл) и обрабатывали 4М НО/диоксан (0,2 мл). Полученную смесь встряхивали при 40°С в течение 1 ч, затем сушили в токе азота при 30°С в течение 18 ч с получением гидрохлоридной соли соединения 18А-1 в виде твердого вещества (4,2 мг; 10%): +ESI MS (М+1) 394,3; 1Н ЯМР (500 МГц, CD3OD) 5 8,36 (s, 1H), 7,72 (t, J=7,8 Гц, 1Н), 7,59 (m, 1H), 7,51 (d, J=8,8 Гц, 2H), 7,40-7,33 (m, 3H), 7,14 (t, J=9,3 Гц, 1H), 4,49 (br s, 2H), 3,84 (br s, 2H), 2,24 (br s, 4H). Соединения, перечисленные ниже в табл. 15, были получены по методикам, аналогичным описанным выше для синтеза соединения 18А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше способам получения других промежуточных соединений. Перечисленные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 15 CI- = N Пример № MS (М+Н) + 18A-2 2-цианофенил 401,2 18A-3 3-цианофенил 401,2 18A-4 3-фторфенил 394,2 18A-5 2,4-диметоксифенил 436,2 18A-6 4-трифторметилфенил 444,2 18A-7 4-хлор-2-метоксифенил 440,2 18A-8 2-этоксифенил 420,2 18A-9 3,4-дифторфенил 412,2 18A-10 3-метоксифенил 406,2 18A-11 4-изопропоксифенил 434,2 18A-12 2-метоксифенил 406,2 18A-13 3 -хлор-4-фторфенил 428,0 18A-14 З-фтор-2-метилфенил 408,2 18A-15 4-дифторметоксифенил 442,2 18A-16 4-хлор-2-фторфенил 428,0 18A-17 3-дифторметоксифенил 442,2 I8A-18 фенил 376,2 18A-19 2,3-дифторфенил 412,2 18A-20 2,4-дифторфенил 412,2 18A-21 2-хлор-4-фторфенил 428,0 18A-22 З-хлор-2-фторфенил 428,0 18A-23 380,4 18A-24 416,4 18A-25 451,4 - 58 - 008176 18А-26 378,9 18А-27 396,7 18А-28 416,7 18А-29 380,9 18А-30 382,0 18А-31 418,2 18А-32 436,2 18А-33 394,2 18А-34 wvLv F 448,2 18А-35 396,2 18А-36 446,0 18А-37 445,2 18А-38 418,2 18А-39 377,2 18А-40 391,2 18А-41 382,0 18А-42 (TP 377,2 18А-43 ос, 411,0 18А-44 411,0 18А-45 411,0 18А-46 391,2 - 59 - 008176 Пример 19. Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-иламино]циклопентанкар-боновой кислоты, калиевой соли (19А-1). 19А-1 1-Аминоциклопентанкарбоновую кислоту (36 мг; 0,28 ммоль) и Na2SO4 (15 мг; 0,14 ммоль) объединяли в воде (1 мл). 6-Хлор-9-(4-хлор-фенил)-8-(2-хлорфенил)-9Н-пурин 1-(4А-7)с (57,5 мг; 0,137 ммоль) добавляли в реакционную смесь и нагревали до температуры дефлегмации в течение ночи. Реакционную смесь разбавляли 1М НС1 и полученные твердые вещества собирали фильтрованием и сушили под высоким вакуумом с получением смеси 2:1 продукта и исходного пурина (49 мг). Остаток растворяли в метиленхлориде (1,5 мл) и обрабатывали триметилсиланолатом калия (21 мг). К медленно перемешиваемой реакционной смеси добавляли эфир, и происходило образование осадка. Твердые вещества выделяли фильтрованием, промывали смесью 1:1 метиленхлорид/эфир и сушили под высоким вакуумом с получением указанного в заголовке соединения 19А-1 (28 мг; 44%): +ESI MS (M+1) 468,1; 1Н ЯМР (400 МГц, CD3OD) 5 8,21 (s, 1Н), 7,60 (dd, J=7,5, 1,7 Гц, 1H), 7,50-7,35 (m, 5H), 7,29 (d, J=8,7 Гц, 2H), 2,42-2,33 (br m, 2H), 2,26-2,17 (br m, 2H), 1,87 (br s, 4H). Получение 4-амино-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-карбоновой кислоты, калиевой соли (19A-2). 19A-2 4-Амино-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-карбоновую кислоту получали по методике, аналогичной описанной выше для синтеза соединения 19А-1: +ESI MS 483,1. Пример 20. Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амида (20А-1). 20А-1 К бледно-оранжевому раствору 6-хлор-9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурина Ц4А-7)с (1,00 г; 2,66 ммоль) в ацетоне (13 мл) при комнатной температуре добавляли триэтиламин (410 мкл; 2,94 ммоль). Затем добавляли раствор 4-этиламинопиперидин-4-карбоновой кислоты амида I-(7A-80)f в воде (1,5 мл) с получением прозрачного желтого реакционного раствора. После перемешивания при комнатной температуре в течение 3 суток мутную белую реакционную смесь разбавляли водой (11 мл). После перемешивания в течение 1 ч при комнатной температуре, затем 1 ч при 0°С осадок собирали на воронке из пористого стекла и промывали холодной смесью ацетон/Н2О (1:1). Твердое вещество сушили в вакууме с получением указанного в заголовке соединения 20А-1 в виде бесцветного твердого вещества (1,22 г; 90%): +ESI MS (М+1) 510,2; 1Н ЯМР (400 МГц, CD3OD) 5 8,19 (s, 1H), 7,57 (d, J=7,0 Гц, 1H), 7,45-7,35 (m, 5H), 7,26 (d, J=8,7 Гц, 2H), 4,54 (br s, 2H), 4,24 (br s, 2H), 2,51 (q, J=7,0 Гц, 2H), 2,12-2,06 (m, 2H), 1,76-1,72 (m, 2H), 1,10 (t, J=7,0 Гц, 3Н). Указанное выше твердое вещество (1,00 г; 1,96 ммоль) суспендировали в изопропаноле (16 мл) с последующим добавлением THF (6 мл) и получением прозрачного раствора. При комнатной температуре в течение 1 мин добавляли водный 2М НС1 (1,3 мл; 2,6 ммоль), затем перемешивали при комнатной температуре в течение 1 ч с последующим нагреванием до температуры дефлегмации и перемешиванием в течение 16 ч. После охлаждения смесь перемешивали в ледяной бане 2 ч. Бесцветный осадок собирали на воронке из пористого стекла и промывали холодной смесью изопропанол/Н2О (95:5), затем сушили в вакууме с получением 20А-1 в виде бесцветного твердого вещества (0,86 г; 79%). Часть этого вещества (0,81 г; 1,48 ммоль) суспендировали в 15 мл смеси изопропанол/Н2О (95:5), затем нагревали до темпера - 60 - 008176 туры дефлегмации и перемешивали в течение 17 ч. Суспензию охлаждали до комнатной температуры, перемешивали в течение 2 ч, затем собирали на воронке из пористого стекла со средним размером пор и промывали смесью изопропанол/Н2О (95:5) при комнатной температуре. После дополнительного высушивания в вакууме получали гидрохлоридную соль соединения 20А-1 в виде бесцветного твердого вещества (0,72 г; 89%): +ESI MS (М+1) 510,2; 1Н ЯМР (400 МГц, CD3OD): 5 8,31 (s, 1H), 7,60 (d, J=7,4 Гц, 1H), 7,51-7,40 (m, 5H), 7,29 (d, J=8,7 Гц, 2H), 4,78 (br s, 2H), 4,22 (br s, 2H), 3,07 (q, J=7,0 Гц, 2H), 2,56-2,52 (m, 2H), 2,09-2,03 (m, 2H), 1,36 (t, J=7,0 Гц, 3Н). Бензолсульфонатную и метансульфонатную соли соединения 20А-1 получали аналогичным образом. Пример 21. Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-карбоновой кислоты метилового эфира (21А-1). 21А-1 1-[9-(4-Хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-карбоновой кислоты амид 7А-87 (пример 164; 53 мг; 0,093 ммоль) и Amberlyst 15 (0,8 г) в метаноле (5 мл) герметично закрывали в пробирке и затем нагревали до 60°С в течение 20 ч. Смолу удаляли фильтрованием, промывали смесью метанол/триэтиламин (2:1) и затем 10% NH4OH в метаноле. Объединенные органические слои концентрировали и затем очищали на колонке Biotage(tm) Flash 12S, используя смесь 0-2-4% метанола в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения 21 А-1 в виде твердого вещества светло-коричневой окраски (26 мг; 55%): +ESI MS (М+1) 511,1; 1Н ЯМР (400 МГц, CD2Q2): 5 8,28 (s, 1H), 7,52 (d, J=8,3 Гц, 1H), 7,44-7,32 (m, 5H), 7,21 (d, J=8,7 Гц, 2H), 5,55 (v br s, 1H), 4,65 (v br s, 2H), 4,13 (v br s, 2H), 3,71 (s, 3H), 2,28 (s, 3H), 2,07 (ddd, J=13,7, 9,6, 3,7 Гц, 2Н), 1,79 (dt, J=13,7, 3,9 Гц, 2Н). Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты метилового эфира (21А-2). 21А-2 1-[9-(4-Хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты метиловый эфир получали, используя методики, аналогичные описанным выше для синтеза шединения 21А-1: +APCI MS (M+1) 525,3. Пример 22. Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-изопропиламинопи-перидин-4-карбонитрила (22А-1). 22 А-1 Суспензию 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-она 7А-96 (48 мг; 0,11 ммоль) в метаноле (0,4 мл) охлаждали до 0°С, затем обрабатывали 2-пропиламином (15 мкл; 0,15 ммоль) и затем концентрированным водным НС^ После перемешивания в течение 5 мин добавляли раствор цианида натрия (8,1 мг; 0,16 ммоль) в воде (0,4 мл) и эту гетерогенную реакционную смесь нагревали до комнатной температуры и затем оставляли перемешиваться в течение ночи. Далее для растворения всех реагентов добавляли тетрагидрофуран (0,4 мл). Добавляли дополнительное количество цианида натрия (8 мг; 0,16 ммоль) и 2-пропиламина (3 капли) и перемешивали в течение ночи. Реакционную смесь фильтровали и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения 22А-1 (27 мг; 48%) в виде бесцветного твердого вещества: +ESI MS (M+1) 506,1; 1Н ЯМР (400 МГц, CD2Q2): 5 8,32 (s, 1H), 7,52 (d, J=7,9 Гц, 1Н), 7,45-7,33 (m, 5H), 7,21 (d, J=8,7 Гц, 2H), 5,50 (v br s, 2H), 3,88 (v br s, 2H), 3,18 (септуплет, J=6,0 Гц, 1H), 2,16 (m, 2H), 1,82 (ddd, J=13,3, 10,4, 3,7 Гц, 2Н), 1,16 (d, J=6,2 Гц, 6H). - 61 - 008176 Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбонитрила (22А-2). N^N У м---. \Jra 22А-2 1-[9-(4-Хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбонитрил получали, используя методики, аналогичные описанным выше для синтеза соединения 22А-1: +ESI MS (M+1) 492,1. Пример 23. Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-гидроксипиперидин-4-карбоновой кислоты метилового эфира (23А-1). N^N С1^^ II Г=( он 23А-1 Хлор-9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин I-(4А-7)с (59 мг; 0,16 ммоль) и 4-гидроксипипе-ридин-4-карбоновую кислоту (22 мг; 0,14 ммоль) сочетали в соответствии с общим способом из примера 19. Неочищенный продукт (ESI MS (M+1) 484) растворяли в смеси 1:1 метанол/бензол (0,6 мл) и затем обрабатывали триметилсилилдиазометаном (2М в гексанах; 0,17 мл; 0,34 ммоль). После перемешивания в течение 1 ч реакционную смесь концентрировали под струей азота и затем очищали препаративной ТСХ, используя смесь 4% метанола в метиленхлориде, с получением указанного в заголовке соединения 23А-1 (31 мг; 44%). Раствор вещества в смеси эфир/метиленхлорид обрабатывали избытком 1М НС1 в эфире, концентрировали под струей азота и затем растирали с эфиром с получением гидрохлоридной соли соединения 23А-1 (27 мг; общий выход 36%) в виде твердого вещества бледного рыжевато-коричневого цвета: +ESI MS (M+1) 498,1; 1Н ЯМР (400 МГц, CD3OD): 5 8,38 (s, 1H), 7,62-7,59 (m, 1H), 7,51-7,40 (m, 5H), 7,34 (d, J=8,7 Гц, 2Н), 3,90 (v br s, 2H), 3,75 (s, 3H), 2,25 (td, J=13,1, 4,1 Гц, 2Н), 1,97 (br d, J=12,4 Гц, 2Н). Пример 24. Получение {1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-метиламинопипери-дин-4-ил}метанола (24A-1). 24A-1 Раствор 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-карбоновой кислоты метилового эфира 21А-1 (91 мг; 0,18 ммоль) в тетрагидрофуране (1,5 мл) при 0°С обрабатывали гидридом диизобутилалюминия (1 М в тетрагидрофуране; 0,94 мл), затем нагревали до комнатной температуры и оставляли перемешиваться в течение ночи. Смесь гасили 0,6М NaOH (25 мл), экстрагировали этилацетатом, сушили (Nа2SO4), концентрировали (80 мг) и затем очищали на колонке Biotage(tm) Flash 12M, используя смесь 5-10% метанола и 0,5% NH4OH в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения 24А-1 (48 мг; 55%): +ESI MS (M+1) 483,1; 1Н ЯМР (400 МГц, CD2CI2): 5 8,28 (s, 1H), 7,52 (d, J=8,3 Гц, 1Н), 7,44-7,32 (m, 5H), 7,21 (d, J=8,7 Гц, 2Н), 4,67 (v br s, 2H), 3,98 (br s, 2H), 3,40 (s, 2H), 2,31 (s, 3H), 1,72 (dt, J=14,1, 4,6 Гц, 2Н), 1,62 (ddd, J=14,1, 9,6, 4,2 Гц, 2Н). Пример 25. Получение 8-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-изопропил-3-метил-1,3,8-триазаспиро[4,5]декан-4-она соли гидрохлорида (25А-1). _ N^N V> C1 ° L 25 A-1 Суспензию 8-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5] декан-4-она 13А-1 (86 мг; 0,16 ммоль) и метилиодида (2М в МТВЕ; 16 мкл) в смеси 1:1 тетрагидрофу-ран/диметилформамид (2 мл) обрабатывали гидридом натрия (60% дисперсия в масле; 12 мг; 0,3 ммоль). После перемешивания в течение 2 ч смесь экстрагировали из насыщенного водного бикарбоната натрия - 62 - 008176 этилацетатом, сушили (Na2SO4), концентрировали (123 мг) и затем очищали флэш-хроматографией, используя 4% метанол, с получением указанного в заголовке соединения 25А-1 в виде масла (87 мг; количественный выход). Метиленхлоридный раствор вещества обрабатывали избытком 1М НС1 в эфире, концентрировали под струей азота и затем растирали с эфиром с получением гидрохлоридной соли соединения 25А-1 (82 мг; общий выход 82%) в виде бесцветного твердого вещества: +ESI MS (М+1) 550,2; 1Н ЯМР (400 МГц, CD3OD): 5 8,34 (s, 1H), 7,60 (d, J=7,9 Гц, 1H), 7,51-7,39 (m, 5H), 7,31 (d, J=8,3 Гц, 2H), 4,76 (s, 2H), 4,14 (br s, 2H), 3,78 (br s, 1H), 2,96 (s, 3H), 2,28 (br s, 4H), 1,32 (d, J=6,2 Гц, 6Н). Пример 26. Получение 4-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-2-карбоновой кислоты амида (26А-1). 26А-1 Через раствор 4-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-2-карбоновой кислоты этилового эфира 13А-9 (32 мг; 0,064 ммоль) в метаноле (4 мл) при 0°С барботировали NH3 с умеренной скоростью в течение 15 мин. Сосуд герметично закрывали, нагревали до комнатной температуры и оставляли перемешиваться в течение 4 суток. Смесь концентрировали при пониженном давлении (123 мг) и затем очищали на колонке Biotage(tm) Flash 12S, используя смесь 3-6% метанола в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения 26А-1 (30 мг; количественный выход). Метиленхлоридный раствор этого вещества обрабатывали избытком 1М НС1 в эфире, концентрировали под струей азота и затем растирали с эфиром с получением соли гидрохлорида соединения 26А-1 в виде не совсем белого твердого вещества: +ESI MS (М+1) 468,3; 1Н ЯМР (400 МГц, CD3OD): 5 8,47 (s, 1Н), 7,64-7,61 (m, 1H), 7,53-7,36 (m, 5H), 7,35 (d, J=8,7 Гц, 2Н), 5,52 (br d, J=14,5 Гц, 2H), 4,28 (dd, J=10,0, 3,7 Гц, 1H), 3,95-3,88 (m, 2H), 3,63 (dt, J=12,9, 3,3 Гц, 1H), 3,44-3,39 (m, 1H). Соединения, приведенные ниже в табл. 18, были получены по методикам, аналогичным описанным выше для синтеза соединения 26А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше способам получения других промежуточных соединений. Приведенные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 18 Пример № -NRR' MS (M+H) + 26A-2 2-хлорфенил 524 26A-3 2-хлорфенил k^%" 482 Пример 27. Получение 9-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-метил-4-окса-1,9-ди-азаспиро[5,5]ундекан-2-она (27А-1). 27 А-1 - 63 - 008176 К раствору {1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-ил}ме-танола 24А-1 (44 мг; 0,091 ммоль) при 0°С и триэтиламина в метиленхлориде (1 мл) по каплям добавляли 2-хлорацетилхлорид и эту реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Смесь затем разбавляли до 3 мл метиленхлоридом, добавляли 50% водный NaOH (0,6 мл) и перемешивание продолжали в течение ночи. Реакционную смесь экстрагировали из насыщенного водного бикарбоната натрия метиленхлоридом, сушили (№2SO4), концентрировали (123 мг), концентрировали при пониженном давлении (123 мг) и затем очищали на колонке Biotage(tm) Flash 12S, используя смесь 2,5-10% метанола в метиленхлориде с 0,5% NH4OH в качестве элюента, с получением указанного в заголовке соединения 27А-1 (15 мг; 32%). Метиленхлоридный раствор этого вещества обрабатывали избытком 1М НС1 в эфире, концентрировали под струей азота и затем растирали с эфиром с получением гидрохлоридной соли соединения 27А-1 в виде не совсем белого твердого вещества: +ESI MS (М+1) 523,3; 1Н ЯМР (400 МГц, CD2Q2): 5 8,32 (s, 1H), 7,53 (d, J=7,9 Гц, 1Н), 7,45-7,33 (m, 5H), 7,22 (d, J=8,7 Гц, 2H), 5,55 (v br s, 2H), 4,18 (s, 2H), 4,01 (s, 2H), 3,19 (br m, 2H), 2,85 (s, 3H), 2,14 (td, J=13,3, 5,4 Гц, 2Н), 1,88 (br d, J=14,5 Гц, 2Н). Пример 28. Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-гидроксиазетидин-3-карбоновой кислоты метилового эфира (28А-1). 28 А-1 К раствору 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-гидроксиазетидин-3-карбоновой кислоты амида 13А-10 (83 мг; 0,18 ммоль) в метаноле (2 мл) при 0°С добавляли НС1 (1М в эфире; 0,27 мл). Через 15 мин реакционную смесь концентрировали при пониженном давлении. Неочищенный продукт очищали на Хроматотроне (Chromatotron), используя смесь метиленхлорид/метанол/№[4ОН от 30:1:0,05 до 20:1:0,1 в качестве элюента (14 мг; 17%): +ESI MS (М+1) 470,2; 1H ЯМР (400 МГц, CD3OD): 5 8,25 (s, 1Н), 7,61 (d, J=7,5 Гц, 1H), 7,48-7,39 (m, 5H), 7,30 (d, J=8,7 Гц, 2H), 3,83 (s, 3H). Пример 29. Получение 1-{1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ил}этанона (29А-1). сь о 29А-1 К раствору 6-хлор-9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурина Ь(4А-7)с (68 мг; 0,18 ммоль) в смеси 1:1 метиленхлорид/этанол (2 мл) добавляли 1-(4-фенилпиперидин-4-ил)этанон (48 мг; 0,2 ммоль) и триэтиламин (70 мкл; 0,5 ммоль). Смесь перемешивали в течение ночи, концентрировали при пониженном давлении и затем очищали на колонке Biotage(tm) Flash 12S, используя смесь 5-10% метанола в метиленхлориде в качестве элюента, с получением указанного в заголовке соединения 29А-1 (77 мг; 78%). Раствор этого вещества в смеси 1:1 метанол/метиленхлорид обрабатывали избытком 1 М НС1 в эфире, концентрировали под струей азота и затем растирали с эфиром с получением гидрохлоридной соли соединения 29А-1 (77 мг): +ESI MS (M+1) 542,5; 1Н ЯМР (400 МГц, CD3OD): 5 8,35 (s, 1H), 7,60 (d, J=8,7 Гц, 1Н), 7,51 (t, J=7,8 Гц, 1H), 7,46-7,40 (m, 9H), 7,34-7,29 (m, 3H), 2,70 (br m, 2H), 1,98 (br m, 2H). Соединения, приведенные ниже в табл. 19, были получены по методикам, аналогичным описанным выше для синтеза соединения 29А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше способам получения других промежуточных соединений. Приведенные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 19 - 64 - 008176 Пример № -NRR' MS (M+H)+ 29А-2 2-хлорфенил 516 29А-3 2-хлорфенил [LOH 534 29А-4 2-хлорфенил 534 29А-5 2-хлорфенил 1 L-он 530 29А-6 2-хлорфенил 466,1 29А-7 2-хлорфенил 480,1 29А-8 2-хлорфенил H |\ 532,4 Пример 30. Получение 3-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-6-морфолин-4-ил-3-аза-бицикло[3,1,0]гексан-6-карбоновой кислоты амида (30А-1), Г\п < Н 0^NH2 Смесь 3-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-6-морфолин-4-ил-3-азабицикло[3,1,0]гексан-6-карбонитрила 29А-8 (28 мг; 0,052 ммоль) в концентрированой H2SO4 (0,6 мл) нагревали при 200°С в течение 2 ч. Реакционную смесь оставляли охлаждаться до комнатной температуры и перемешивали в течение ночи, после чего ее охлаждали в ледяной бане и затем осторожно гасили 5М водным NaOH до рН 11. Смесь экстрагировали этилацетатом, а затем объединенные органические слои промывали рассолом, сушили (MgSO4) и концентрировали в вакууме. Остаток очищали на колонке Biotage(tm) Flash 12S, используя смесь 0-6% метанола в метиленхлориде в качестве элюента, с получением после растирания со смесью метиленхлорид/гексаны указанного в заголовке соединения 30А-1 (24 мг; 83%): +ESI MS (M+1) 550,4; 1Н ЯМР (400 МГц, CD2Q2): 5 8,27 (s, 1Н), 7,52-7,49 (m, 1H), 7,44-7,32 (m, 5H), 7,20 (d, J=8,7 Гц, 2H), 5,54 (s, 1H), 5,47 (s, 1H), 5,03 (d, J=12,0 Гц, 1Н), 4,37 (d, J=12,0 Гц, 1Н), 3,97 (br d, J=9,1 Гц, 1Н), 3,68 - 65 - 008176 3,55 (m, 5H), 2,73-2,63 (m, 4H), 2,01 (br s, 1H), 1,96 (br s, 1H). Пример 31. Получение 9-(4-хлорфенил)-8-(2-хлорфенил)-6-изопропокси-9Н-пурина (31 A-l). 31A-1 9-(4-Хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ол (I-(4A-7)b; 50 мг; 0,14 ммоль), 2-йодпропан (26 мг; 0,15 ммоль) и карбонат цезия (50 мг; 0,15 ммоль) объединяли в диметилформамиде (0,7 мл) и перемешивали в течение ночи. Добавляли дополнительное количество 2-йодпропана (13 мг; 0,076 ммоль) и карбоната цезия (25 мг; 0,076 ммоль) и перемешивали в течение дополнительных суток. Реакционную смесь разбавляли этиловым эфиром, затем промывали насыщенным водным бикарбонатом натрия и рассолом. Органический слой сушили (Na2SO4), упаривали досуха и затем очищали на колонке Biotage(tm) Flash 12S, используя смесь 0-70% этилацетата в гексанах в качестве элюента, с получением указанного в заголовке соединения 31А-1 (34 мг; 56%): +ESI MS (M+1) 399,4; 1Н ЯМР (400 МГц, CD2Q2): 5 8,51 (s, 1H), 7,56 (dd, J=7,5, 1,7 Гц, 1H), 7,47-7,34 (m, 5H), 7,23 (d, J=9,1 Гц, 2H), 5,71 (септуплет, J=6,2 Гц, 1Н), 1,50 (d, J=6,2 Гц, 6Н). Соединения, приведенные ниже в табл. 20, были получены по методикам, аналогичным описанным выше для синтеза соединения 31А-1, с использованием соответствующих исходных веществ, которые приобретены коммерческим путем, получены с использованием хорошо известных специалистам в данной области техники способов или получены аналогично описанным выше способам получения других промежуточных соединений. Приведенные ниже соединения сначала выделяли в виде свободного основания, а затем, как правило, превращали в их соответствующую гидрохлоридную соль для тестирования. Таблица 20 Пример № -OR MS (M+H)+ 31А-2 2-хлорфенил CF3 -OEt 419,2 31А-3 4-хлорфенил CF3 -OEt 419,2 31А-4 2-метилфенил CF3 -OEt 399,3 31А-5 3-хлорфенил -OEt 385,2 31А-6 4-хлорфенил -OEt 385,2 31А-7 2-метилфенил -OEt 365,4 31А-8 2-хлорфенил CF3 -О-изо-Рг 433,3 31А-9 4-хлорфенил CF3 -О-изо-Рг 433,4 31А-10 2-метилфенил CF3 -О-изо-Рг 413,4 31А-П 4-хлорфенил -О-изо-Рг 399,4 31А-12 2-метилфенил -О-изо-Рг 379,4 31А-13 2-хлорфенил CF3 -OCH2CF3 473,4 31А-14 3-хлорфенил CF3 -OCH2CF3 473,4 31А-15 4-хлорфенил CF3 -OCH2CF3 473,4 31А-16 2-метилфенил CF3 -OCH2CF3 453,4 31А-17 3-хлорфенил -OCH2CF3 439,3 Пример 32. Получение 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-она оксима (32A-1). 32 A-1 - 66 - 008176 Смесь 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-она 7А-96 (75 мг; 0,17 ммоль) и гидроксиламина гидрохлорида (11,9 мг; 0,17 ммоль) в метаноле (0,3 мл) перемешивали в течение ночи при комнатной температуре. Реакционную смесь затем экстрагировали из насыщенного водного бикарбоната натрия, объединенные органические слои сушили (Na2SO4) и концентрировали с получением указанного в заголовке соединения 32А-1 (75 мг; 97%) в виде твердого вещества: +ESI MS (М+1) 453,4; 1Н ЯМР (400 МГц, DMSO-d6): 5 10,49 (s, 1H), 8,28 (s, 1H), 7,70 (dd, J=7,7, 1,5 Гц, 1H), 7,53-7,41 (m, 5H), 7,31 (d, J=8,7 Гц, 2Н), 4,45-4,18 (v br s, 4H), 2,61 (t, J=6,0 Гц, 2Н), 2,39 (t, J=5,8 Гц, 2Н). Фармакологическое тестирование Полезность соединений по настоящему изобретению в практике представленного изобретения может быть продемонстрирована активностью по меньшей мере в одном из протоколов, описанных в данном описании ниже. В описанных ниже протоколах использованы следующие сокращения: BSA - бычий сывороточный альбумин DMSO - диметилсульфоксид EDTA - этилендиаминтетрауксусная кислота PBS - забуференный фосфатом физиологический раствор EGTA - этиленгликоль-бисф-аминоэтиловый эфир) N,N,N',N'-тeтpayкcycнaя кислота GDP - гуанозиндифосфат sc - подкожно ро - перорально ip - интраперитонеально icv - интрацеребровентрикулярно iv - внутривенно [3H]SR141716A - меченный радиоактивной меткой №(пиперидин-1-ил)-5-(4-хлорфенил)-1-(2,4-ди-хлорфенил)-4-метил-1 Н-пиразол-3-карбоксамида гидрохлорид, приобретенный у Amersham Biosciences, Piscataway, NJ [3H]CP-55940 - меченный радиоактивной меткой 5-(1,1-диметилгептил)-2-[5-гидрокси-2-(3-гидрок-сипропил)циклогексил]фенол, приобретенный у NEN Life Science Products, Boston, MA AM251 - N-(пиперидин-1-ил)-1-(2,4-дихлорфенил)-5-(4-иодфенил)-4-метил-1Н-пиразол-3-карбоксамид, приобретенный у Tocris(tm), Ellisville, МО Все соединения, приведенные выше в разделе "Примеры", были протестированы в приведенном ниже анализе на связывание СВ-1 рецептора. Соединения имели активность связывания в пределах от 0,17 нМ до 1 мкМ, за исключением соединения примера 19А-1, которое имело активность связывания 2,8 нМ, и соединения примера 19А-2, которое продемонстрировало активность связывания 1,2 нМ. Соединения, имеющие активность <20 нМ, были затем протестированы в анализе на GTPy-[35S]-связывание СВ-1 и в анализе на связывание СВ-2, описанных ниже в разделе "Биологические анализы на связывание". Выбранные соединения затем были протестированы in vivo с использованием одного или более функциональных анализов, описанных ниже в разделе Биологические функциональные анализы. Биологические анализы in vitro Биоаналитические системы для определения связывающих СВ-1 и СВ-2 свойств и фармакологической активности лигандов каннабиноидных рецепторов описаны Roger G. Pertwee в "Pharmacology of Cannabinoid Receptor Ligands", Current Medicinal Chemistry, 6, 635-664 (1999) и в WO 92/02640 (заявка на патент США № 07/564075, поданная 8 августа 1990 года; включена в данное описание посредством ссылки). Следующие далее анализы были разработаны для обнаружения соединений, ингибирующих связывание [3H]SR141716A (селективного меченного радиоактивной меткой лиганда СВ-1) и [3Н]-5-(1,1-диметилгептил)-2-[5-гидрокси-2-(3-гидроксипропил)циклогексил]фенола ([3Н]СР-55940; меченного радиоактивным изотопом лиганда СВ-1/СВ-2) с их соответственными рецепторами. Протокол связывания СВ-1 рецептора крысы. Мозги PelFreeze (приобретенные у Pel Freeze Biologicals, Rogers, Arkansas) разрезали на куски и помещали в буфер для подготовки ткани (5 мМ трис НС1, рН=7,4 и 2 мМ EDTA), обрабатывали на политроне с высокой скоростью и выдерживали на льду в течение 15 мин. Гомогенат затем центрифугировали при 1000 х g в течение 5 мин при 4°С. Отделяли супернатант и центрифугировали при 100000 х g в течение 1 ч при 4°С. Осадок затем ресуспендировали в 25 мл ТМЕ (25 нМ Tris, рН=7,4; 5 мМ MgCl2 и 1 мМ EDTA) на использованный мозг. Проводили анализ белка и 200 мкл ткани, насчитывающей в сумме 20 мкг, добавляли в образец для анализа. Тестируемые соединения разбавляли в лекарственном буфере (0,5% BSA, 10% DMSO и ТМЕ) и затем добавляли по 25 мкл в полипропиленовый планшет с глубокими лунками. [3H]SR141716A разбавляли в буфере для лиганда (0,5% BSA плюс ТМЕ) и добавляли по 25 мкл в планшет. Для определения соответствующей концентрации белка в ткани использовали ВСА-белковый анализ и затем по 200 мкл ткани мозга крысы с соответствующей концентрацией добавляли в планшет. Планшеты закрывали и помещали в инкубатор на 20°С на 60 мин. По окончании периода инкубации в реакционный планшет добавляли 250 мкл стоп-буфера (5% BSA плюс ТМЕ). Далее с планшетов производили сбор с помощью Skatron на GF/B - 67 - 008176 фильтры, предварительно вымоченные в BSA (5 мг/мл) плюс ТМЕ. Каждый фильтр промывали дважды. Фильтры сушили в течение ночи. Утром фильтры считывали на счетчике Wallac Betaplate(tm) (приобретенном у PerkinElmer Life Sciences(tm), Boston, MA). Протокол связывания СВ-1 рецептора человека. Клетки почки эмбриона человека 293 (НЕК 293), трансфицированные кДНК СВ-1 рецептора (полученной от Dr. Debra Kendall, University of Connecticut), собирали в буфере для гомогенизации (10 мМ EDTA; 10 мМ EGTA; 10 мМ Na-бикарбонат; ингибиторы протеаз; рН=7,4) и гомогенизировали с использованием гомогенизатора Dounce. Гомогенат затем центрифугировали при 1000 х g в течение 5 мин при 4°С. Отделяли супернатант и центрифугировали при 25000 х g в течение 20 мин при 4°С. Осадок затем ресуспендировали в 10 мл буфера для гомогенизации и повторно центрифугировали при 25000 х g в течение 20 мин при 4°С. Окончательно осадок ресуспендировали в 1 мл ТМЕ (25 мМ Tris-буфер (рН=7,4), содержащий 5 мМ MgCl2 и 1 мМ EDTA). Проводили анализ белка и по 200 мкл ткани, насчитывающей в сумме 20 мкг, добавляли в образец для анализа. Тестируемые соединения разбавляли в лекарственном буфере (0,5% BSA, 10% DMSO и ТМЕ) и затем добавляли по 25 мкл в полипропиленовый планшет с глубокими лунками. [3H]SR141716A разбавляли в буфере для лиганда (0,5% BSA плюс ТМЕ) и по 25 мкл добавляли в планшет. Планшеты закрывали и помещали в инкубатор на 30°С на 60 мин. По окончании периода инкубации в реакционный планшет добавляли по 250 мкл стоп-буфера (5% BSA плюс ТМЕ). Далее с планшетов производили сбор с помощью Skatron на GF/B-фильтры, предварительно вымоченные в BSA (5 мг/мл) плюс ТМЕ. Каждый фильтр промывали дважды. Фильтры сушили в течение ночи. Утром фильтры считывали на счетчике Wallac Betaplate(tm) (приобретенном у PerkinElmer Life Sciences(tm), Boston, MA). Протокол связывания СВ-2 рецептора. Клетки яичников китайского хомяка-К1 (СНО-К1), трансфицированные кДНК СВ-2 (полученной от Dr. Debra Kendall, University of Connecticut), собирали в буфере для подготовки ткани (5 мМ Tris-HCl (pH=7,4), содержащий 2 мМ EDTA), обрабатывали на политроне с высокой скоростью и выдерживали на льду в течение 15 мин. Гомогенат далее центрифугировали при 1000 х g в течение 5 мин при 4°С. Супер-натант отделяли и центрифугировали при 100000 х g в течение 1 ч при 4°С. Осадок затем ресуспендиро-вали в 25 мл ТМЕ (25 мМ Tris-буфер (рН=7,4), содержащий 5 мМ MgCl2 и 1 мМ EDTA). Проводили анализ белка и по 200 мкл ткани, насчитывающих в сумме 10 мкг, добавляли в образец для анализа. Тестируемые соединения разбавляли в лекарственном буфере (0,5% BSA, 10% DMSO и 80,5% ТМЕ) и затем по 25 мкл добавляли в полипропиленовый планшет с глубокими лунками. [3Н]СР-55940 разбавляли в буфере для лиганда (0,5% BSA и 99,5% ТМЕ) и затем по 25 мкл добавляли в каждую лунку в концентрации 1 нМ. Для определения соответствующей концентрации белка в ткани использовали ВСА-белковый анализ и затем по 200 мкл ткани с соответствующей концентрацией добавляли в планшет. Планшеты закрывали и помещали в инкубатор на 30°С на 60 мин. По окончании периода инкубации в реакционный планшет добавляли по 250 мкл стоп-буфера (5% BSA плюс ТМЕ). Затем с планшетов производили сбор в формате Skatron на GF/B-фильтры, предварительно вымоченные в BSA (5 мг/мл) плюс ТМЕ. Каждый фильтр промывали дважды. Фильтры сушили в течение ночи. Затем фильтры считывали на счетчике Wallac Betaplate(tm). Анализ GTPy-[35S]-связывания СВ-1. Мембраны готовили из СНО-К1 клеток, стабильно трансфицированных кДНК СВ-1 рецептора человека. Мембраны готовили из клеток, как описано Bass et al. в "Identification and characterization of novel somatostatin antagonists", Molecular Pharmacology, 50, 709-715 (1996). Анализы на GТРy-[35S]-связывание проводили в 96-луночном формате FlashPlate(tm) в двух параллелях, используя 100 пМ GTPy-[35S] и 10 мкг мембран на лунку в буфере для анализа, состоящем из 50 мМ Tris-HCl, pH 7,4; 3 мМ MgCl2, pH 7,4; 10 мМ MgCl2, 20 мМ EGTA, 100 мМ NaCl, 30 мкМ GDP, 0,1% бычьего сывороточного альбумина и следующих ингибиторов протеаз: 100 мкг/мл бацитрацина, 100 мкг/мл бензамидина, 5 мкг/мл апротинина, 5 мкг/мл лейпептина. Затем анализируемую смесь инкубировали с антагонистом в возрастающих концентрациях (от 10-10 М до 10-5 М) в течение 10 мин и вводили каннабиноидный агонист СР-55940 (10 мкМ). Анализы проводили при 30°С в течение 1 ч. Затем FlashPlates(tm) центрифугировали при 2000 х g в течение 10 мин. Стимулирование GТРy-[35S]-связывания далее количественно подсчитывали, используя Wallac Microbeta. Расчеты ЕС50 выполняли, используя Prism(tm) посредством Graphpad. Обратный агонизм измеряли в отсутствие агониста. Протокол функционального анализа СВ-1 на основе FLIPR. Для этого анализа использовали СНО-К1 клетки, совместно трансфицированные кДНК СВ-1 рецептора человека (полученной от Dr. Debra Kendall, University of Connecticut) и промискуитетного G-белка G16. Клетки культивировали 48 ч до 12500 клеток на лунку на покрытых коллагеном 384-луночных черных прозрачных аналитических планшетах. Клетки инкубировали в течение 1 ч с 4 мкМ Fluo-4 AM (Molecular Probes) в DMEM (Gibco), содержащей 2,5 мМ пробенецид и плуроновую кислоту (0,04%). Далее планшеты промывали 3 раза HEPES-забуференным физиологическим раствором (содержащим пробенецид; 2,5 мМ) для удаления избытка красителя. Через 20 мин планшеты по одному помещали в FLIPR и уровни флуо - 68 - 008176 ресценции непрерывно регистрировали в течение 80-секундного периода времени. Добавление соединений производили одновременно во все 384 лунки через 20 с записи базовой линии. Анализы проводили в трех повторах и строили кривые "концентрация-ответ" по 6 точкам. Соединения-антагонисты затем заменяли 3 мкМ WIN 55212-2 (агонист). Данные анализировали с использованием Graph Pad Prism. Обнаружение обратных агонистов. Для определения активности обратных агонистов использовали приведенный ниже протокол цикло-АМФ-анализа с использованием интактных клеток. Клетки культивировали на 96-луночном планшете до плотности 10000-14000 клеток на лунку при содержании 100 мкл на лунку. Планшеты инкубировали в течение 24 ч в инкубаторе при 37°С. Среду удаляли и добавляли среду, не содержащую сыворотки (100 мкл). Далее планшеты инкубировали в течение 18 ч при 37°С. Среду, не содержащую сыворотки и содержащую 1 мМ IBMX, добавляли в каждую лунку с последующим добавлением 10 мкл тестируемого соединения (1:10 концентрированный раствор (25 мМ соединение в DMSO) в 50% DMSO/PBS), разбавленного 10х в PBS с 0,1% BSA. После инкубации в течение 20 мин при 37°С добавляли 2 мкМ форсколин и затем инкубировали в течение еще 20 мин при 37°С. Среду удаляли, добавляли 100 мкл 0,01н НС1 и затем инкубировали в течение 20 мин при комнатной температуре. Клеточный лизат (75 мкл) вместе с 25 мкл буфера для анализа (входящего в состав набора для цАМФ-анализа FlashPlate, поставляемого NEN Life Science Products Boston, MA) добавляли в FlashPlate. Следуя приложенному к наборам протоколу, добавляли стандарты цАМФ (циклический аденозинмонофосфат) и меченый цАМФ. Планшеты затем инкубировали в течение 18 ч при 4°С. Содержимое лунок извлекали и считывали на сцинтилляционном счетчике. Биологические анализы in vivo Было показано, что каннабиноидные агонисты, такие как А9-тетрагидроканнабинол (А9-ТНС) и СР-55940, оказывают влияние на четыре характерных свойства у мышей, в совокупности известных как тетрада. Описание этих свойств см. в Smith P.B. et al., "The pharmacological activity of anandamide, a putative endogenous cannabinoid, in mice." J. Pharmacol. Exp. Ther., 270(1), 219-227 (1994) и Wiley J. et al., "Discriminative stimulus effects of anandamide in rats." Eur. J. Pharmacol., 276(1-2), 49-54 (1995). Реверсирование этих активностей в анализах на локомоторную активность, каталепсию, гипотермию и в анализе с использованием горячей пластины, описанных ниже, обеспечивает скрининг СВ-1 антагонистов по активности in vivo. Все данные представлены в виде % реверсирования от одного агониста с использованием следующей формулы: (СР/агонист - носитель/агонист)/(носитель/носитель - носитель/агонист). Отрицательные числа указывают на потенцирование агонистической активности или на неантагонистическую активность. Положительные числа указывают на реверсирование активности для данного конкретного теста. Локомоторная активность. Самцов мышей ICR (n=6; 17-19 г; Charles River Laboratories, Inc., Wilmington, MA) предварительно обрабатывали тестируемым соединением (sc, po, ip или icv). Спустя 15 мин мышам вводили СР-55940 (sc). Через 25 мин после инъекции агониста мышей размещали в прозрачных акриловых клетках (431,8 см х 20,9 см х 20,3 см), содержащих чистые деревянные стружки. Субъектам давали возможность исследовать окружение в общем в течение примерно 5 мин и активность регистрировали с использованием инфракрасных детекторов движения (приобретенных у Coulboum Instruments(tm) Allentown, PA), которые были расположены сверху на клетках. Данные собирали с помощью компьютера и выражали в виде "единиц движения". Каталепсия. Самцов мышей ICR (n=6; 17-19 г по прибытии) предварительно обрабатывали тестируемыми соединениями (sc, po, ip или icv). Спустя 15 мин мышам вводили СР-55940 (sc). Через 90 мин после инъекции мышей размещали на стальном кольце (6,5 см), присоединенном к стойке для кольца на высоте приблизительно 12 дюймов (29,5 см). Кольцо устанавливали в горизонтальной ориентации и мышь подвешивали в зазоре кольца за передние и задние лапы, зацепляя их по периметру. Длительность времени, в течение которого мышь оставалась полностью неподвижной (за исключением дыхательных движений), регистрировали за период времени 3 мин. Данные представляли в виде процента степени неподвижности. Эту степень рассчитывали путем деления числа секунд, в течение которых мышь оставалась неподвижной, на общее время периода наблюдения и умножения результата на 100. Затем рассчитывали процент реверсирования агониста. Гипотермия. Самцов мышей ICR (n=5; 17-19 г по прибытии) предварительно обрабатывали тестируемыми соединениями (sc, po, ip или icv). Спустя 15 мин мышам вводили каннабиноидный агонист СР-55940 (sc). Через 65 мин после инъекции агониста измеряли ректальную температуру тела. Это выполняли путем помещения небольшого термостатического зонда приблизительно на 2-2,5 см вглубь прямой кишки. Температуры регистрировали с точностью до одной десятой градуса. Горячая пластина. Самцов мышей ICR (n=7; 17-19 г по прибытии) предварительно обрабатывали тестируемыми соединениями (sc, po, ip или iv). Спустя 15 мин мышам вводили каннабиноидный агонист СР-55940 (sc). - 69 - 008176 Через 45 мин каждую мышь тестировали на реверсирование аналгезии, используя стандартный измерительный прибор типа горячей пластины (Columbus Instruments). Горячая пластина имела размеры 10"х10"х0,75" (24,5 см х 24,5 см х 1,8 см) с прозрачной акриловой стенкой вокруг нее. Задержку отталкивания, быстрого реагирования или резкого движения задней лапы или отпрыгивания от платформы регистрировали с точностью до одной десятой секунды. Таймер запускал экспериментатор, и каждый тест имел 40-секундную отсечку. Данные представляли в виде процента реверсирования индуцированной агонистом аналгезии. Потребление пищи. Для оценки эффективности тестируемых соединений в отношении ингибирования потребления пищи у крыс Sprague-Dawley после того, как им не давали пищи в течение ночи, использовали следующий способ скрининга. Самцов крыс Sprague-Dawley получали из Charles River Laboratories, Inc. (Wilmington, MA). Животных размещали индивидуально и кормили порошкообразным кормом. Их содержали в условиях 12-часового цикла свет/темнота, и они получали пищу и воду без ограничений. Животным давали возможность акклиматизироваться в виварии в течение 1 недели до проведения тестирования. Тестирование заканчивали во время светлой части цикла. Для проведения скрининга на эффективность потребления пищи крыс переводили в индивидуальные клетки для тестирования, не давая пищи вечером перед тестированием и в течение ночи. После того как животных не кормили в течение ночи, крысам на следующее утро давали носитель и тестируемые соединения. В качестве положительного контроля давали известный антагонист (3 мг/кг), а контрольная группа получала только носитель (без соединения). Тестируемые соединения давали в дозе в пределах от 0,1 до 100 мг/кг в зависимости от соединения. Стандартным носителем была 0,5% (мас./об.) метилцел-люлоза в воде, и стандартным способом введения был пероральный. Однако, когда это было необходимо для различных соединений, использовались различные носители и способы введения. Пищу давали крысам через 30 мин после дозирования и запускали автоматизированную систему регистрации потребления пищи Oxymax (Columbus Instruments, Columbus, Ohio). Индивидуальное потребление пищи крысами непрерывно регистрировали с 10-минутными интервалами в течение периода времени 2 ч. При необходимости потребление пищи регистрировали вручную, используя электронные весы; пищу взвешивали каждые 30 мин после того, как она была предоставлена, в течение 4 ч после предоставления пищи. Эффективность соединения определяли, сравнивая потребление пищи крысами, обработанными соединением, с потреблением пищи животными, получавшими носитель, и животными, использованными в качестве положительного контроля. Потребление алкоголя. С использованием приведенного ниже протокола оценивали эффекты потребления алкоголя у алко-гользависимых (Р) самок крыс (выведенных в Indiana University) с длительной предысторией потребления алкоголя. В приведенных ниже ссылках дается подробное описание Р-крыс: Li, T.-K., et al., "Indiana selection studies on alcohol related behaviors" в Development of Animal Models as Pharmacoqenetic Tools (eds McClearn CE., Deitrich R.A. and Erwin V.G.), Research Monograph 6, 171-192 (1981) NIAAA, ADAMHA, Rockville, MD; Lumeng, L., et al., "New strains of rats with alcohol preference and nonpreference", Alcohol And Aldehyde Metabolizing Systems, 3, Academic Press, New York, 537-544 (1977); и Lumeng, L., et al., "Different sensitivities to ethanol in alcohol-preferring and -nonpreferring rats", Pharmacol. Biochem. Behav., 16, 125-130 (1982). Самкам крыс давали 2-часовой доступ к алкоголю (10% (об./об.) и вода, 2 бутылки по выбору) ежесуточно при наступлении темной части цикла. Для облегчения взаимодействий экспериментаторов крыс содержали в условиях обратного цикла. Изначально животных распределяли по четырем группам, уравненных по потреблению алкоголя: группа 1 - носитель (n=8); группа 2 - положительный контроль (например 5,6 мг/кг АМ251; n=8); группа 3 - тестируемое соединение в низкой дозе (n=8); и группа 4 - тестируемое соединение в высокой дозе (n=8). В общем, тестируемые соединения смешивали с носителем, 30% (мас./об.) в-циклодекстрином в дистиллированной воде, в объеме 1-2 мл/кг. В течение первых 2 суток эксперимента инъекции носителя делали всем группам. За этим следовали 2 дня инъекций лекарственного средства (соответствующим группам) и инъекции носителя в последний день. В дни инъекций лекарственного средства лекарственные средства вводили sc за 30 мин до 2-часового периода доступа к алкоголю. На протяжении периода тестирования для всех животных измеряли потребление алкоголя и для определения влияния соединений на алкогольную зависимость производили сравнение между животными, обработанными лекарственным средством и носителем. Дополнительные исследования по потреблению алкоголя проводили с использованием самок мышей C57BI/6 (Charles River). В нескольких исследованиях было показано, что мыши этой линии охотно потребляют алкоголь, для чего не требуется никаких манипуляций или требуются минимальные манипуляции (Middaugh et al., "Ethanol Consumption by C57BL/6 Mice: Influence of Gender and Procedural Variables", Alcohol, 17(3), 175-183, 1999; Le et al., "Alcohol Consumption by C57BL/6, BALA/c, and DBA/2 Mice in a Limited Access Paradigm", Pharmacology Biochemistry and Behavior, 47, 375-378, 1994). Во всех случаях мышей (17-19 г) по прибытии размещали индивидуально и предоставляли неограни - 70 - 008176 ченный доступ к порошкообразному корму для крыс, воде и 10% (мас./об.) раствору спирта. Через 2-3 недели неограниченного доступа доступ к воде ограничивали 20 часами и доступ к алкоголю ограничивали только 2 часами ежедневно. Это делали, чтобы период доступа приходился на 2 последних часа темной части светового цикла. Как только питьевой режим стабилизировался, начинали тестирование. Состояние мыши считали стабильным, когда среднее потребление алкоголя в течение 3 суток составляло ±20% от среднего в течение всех 3 суток. Тестирование в первые сутки заключалось во введении всем мышам инъекции растворителя (sc или ip). Через 30-120 мин после инъекции предоставляли доступ к алкоголю и воде. Подсчитывали потребление алкоголя в этот день (г/кг) и распределение по группам (n=7-10) производили так, чтобы все группы характеризовались одинаковым потреблением алкоголя. На 2-е и 3-и сутки мышам вводили инъекции носителя или тестируемого соединения, следуя протоколу предыдущего дня. 4-е сутки пропускали и никаких инъекций не производили. Данные анализировали с использованием ANOVA (од-нофакторный дисперсионный анализ) для повторных измерений. Изменение в потреблении воды или алкоголя сравнивали с группой, получавшей носитель в течение каждых суток тестирования. Положительным результатом считается такой результат, при котором соединение способно значительно снижать потребление алкоголя, не влияя на потребление воды. Потребление кислорода. Способы. Потребление кислорода целыми животными измеряют с использованием непрямого калориметра (Охугпах от Columbus Instruments, Columbus, ОН) на самцах крыс Sprague-Dawley (если используется другая линия крыс или самки крыс, это будет конкретизировано). Крыс (весом 300-380 г) помещают в камеры калориметра и эти камеры помещают в мониторы активности. Эти исследования выполняют в течение светового цикла. Перед измерением потребления кислорода крыс кормят стандартным кормом без ограничения. В процессе измерения потребления кислорода корм не предоставляется. Базальное потребление кислорода и двигательную активность перед дозированием измеряют каждые 10 мин в течение от 2,5 до 3 ч. По окончании базального периода перед дозированием камеры открывают и посредством перорального кормления через желудочный зонд (или другого способа введения, то есть sc, ip, iv) животным вводят разовую дозу соединения (обычный дозовый интервал составляет от 0,001 до 10 мг/кг). Лекарственные средства готовят в метилцеллюлозе, воде или в конкретном носителе (примеры включают PEG400, 30% бета-циклодекстрин и пропиленгликоль). Потребление кислорода и двигательную активность измеряют каждые 10 мин в течение еще 1-6 ч после дозирования. Компьютерная программа калориметра Охугпах подсчитывает потребление кислорода (мл/кг/ч) по скорости потока воздуха через камеры и разности в содержании кислорода во входном и выходном отверстиях. Мониторы активности имеют 15 инфракрасных лучей, расположенных с промежутком в 1 дюйм на каждой оси; двигательную активность регистрируют, когда два последовательных луча оказываются прерванными, и результаты регистрируют в виде числа импульсов. Потребление кислорода в состоянии покоя за период времени перед дозированием и после него рассчитывают путем усреднения величин 10-минутного потребления О2, за исключением периодов времени высокой двигательной активности (когда двигательная активность > 100) и за исключением первых 5 величин периода времени перед дозированием и первой величины из периода времени после дозирования. Изменение в потреблении кислорода представляют в виде процентов и рассчитывают путем деления величины потребления кислорода в состоянии покоя после дозирования на величину потребления кислорода перед дозированием х100. Эксперименты обычно осуществляют с крыс в количестве n=4-6 и результаты представляют в виде среднего значения +/- средняя квадратичная ошибка (СКО). Интерпретация. Увеличение потребления кислорода > 10% рассматривается как положительный результат. Статистически, обработанные носителем крысы не имели изменения в потреблении кислорода относительно базального периода перед дозированием. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) Vvy. (I) где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R1 представляет собой водород, (С1-С4)алкил, галогенозамещенный (С1-С4)алкил или (С1-С4)алкокси; - 71 - 008176 R4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB) где R a представляет собой водород или (С1-С3)алкил; R4b и R4b, каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-Сз)алкил-0-С(0)-, (Сl-С4)алкил-NH-C(O)-, ((Сl-С4)алкил)2N-С(O)-, (С1-Сб)алкиламино-, ((Сг С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4b, либо R4b, взятый вместе с R4e, R4e, R4f или R4f, образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c и R4c', каждый независимо, представляет собой водород, циано, гидрокси, амино, Н2Ж?(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (Q-Q^ram-O-QO)-, (С1-Q^bcmi-NH-QO)-, ((СгС4)алкил)2№С(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4c, либо R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)-, -C(=N-OH)- или -C(R4d)(R4d')-, где R4d и R4d', каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NH-С(О)-, ((С1-С4)алкил)2N-С(0)-, HO-NH-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гете-роатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d"-, где R4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3)алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-0-С(0)-, фенила и ге-тероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e и R4e', каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-М1-С(0)-, ((C1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4e, либо R4e', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; и R4f и R4f, каждый независимо, представляет собой водород, циано, гидрокси, амино, Н2ЖС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (Сl-С4)алкил-NH-C(0)-, ((Сl-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ди(Сг - 72 - 008176 С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4f, либо R4f, взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; при условии, что когда R4 представляет собой группу формулы (IA), тогда (а) по меньшей мере один из R4b, R4b', R4c, R4c', R4d, R4d', R4d", R4e, R4e', R4f и R4f' является иным, чем водород, (С1-С4)алкил или галогенозамещенный (С1-С4)алкил; и (б) Y не представляет собой кислород, серу или -NH-, когда X и Z представляют собой связь, -СН2- или -СН2СН2-, и R4b, R4b, R4f и R4f представляют собой водород; или (2) группу, имеющую формулу (1С) (1С) где R5 и R6, каждый независимо, представляет собой водород или (С1-С4)алкил, и R7 представляет собой (С1-С4)алкил-, галогенозамещенный (С1-С4)алкил-, (C1-С4)алкокси(С1-С4)алкил-, (С1-С4)алкиламино(С1-С4)алкил-, ди(С1-С4)алкиламино(С1-С4)алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R5 и R6 или R5 и R7, взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гете-роатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 2. Соединение по п.1, где R4 представляет собой группу, имеющую формулу (IA) где R4b и R4b', каждый независимо, представляет собой водород, ЩЧС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4b или R4b', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, (C1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4c, взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик, и R4c представляет собой водород, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (СгС6)алкила, ацила, (СгС3)алкил-0-С(0)-, (^-С^ал^ш-МН-С^)-, ((СгС^алкил^Н-С(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4c, взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый - 73 - 008176 мостик; Y представляет собой кислород, серу, -С(О)- или -C(R4d)(R4d')-, где R4d представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (СгОалкил-КГН-СГО)-, ((С1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, и R4d представляет собой водород, Н^^О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С^Оалкил)^-С(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гете-роатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d -, где R4d представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3)алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-0-С(0)-, фенила и ге-тероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (C1-C4)алкил-NH-C(0)-, ((С1-С4)алкил)2N-С(0)-, (C1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4e, взятый вместе с R4b, R4b, R4c или R4c, образует связь, метиленовый мостик или этиленовый мостик, и R4i! представляет собой водород, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NH-С(0)-, ((С1-С4)алкил)2N-С(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4e', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик, и R4f и R4f', каждый независимо, представляет собой водород, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-C4)алкил-NH-C(O)-, ((C1-C4)алкил)2N-C(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4f или R4f', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гете-роатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 3. Соединение по п.1, где R4 представляет собой группу формулы (IB) - 74 - 008176 (IB) где R a такой, как определено в п.1; R4b представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((C1-C4)алкил)2N-C(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, R4b представляет собой водород, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NН-С(0)-, ((^-0!^^^^-C(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4b или R4b, взятый вместе с R4e, R4e, R4f или R4f, образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, (C1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4c, взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик, и R4c представляет собой водород, Н^^О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NН-С(0)-, ((C1-C4)алкил)2N-C(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R4d)(R4d')-, где R4d представляет собой водород, циано, гидрокси, амино, Н2ЖХО)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-О-С(О)-, (С1-С4)алкил-NH-С(0)-, ((С1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, и R4d' представляет собой водород, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NН-С(0)-, ((C1-C4)алкил)2N-C(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гете-роатом, выбранный из кислорода, азота или серы; Y представляет собой -NR4d -, где R4d представляет собой водород или химическую группировку, - 75 - 008176 выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3)алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-0-С(0)-, фенила и ге-тероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e представляет собой водород, циано, гидрокси, амино, Н^С(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((C1-C4)алкил)2N-C(0)-, (C1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4e, взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик, и R4e' представляет собой водород, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4e', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; R4f представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (Сl-С4)алкил-NН-С(0)-, ((Cl-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена; и R4f представляет собой водород, Н2NС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4f или R4f', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гете-роатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 4. Соединение по пп.1, 2 или 3, где X представляет собой -C(R4c)(R4c')-, где R4c и R4c', каждый независимо, представляет собой водород, H2NC(O)-, возможно замещенный (С1-С6)алкил, (C1-С4)алкил-NH-С(0)- или ((C1-C4)алкил)2N-C(0)-, или либо R4c, либо R4c', взятый вместе с R4e, R4e', R4f или R4f', образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой -NR4d -, где R4d представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонила, (С1-С3)алкиламиносульфонила, ди(С1-С3)алкиламиносульфонила, ацила, (С1-С6)алкил-0-С(0)-, фенила и ге-тероарила, где указанная группировка возможно замещена; Z представляет собой -C(R4e)(R4e')-, где R4e и R4e', каждый независимо, представляет собой водород, H2NC(O)-, возможно замещенный (С1-С6)алкил, (С1-С4)алкил-NН-С(0)- или ((C1-C4)алкил)2N-C(0)-, или либо R4e, либо R4e', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гете-роатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 5. Соединение по пп.1, 2 или 3, где Y представляет собой -C(R4d)(R4d')-, где R4d представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((С1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, - 76 - 008176 гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, R4d' представляет собой водород, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, ацила, (С1-С3)алкил-0-С(0)-, (C1-C4)алкил-NH-C(0)-, ((С1-С4)алкил)2N-С(0)-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гете-роатом, выбранный из кислорода, азота или серы; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гете-роатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 6. Соединение по п.5, где R4b, R4b', R4f и R4f', все представляют собой водород; и R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5-или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо или указанное лактамовое кольцо возможно содержит дополнительный гетероатом, выбранный из кислорода, азота или серы; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 7. Соединение по п.1, где R4 представляет собой группу, имеющую формулу (1С), (1С) где R5 и R6, каждый независимо, представляет собой водород или (С1-С4)алкил, и R7 представляет собой (С1-С4)алкил-, галогенозамещенный (С1-С4)алкил-, (С1-С4)алкокси(С1-С4)алкил-, (С1-С4)алкиламино(С1-С4)алкил-, ди(С1-С4)алкиламино(С1-С4)алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R5 и R6 или R5 и R7, взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; его фармацевтически приемлемая соль, или сольват, или гидрат указанного соединения или указанной соли. 8. Соединение по любому из пп.1-7, где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из гало-гено, (С1-С4)алкокси, (С1-С4)алкила, галогенозамещенного (С1-С4)алкила и циано; его фармацевтически приемлемая соль или сольват или гидрат указанного соединения или указанной соли. 9. Соединение по п.1, выбранное из группы, состоящей из 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиридин-2-илпиперазин-1-ил)-9Н-пурина; 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-(4-пиримидин-2-илпиперазин-1-ил)-9Н-пурина; 4-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперазин-2-карбоновой кислоты метиламида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-этиламиноазетидин-3-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-3-изопропиламиноазетидин-3-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой ки - 77 - 008176 слоты амида; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-9Н-пурин-6-ил]-4-пропиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-фторфенил)-2-метил-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-кар-боновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-пирролидин-1-илпиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-изопропиламинопиперидин-4-карбоновой кислоты амида; 4-амино-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-карбоновой кислоты амида; 1-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-4-метиламинопиперидин-4-карбоновой кислоты амида; 1-{1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ил}этанона; {3-[9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-3-(1а,5а,6а)азабицикло[3,1,0]гекс-6-ил}диметиламина; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-(4-фторфенил)пиперидин-4-ола; 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-фенилпиперидин-4-ола; 4-бензил-1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]пиперидин-4-ола; 8-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4- она; 8- [9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурин-6-ил]-1-изопропил-1,3,8-триазаспиро[4,5]декан-4-она; 9- [9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-1-метил-4-окса-1,9-диазаспиро[5,5]ундекан-2- она; 6-(1-бензилпирролидин-3-илокси)-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина; 9-(4-хлорфенил)-6-(1-циклогексилазетидин-3-илокси)-8-(2,4-дихлорфенил)-9Н-пурина; 6-трет-бутокси-9-(4-хлорфенил)-8-(2,4-дихлорфенил)-9Н-пурина; и 9-(4-хлорфенил)-8-(2,4-дихлорфенил)-6-изопропокси-9Н-пурина; их фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли. 10. Соединение, представляющее собой 1-[9-(4-хлорфенил)-8-(2-хлорфенил)-9Н-пурин-6-ил]-4-этиламинопиперидин-4-карбоновой кислоты амид или его фармацевтически приемлемую соль. 11. Соединение по п.10, где фармацевтически приемлемая соль выбрана из солей гидрохлорид, ме-зилат и безилат. 12. Фармацевтическая композиция, содержащая (1) соединение по любому из пп.1-11, фармацевтически приемлемую соль указанного соединения или сольват или гидрат указанного соединения или указанной соли; и (2) фармацевтически приемлемый эксципиент, разбавитель или носитель. 13. Фармацевтическая композиция по п.12, дополнительно содержащая по меньшей мере один дополнительный фармацевтический агент, выбранный из частичного агониста никотинового рецептора, антагониста опиоида, допаминергического агента, агента против ADHD или агента против ожирения. 14. Соединение формулы (lc/d) (lc/d) где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С1-С4)алкокси, (С1-С4)алкила, га-логенозамещенного (С1-С4)алкила и циано; R1 представляет собой водород, (С1-С4)алкил, галогенозамещенный (С1-С4)алкил или (С1-С4)алкок- си; и R4 представляет собой гидрокси или галогено. 15. Соединение формулы (1b) - 78 - 008176 H I HNy0 (lb) A где А и В, каждый независимо, представляет собой фенил, замещенный заместителями в количестве от 1 до 3, независимо выбранными из группы, состоящей из галогено, (С1-С4)алкокси, (С1-С4)алкила, галогенозамещенного (С1-С4)алкила и циано; и R1 представляет собой водород, (С1-С4)алкил, галогенозамещенный (С1-С4)алкил или (С1-С4)алкокси. 16. Способ лечения заболевания, состояния или расстройства, которое модулируется антагонистом каннабиноидного рецептора, у животных, включающий стадию введения животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (II) (И) где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R1 представляет собой водород, (С1-С4)алкил, галогенозамещенный (С1-С4)алкил или (С1-С4)алкокси; R4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), <ЛЛ|\ЛЛЛ R4f\ ^N. R4b R" > л R4b R4f^f -4b' R4HT PR4V OA) (IB) где R4a представляет собой водород или (С1-С3)алкил; R4b и R4b, каждый независимо, представляет собой водород, циано, гидрокси, амино, Н2ЖС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-Сз)алкил-0-С(0)-, (С1-С4)алкил-КИ-С(0)-, ((СгС4)алкил)2№С(0)-, (СгСб)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4b, либо R4b, взятый вместе с R4e, R4e, R4f или R4f, образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c)-, где R4c и R4c, каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-МН-С(0)-, ((C1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)цикло-алкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероари-ла, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероато-мов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4c, либо R4c, взятый вместе с R4e, R4e, R4f или R4f, образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R4d)(R4d')-, где R4d и R4d', каждый независимо, представляет собой водород, циано, гидрокси, амино, Н2ЖС(О)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NH-С(0)-, ((C1-C4)алкил)2N-C(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщен - 79 - 008176 ного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4d и R4d, взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гете-роатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d"-, где R4d" представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3)алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-0-С(0)-, фенила и ге-тероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e')-, где R4e и R4e', каждый независимо, представляет собой водород, циано, гидрокси, амино, Н^С(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-№Н-С(0)-, ((C1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)цик-лоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероа-рила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероа-томов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4e, либо R4e', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; и R4f и R4f', каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (Сl-С4)алкил-NH-C(0)-, ((Сl-С4)алкил)2N-С(N)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4f, либо R4f', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; или (2) группу, имеющую формулу (1С), где R5 и R6, каждый независимо, представляет собой водород или (С1-С4)алкил, и R7 представляет собой (С1-С4)алкил-, галогенозамещенный (С1-С4)алкил-, (С1-С4)алкокси(С1-С4)алкил-, (С1-С4)алкиламино(С1-С4)алкил-, ди(С1-С4)алкиламино(С1-С4)алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R5 и R6 или R5 и R7, взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; (3) аминогруппу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из (С1-С8)алкила, фенил(С1-С4)алкила, частично или полностью насыщенного (С3-С8)циклоалкила, гидрокси(С1-С6)алкила, (С1-С3)алкокси(С1-С6)алкила, гетероарил(С1-С3)алкила и частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; или (4) (С1-С6)алкильную группу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из гидрокси, (С1-С6)алкокси, амино, (С1-С6)алкиламино, ди((С1-С6)алкил)амино, (С1-С3)алкилсульфонила, (С1-С3)алкилсульфамида, ди((С1-С3)алкил)сульфамила, аци-локси, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероа-томов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного циклоалкила; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гете-роатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемой соли, или сольвата, или гидрата указанного соединения или указанной соли. 17. Применение соединения формулы (II) в производстве лекарства для лечения заболевания, со - 80 - 008176 стояния или расстройства, которое модулируется антагонистом каннабиноидного рецептора, (И) где А представляет собой возможно замещенный фенил или возможно замещенный гетероарил; В представляет собой возможно замещенный фенил или возможно замещенный гетероарил; R1 представляет собой водород, (СгС4)алкил, галогенозамещенный (С1-С4)алкил или (Сг С4)алкокси; R4 представляет собой (1) группу, имеющую формулу (IA) или формулу (IB), RVN^R4b R4> CR4b OA) (IB) где R4a представляет собой водород или (С1-С3)алкил; R4b и R4b, каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(O)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-Сз)алкил-0-С(0)-, (Сl-С4)алкил-NH-C(O)-, ((CrC4^iaui)2N-C(0)-, (С1-Сб)алкиламино-, ((С1-С4)алкил)2амино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4b, либо R4b, взятый вместе с R4e, R4e, R4f или R4f, образует связь, метиленовый мостик или этиленовый мостик; X представляет собой связь, -СН2СН2- или -C(R4c)(R4c')-, где R4c и R4c', каждый независимо, представляет собой водород, циано, гидрокси, амино, Н2ЖХО)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-C4)алкил-NH-C(0)-, ((C1-С4)алкил)2N-С(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4c, либо R4c, взятый вместе с R4e, R4e, R4f или R4f, образует связь, метиленовый мостик или этиленовый мостик; Y представляет собой кислород, серу, -С(О)- или -C(R4d)(R4d')-, где R4d и R4d', каждый независимо, представляет собой водород, циано, гидрокси, амино, Н^С(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1-С4)алкил-NН-С(0)-, ((C1-С4)алкил)2Н-С(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или R4d и R4d', взятые вместе, образуют частично или полностью насыщенное 3-6-членное гетероциклическое кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, 5- или 6-членное лактоновое кольцо или 4-6-членное лактамовое кольцо, где указанное гетероциклическое кольцо, указанное лактоновое кольцо и указанное лактамовое кольцо возможно замещены и указанное лактоновое кольцо и указанное лактамовое кольцо возможно содержат дополнительный гете-роатом, выбранный из кислорода, азота или серы, или Y представляет собой -NR4d -, где R4d представляет собой водород или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С3-С6)циклоалкила, (С1-С3)алкилсульфонил-, (С1-С3)алкиламиносульфонил-, ди(С1-С3)алкиламиносульфонил-, ацила, (С1-С6)алкил-0-С(0)-, фенила и ге-тероарила, где указанная группировка возможно замещена; Z представляет собой связь, -СН2СН2- или -C(R4e)(R4e)-, где R4e и R4e, каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (С1- - 81 - 008176 С4)алкил-№Н-С(0)-, ((^-О^алкил^-С^)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4e, либо R4e, взятый вместе с R4b, R4b, R4c или R4c, образует связь, метиленовый мостик или этиленовый мостик; и R4f и R4f', каждый независимо, представляет собой водород, циано, гидрокси, амино, H2NC(0)- или химическую группировку, выбранную из группы, состоящей из (С1-С6)алкила, (С1-С6)алкокси, ацилокси, ацила, (С1-С3)алкил-0-С(0)-, (Сl-С4)алкил-NH-C(0)-, ((С1-С,)алкил)2Н-С(0)-, (С1-С6)алкиламино-, ди(С1-С4)алкиламино-, (С3-С6)циклоалкиламино-, ациламино-, фенил(С1-С4)алкиламино-, гетероарил(С1-С4)алкиламино-, фенила, гетероарила, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного карбоциклического кольца, где указанная группировка возможно замещена, или либо R4f, либо R4f', взятый вместе с R4b, R4b', R4c или R4c', образует связь, метиленовый мостик или этиленовый мостик; или (2) группу, имеющую формулу (1С), (1С) где R5 и R6, каждый независимо, представляет собой водород или (С1-С4)алкил, и R7 представляет собой (С1-С4)алкил-, галогенозамещенный (С1-С4)алкил-, (С1-С4)алкокси(С1-С4)алкил-, (С1-С4)алкиламино(С1-С4)алкил-, ди(С1-С4)алкиламино(С1-С4)алкил- или частично или полностью насыщенное 4-6-членное гетероциклическое кольцо, содержащее от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, или R5 и R6 или R7, взятые вместе, образуют 5- или 6-членный лактон, 4-6-членный лактам или частично или полностью насыщенный 4-6-членный гетероцикл, содержащий от 1 до 2 гетероатомов, независимо выбранных из кислорода, серы или азота, где указанный лактон, указанный лактам и указанный гетероцикл возможно замещены; (3) аминогруппу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из (С1-С8)алкила, фенил(С1-С4)алкила, частично или полностью насыщенного (С3-С8)циклоалкила, гидрокси(С1-С6)алкила, (С1-С3)алкокси(С1-С6)алкила, гетероарил(С1-С3)алкила и частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота; или (4) (С1-С6)алкильную группу, замещенную одним или более чем одним заместителем, независимо выбранным из группы, состоящей из гидрокси, (С1-С6)алкокси, амино, (С1-С6)алкиламино, ди((С1-С6)алкил)амино, (C1-С3)алкилсульфонила, (С1-С3)алкилсульфамила, ди((С1-С3)алкил)сульфамила, аци-локси, частично или полностью насыщенного 3-6-членного гетероцикла, содержащего от 1 до 3 гетероа-томов, независимо выбранных из кислорода, серы и азота, и частично или полностью насыщенного 3-8-членного циклоалкила; где указанный гетероарил представляет собой 5-6-членный гетероарил, содержащий от 1 до 3 гете-роатомов, независимо выбранных из кислорода, серы и азота; его фармацевтически приемлемой соли. или сольвата, или гидрата указанного соединения или указанной соли. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6 - 82 - 
|