|
Патентная документация ЕАПВ |
|
||
| Запрос: | ea000008172b*\id |
|
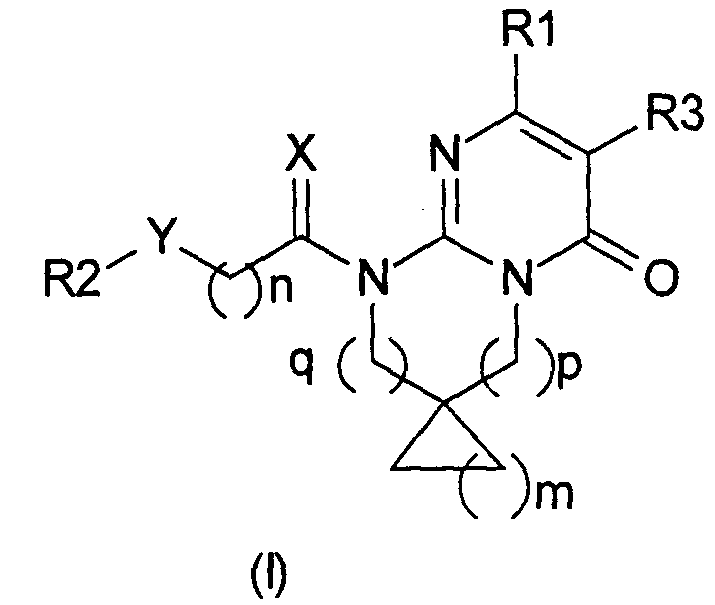
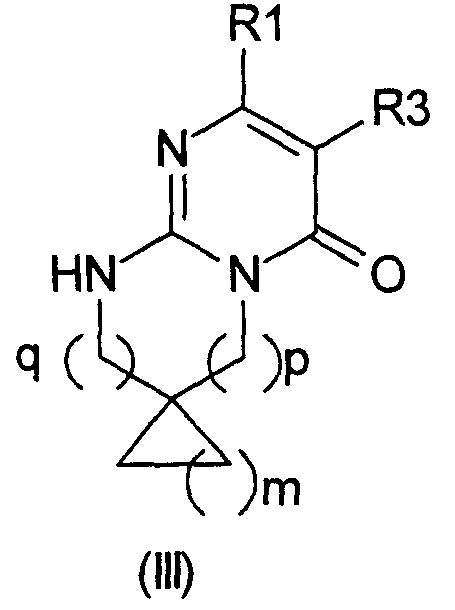
Термины запроса в документе Реферат 1. Производное дигидроспиро[циклоалкил]пиримидона, представленное формулой (I), или его соль, либо их сольват, или их гидрат где X представляет собой два атома водорода, атом серы, атом кислорода или C 1-2 алкильную группу и атом водорода; Y представляет собой связь, карбонильную группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C 1-6 алкильной группы, гидроксильной группы, C 1-4 алкокси-группы, C 1-2 пергалогенированной алкильной группы или аминогруппы; R1 представляет собой 2-, 3- или 4-пиридиновое кольцо или 2-, 4- или 5-пиримидиновое кольцо, причем кольцо возможно замещено C 1-4 алкильной группой,C 1-4 алкоксигруппой или атомом галогена; R2 представляет собой бензольное кольцо или нафталиновое кольцо, причем кольца возможно замещены заместителями в количестве от 1 до 4, выбранными из C 1-6 алкильной группы, группы метилендиокси, атома галогена, C 1-2 пергалогенированной алкильной группы, C 1-3 галогенированной алкильной группы, гидроксильной группы, C 1-4 алкоксигруппы, нитро, циано, амино, C 1-5 моноалкиламиногруппы или C 2-10 диалкиламиногруппы; R3 представляет собой атом водорода, C 1-6 алкильную группу или атом галогена; m означает от 1 до 4; n означает от 0 до 3; р означает от 0 до 2 и q означает от 0 до 2, причем р+q меньше 4. 2. Производное дигидроспиро[циклоалкил]пиримидона, или его соль, либо их сольват, или их гидрат по п.1, где R1 представляет собой незамещенную 4-пиридинильную группу или незамещенную 4-пиримидинильную группу. 3. Производное дигидроспиро[циклоалкил]пиримидона, или его соль, либо их сольват, или их гидрат по п.1 или 2, где R1 представляет собой незамещенное 4-пиридиновое кольцо или 4-пиримидиновое кольцо; и R2 представляет собой бензольное кольцо, причем кольцо возможно замещено заместителями в количестве от 1 до 4, выбранными из C 1-3 алкильной группы, атома галогена, гидроксильной группы или C 1-2 алкоксигруппы; и R3 представляет собой атом водорода; и X представляет собой два атома водорода; и Y представляет собой связь, карбонильную группу или метиленовую группу, возможно замещенную гидроксильной группой; и р равно 2 и q равно 0. 4. Производное дигидроспиро[циклоалкил]пиримидона, выбранное из группы, состоящей из 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[2-оксо-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а] пиримидин]-6'(1'Н)-она; 1'-[2-оксо-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'H)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3',4 , -дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-гидрокси-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она, или его соли, либо их сольвата, или их гидрата. 5. Соединение формулы (III) где R1, R3, m, p и q являются такими, как определено для соединения формулы (I) по п.1. 6. Лекарственное средство, включающее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного дигидроспиро[циклоалкил]пиримидона, представленного формулой (I), или его солей, либо их сольвата, или их гидрата по п.1. 7. Ингибитор GSK3 b (киназы 3 b гликогенсинтазы), выбранный из группы производного дигидроспиро[циклоалкил]пиримидона, представленного формулой (I), или его солей, либо их сольвата, или их гидрата по п.1. 8. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3 b . 9. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения нейродегенеративного заболевания. 10. Применение соединения по п.9, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, таупатий, сосудистой деменции; инсульта, травматических поражений; поражений сосудов головного мозга, травмы головного мозга, травмы спинного мозга; периферических нейропатий; ретинопатий или глаукомы. 11. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения инсулиннезависимого диабета; ожирения; маниакально-депрессивного заболевания; шизофрении; алопеции или видов рака. 12. Применение по п.11, где рак представляет собой рак молочной железы, немелкоклеточную карциному легких, рак щитовидной железы, Т- или В-клеточную лейкемию или опухоли, вызванные вирусами.
Полный текст патента (57) Реферат / Формула: где X представляет собой два атома водорода, атом серы, атом кислорода или C 1-2 алкильную группу и атом водорода; Y представляет собой связь, карбонильную группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C 1-6 алкильной группы, гидроксильной группы, C 1-4 алкокси-группы, C 1-2 пергалогенированной алкильной группы или аминогруппы; R1 представляет собой 2-, 3- или 4-пиридиновое кольцо или 2-, 4- или 5-пиримидиновое кольцо, причем кольцо возможно замещено C 1-4 алкильной группой,C 1-4 алкоксигруппой или атомом галогена; R2 представляет собой бензольное кольцо или нафталиновое кольцо, причем кольца возможно замещены заместителями в количестве от 1 до 4, выбранными из C 1-6 алкильной группы, группы метилендиокси, атома галогена, C 1-2 пергалогенированной алкильной группы, C 1-3 галогенированной алкильной группы, гидроксильной группы, C 1-4 алкоксигруппы, нитро, циано, амино, C 1-5 моноалкиламиногруппы или C 2-10 диалкиламиногруппы; R3 представляет собой атом водорода, C 1-6 алкильную группу или атом галогена; m означает от 1 до 4; n означает от 0 до 3; р означает от 0 до 2 и q означает от 0 до 2, причем р+q меньше 4. 2. Производное дигидроспиро[циклоалкил]пиримидона, или его соль, либо их сольват, или их гидрат по п.1, где R1 представляет собой незамещенную 4-пиридинильную группу или незамещенную 4-пиримидинильную группу. 3. Производное дигидроспиро[циклоалкил]пиримидона, или его соль, либо их сольват, или их гидрат по п.1 или 2, где R1 представляет собой незамещенное 4-пиридиновое кольцо или 4-пиримидиновое кольцо; и R2 представляет собой бензольное кольцо, причем кольцо возможно замещено заместителями в количестве от 1 до 4, выбранными из C 1-3 алкильной группы, атома галогена, гидроксильной группы или C 1-2 алкоксигруппы; и R3 представляет собой атом водорода; и X представляет собой два атома водорода; и Y представляет собой связь, карбонильную группу или метиленовую группу, возможно замещенную гидроксильной группой; и р равно 2 и q равно 0. 4. Производное дигидроспиро[циклоалкил]пиримидона, выбранное из группы, состоящей из 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[2-оксо-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а] пиримидин]-6'(1'Н)-она; 1'-[2-оксо-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'H)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3',4 , -дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-гидрокси-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она, или его соли, либо их сольвата, или их гидрата. 5. Соединение формулы (III) где R1, R3, m, p и q являются такими, как определено для соединения формулы (I) по п.1. 6. Лекарственное средство, включающее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного дигидроспиро[циклоалкил]пиримидона, представленного формулой (I), или его солей, либо их сольвата, или их гидрата по п.1. 7. Ингибитор GSK3 b (киназы 3 b гликогенсинтазы), выбранный из группы производного дигидроспиро[циклоалкил]пиримидона, представленного формулой (I), или его солей, либо их сольвата, или их гидрата по п.1. 8. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3 b . 9. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения нейродегенеративного заболевания. 10. Применение соединения по п.9, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, таупатий, сосудистой деменции; инсульта, травматических поражений; поражений сосудов головного мозга, травмы головного мозга, травмы спинного мозга; периферических нейропатий; ретинопатий или глаукомы. 11. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения инсулиннезависимого диабета; ожирения; маниакально-депрессивного заболевания; шизофрении; алопеции или видов рака. 12. Применение по п.11, где рак представляет собой рак молочной железы, немелкоклеточную карциному легких, рак щитовидной железы, Т- или В-клеточную лейкемию или опухоли, вызванные вирусами.
008172 Техническая область изобретения Настоящее изобретение относится к соединениям, которые полезны в качестве активного ингредиента лекарственного средства для профилактического и/или терапевтического лечения нейродегенера-тивных заболеваний, вызванных аномальной активностью киназы 3P гликогенсинтазы (GSK3P). Предшествующий уровень техники GSK3P (киназа 3P гликогенсинтазы) представляет собой пролинзависимую сериновую треонино-вую киназу, которая играет важную роль в контроле метаболизма, дифференцировки и выживания. Изначально она была идентифицирована как фермент, способный фосфорилировать и, следовательно, ин-гибировать гликогенсинтазу. Позже было обнаружено, что GSK3P идентична тау протеинкиназе 1 (TPK1), представляющей собой фермент, фосфорилирующий белок тау в эпитопах, которые, как было также обнаружено, гиперфосфорилируются при болезни Альцгеймера и некоторых таупатиях. Любопытно, что фосфорилирование GSK3P протеинкиназой В (АКТ) приводит в результате к утрате ее киназ-ной активности, и было выдвинуто предположение, что это ингибирование может опосредовать некоторые из эффектов нейротрофических факторов. Кроме того, осуществляемое GSK3P фосфорилирование P-катенина, представляющего собой белок, вовлеченный в клеточное выживание, приводит в результате к его деградации посредством зависимого от убиквитинилирования протеосомного пути. Таким образом, полагают, что ингибирование активности GSK3P может приводить в результате к нейротрофической активности. Действительно, существует доказательство того, что литий, представляющий собой неконкурентный ингибитор GSK3P, усиливает нейритогенез в некоторых моделях и также увеличивает выживание нейронов путем индукции факторов выживания, таких как Вс1-2, и ингиби-рования экспрессии проапоптотических факторов, таких как Р53 и Вах. Недавние исследования продемонстрировали, что P-амилоид увеличивает активность GSK3P и фосфорилирование белка тау. Кроме того, это гиперфосфорилирование, а также нейротоксические эффекты P-амилоида блокируются хлоридом лития и антисмысловой мРШС GSK3P. Эти наблюдения уверенно свидетельствуют о том, что GSK3P может представлять собой связующее звено между двумя основными патологическими процессами при болезни Альцгеймера: аномальным процессингом АРР (амилоидного белка-предшественника) и гиперфосфорилированием белка тау. Хотя гиперфосфорилирование тау приводит в результате к дестабилизации нейронального цитоске-лета, патологические следствия аномальной активности GSK3P, наиболее вероятно, не являются следствием исключительно патологического фосфорилирования белка тау, поскольку, как упомянуто выше, чрезмерная активность этой киназы может влиять на выживание путем модулирования экспрессии апоп-тотических и противоапоптотических факторов. Кроме того, было показано, что индуцированное P-ами-лоидом увеличение активности GSK3P приводит в результате к фосфорилированию и, следовательно, ингибированию пируватдегидрогеназы, представляющей собой основной фермент при выработке энергии и синтезе ацетилхолина. Вместе эти экспериментальные наблюдения указывают на то, что GSK3P может иметь применение при лечении нейропатологических следствий, и когнитивного дефицита, и дефицита внимания, связанных с болезнью Альцгеймера, а также других острых и хронических нейродегенеративных заболеваний. Эти заболевания включают болезнь Паркинсона, таупатии (например, лобно-височно-теменную демен-цию, кортикобазальную дегенерацию, болезнь Пика, прогрессирующий супрануклеарный паралич) и другие деменции, включая сосудистую деменцию; инсульт и другие травматические поражения; поражения сосудов головного мозга (например, обусловленную возрастом дегенерацию желтого пятна); травму головного и спинного мозга; периферические нейропатии; ретинопатии и глаукому, но не ограничиваются ими. В дополнение, GSK3P может находить применение при лечении других заболеваний, таких как ин-сулиннезависимый диабет (например, диабет II типа) и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; виды рака, такие как рак молочной железы, немелкоклеточная карцинома легких, рак щитовидной железы, Т- или В-клеточная лейкемия и некоторые опухоли, вызванные вирусами. Подробное описание изобретения Задача настоящего изобретения заключается в том, чтобы предложить соединения, полезные в качестве активного ингредиента лекарственного средства для профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3P, в частности нейродегенеративных заболеваний. Более конкретно, задача заключается в том, чтобы предложить новые соединения, полезные в качестве активного ингредиента лекарственного средства, которое дает возможность для профилактики и/или лечения нейродегенеративных заболеваний, таких как болезнь Альцгеймера. Таким образом, авторы настоящего изобретения идентифицировали соединения, обладающие инги-бирующей активностью в отношении GSK3P. В результате они обнаружили, что соединения, представленные следующей формулой (I), обладают желаемой активностью и полезны в качестве активного ингредиента лекарственного средства для профилактического и/или терапевтического лечения вышеупомянутых заболеваний. - 1 - 008172 Таким образом, в настоящем изобретении раскрыты производные дигидроспиро[циклоалкил]пири-мидона, представленные формулой (I), или их соли, либо их сольваты, или их гидраты: X представляет собой два атома водорода, атом серы, атом кислорода или С1-2алкильную группу и атом водорода; Y представляет собой связь, карбонильную группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из С1-6алкильной группы, гидроксильной группы, С1-4алкокси-группы, С1-2пергалогенированной алкильной группы или аминогруппы; R1 представляет собой 2-, 3- или 4-пиридиновое кольцо или 2-, 4- или 5-пиримидиновое кольцо, причем кольцо возможно замещено С1-4алкильной группой, С1-4алкоксигруппой или атомом галогена; R2 представляет собой бензольное кольцо или нафталиновое кольцо, причем кольца возможно замещены заместителями в количестве от 1 до 4, выбранными из С1-6алкильной группы, группы метилен-диокси, атома галогена, С1-2пергалогенированной алкильной группы, С1-3галогенированной алкильной группы, гидроксильной группы, С1-4алкоксигруппы, нитро, циано, амино, С1-5моноалкиламиногруппы или С2-10диалкиламиногруппы; R3 представляет собой атом водорода, С1-6алкильную группу или атом галогена; m означает от 1 до 4; n означает от 0 до 3; р означает от 0 до 2; и q означает от 0 до 2, причем р+q меньше 4. В соответствии еще с одним аспектом настоящего изобретения предложено лекарственное средство, включающее в качестве активного ингредиента вещество, выбранное из группы, состоящей из пири-мидоновых производных, представленных формулой (I), и их физиологически приемлемых солей, и их сольватов и гидратов. В качестве предпочтительных воплощений лекарственного средства предложено вышеупомянутое лекарственное средство, которое применяют для профилактического и/или терапевтического лечения заболеваний, вызванных аномальной активностью GSK3P, и вышеупомянутое лекарственное средство, которое применяют для профилактического и/или терапевтического лечения нейроде-генеративных заболеваний и, в дополнение, других заболеваний, таких как инсулиннезависимый диабет (например, диабет II типа) и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; виды рака, такие как рак молочной железы, немелкоклеточная карцинома легких, рак щитовидной железы, Т- или В-клеточная лейкемия и некоторые опухоли, вызванные вирусами. В качестве дополнительных предпочтительных воплощений настоящего изобретения предложено вышеупомянутое лекарственное средство, где заболевания представляют собой нейродегенеративные заболевания и выбраны из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, таупатий (например, лобно-височно-теменная деменция, кортикобазальная дегенерация, болезнь Пика, прогрессирующий супрануклеарный паралич) и других деменций, включающих сосудистую деменцию; инсульта и других травматических поражений; поражений сосудов головного мозга (например, обусловленная возрастом дегенерация желтого пятна); травмы головного и спинного мозга; периферических нейропатий; ретинопатий и глаукомы, и вышеупомянутое лекарственное средство в форме фармацевтической композиции, содержащей вышеуказанное вещество в качестве активного ингредиента, вместе с одной или более чем одной фармацевтической добавкой. Кроме того, в настоящем изобретении предложен ингибитор активности GSK3P, включающий в качестве активного ингредиента вещество, выбранное из группы, состоящей из производных дигидроспи-ро[циклоалкил]пиримидона формулы (I), и их солей, и их сольватов, и их гидратов. В соответствии с другими аспектами настоящего изобретения предложен способ профилактического и/или терапевтического лечения нейродегенеративных заболеваний, вызванных аномальной активностью GSK3P, при котором осуществляют стадию введения пациенту профилактически и/или терапевтически эффективного количества вещества, выбранного из группы, состоящей из производных дигидро-спиро[циклоалкил]пиримидона формулы (I), и их физиологически приемлемых солей, и их сольватов, и их гидратов; и применение вещества, выбранного из группы, состоящей из производных дигидроспи-ро[циклоалкил]пиримидона формулы (I), и их физиологически приемлемых солей, и их сольватов, и их гидратов для приготовления вышеупомянутого лекарственного средства. При использовании здесь С1-6алкильная группа представляет собой прямоцепочечную или разветв (I) где - 2 - 008172 ленную алкильную группу, имеющую 1-( атомов углерода, например метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, втор-бутильную группу, трет-бутильную группу, н-пентильную группу, изопентильную группу, неопен-тильную группу, 1,1-диметилпропильную группу, н-гексильную группу, изогексильную группу и т.п. С1-4алкоксильная группа представляет собой алкоксильную группу, имеющую 1-4 атома углерода, например метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутоксигруппу, изобуток-сигруппу, втор-бутоксигруппу, трет-бутоксигруппу и т.п. Атом галогена представляет собой атом фтора, хлора, брома или йода. С1-2пергалогенированная алкильная группа представляет собой алкильную группу, где все атомы водорода замещены на галогено, например СБ3 или С2Б5. С1-3галогенированная алкильная группа представляет собой алкильную группу, где по меньшей мере один атом водорода не замещен атомом галогена. С1-5моноалкиламиногруппа представляет собой аминогруппу, замещенную одной С1-6алкильной группой, например метиламиногруппу, этиламиногруппу, пропиламиногруппу, изопропиламиногруппу, бутиламиногруппу, изобутиламиногруппу, трет-бутиламиногруппу, пентиламиногруппу и изопентил-аминогруппу. С2-10диалкиламиногруппа представляет собой аминогруппу, замещенную двумя С1-5алкильными группами, например диметиламиногруппу, этилметиламиногруппу, диэтиламиногруппу, метилпропил-аминогруппу и диизопропиламиногруппу. Уходящая группа L представляет собой группу, которая может быть легко отщеплена и замещена, такая группа может представлять собой, например, тозил, мезил бромид и т.п. Соединения, представленные вышеупомянутой формулой (I), могут образовывать соль. Примеры соли включают, когда имеется кислая группа, соли щелочных металлов и щелочно-земельных металлов, таких как литий, натрий, калий, магний и кальций; соли аммиака и амины, такие как метиламин, диметил-амин, триметиламин, дициклогексиламин, трис(гидроксиметил)аминометан, ]Ч,]Ч-бис(гидроксиэтил)пи-перазин, 2-амино-2-метил-1-пропанол, этаноламин, N-метилглюкамин и L-глюкамин; или соли с основными аминокислотами, такими как лизин, 5-гидроксилизин и аргинин. Соли присоединения основания кислыми соединениями получают с использованием стандартных способов, хорошо известных из уровня техники. Когда имеется основная группа, примеры включают соли с неорганическими кислотами, такими как соляная кислота, бромоводородная кислота, серная кислота, азотная кислота, ортофосфорная кислота; соли с органическими кислотами, такими как метансульфоновая кислота, бензолсульфоновая кислота, паратолуолсульфоновая кислота, уксусная кислота, пропионовая кислота, винная кислота, фумаровая кислота, малеиновая кислота, яблочная кислота, щавелевая кислота, янтарная кислота, лимонная кислота, бензойная кислота, миндальная кислота, коричная кислота, молочная кислота, гликолевая кислота, глю-куроновая кислота, аскорбиновая кислота, никотиновая кислота и салициловая кислота; или соли с кислыми аминокислотами, такими как аспарагиновая кислота и глутаминовая кислота. Соли присоединения кислоты основных соединений получают с использованием стандартных способов, хорошо известных из уровня техники, которые включают растворение свободного основания в водном спиртовом растворе, содержащем соответствующую кислоту, и выделение соли путем выпаривания раствора или путем реакции свободного основания и кислоты в органическом растворителе, в случае чего соль отделяют непосредственно, или осаждают вторым органическим растворителем, или могут получать путем концентрирования раствора, но не ограничиваются ими. Кислоты, которые могут быть использованы для получения солей присоединения кислоты, включают предпочтительно кислоты, которые при комбинировании со свободным основанием приводят к образованию фармацевтически приемлемых солей, т. е. солей, анионы которых относительно безвредны для организма животного в фармацевтических дозах солей, таким образом, благоприятные свойства, присущие свободному основанию, не компрометируются побочными действиями, присущими анионам. Хотя предпочтительными являются приемлемые для медицины соли основных соединений, все соли присоединения кислоты находятся в объеме настоящего изобретения. В дополнение к производным дигидроспиро[циклоалкил]пиримидона, представленным вышеупомянутой формулой (I), и их солям, их сольваты и их гидраты также находятся в объеме настоящего изобретения. Производные дигидроспиро[циклоалкил]пиримидона, представленные вышеупомянутой формулой (I), могут иметь один или более чем один асимметричный атом углерода. Относительно стереохимии таких асимметричных атомов углерода, они могут независимо находиться в (R) и (S) конфигурации, и производное может существовать в виде стереоизомеров, таких как оптические изомеры или диастереои-зомеры. Любые стереоизомеры в чистой форме, любые смеси стереоизомеров, рацематы и т.п. находятся в объеме настоящего изобретения. Примеры соединений по настоящему изобретению представлены в таблице, которая следует ниже. Тем не менее, объем настоящего изобретения не ограничивается этими соединениями. Одно из воплощений настоящего изобретения включает соединения формулы (I), где: - 3 - 008172 (1) R1 представляет собой 3- или 4-пиридиновое кольцо и более предпочтительно 4-пиридиновое кольцо; или 4- или 5-пиримидиновое кольцо и более предпочтительно 4-пиримидиновое кольцо, причем кольца возможно замещены С1-2алкильной группой, С1-2алкоксигруппой или атомом галогена; и/или (2) R2 представляет собой бензольное кольцо или нафталиновое кольцо, причем кольцо возможно замещено заместителями в количестве от 1 до 4, выбранными из С1-3алкильной группы, атома галогена, гидроксильной группы или С1-2алкоксигруппы; и/или (3) R3 представляет собой атом водорода, С1-3алкильную группу или атом галогена; более предпочтительно атом водорода; и/или (4) Y представляет собой связь, карбонильную группу или метиленовую группу, возможно замещенную одной или двумя группами, выбранными из С1-3алкильной группы, гидроксильной группы, С1-4алкокси-группы, С1-2пергалогенированной алкильной группы или аминогруппы; (5) р+q равно 2 или 3, предпочтительно 2; и более конкретно, когда R1, R2, R3 и Y являются такими, как определено выше. Еще одно воплощение настоящего изобретения включает соединения формулы (I), где: (1) R1 представляет собой незамещенное 4-пиридиновое кольцо или 4-пиримидиновое кольцо; и/или (2) R2 представляет собой бензольное кольцо, причем кольцо возможно замещено заместителями в количестве от 1 до 4, выбранными из С1-3алкильной группы, атома галогена, гидроксильной группы или С1-2алкоксигруппы; и/или (3) R3 представляет собой атом водорода; и/или (4) X представляет собой два атома водорода; и/или (5) Y представляет собой связь, карбонильную группу или метиленовую группу, возможно замещенную гидроксильной группой; и/или (() р представляет собой 2 и q представляет собой 0; и более конкретно, где R1, R2, R3, X, Y, р и q являются такими, как определено выше. Конкретные соединения по настоящему изобретению, представленные формулой (I), включают соединения таблицы, следующей ниже. 1. 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопропан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'Н)-он. 2. 1'-(2-Оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пи-римидин]-6'(1'Н)-он. 3. 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он. 4. 1'-[ДО)-2-Гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он. 5. 1'-(2R)-2-Гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он. 6. 1'-[2-Оксо-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а] пиримидин]-('(1'Н)-он. 7. 1'-(2-Оксо-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пи-римидин]-6'( 1 'Н)-он. 8. 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он. 9. 1'-(2-Оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пи-римидин]-6'( 1 'Н)-он. 10. 1'-(2-Оксо-2-фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1 'Н)-он. 11. 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'Н)-он. 12. 1'-[(2R)-2-Гидрокси-2фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'Н)-он. 13. 1'-[(2R)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он. 14. 1'-(Фенилметил)-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а] пирими-дин]-6'(1'Н)-он. 15. 1'-[(2R)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он. 16. 1'-(Фенилметил)-8'-пиримидин-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пири-мидин]-6'( 1 'Н)-он. 17. 1'-(Фенилметил)-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопропан-1,2'-пиримидо [1,2-а] пирими-дин]-6'(1'Н)-он. 18. 1'-(Фенилметил)-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пиримидин] - 4 - 008172 6'(ГН)-он. 19. 1'-(Фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он. 20. 1'-(Фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он. 21. 1'-(Фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он. 22. 1'-(Фенилэтил)-8'-пиридин-4-ил-3,,4,-дигидроспиро[циклопропан-1,2,-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он. 23. 1'-(Фенилэтил)-8'-пиримидин-4-ил-3,,4,-дигидроспиро[циклобутан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он. 24. 1'-(Фенилэтил)-8'-пиримидин-4-ил-3,,4,-дигидроспиро[циклопентан-1,2,-пиримидо[1,2-а]пирими-дин]-6'(1'Н)-он. 25. 1'-(2-Гидрокси-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пи-римидо[1,2-а]пиримидин]-6'( 1 'Н)-он. 26. 1'-(2-Оксо-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'( 1 'Н)-он. В качестве еще одной задачи настоящее изобретение также охватывает способы получения дигид-роспиро[циклоалкил]пиримидоновых соединений, представленных вышеупомянутой формулой (I). Эти соединения могут быть получены, например, в соответствии со способами, приведенными ниже. Способ получения Дигидроспиро[циклоалкил]пиримидоновые соединения, представленные вышеупомянутой формулой (I), могут быть получены в соответствии со способом, раскрытым на схеме 1. Схема 1 R2' R2^Y^^N^N^ (На вышеприведенной схеме обозначения R1, R2, R3, X, Y, m, n, p и q являются такими, как описано для соединения формулы (I).) В соответствии с этим способом пиримидиноновому производному, представленному вышеприведенной формулой (III), где R1, R3, m, n, p и q являются такими, как определено для соединения формулы (I), дают возможность вступать в реакцию с основанием, таким как гидрид натрия, карбонат натрия или карбонат калия, в растворителе, таком как ^^диметилформамид, N-метилпирролидон, ^^диметил-ацетамид или хлороформ, при подходящей температуре в диапазоне от 0 до 130°С в обычной атмосфере, затем с соединением формулы (II), где R2, X, Y и n являются такими, как определено для соединения формулы (I), и L представляет собой уходящую группу, предпочтительно бромид или мезильную группу, с получением соединения вышеупомянутой формулы (I). Альтернативно, соединения формулы (I), где Y представляет собой карбонильную группу, могут быть получены путем окисления соединения формулы (I), где Y представляет собой метиленовую группу, замещенную гидроксильной группой, в соответствии со способами, хорошо известными специалисту в данной области техники. Соединение формулы (II) имеется в продаже или может быть синтезировано в соответствии со способами, хорошо известными специалисту в данной области техники. Соединение формулы (III) может быть получено в соответствии со способом, определенным на схеме 2. Схема 2 NH2 •R1 0Д^КЗ (V) HN^Cr^O -* Ч(У?Р (IV) (III) (На вышеприведенной схеме обозначения R1, R3, m, p и q являются такими, как уже было описано.) - 5 - 008172 В соответствии с этим способом 3-кетоэфиру формулы (IV), где R1 и R3 являются такими, как определено для формулы (I), и R представляет собой алкильную группу, такую как, например, метил или этил, дают возможность вступить в реакцию с соединением формулы (V). Реакция может быть осуществлена в присутствии основания, такого как карбонат калия, в спиртовом растворителе, таком как метанол, этанол и т.п., или без него, при подходящей температуре в диапазоне от 25 до 140°С в обычной атмосфере. Альтернативно, соединение формулы (III), где R3 представляет собой атом водорода, может быть галогенировано с получением соединений формулы (III), где R3 представляет собой атом галогена, такой как атом брома или хлора. Реакция может быть осуществлена в кислой среде, такой как уксусная кислота или пропионовая кислота, в присутствии бромсукцинимида, или хлорсукцинимида, или брома. В дополнение, соединения формулы (III), где R3 представляет собой атом фтора, могут быть получены по аналогии со способом, раскрытым в Tetrahedron Letters, vol. 30, № 45, рр. 6113-6116, 1989. В качестве еще одной задачи настоящее изобретение охватывает также соединение формулы (III) в качестве промежуточного соединения для получения соединения формулы (I). Соединение формулы (IV) имеется в продаже или может быть синтезировано в соответствии со способами, хорошо известными специалисту в данной области техники. Например, соединения формулы (IV), где R1 представляет собой пиридиновое или пиримидиновое кольцо, возможно замещенное C1-4алкильной группой, C1-4алкоксигруппой или атомом галогена, могут быть получены путем взаимодействия соответственно изоникотиновой кислоты или пиримидинкарбоно-вой кислоты, возможно замещенной C1-4алкильной группой, C1-4алкоксигруппой или атомом галогена, с соответствующим моноэфиром малоновой кислоты. Реакция может быть проведена с использованием способов, хорошо известных специалисту в данной области техники, таких как, например, в присутствии связывающего агента, такого как 1,1'-карбонилбис-1Н-имидазол, в растворителе, таком как тетрагидро-фуран, при температуре в диапазоне от 20 до 70°С. Соединение формулы (V) имеется в продаже или может быть синтезировано в соответствии со способами, хорошо известными специалисту в данной области техники. Например, соединение формулы (V), где m означает 1, р означает 2 и q означает 0, может быть получено в соответствии со способом, раскрытым на схеме 3, и в соответствии со способом, раскрытым Smith and Christensen (J. Org. Chem. 1955, 20, 829) для последней стадии. Условия, которые могут быть использованы, приведены в химических примерах. Схема 3 NH, Удаление запиты Введение защитной ¦ 2 NH2 группы амино NHPg Введение уходящей группы (VI) (VII) т NH2 X NH2 NHPg HN ^ N Циклизация | _ Удаление защиты ] 4NH2 ""- V^^^NPg (V) (IX) ' (VIII) (На вышеприведенной схеме Pg представляет собой защитную группу амино и L представляет собой уходящую группу.) В качестве еще одного примера соединение формулы (V), где m равно 3, р означает 2 и q означает 0, может быть получено в соответствии со способом, определенным на схеме 4, и в соответствии со способом, раскрытым Smith and Christensen (J. Org. Chem. 1955, 20, 829) для последней стадии. Условия, которые могут быть использованы, приведены в химических примерах. - 6 - 008172 Схема 4 (V) (XIII) (На вышеприведенной схеме Pgпредставляет собой защитную группу.) Соединение формулы (VI) может быть синтезировано в соответствии со способом, раскрытым Bertus and Szymoniak (Chem. Commun. 2001, 1792). Соединение формулы (X) может быть синтезировано в соответствии со способом, раскрытым Suzuki et al. (Synthetic Communication 1998, 28 (4), 701). В вышеприведенных реакциях иногда может быть необходимо введение защиты функциональной группы или ее удаление. Может быть выбрана подходящая защитная группа Pg в зависимости от типа функциональной группы, и может быть применен способ, раскрытый в литературе. Примеры защитных групп, способов введения и удаления защиты приведены, например, в Protective groups in Organic Synthesis, Greene et al., 2nd Ed. (John Wiley & Sons, Inc., New York). Соединения по настоящему изобретению обладают ингибирующим действием в отношении GSK3p. Соответственно, соединения по настоящему изобретению являются полезными в качестве активного ингредиента для приготовления лекарственного средства, обеспечивающего профилактическое и/или терапевтическое лечение заболевания, вызванного аномальной активностью GSK3P, и более конкретно ней-родегенеративных заболеваний, таких как болезнь Альцгеймера. В дополнение, соединения по настоящему изобретению также полезны в качестве активного ингредиента для приготовления лекарственного средства для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, таких как болезнь Паркинсона, таупатии (например, лобно-височно-теменная деменция, кортикобазаль-ная дегенерация, болезнь Пика, прогрессирующий супрануклеарный паралич) и другие деменции, включая сосудистую деменцию; инсульт и другие травматические поражения; поражения сосудов головного мозга (например, обусловленная возрастом дегенерация желтого пятна); травма головного и спинного мозга; периферические нейропатии; ретинопатии и глаукома; и другие заболеваний, таких как инсулин-независимый диабет (например, диабет II типа) и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; виды рака, такие как рак молочной железы, немелкоклеточная карцинома легких, рак щитовидной железы, Т- или В-клеточная лейкемия и некоторые опухоли, вызванные вирусами. Настоящее изобретение, кроме того, относится к способу лечения нейродегенеративных заболеваний, вызванных аномальной активностью GSK3P, и вышеупомянутых заболеваний, при котором в организм млекопитающего, нуждающегося в таком лечении, вводят эффективное количество соединения формулы (I). В качестве активного ингредиента лекарственного средства по настоящему изобретению может быть использовано вещество, которое выбрано из группы, состоящей из соединения, представленного вышеупомянутой формулой (I), и его фармакологически приемлемых солей, и их сольватов, и их гидратов. Вещество само по себе может быть введено в качестве лекарственного средства по настоящему изобретению, тем не менее, желательно вводить лекарственное средство в форме фармацевтической композиции, включающей в качестве активного ингредиента вышеупомянутое вещество и одну или более чем одну фармацевтическую добавку. В качестве активного ингредиента лекарственного средства по настоящему изобретению могут быть использованы в комбинации два или более чем два вышеупомянутых вещества. Вышеупомянутая фармацевтическая композиция может быть дополнена активным ингредиентом другого лекарственного средства для лечения вышеупомянутых заболеваний. Тип фармацевтической композиции конкретно не ограничен, и может быть предложена композиция в виде препарата для перо - 7 - 008172 рального или парентерального введения. Например, фармацевтическая композиция может быть приготовлена в форме фармацевтических композиций для перорального введения, таких как гранулы, мелкие гранулы, порошки, твердые капсулы, мягкие капсулы, сиропы, эмульсии, суспензии, растворы и т.п., или в форме фармацевтических композиций для парентерального введения, таких как инъекции для внутривенного, внутримышечного или подкожного введения, капельные инфузии, препараты для трансдер-мального введения, препараты для введения через слизистые оболочки, капли в нос, ингаляторы, суппозитории и т.п. Инъекции или капельные инфузии могут быть приготовлены в виде порошкообразных препаратов, таких как в форме лиофилизированнх препаратов, и могут быть использованы путем растворения непосредственно перед использованием в подходящей водной среде, такой как физиологический раствор. Препараты длительного высвобождения, такие как препараты, покрытые полимером, могут быть непосредственно введены интрацеребрально. Типы фармацевтических добавок, используемых для приготовления фармацевтической композиции, отношения фармацевтических добавок к активному ингредиенту и способы приготовления фармацевтической композиции могут быть выбраны подходящим образом специалистом в данной области техники. В качестве фармацевтических добавок могут быть использованы неорганические или органические вещества или твердые или жидкие вещества. Как правило, фармацевтические добавки могут быть включены в отношении, находящемся в диапазоне от 1 до 90 мас.%, основываясь на массе активного ингредиента. Примеры эксципиентов, используемых для приготовления твердых фармацевтических композиций, включают, например, лактозу, сахарозу, крахмал, тальк, целлюлозу, декстрин, каолин, карбонат кальция и т.п. Для приготовления жидких композиций для перорального введения может быть использован обычный инертный разбавитель, такой как вода или растительное масло. Жидкая композиция может содержать в дополнение к инертному разбавителю дополнительные вещества, такие как увлажнители, агенты, способствующие суспендированию, подсластители, ароматизаторы, красители и консерванты. Жидкая композиция может быть заполнена в капсулы, приготовленные из абсорбируемого вещества, такого как желатин. Примеры растворителей или сред для суспендирования, используемых для приготовления композиций для парентерального введения, например инъекций, суппозиториев, включают воду, пропиленгликоль, полиэтиленгликоль, бензиловый спирт, этилолеат, лецитин и т.п. Примеры основных веществ, используемых для суппозиториев, включают, например, масло какао, эмульгированное масло какао, лауриновый липид, витепсол (witepsol). Доза и частота введения лекарственного средства по настоящему изобретению конкретно не ограничены и могут быть подходящим образом выбраны в зависимости от условий, таких как задача профилактического и/или терапевтического лечения, тип заболевания, масса тела или возраст пациента, тяжесть заболевания и т.п. Как правило, суточная доза для перорального введения взрослому человеку может составлять от 0,01 до 1000 мг (масса активного ингредиента) и доза может быть введена 1 раз в сутки или несколько раз в сутки в виде дробных доз или 1 раз в несколько суток. Когда лекарственное средство используется в виде инъекции, введения могут быть предпочтительно осуществлены взрослому человеку непрерывно или с перерывами в суточной дозе от 0,001 до 100 мг (масса активного ингредиента). Химические примеры Настоящее изобретение более конкретно раскрывается со ссылкой на следующие общие примеры, тем не менее, объем настоящего изобретения не ограничен этими примерами. Пример 1 (соединение № 1 нижеследующей таблицы). 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он (1:1) (гидрохлорид). 1.1. Гидрохлорид 2-(1-аминоциклопропил)этанола (1:1). К раствору 8,63 г (45,11 ммоль) 1-(2-бензилоксиэтил)циклопропиламина и 3 г палладия 10 мас.% на активированном угле в 100 мл изопропанола добавляли 100 мл раствора соляной кислоты в изопропано-ле (5-6н.). Смесь встряхивали при 40°С под давлением водорода 4,053 Па (4 атмосферы) до прекращения поглощения водорода. Катализатор удаляли путем фильтрования и промывали изопропанолом. Фильтрат выпаривали досуха с получением 6,22 г чистого продукта в виде вязкого масла. 1.2. трет-Бутил-1-(2-гидроксиэтил)циклопропилкарбамат. К раствору 6,21 г (45,11 ммоль) гидрохлорида 2-(1-аминоциклопропил)этанола (1:1) в 63 мл тетра-гидрофурана добавляли 1 мл воды, 12,68 мл (90,22 ммоль) триэтиламина и 9,84 г (45,11 ммоль) ди-трет-бутилдикарбоната в 21 мл тетрагидрофурана. Полученную в результате смесь перемешивали при комнатной температуре в течение 16 ч. Смесь упаривали, растворяли в 100 мл диэтилового эфира и обрабатывали водным раствором соляной кислоты (0,1н.). Объединенные экстракты промывали насыщенным водным хлоридом натрия и упаривали. Неочищенный продукт перетирали с водой и фильтровали с получением 6,68 г чистого продукта в виде белого твердого вещества. Т.пл.: 93-95°С. 1.3. 2{1-[(трет-Бутоксикарбонил)амино]циклопропил}этилметансульфонат. К раствору 6,472 г (32,16 ммоль) трет-бутил-1-(2-гидроксиэтил)циклопропилкарбамата в 61 мл безводного дихлорметана добавляли 12,79 мл (91 ммоль) безводного триэтиламина. Получающуюся в ре - 8 - 008172 зультате смесь охлаждали при -20°С. Затем добавляли 3,54 мл (45,66 ммоль) мезилхлорида в 11 мл безводного дихлорметана. Получающуюся в результате смесь перемешивали при комнатной температуре в течение 2 ч. Смесь выливали в смесь лед-вода и органический слой промывали насыщенным водным хлоридом натрия, сушили над сульфатом магния и упаривали. Неочищенный продукт перетирали с петролей-ным эфиром и фильтровали с получением 7,82 г чистого продукта в виде оранжевого твердого вещества. Т.пл.: 88-89°С. 1.4. трет-Бутил-1-[2-(1,3-диоксо-1,3-дигидро-2Н-изоиндол-2-ил)этил]циклопропилкарбамат. К раствору 7,82 г (28 ммоль) 2-{1-[(трет-бутоксиарбонил)амино]циклопропил}этилметансульфоната в 35 мл безводного диметилформамида добавляли 5,45 г (29,4 ммоль) фталимида калия. Получающуюся в результате смесь перемешивали при 150°С в течение 18 ч. Смесь затем фильтровали и промывали диэти-ловым эфиром. Фильтрат упаривали досуха, неочищенный продукт нагревали в воде и остаток фильтровали. Продукт сушили с получением 4,63 г чистого соединения в виде оранжевого твердого вещества. Т.пл.: 125-127°С. 1.5. трет-Бутил-1-(2-аминоэтил)циклопропилкарбамат. К раствору 4,57 г (13,83 ммоль) трет-бутил-1-[2-(1,3-диоксо-1,3-дигидро-2H-изоиндол-2-ил)этил]цикло-пропилкарбамата в 80 мл этанола добавляли 3,36 мл (69,16 ммоль) гидрата гидразина и получающуюся в результате смесь кипятили с обратным холодильником в течение 16 ч. Смесь фильтровали и промывали диэти-ловым эфиром. Фильтрат выпаривали досуха с получением 2,3 г чистого соединения в виде оранжевого масла. 1.6. Гидробромид 1-(2-аминоэтил)циклопропанамина (1:2). К раствору 20 мл гидробромида (33%) в уксусной кислоте добавляли 2,29 г (11,46 ммоль) трет-бутил-1-(2-аминоэтил)циклопропилкарбамата и получающийся в результате раствор перемешивали при 60°С в течение 1 ч. Смесь охлаждали и добавляли диэтиловый фэир. Получающийся в результате осадок фильтровали. Продукт сушили с получением 2,69 г чистого соединения в виде коричневого твердого вещества. Т.пл.: 233-235°С. 1.7. Гидробромид 4,6-диазаспиро[2,5]окт-5-ен-5-амина (1:1). К раствору 2,65 г (10,11 ммоль) гидробромида 1-(2-аминоэтил)циклопропанамина в 21 мл метанола добавляли 3,83 мл (21,24 ммоль) раствора метоксида натрия в метаноле (5,55н.). Смесь перемешивали при комнатной температуре в течение 2 ч. Осадок фильтровали и фильтрат упаривали. Неочищенный продукт растворяли в 9 мл воды и порциями добавляли 1,07 г (10,11 ммоль) цианогенбромида. Получающуюся в результате смесь перемешивали при комнатной температуре в течение 2 ч и упаривали досуха в с получением 2,08 г чистого соединения в виде оранжевого масла. 1.8. 8'-Пиридинил-4-ил-3',4'-дигидроспиро [циклопропан-1,2'-пиримидо [1,2-а]пиримидин]-6'( 1 'Н)-он. Смесь 1,77 г (9,19 ммоль) этил-3-(пиридин-4-ил)-3-оксопропионата, 2,084 г (10,11 ммоль) гидробромида 4,6-диазаспиро[2,5]окт-5-ен-5-амина и 2,79 г (20,22 ммоль) карбоната калия в 17 мл этанола кипятили при температуре дефлегмации в течение 12 ч. Охлажденный раствор упаривали для удаления растворителя, остаток обрабатывали водой и остаток фильтровали с получением 0,88 г продукта в виде желтого порошка. Т.пл.: 277-278°С. 1.9. 1'-(2S)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопропан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он (1:1) (гидрохлорид). К раствору 0,5 г (1,97 ммоль) 8'-пиридинил-4-ил-3',4'-дигидроспиро[циклопропан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она в 10 мл безводного диметилформамида добавляли 0,173 г (4,33 ммоль) гидрида натрия (60% суспензия в минеральном масле). Смеси давали возможность перемешиваться при 50°С в течение 1 ч. Затем добавляли 0,4 г (2,56 ммоль) (^)-2-хлор-1-фенилэтанола и смеси давали возможность перемешиваться при 120°С в течение 16 ч. Добавляли воду и смесь экстрагировали этилацетатом. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и упаривали с получением неочищенного продукта. Очистка путем хроматографии на силикагеле с элюцией смесью этилдихлорметан/метанол в соотношении от 100/0 до 95/5 позволила получить соединение в форме свободного основания. Основание переводили в его соль гидрохлорид с получением 0,443 г чистого продукта. Т.пл.: 219-221°С, [a]D=-9,5 (c=0,4, СН3ОН). Ядерно-магнитный резонанс (ЯМР) (200 МГц; диметилсульфоксид (]]MCO)-d6): 8 8,90 (d, 2H); 8,35 (d, 2H); 7,12-7,46 (m, 5H); 6,61 (s, 1H); 4,88 (t, 1H); 3,4-4,05 (m, 4Н); 1,83 (t, 2Н); 1,03-1,33 (m, 2Н); 0,58-0,85 (m, 2Н). Пример 2 (соединение № 2 нижеследующей таблицы). 1'-(2-Оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро [циклопропан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он (1:1) (гидрохлорид). 0,31 г (0,83 ммоль) 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[цикло-пропан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она растворяли в 8 мл безводного дихлорметана и смешивали с 0,145 г (1,24 ммоль) N-оксида N-метилморфолина, 0,003 г (0,0083 ммоль) перрутената тетра-n-пропиламмония и 1 г порошкообразных молекулярных сит (4 А). Смесь перемешивали при 20°С в атмосфере азота в течение 12 ч. Смесь фильтровали. Фильтрат промывали насыщенным водным раствором хлорида аммония, сушили - 9 - 008172 и упаривали с получением неочищенного продукта. Очистка путем хроматографии на силикагеле с элюци-ей смесью дихлорметан/метанол в соотношении от 100/0 до 95/5 позволила получить соединение в форме свободного основания, которое превращали в его соль гидрохлорид с получением 0,078 г чистого продукта. Т.пл.: 232-234°С. ЯМР (200 МГц; ДМСО^6): 8 8,62 (d, 2H); 8,03 (d, 2Н); 8,00 (d, 2H); 7,51-7,78 (m, 3H); 6,61 (s, 1H); 5,15 (s, 2H); 4,01 (t, 2H); 2,04 (t, 2H); 1,17 (t, 2H); 0,78 (t, 2Н). Пример 3 (соединение № 3 нижеследующей таблицы). 1'-(2S)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он (1:1) (гидрохлорид). 3.1. (1 -Аминоциклопентил)ацетонитрил. Раствор 15,91 г (0,15 моль) циклопентилиденацетонитрила в 170 мл водного раствора аммиака (29%) и 57 мл метанола нагревали при 100°С в запаянной пробирке в течение 24 ч. Реакционную смесь концентрировали и остаток подвергали хроматографии на силикагеле, элюируя смесью дихлорметан/ме-танол в соотношении 90/10, с получением 12,15 г продукта в виде бесцветного масла. 3.2. трет-Бутил-1-(цианометил)циклопентилкарбамат. Продукт получали по аналогии со способом, раскрытым на стадии 1.2, и с использованием (1-аминоциклопентил)ацетонитрила. Соединение использовали на следующей стадии. 3.3. трет-Бутил-1-(2-аминоэтил)циклопентилкарбамат. К суспензии 8,48 г (223,63 ммоль) алюмогидрида лития в 687 мл диэтилового эфира при 0°С по каплям добавляли 16,7 г (74,54 ммоль) трет-бутил-1-(цианометил)циклопентилкарбамата, растворенного в 344 мл диэтилового эфира. Получающуюся в результате смесь перемешивали при 0°С в атмосфере азота в течение 1 ч. Реакционную смесь разбавляли 100 мл диэтилового эфира при 0°С и обрабатывали избытком насыщенного водного раствора сульфата натрия. Добавляли дополнительное количество сульфата натрия и органическую фазу фильтровали для удаления солей. Растворитель выпаривали досуха с получением 13,83 г продукта в виде масла. 3.4. Гидробромид 1-(2-аминоэтил)циклопентанамина (1:2). Продукт получали по аналогии со способом, раскрытым на стадии 1.6, и с использованием трет-бутил-1-(2-аминоэтил)циклопентилкарбамата. Соединение использовали на следующей стадии. Т.пл.: 194-196°С. 3.5. Гидробромид 6,8-диазаспиро[4,5]дец-7-ен-7-амина (1:1). Продукт получали по аналогии со способом, раскрытым на стадии 1.7, и с использованием гидробромида 1-(2-аминоэтил)циклопентанамина. Соединение использовали на следующей стадии. 3.6. 8'-Пиридин-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1 'Н)-он. Продукт получали по аналогии со способом, раскрытым на стадии 1.8, и с использованием гидробромида 6,8-диазаспиро[4,5]дец-7-ен-7-амина (1:1). Соединение использовали на следующей стадии. Т.пл.: 241-243°С. 3.7. 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он (1:1) (гидрохлорид). Продукт получали по аналогии со способом, раскрытым на стадии 1.9, и с использованием 8'-пиридинил-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1 'Н)-она. Т.пл.: 221-223°С, [a]D=-32,8 (c=1,036, СН3ОН). ЯМР (200 МГц; ДМСО^6): 8 8,91 (d, 2H); 8,41 (d, 2H); 7,13-7,47 (m, 5H); 6,67 (s, 1Н); 5,22 (dd, 1Н); 3,71-4,04 (m, 3Н); 3,38-3,59 (m, 1Н); 2,26-2,62 (m, 2Н); 1,76-2,15 (dm, 2Н); 1,30-1,76 (m, 6Н). Пример 4 (соединение № 4 нижеследующей таблицы). 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он. 4.1. 8'-Пиримидинил-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо[1,2-а]пиримидин]-6'(1'Н)-он. Продукт получали по аналогии со способом, раскрытым на стадии 1.8, и с использованием этил-3-(4- пиримидинил)-3-оксопропионата (полученного по аналогии со способом, раскрытым в патенте DE 2705582) и гидробромида 6,8-диазаспиро[4,5]дец-7-ен-7-амина (1:1) (полученным по аналогии с примером 3.5). Полученное соединение обрабатывали водой и осадок выделяли путем фильтрования с получением 2,92 г продукта. Т.пл.: 243-244°С. 4.2. 1'-[(2S)-2-Гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-он. Продукт получали по аналогии со способом, раскрытым на стадии 1.9, и с использованием 8'-пиримидин-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'( 1 'Н)-она. Т.пл.: 157-158°С, [a]D=-28,9 (c=1,018, СН3ОН). ЯМР (200 МГц; ДМСО^6): 8 9,28 (s, 1H); 9,01 (d, 1H); 8,14 (d, 1H); 7,15-7,50 (m, 5Н); 6,72 (s, 1Н); 5,19 (t, 1Н); 3,70-4,04 (m, 3Н); 3,38-3,58 (m, 1Н); 2,26-2,55 (m, 2Н); 1,74-2,12 (dm, 2Н); 1,25-1,74 (m, 6Н). Список химических структур и физических данных для соединений вышеупомянутой формулы (I), иллюстрирующих настоящее изобретение, приведен в нижеследующей таблице. Соединения были получены в соответствии со способами примеров. В таблице R1 представляет собой незамещенную пиримидин-4-ильную группу или незамещенную - 10 - 008172 пиридин-4-ильную группу, р означает 2, q означает 0, Ph обозначает фенильную группу, (S), (R) или (рац.) указывают в колонке "Y" стереохимию атома углерода: (рац.) означает рацемическую смесь, (R) означает абсолютную конфигурацию R, (S) означает абсолютную конфигурацию S. Y I 1 1 q(^)p (T)m X I R1 I R3 I m I N I Т.пл. Т.пл. °C Соль CH(OH)(S) H,H 219221 (1:1) (гидрохлорид) H,H 232234 (1:1) (гидрохлорид) CH(OH)(S) H,H 221223 (1:1) (гидрохлорид) CH(OH)(S) H,H 157158 Свободное основание CH(OH)(R) H,H 155156 Свободное основание H,H 194196 Свободное основание H,H 161162 (1:1) (гидрохлорид) CH(OH)(S) H,H 214216 (1:1) (гидрохлорид) H,H 242244 (1:1) (гидрохлорид) H,H 207208 Свободное основание CH(OH)(S) H,H 186187 Свободное основание CH(OH)(R) H,H 182184 Свободное основание CH(OH)(R) H,H 218220 (1:1) (гидрохлорид) - 11 - 008172 связь н,н 149150 Свободное основание CH(OH)(R) н,н 221222 (1:1) (гидрохлорид) связь Н,Н 191193 Свободное основание связь Н,Н 233235 (1:1) (гидрохлорид) связь Н,Н 213215 (1:1) (гидрохлорид) связь Н,Н 227228 (1:1) (гидрохлорид) связь Н,Н 208210 (1:1) (гидрохлорид) связь Н,Н 210211 (1:1) (гидрохлорид) связь Н,Н 224225 (1:1) (гидрохлорид) связь Н,Н 166- Свободное 167 основание связь Н,Н 190- Свободное 191 основание С(Н)(ОН) н,н 177- Свободное Вг- (рац.) 178 основание н,н 169- Свободное Br-Ph 171 основание Пример теста. Ингибирующая активность лекарственного средства по настоящему изобретению в отношении GSK3p. Могут быть использованы два различных протокола. В первом протоколе: 7,5 мкМ предварительно фосфорилированного пептида GS1 и 10 мкМ АТФ (содержащего 300000 имп./мин 33Р-АТФ) инкубировали в 25 мМ Tris-HCl, pH 7,5, 0,6 мМ дитиотрейтола, 6 мМ MgCl2, 0,6 мМ этиленгликолевой тетрауксусной кислоты (ЭГТА), 0,05 мг/мл буфера бычьего сывороточного альбумина (БСА) в течение 1 ч при комнатной температуре в присутствии GSK3p (общий реакционный объем: 100 мкл). Во втором протоколе: 4,1 мкМ предварительно фосфорилированного пептида GS1 и 42 мкМ АТФ (содержащего 260000 имп./мин 33Р-АТФ) инкубировали в 80 мM Mes-NaOH, pH 6,5, 1 мМ ацетата магния Mg, 0,5 мМ ЭГТА, 5 мМ 2-меркаптоэтанола, 0,02% Tween 20, 10% глицеролового буфера в течение 2 ч при комнатной температуре в присутствии GSK3p. Ингибиторы были растворены в ДМСО (конечная концентрация растворителя в реакционной среде, 1%). Реакцию останавливали 100 мкл раствора, приготовленного из 25 г полифосфорной кислоты (85% P2O5), 126 мл 85% Н3РO4, I-[2O до 500 мл, и затем разбавляли до 1:100 перед применением. Аликвоту ре - 12 - 008172 акционной смеси затем переносили на катионообменные фильтры Whatman P81 и промывали описанным выше раствором. Заключенную 33Р радиактивность определяли путем жидкостной сцинтилляционной спектрометрии. Фосфорилированный пептид GS-1 имеет следующую последовательность: NH2-YRRAAVPPSPSLSRHSSPHQS(P)EDEE-COOH. Ингибирующую GSK3p активность соединения по настоящему изобретению выражают в виде значения средней ингибирующей концентрации IC50, и в качестве иллюстрации диапазон IC50 соединений в вышеприведенной таблице составляет от концентрации 1 наномоль до концентрации 1 микромоль. Например, соединение № 10 таблицы демонстрирует значение IC50 0,0006 мкМ. Пример препарата. (1) Таблетки. Приведенные ниже ингредиенты были смешаны с использованием обычного способа и спрессованы с использованием обычного аппарата. Соединение примера 1 30 мг Кристаллическая целлюлоза 60 мг Кукурузный крахмал 100 мг Лактоза 200 мг Стеарат магния 4 мг (2) Мягкие капсулы. Приведенные ниже ингредиенты были смешаны с использованием обычного способа и заполнены в мягкие капсулы. Соединение примера 1 30 мг Оливковое масло 300 мг Лецитин 20 мг (3) Препараты для парентерального введения. Приведенные ниже ингредиенты были смешаны с использованием обычного способа приготовления инъекций, содержащихся в ампуле объемом 1 мл. Соединение примера 1 3 мг Хлорид натрия 4 мг Дистиллированная вода для инъекции 1 мл Промышленная применимость Соединения по настоящему изобретению обладают активностью, ингибирующей GSK3p, и полезны в качестве активного ингредиента лекарственного средства для профилактического и/или терапевтического лечения заболеваний, вызванных аномальной активностью GSK3p, и более конкретно нейродеге-неративных заболеваний. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производное дигидроспиро[циклоалкил]пиримидона, представленное формулой (I), или его соль, либо их сольват, или их гидрат где X представляет собой два атома водорода, атом серы, атом кислорода или ^^кильную группу и атом водорода; Y представляет собой связь, карбонильную группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из ^^алкильной группы, гидроксильной группы, ^^алкокси-группы, ^^пергалогенированной алкильной группы или аминогруппы; R1 представляет собой 2-, 3- или 4-пиридиновое кольцо или 2-, 4- или 5-пиримидиновое кольцо, причем кольцо возможно замещено ^^алкильной группой^^алкоксигруппой или атомом галогена; R2 представляет собой бензольное кольцо или нафталиновое кольцо, причем кольца возможно замещены заместителями в количестве от 1 до 4, выбранными из ^^алкильной группы, группы метилен-диокси, атома галогена, C1-2пергалогенированной алкильной группы, ^^галогенированной алкильной группы, гидроксильной группы, C1-4алкоксигруппы, нитро, циано, амино, C1-5моноалкиламиногруппы или C2-10диалкиламиногруппы; R3 представляет собой атом водорода, ^^кильную группу или атом галогена; - 13 - 008172 m означает от 1 до 4; n означает от 0 до 3; р означает от 0 до 2 и q означает от 0 до 2, причем р+q меньше 4. 2. Производное дигидроспиро[циклоалкил]пиримидона, или его соль, либо их сольват, или их гидрат по п.1, где R1 представляет собой незамещенную 4-пиридинильную группу или незамещенную 4-пиримидинильную группу. 3. Производное дигидроспиро[циклоалкил]пиримидона, или его соль, либо их сольват, или их гидрат по п.1 или 2, где R1 представляет собой незамещенное 4-пиридиновое кольцо или 4-пиримидиновое кольцо; и R2 представляет собой бензольное кольцо, причем кольцо возможно замещено заместителями в количестве от 1 до 4, выбранными из ^^10^^^ группы, атома галогена, гидроксильной группы или C1-2алкоксигруппы; и R3 представляет собой атом водорода; и X представляет собой два атома водорода; и Y представляет собой связь, карбонильную группу или метиленовую группу, возможно замещенную гидроксильной группой; и р равно 2 и q равно 0. 4. Производное дигидроспиро[циклоалкил]пиримидона, выбранное из группы, состоящей из 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопропан-1,2'- пиримидо [1,2-а]пиримидин]-6'( 1 'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиридин-4-ил-3',4'-дигидроспиро [циклопропан-1,2'-пиримидо [1,2-а]пи-римидин]-6'( 1 'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пирими-до [1,2-а]пиримидин]-6'( 1 'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пирими-до [1,2-а]пиримидин]-6'( 1 'Н)-она; 1'-[2-оксо-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'Н)-она; 1'-[2-оксо-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пири-мидин]-6'(1'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пири-мидин]-6'(1'Н)-она; 1'-(2-оксо-2-фенилэтил)-8'-пиримидин-4-ил-3',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пи-римидин]-6'( 1 'Н)-она; 1'-[(2S)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиримидин-4-ил-3',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пирими-дин]-6'(1'Н)-она; 1'-[(2R)-2-гидрокси-2-фенилэтил]-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиримидин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а] пирими-дин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро [циклопропан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'H)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклобутан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'Н)-она; 1'-(фенилметил)-8'-пиридин-4-ил-3',4'-дигидроспиро[циклопентан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3 ',4'-дигидроспиро [циклопентан-1,2'-пиримидо [1,2-а] пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиридин-4-ил-3 ',4-дигидроспиро [циклобутан-1,2'-пиримидо [1,2-а]пиримидин]-6'(1'Н)-она; - 14 - 008172 1'-(фенилэтил)-8'-пиридин-4-ил-3,,4,-дигидроспиро[циклопропан-1,2,-пиримидо[1,2-а]пиримидин]-6,(1,Н)-она; 1'-(фенилэтил)-8'-пиримидин-4-ил-3,,4,-дигидроспиро[циклобутан-1,2,-пиримидо[1,2-а]пиримидин]-6'(1'Н)-она; 1'-(фенилэтил)-8'-пиримидин-4-ил-3,,4,-дигидроспиро[циклопентан-1,2,-пиримидо[1,2-а]пирими-дин]-6'(1'Н)-она; 1'-(2-гидрокси-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3,,4,-дигидроспиро[циклобутан-1,2,-пири-мидо[1,2-а]пиримидин]-6'(1 'Н)-она; 1'-(2-оксо-2-(3-бромфенилэтил))-8'-пиримидин-4-ил-3,,4,-дигидроспиро[циклобутан-1,2,-пиримидо [1,2-а]пиримидин]-6'(1 'Н)-она, или его соли, либо их сольвата, или их гидрата. 5. Соединение формулы (III) где R1, R3, m, p и q являются такими, как определено для соединения формулы (I) по п.1. 6. Лекарственное средство, включающее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного дигидроспиро[циклоалкил]пиримидона, представленного формулой (I), или его солей, либо их сольвата, или их гидрата по п.1. 7. Ингибитор GSK3p (киназы 3p гликогенсинтазы), выбранный из группы производного дигидрос-пиро[циклоалкил]пиримидона, представленного формулой (I), или его солей, либо их сольвата, или их гидрата по п.1. 8. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3p. 9. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения нейродегенеративного заболевания. 10. Применение соединения по п.9, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, таупатий, сосудистой деменции; инсульта, травматических поражений; поражений сосудов головного мозга, травмы головного мозга, травмы спинного мозга; периферических нейропатий; ретинопатий или глаукомы. 11. Применение соединения по пп.1-4 для приготовления лекарственного средства для профилактического и/или терапевтического лечения инсулиннезависимого диабета; ожирения; маниакально-депрессивного заболевания; шизофрении; алопеции или видов рака. 12. Применение по п.11, где рак представляет собой рак молочной железы, немелкоклеточную карциному легких, рак щитовидной железы, Т- или В-клеточную лейкемию или опухоли, вызванные вирусами. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6 - 15 - 
|