|
Патентная документация ЕАПВ |
|
||
| Запрос: | ea000008148b*\id |
|
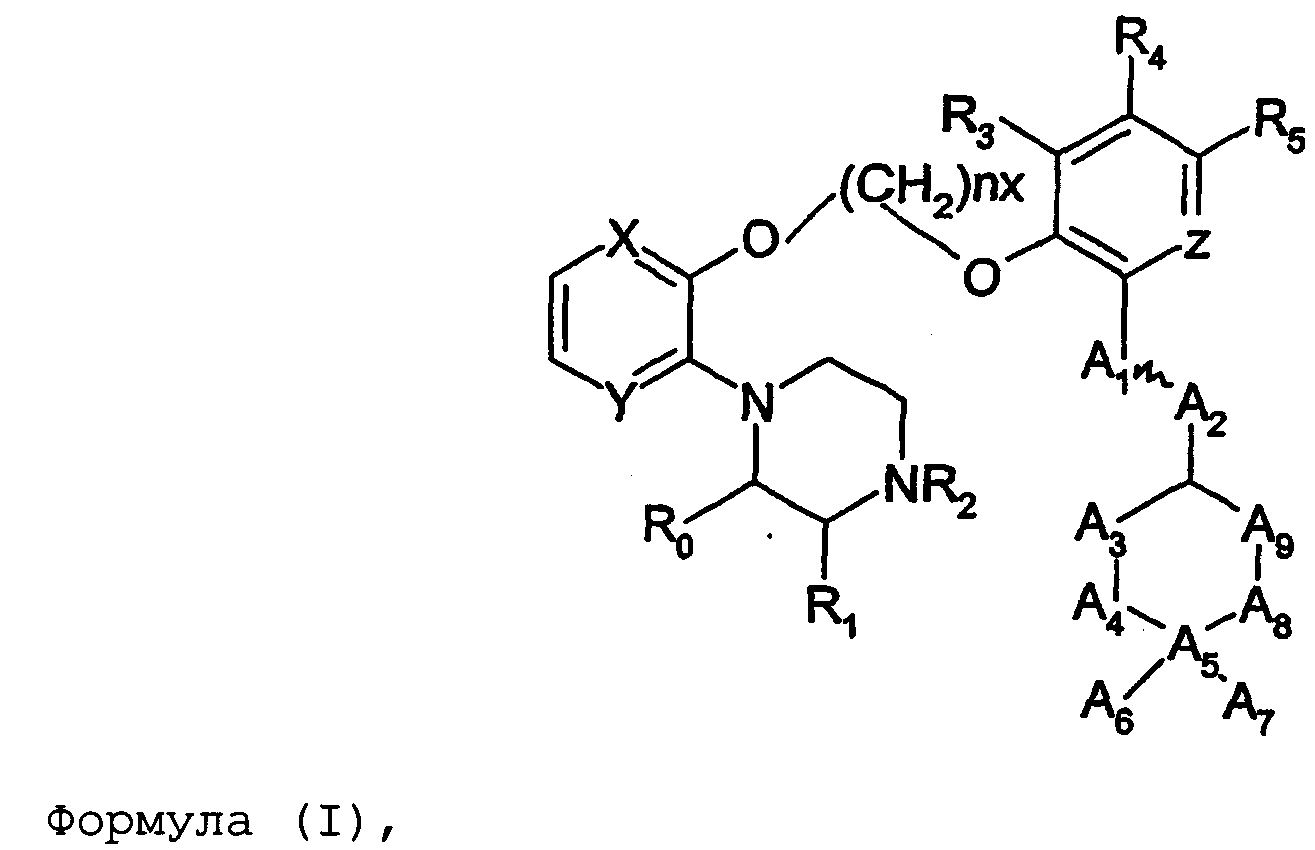
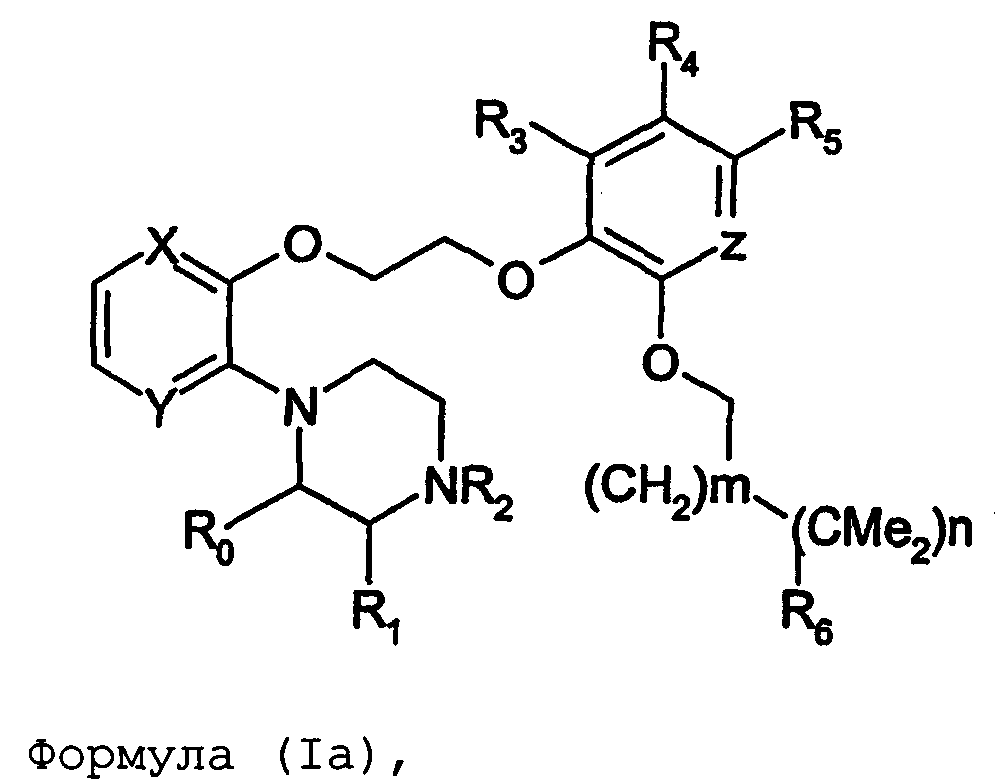
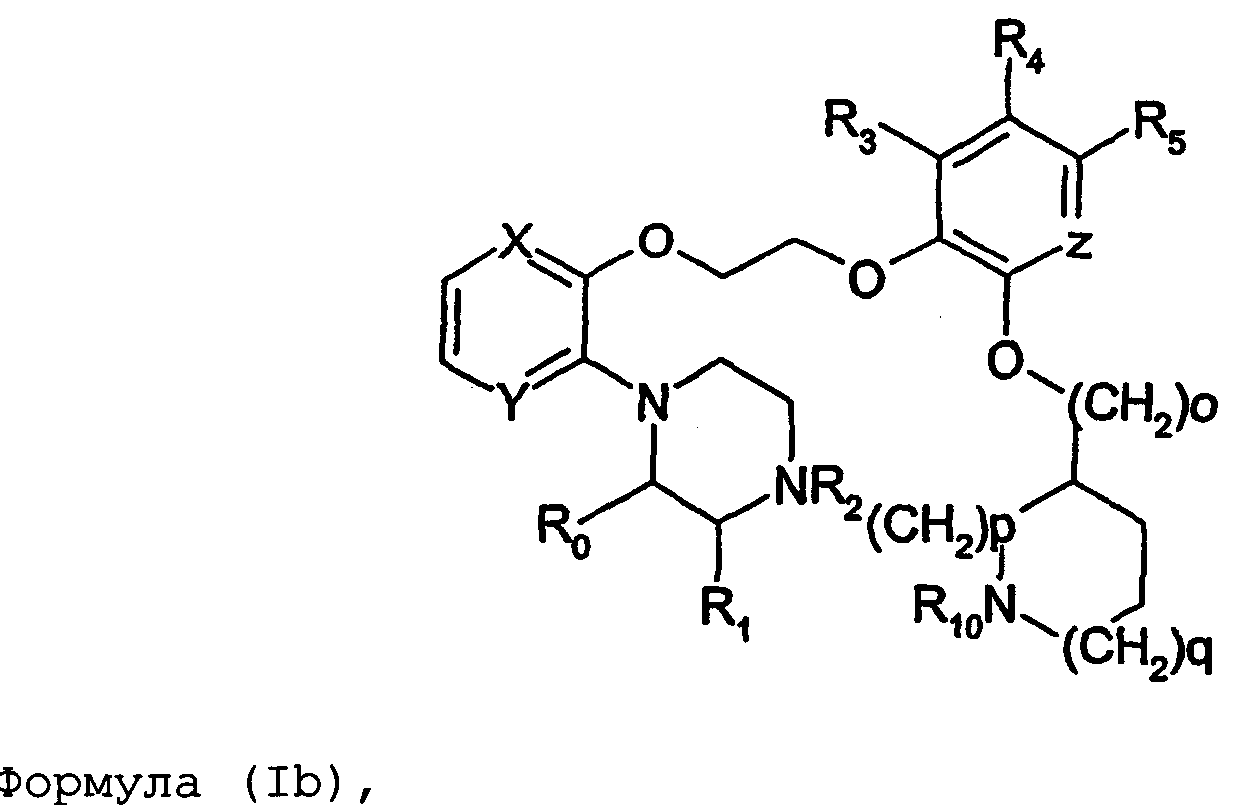
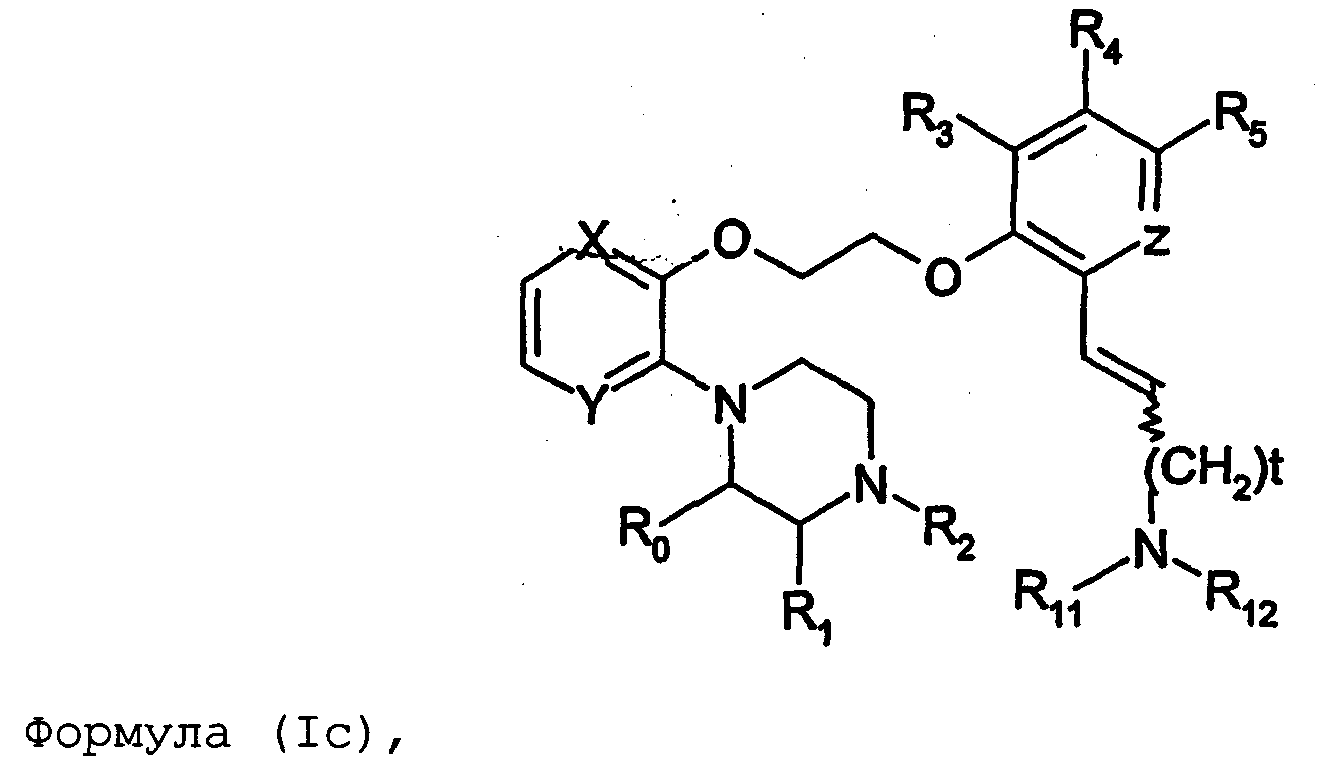
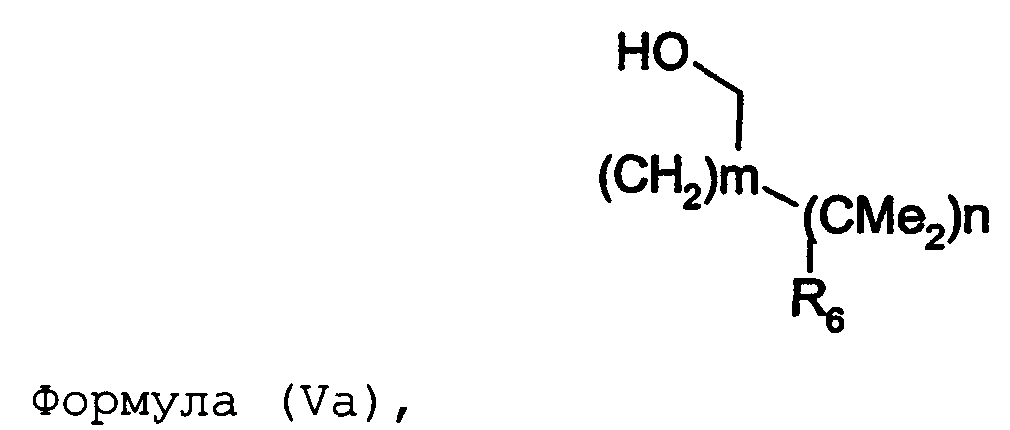
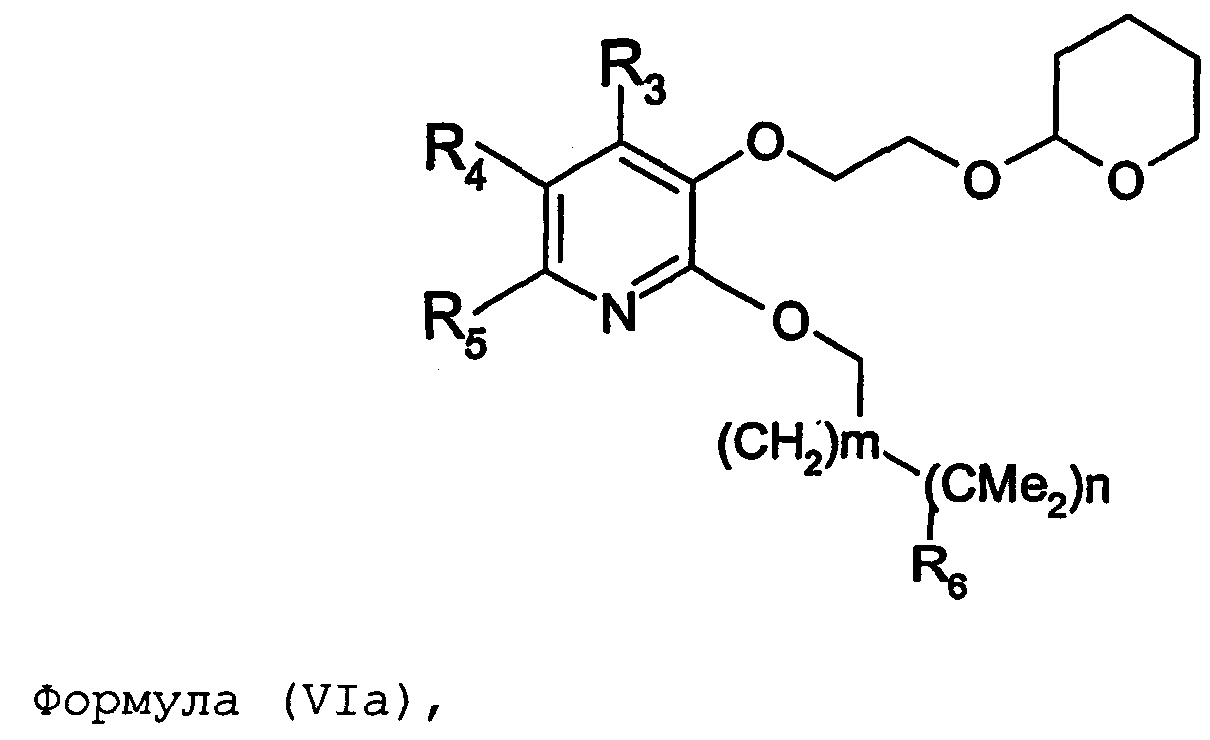
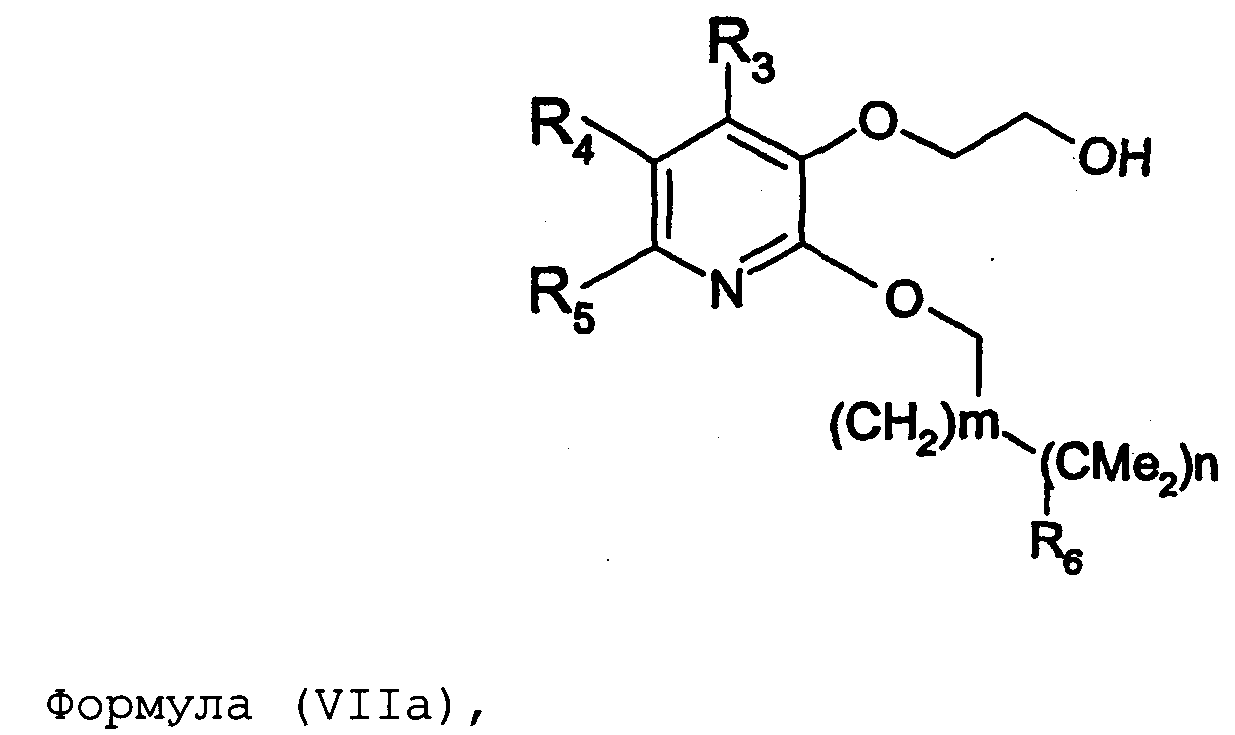
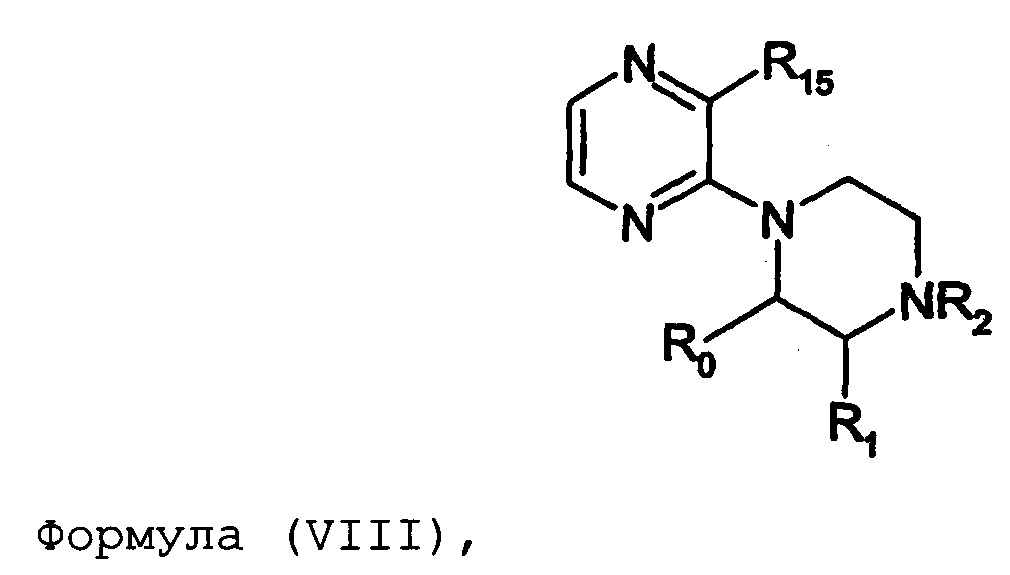
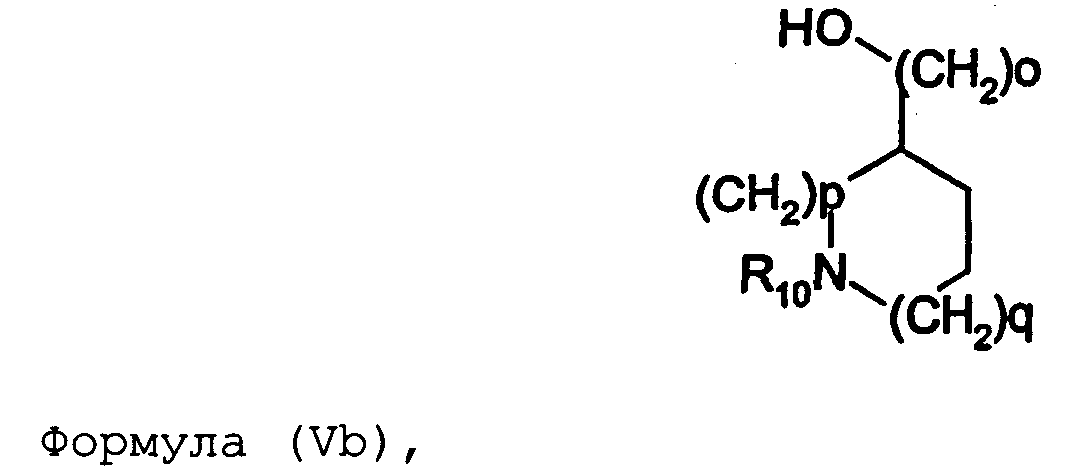
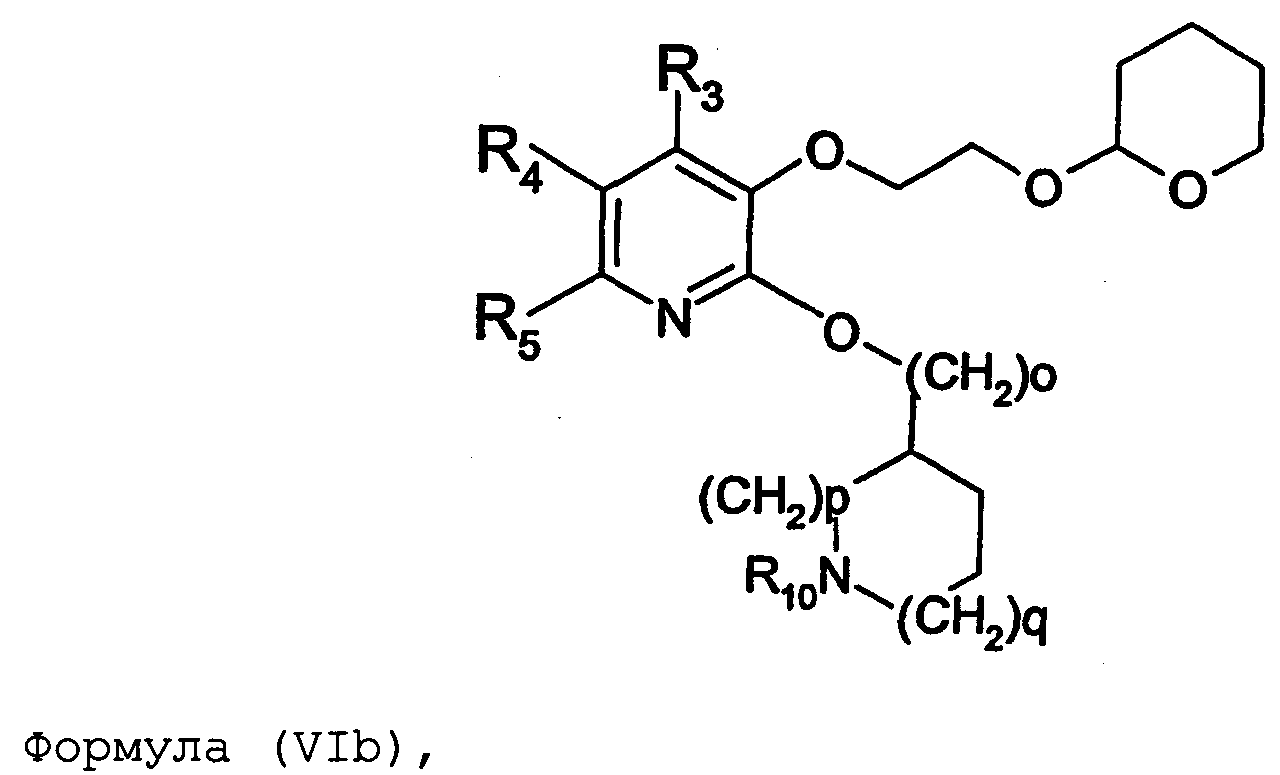
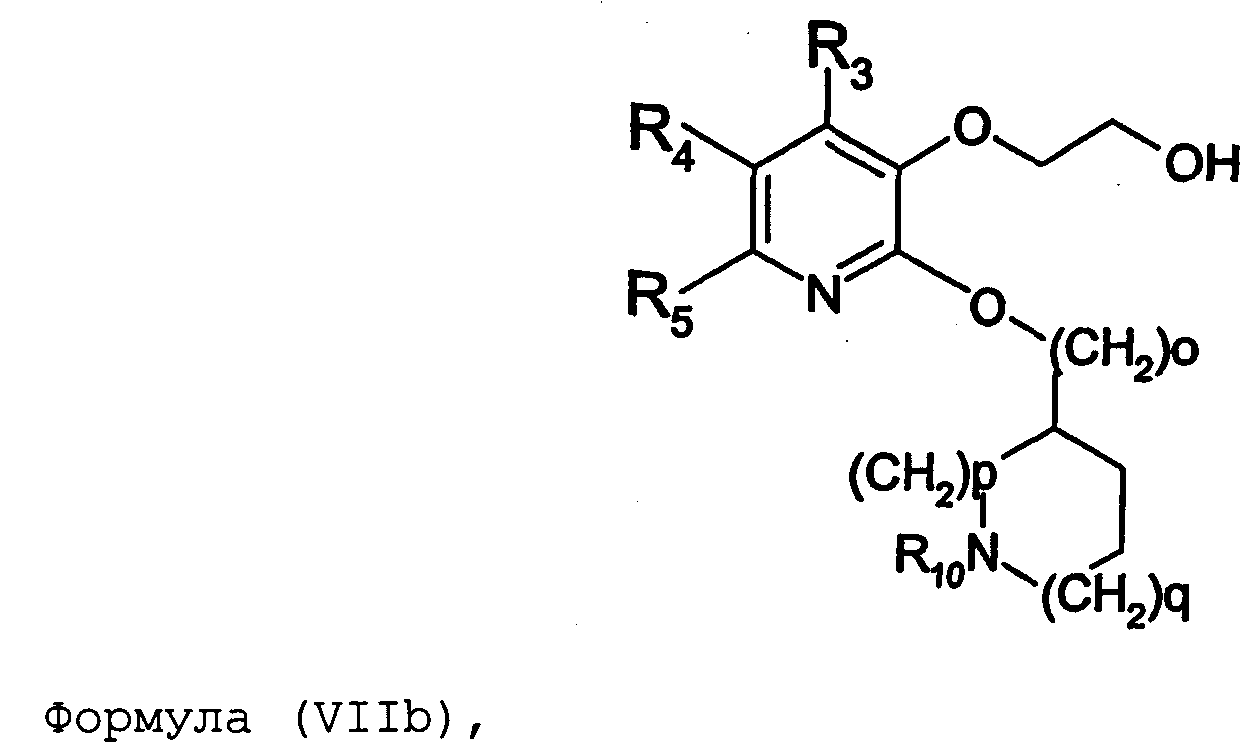
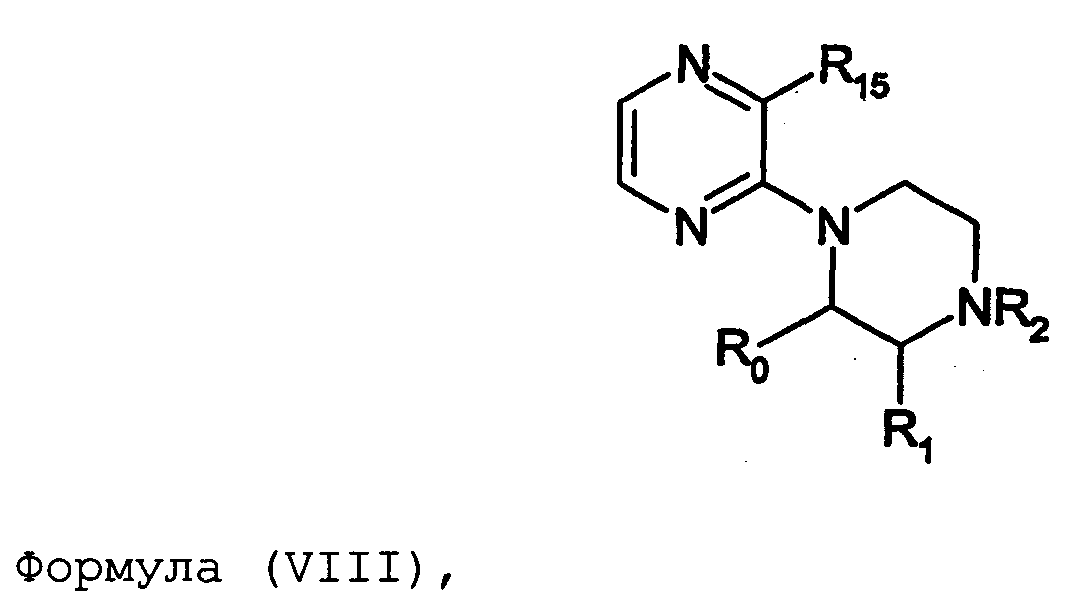
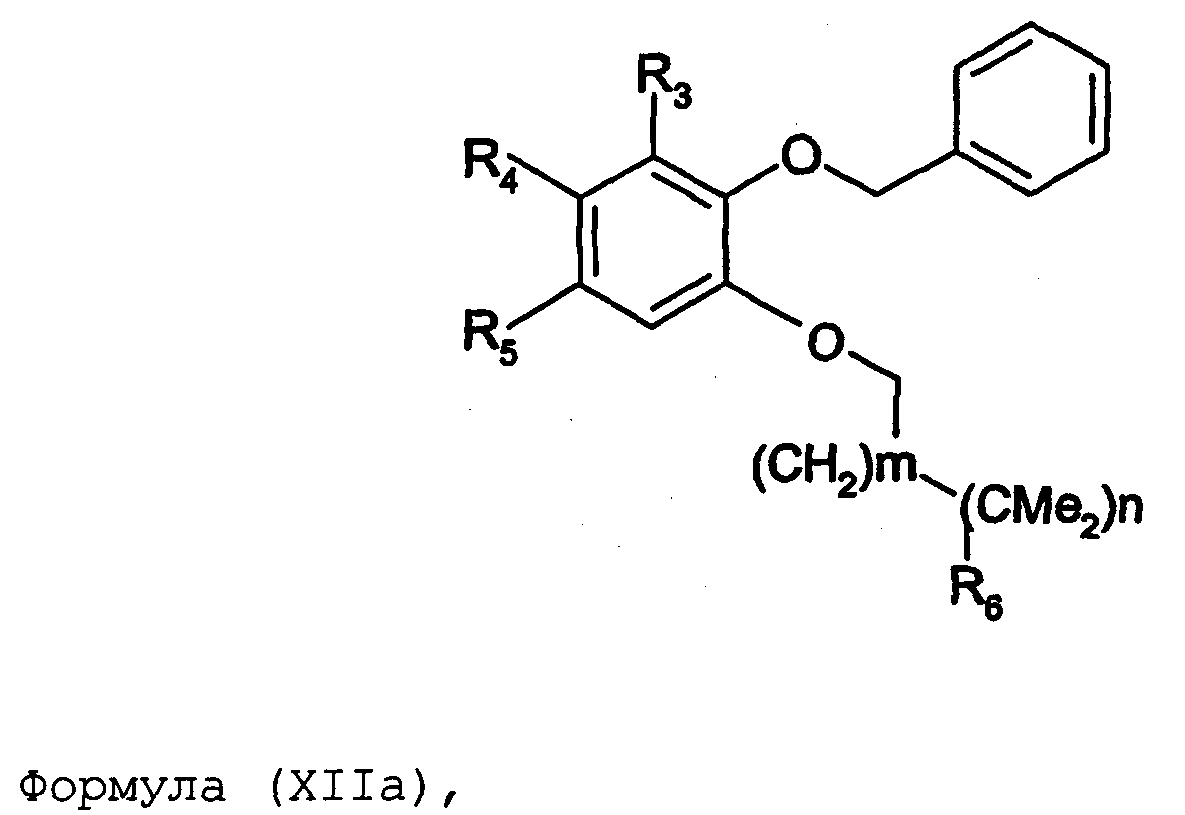
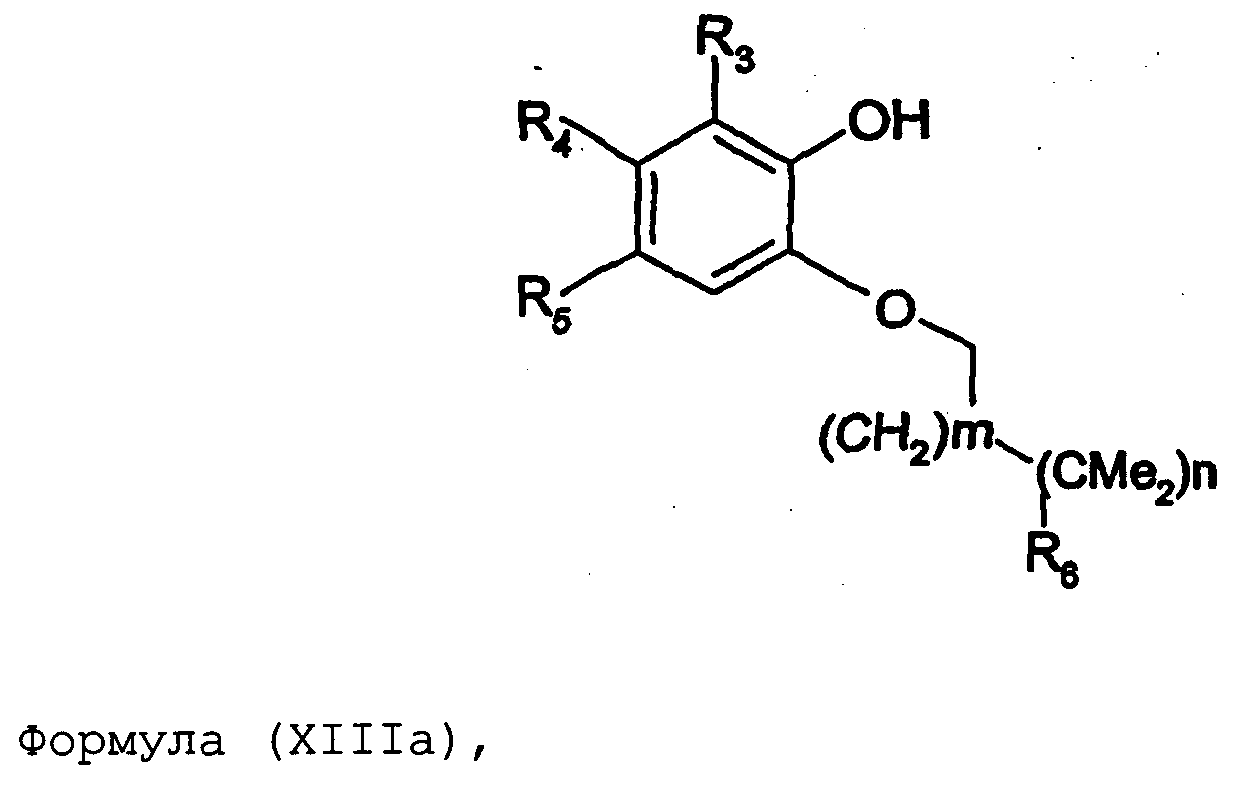
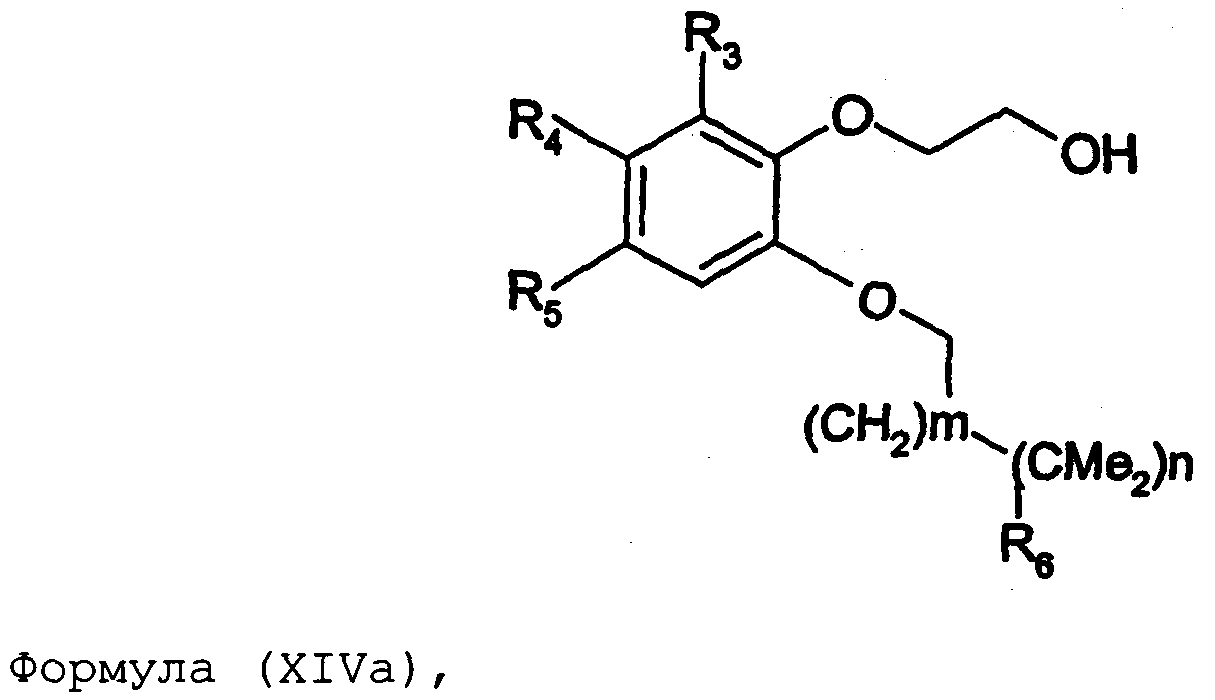
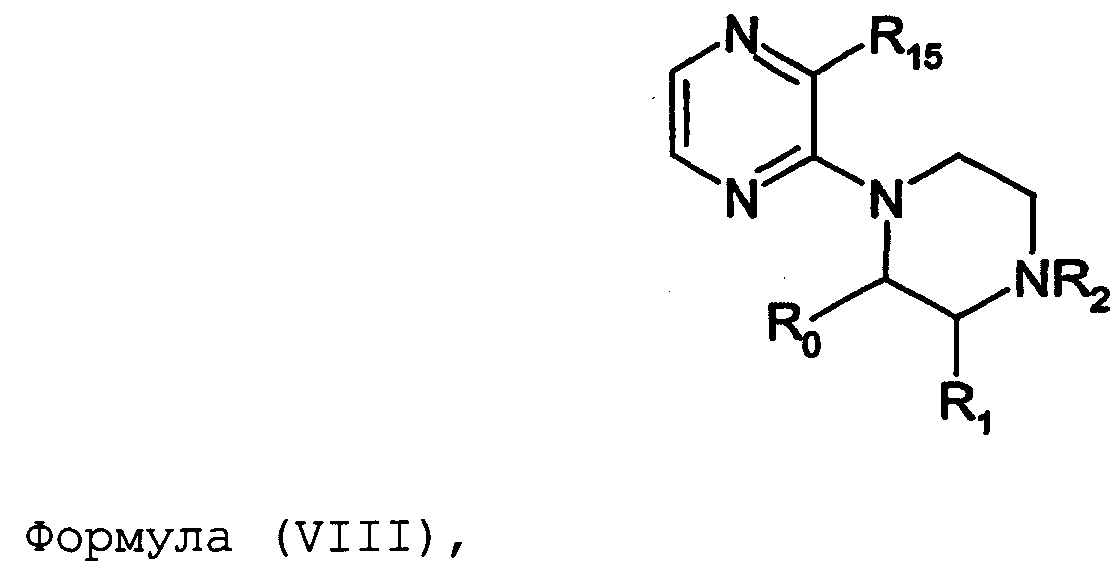
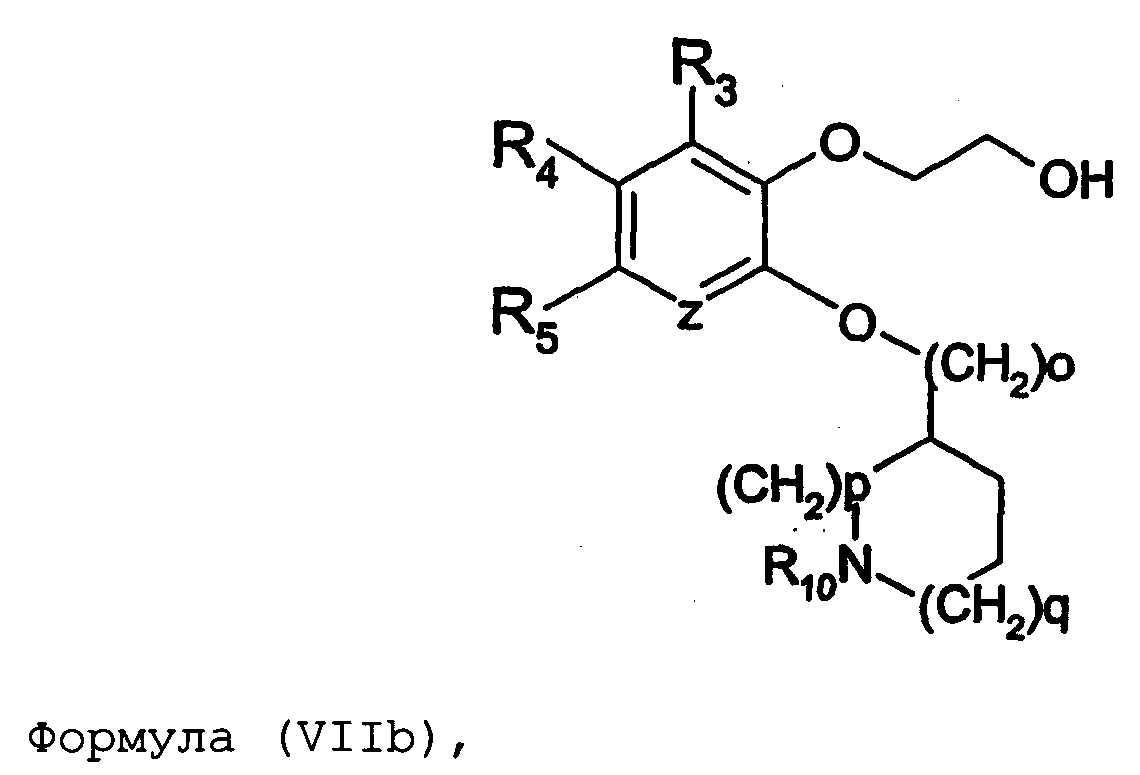
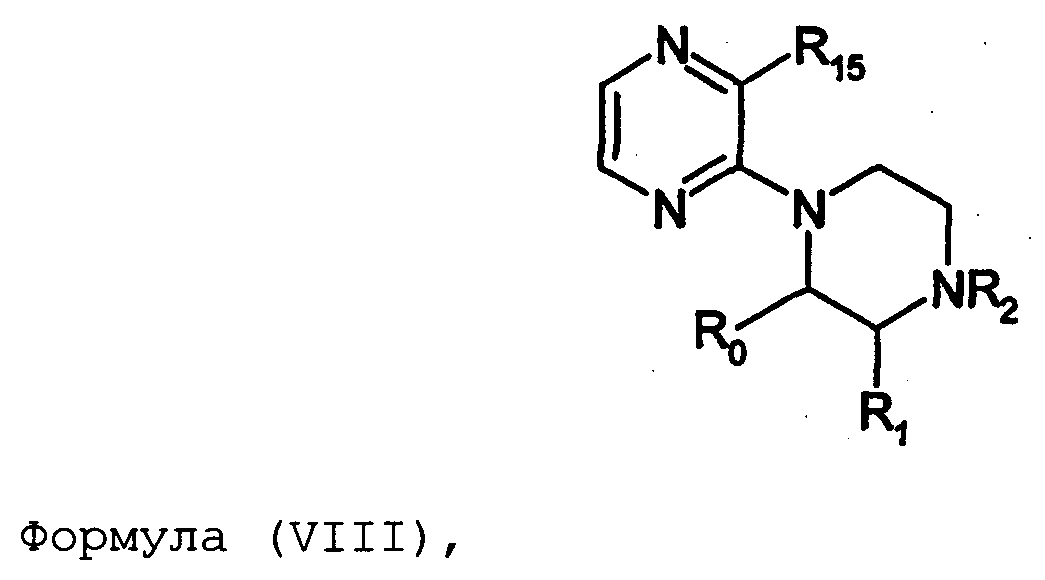
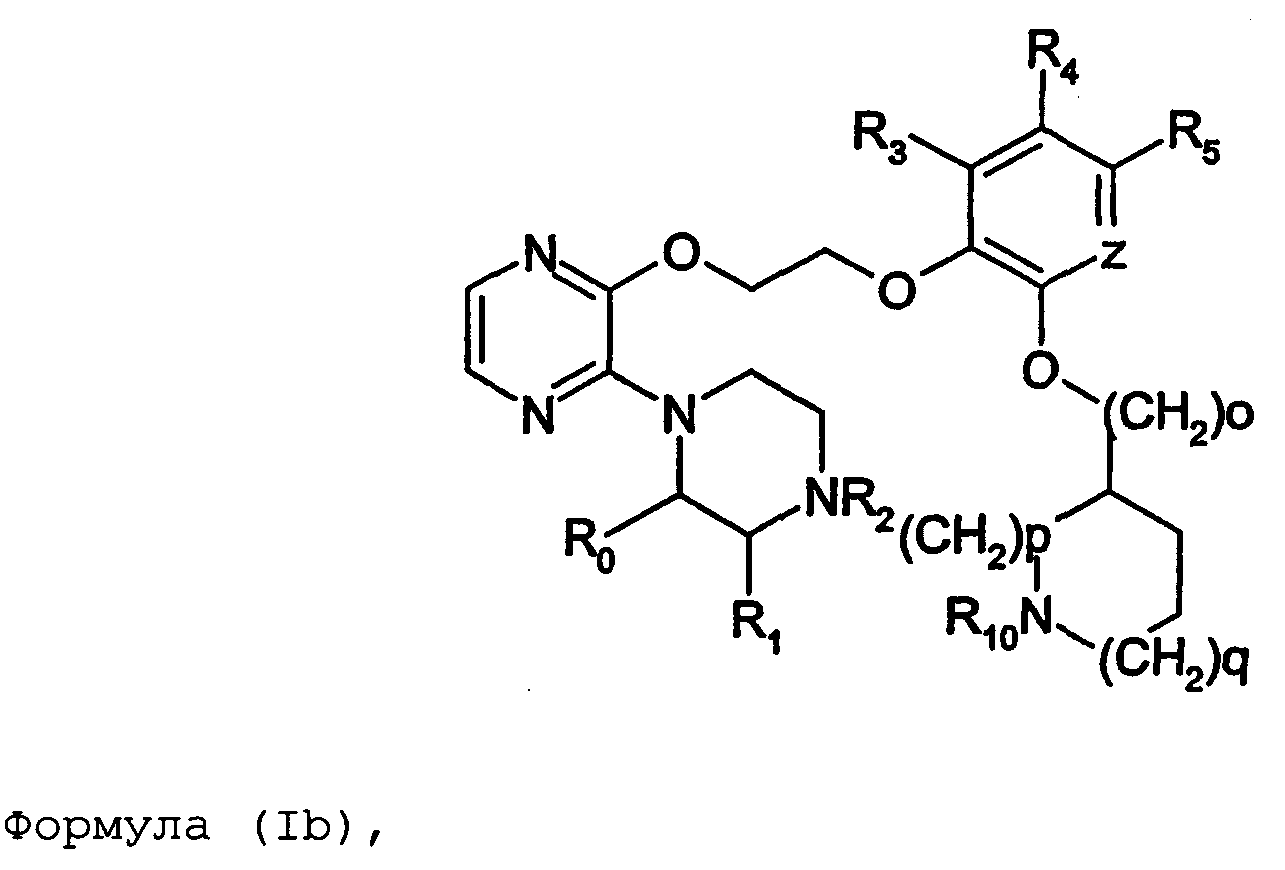
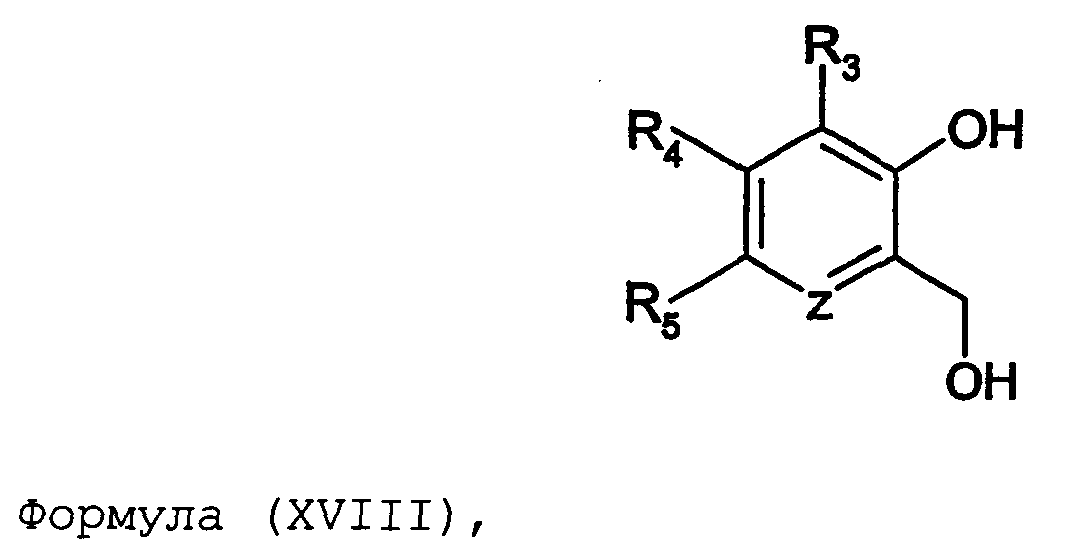
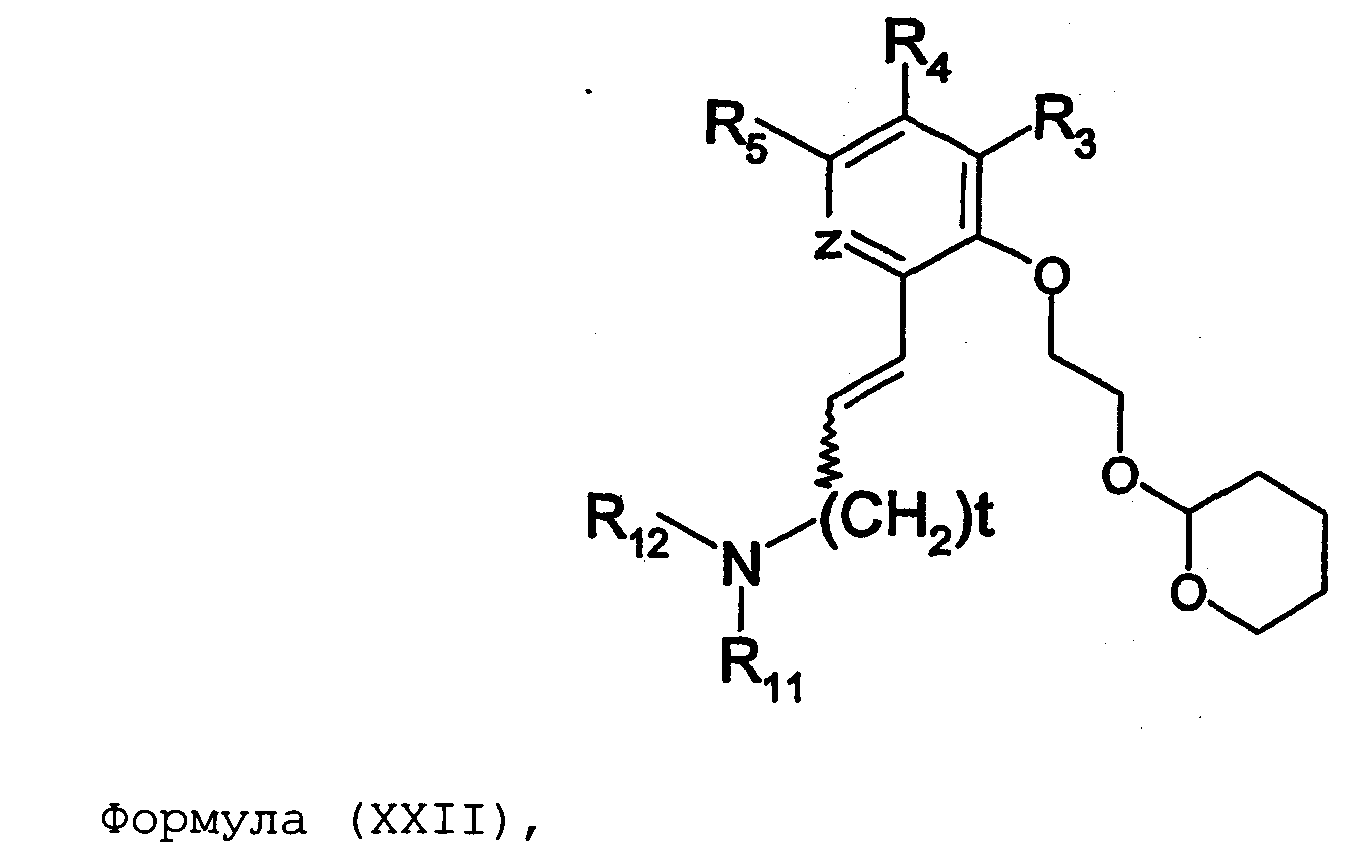
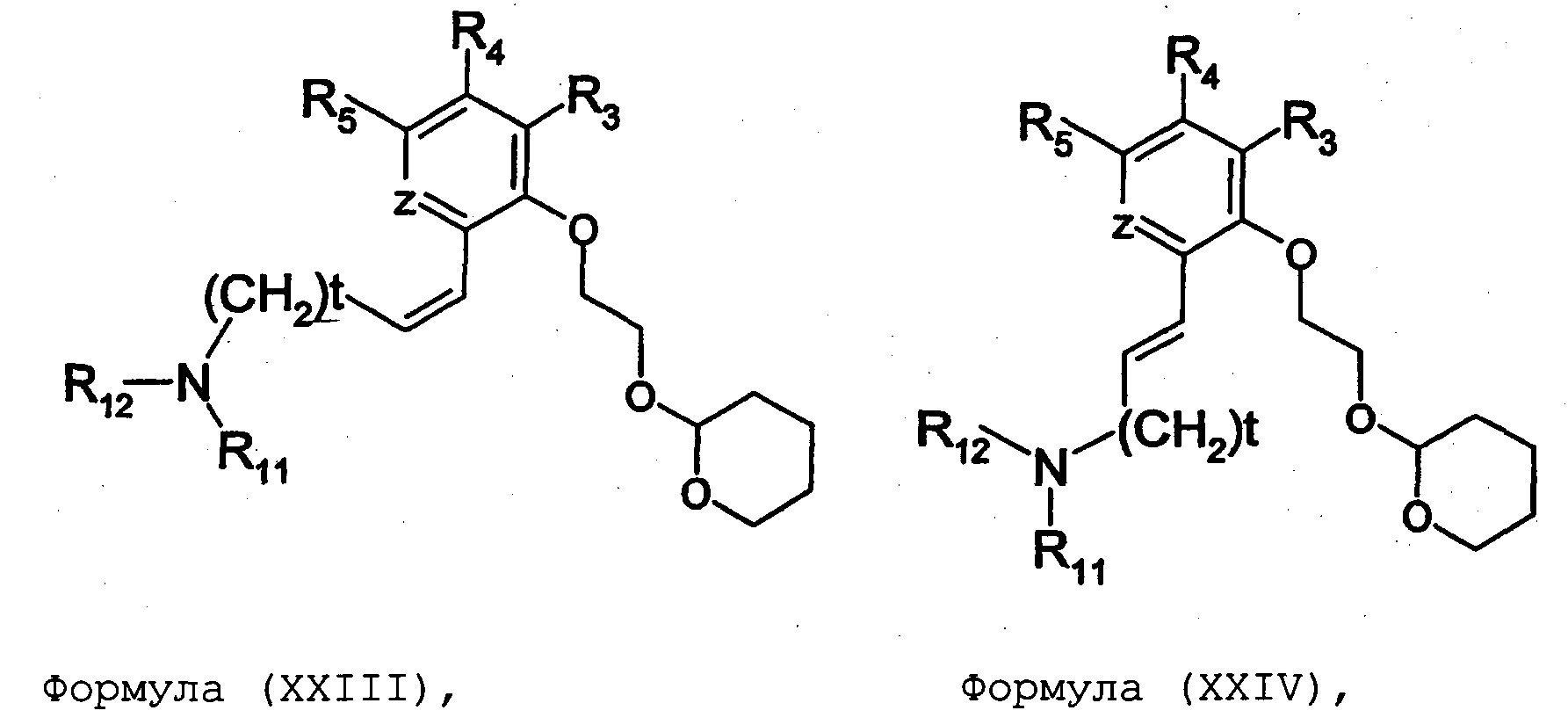
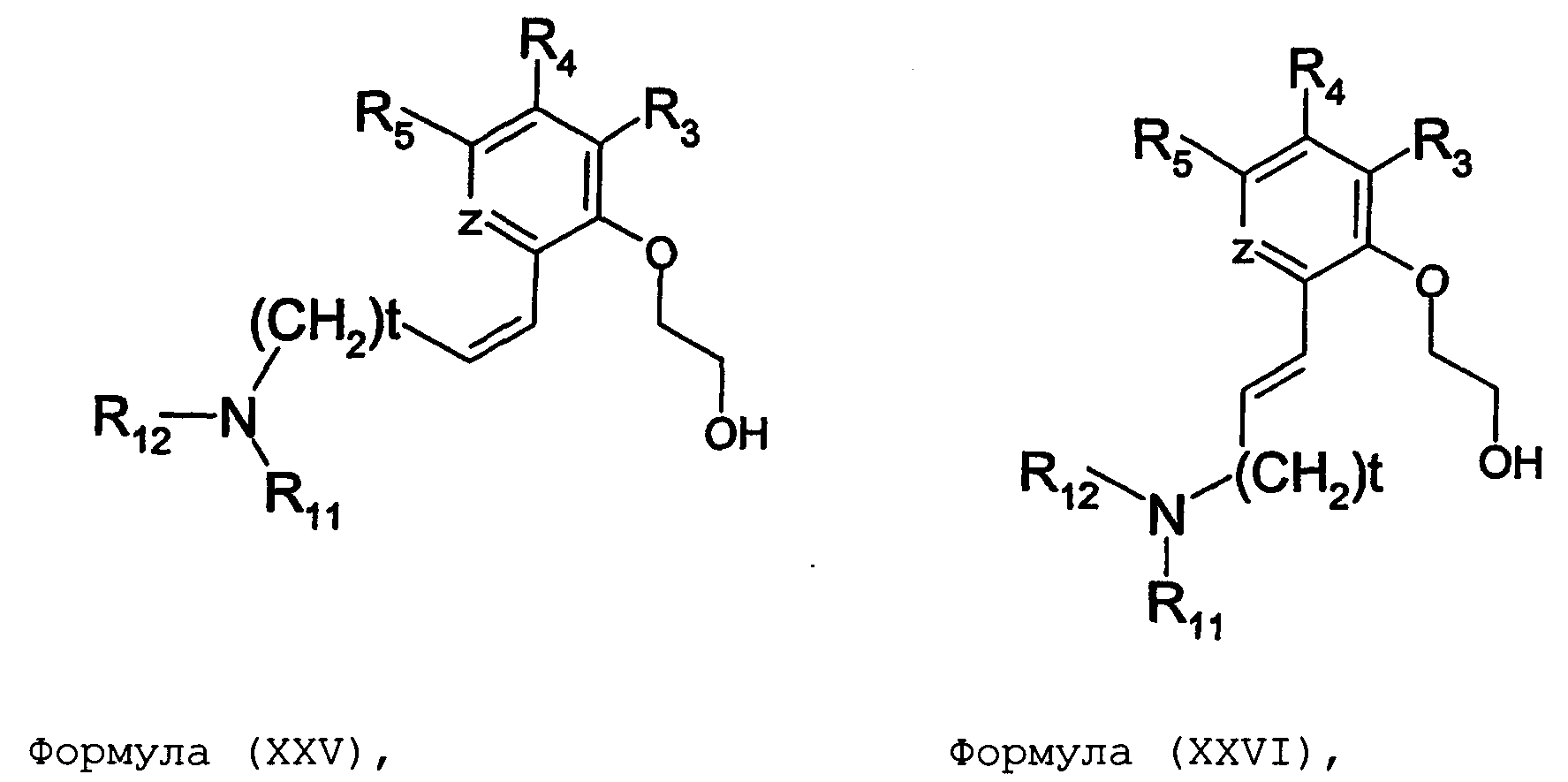
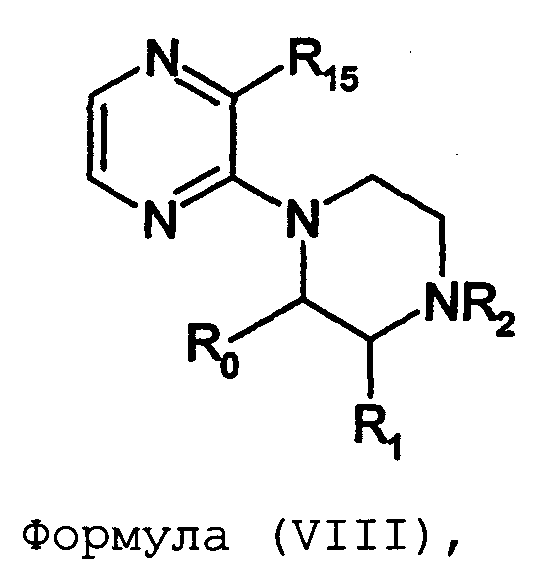
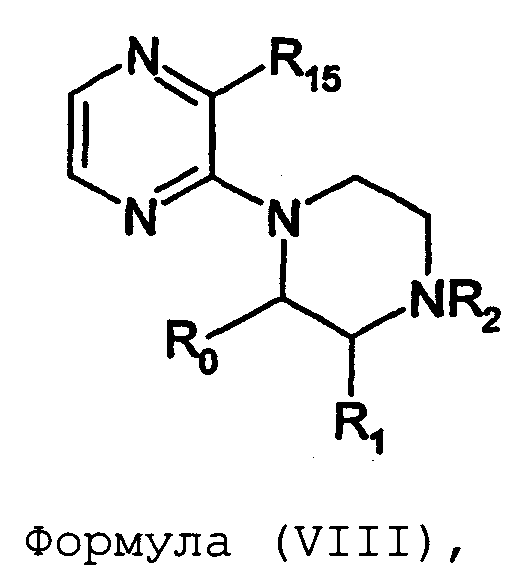
Термины запроса в документе Реферат 1. Соединение формулы (I) где nх равно 2-4, предпочтительно 2; каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 означает Н, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил или тетрагидропиран-2-ил, C 1 -C 4 -ацил или C 1 -C 4 -алкоксикарбонил; каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород; каждый из X, Y и z независимо означает СН или N; A 1 означает О, СН или СН 2 ; A 2 означает О, СН или (CH 2 ) n2 , где n 2 равно целому числу 0-2; Связь между A 1 и А 2 является простой или двойной связью; A 3 означает (СН 2 ) n3 , где n3 равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5; А 4 означает (СМе 2 ) n4 , где n4 равно целому числу 0-1; A 5 означает N или О; при условии, что когда A 5 представляет собой азот, то А 5 замещен только двумя из A 6 , А 7 и A 5 ; когда A 5 представляет собой O, то A 5 замещен только одним из A 6 , А 7 и A 8 ; каждый из A 6 и А 7 независимо означает Н, C 1 -C 4 -алкил, амино-C 2 -C 4 -алкил, N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, C 3 -C 6 -циклоалкил или вместе с A 5 образует насыщенное гетероциклическое кольцо; где насыщенное гетероциклическое кольцо является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N; A 8 означает (СН 2 ) n8 , где n8 равно целому числу 0-2; A 9 означает CH 2 ; или фармацевтически приемлемые соли, сольваты, гидраты, геометрические изомеры, таутомеры, оптические изомеры, N-оксиды и пролекарственные формы указанных соединений. 2. Соединение по п.1, где R 0 означает метил. 3. Соединение по одному из пп.1-2, где атом углерода, к которому присоединена указанная метильная группа R 0 , находится в (R)-конфигурации. 4. Соединение по п.1, где R 0 означает водород. 5. Соединение по одному из пп.1-4, где R 1 означает водород. 6. Соединение по одному из пп.1-5, где X и Y оба означают азот. 7. Соединение по одному из пп.1-6, где R 2 означает Н или метил. 8. Соединение по одному из пп.1-7, где все R 3 -R 5 означают Н. 9. Соединение по одному из пп.1-8, где каждый из A 6 и А 7 независимо означает Н, метил, изопропил, 2-этиламин или взятые вместе образуют пирролидиновое или пиперазиновое кольцо. 10. Соединение имеющее формулу (Ia) где R 0 -R 5 , X, Y и z имеют вышеуказанные значения по одному из пп.1-8, предпочтительно, где z означает N, m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, где насыщенное гетероциклическое кольцо является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил. 11. Соединение по п.10, где R 7 и R 8 выбраны из группы, включающей Н, метил, изопропил, либо указанные группы образуют вместе с атомом азота, к которому присоединены, пирролидиновый или пиперазиновый цикл. 12. Соединение по одному из пп.10 или 11, где R 9 означает 2-аминоэтил. 13. Соединение по одному из пп.10-12, где указанным соединением является N,N-диметил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2']бипиразинил-3'-илокси)этокси]пиридин-2-илокси)этил)амин; N,N-диизопропил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2']бипиразинил-3'-илокси)этокси]пиридин-2-илокси)этил)-амин; N,N-диметил-2-[(3-{2-[(3-пиперазин-1-илпиразин-2-ил)окси]этокси}пиридин-2-ил)окси]этанамин; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(2-пирролидин-1-илэтокси)пиридин-3-ил]окси}этокси)пиразин; N,N-диметил-4-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)бутан-1-амин; N-метил-N-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этил]пропан-2-амин; N,N-диметил-3-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пропан-1-амин; N,N,2-триметил-1-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пропан-2-амин; [2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этил]амин; N-метил-2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этанамин; 2-{2-[{2-[2-(диметиламино)этокси]пиридин-3-ил}окси]этокси}-3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин; 2-[2-(2-[2-(диметиламино)этокси]фенокси)этокси]-3-[(2R)-2-метилпиперазин-1-ил]пиразин; {2-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этокси]этил}амин; [6-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)гексил]амин; [5-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пентил]амин 5-({3-[2-({3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)-N,N-диметилпентан-1-амин; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(2-пиперазин-1-илэтокси)пиридин-3-ил]окси}этокси)пиразин. 14. Соединение по одному из пп.1-9, имеющее формулу (Ib) где R 0 -R 5 , X, Y и z имеют значения по одному из пп.1-8, о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил. 15. Соединение по п.14, где указанным соединением является 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[(1-метилпиперидин-4-ил)окси]пиридин-3-ил}окси)этокси]пиразинтрифторацетат; 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[2-(1-метилпирролидин-2-ил)этокси]пиридин-3-ил}окси)этокси]пиразинтрифторацета ; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(пиперидин-3-илметокси)пиридин-3-ил}окси}этокси)пиразинтрифторацетат; 2-[(2R)-2-метилпиперазин-1-ил]-3-{2-[(2-{[(2S)-1-метилпирролидин-2-ил]метокси}пиридин-3-ил)окси]этокси}пиразинтрифторацетат. 16. Соединение имеющее формулу (Ic) где R 0 -R 5 , X, Y и z имеют вышеуказанные значения, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, ориентация относительно двойной связи может быть либо цис, либо транс; каждый из R 11 и R 12 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; либо R 11 и R 12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, где насыщенное гетероциклическое кольцо, является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N. 17. Соединение по п.16, где R 11 и R 12 оба означают метил. 18. Соединение по одному из пп.16 или 17, где указанным соединением является 2-{2-[{2-[(1z}-3-(диметиламино)проп-1-енил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин; 2-{2-[{2-[(1E)-3-(диметиламино)проп-1-енил]пиридин-3ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. 19. Соединение имеющее формулу (Id) где R 0 -R 5 , X, Y и z имеют вышеуказанные значения, W означает О или CH 2 ; r равно 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, когда W означает CH 2 и, наиболее предпочтительно, когда W означает О; каждый из R 13 и R 14 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; либо R 13 и R 14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; где насыщенное гетероциклическое кольцо, является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N. 20. Соединение по п.19, где W означает О, X=N и Y=N. 21. Соединение по п.19, где r=t, W=СН 2 , X=N, Y=N, R 13 =R 11 и R 14 =R 12 ; где t, R 11 и R 12 имеют значения, указанные для формулы (Ic) по п.16. 22. Соединение по пп.19-21, где R 13 и R 14 оба означают метил. 23. Соединение по одному из пп.19-22, где указанным соединением является 2-{2-[(2-{[2-(диметиламино)этокси]метил}пиридин-3ил)окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил] пиразин или 2-{2-[{2-[3-(диметиламино)пропил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. 24. Соединение по одному из пп.1-23, для применения в терапии человека или животного. 25. Соединение по п.24, где терапия направлена на лечение вызываемого серотонином нарушения или состояния, связанного с рецептором 5-HT 2C . 26. Соединение по п.25, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 27. Применение соединения по одному из пп.1-23 при получении лекарственного средства для лечения или предупреждения вызываемого серотонином нарушения или состояния, связанного с рецептором 5-HT 2C . 28. Применение по п.27, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 29. Фармацевтическая композиция, включающая соединение по одному из пп.1-23 в качестве активного ингредиента вместе с фармацевтически приемлемым носителем. 30. Способ лечения вызываемого серотонином нарушения или состояния, в частности, связанного с рецептором 5-HT 2C , включающий введение нуждающемуся в таком лечении больному эффективного количества соединения по одному из пп.1-23. 31. Способ по п.30, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 32. Способ по одному из п.30 или 31, где больным является человек. 33. Способ по одному из п.30 или 31, где больным является животное. 34. Способ модуляции функции рецептора 5-HT 2C , включающих контактирование рецептора с эффективным стимулирующим или ингибирующим, предпочтительно стимулирующим, количеством соединения по одному из пп.1-23. 35. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (II) где X 1 выбран из F, Cl, Br и I, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) где X 1 и R 3 -R 5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, где m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, приводящее к соединению формулы (VIa) где R 3 -R 6 , m и n имеют вышеуказанные значения, с) обработку соединения формулы (VIa) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (VIIa) где R 3 -R 6 , m и n имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метилтрет-бутиловый эфир или толуол, где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ia), где X=N и Y=N: где R 0 -R 6 , m и n имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ia) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ia), где R 2 означает водород. 36. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (II) где X 1 выбран из F, Cl, Br и I, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) где X 1 и R 3 -R 5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, где о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил; приводящее к соединению формулы (VIb) где R 3 -R 5 и R 10 , о, р и q имеют вышеуказанные значения, с) обработку соединения формулы (VIb) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (VIIb) где R 3 -R 5 и R 10 , о, р и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метил-трет-бутиловый эфир или толуол, где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N: где R 0 -R 5 , R 10 , о, р и q имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ib) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R 2 означает водород. 37. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (X) где R 3 -R 5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (ХIа) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон где Х 2 означает галоген, OMs или OTs; m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, приводящее к соединению формулы (XIIа) где R 3 -R 6 , m и n имеют вышеуказанные значения; с) обработку соединения формулы (XIIа) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (ХIIIа) где R 3 -R 6 , m и n имеют вышеуказанные значения; d) взаимодействие соединения формулы (ХIIIа) с гидроксиэтилирующим агентом, таким как этиленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XIVa) где R 3 -R 6 , m и n имеют вышеуказанные значения; е) взаимодействие соединения формулы (XIVa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ia), где X=N и Y=N: где R 0 -R 6 , m и n имеют вышеуказанные значения; f) пo желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, g) если R 2 в формуле (Ia) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза получают соединение формулы (Ia), где R 2 означает водород. 38. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (X) где R 3 -R 5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (XIb) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон где Х 2 означает галоген, OMs или OTs; о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил; приводящее к соединению формулы (XIIb) где R 3 -R 5 , R 10 , о, р и q имеют вышеуказанные значения, с) обработку соединения формулы (ХIIb) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, приводящее к соединению формулы (XIIIb) где R 3 -R 5 , R 10 , о, р и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (XIIIb) с гидроксиэтилирующим агентом, таким как этиленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XIVb) R 3 -R 5 , R 1 0, о, р и q имеют вышеуказанные значения, е) взаимодействие соединения формулы (XIVb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 1 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N где R 0 -R 5 , R 10 , о, р и q имеют вышеуказанные значения, f) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, если R 2 в формуле (Ib) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R 2 означает водород. 39. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид где X 3 выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (XVI) где R 3 -R 5 , Х 3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид, где m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, приводящее к соединению формулы (XVIIа) где R 3 -R 6 , m, n и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIa) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (VIIa) где R 3 -R 6 , m, n и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид, где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ia), где X=N и Y=N где R 0 -R 6 , m, n и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ia) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ia), где R 2 означает водород. 40. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, где X 1 выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (XVI) где R 3 -R 5 , X 3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид, где о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил; приводящее к соединению формулы (XVIIb) где R 3 -R 5 и R 10 , о, р, q и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIb) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (VIIb) где R 3 -R 5 и R 10 , о, р, q и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N где R 0 -R 5 , R 10 , о, р, q и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ib) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R 2 означает водород. 41. Способ получения соединения формулы (Ic) по одному из пп.16-18, указанный способ включает: а) взаимодействие соединения формулы (XVIII) где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород; z означает СН или N, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) где R 3 -R 5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XVI) в альдегидную функциональную группу в присутствии диметилсульфоксида и оксалилхлорида в дихлорметане, приводящее к соединению формулы (XX) где R 3 -R 5 и z имеют вышеуказанные значения, с) взаимодействие соединения формулы (XX) с соединением формулы (XXI) в присутствии основания, такого как трет-бутилат калия в смеси растворителей, состоящей из тетрагидрофурана и третбутанола где t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1 и каждый из R 11 и R 12 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 11 и R 12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXII) где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; ориентация относительно двойной связи может быть либо цис, либо транс; d) разделение с помощью препаративной ЖХВР и выделение цис- и транс-изомеров соединения формулы (XXII), приводящее к получению индивидуального цис-изомера формулы (XXIII) и индивидуального транс-изомера формулы (XXIV) где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; е) обработку соединений формулы (XXIII) и (XXIV), соответственно, водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединения формулы (XXV) и (XXVI), соответственно; где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; f) взаимодействие соединений формулы (XXV) и (XXVI) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид: где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединениям формулы (XXVII) и (XXVIII) где R 0 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; где соединения формул (XXVII) и (XXVIII) являются изомерами соединения формулы (Ic), где X=N и Y=N; d) если R 2 в формуле (Ic) после стадии f) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ic), где R 2 означает водород. 42. Способ получения соединения формулы (Id) по одному из пп.19 и 21-23, указанный способ включает: а) обработку соединения формулы (XXII) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (XXIX) где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, z означает СН или N, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1; и каждый из R 11 и R 12 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 11 и R 12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; b) обработку соединения формулы (XXIX) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXX) где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; с) взаимодействие соединения формулы (XXX) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид или диоксан где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (XXXI) где R 0 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; где формула (XXXI) соответствует формуле (Id), в которой W=СН 2 , r=t, X=N, Y=N, R 13 =R 11 и R 14 =R 12 , d) если R 2 в формуле (Id) после стадии с) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R 2 означает водород. 43. Способ получения соединения формулы (Id) по одному из пп.19, 20, 22 или 23, указанный способ включает: а) взаимодействие соединения формулы (XVIII) где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород; z означает СН или N, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) где R 3 -R 5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XIX) в подходящую удаляемую группу, например, путем обработки метансульфоновым ангидридом в присутствии триэтиламина в дихлорметане, приводящее к соединению формулы (XXXII) где R 3 -R 5 и z имеют вышеуказанные значения; Y 2 означает галоген, OMs или OTs; с) взаимодействие соединения формулы (XXXII) с соединением формулы (XXXIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как диоксан где W означает О; r равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 2; каждый из R 13 и R 14 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 13 и R 14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXXIV) где r, z, W, R 3 -R 5 и R 13 и R 14 имеют вышеуказанные значения; d) обработку соединения формулы (XXXIV) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXXV) где r, z, W, R 3 -R 5 и R 13 и R 14 имеют вышеуказанные значения; е) взаимодействие соединения формулы (XXXV) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 2 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (XXXVI) где R 0 -R 8 , R 13 , R 14 , r, W и z имеют вышеуказанные значения; где формула (XXXVI) отвечает формуле (Id), в которой X=N и Y=N, f) если R 2 в формуле (Id) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R 2 означает водород. 44. Способ лечения нарушения или состояния, включающий введение нуждающемуся в таком лечении больному эффективного количества соединения по одному из пп.1-23, где нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 45. Применение соединения по одному из пп.1-23 при получении лекарственного средства для лечения или предупреждения нарушения или заболевания, такого как нарушения памяти, такие как болезнь Альцгеймера; шизофрения; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическая зависимость и токсикомания; половые дисфункции, такие как эректильная дисфункция; эпилепсия; глаукома; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение.
Полный текст патента (57) Реферат / Формула: где nх равно 2-4, предпочтительно 2; каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 означает Н, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил или тетрагидропиран-2-ил, C 1 -C 4 -ацил или C 1 -C 4 -алкоксикарбонил; каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород; каждый из X, Y и z независимо означает СН или N; A 1 означает О, СН или СН 2 ; A 2 означает О, СН или (CH 2 ) n2 , где n 2 равно целому числу 0-2; Связь между A 1 и А 2 является простой или двойной связью; A 3 означает (СН 2 ) n3 , где n3 равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5; А 4 означает (СМе 2 ) n4 , где n4 равно целому числу 0-1; A 5 означает N или О; при условии, что когда A 5 представляет собой азот, то А 5 замещен только двумя из A 6 , А 7 и A 5 ; когда A 5 представляет собой O, то A 5 замещен только одним из A 6 , А 7 и A 8 ; каждый из A 6 и А 7 независимо означает Н, C 1 -C 4 -алкил, амино-C 2 -C 4 -алкил, N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, C 3 -C 6 -циклоалкил или вместе с A 5 образует насыщенное гетероциклическое кольцо; где насыщенное гетероциклическое кольцо является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N; A 8 означает (СН 2 ) n8 , где n8 равно целому числу 0-2; A 9 означает CH 2 ; или фармацевтически приемлемые соли, сольваты, гидраты, геометрические изомеры, таутомеры, оптические изомеры, N-оксиды и пролекарственные формы указанных соединений. 2. Соединение по п.1, где R 0 означает метил. 3. Соединение по одному из пп.1-2, где атом углерода, к которому присоединена указанная метильная группа R 0 , находится в (R)-конфигурации. 4. Соединение по п.1, где R 0 означает водород. 5. Соединение по одному из пп.1-4, где R 1 означает водород. 6. Соединение по одному из пп.1-5, где X и Y оба означают азот. 7. Соединение по одному из пп.1-6, где R 2 означает Н или метил. 8. Соединение по одному из пп.1-7, где все R 3 -R 5 означают Н. 9. Соединение по одному из пп.1-8, где каждый из A 6 и А 7 независимо означает Н, метил, изопропил, 2-этиламин или взятые вместе образуют пирролидиновое или пиперазиновое кольцо. 10. Соединение имеющее формулу (Ia) где R 0 -R 5 , X, Y и z имеют вышеуказанные значения по одному из пп.1-8, предпочтительно, где z означает N, m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, где насыщенное гетероциклическое кольцо является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил. 11. Соединение по п.10, где R 7 и R 8 выбраны из группы, включающей Н, метил, изопропил, либо указанные группы образуют вместе с атомом азота, к которому присоединены, пирролидиновый или пиперазиновый цикл. 12. Соединение по одному из пп.10 или 11, где R 9 означает 2-аминоэтил. 13. Соединение по одному из пп.10-12, где указанным соединением является N,N-диметил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2']бипиразинил-3'-илокси)этокси]пиридин-2-илокси)этил)амин; N,N-диизопропил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2']бипиразинил-3'-илокси)этокси]пиридин-2-илокси)этил)-амин; N,N-диметил-2-[(3-{2-[(3-пиперазин-1-илпиразин-2-ил)окси]этокси}пиридин-2-ил)окси]этанамин; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(2-пирролидин-1-илэтокси)пиридин-3-ил]окси}этокси)пиразин; N,N-диметил-4-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)бутан-1-амин; N-метил-N-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этил]пропан-2-амин; N,N-диметил-3-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пропан-1-амин; N,N,2-триметил-1-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пропан-2-амин; [2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этил]амин; N-метил-2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этанамин; 2-{2-[{2-[2-(диметиламино)этокси]пиридин-3-ил}окси]этокси}-3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин; 2-[2-(2-[2-(диметиламино)этокси]фенокси)этокси]-3-[(2R)-2-метилпиперазин-1-ил]пиразин; {2-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этокси]этил}амин; [6-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)гексил]амин; [5-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пентил]амин 5-({3-[2-({3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)-N,N-диметилпентан-1-амин; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(2-пиперазин-1-илэтокси)пиридин-3-ил]окси}этокси)пиразин. 14. Соединение по одному из пп.1-9, имеющее формулу (Ib) где R 0 -R 5 , X, Y и z имеют значения по одному из пп.1-8, о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил. 15. Соединение по п.14, где указанным соединением является 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[(1-метилпиперидин-4-ил)окси]пиридин-3-ил}окси)этокси]пиразинтрифторацетат; 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[2-(1-метилпирролидин-2-ил)этокси]пиридин-3-ил}окси)этокси]пиразинтрифторацета ; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(пиперидин-3-илметокси)пиридин-3-ил}окси}этокси)пиразинтрифторацетат; 2-[(2R)-2-метилпиперазин-1-ил]-3-{2-[(2-{[(2S)-1-метилпирролидин-2-ил]метокси}пиридин-3-ил)окси]этокси}пиразинтрифторацетат. 16. Соединение имеющее формулу (Ic) где R 0 -R 5 , X, Y и z имеют вышеуказанные значения, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, ориентация относительно двойной связи может быть либо цис, либо транс; каждый из R 11 и R 12 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; либо R 11 и R 12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, где насыщенное гетероциклическое кольцо, является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N. 17. Соединение по п.16, где R 11 и R 12 оба означают метил. 18. Соединение по одному из пп.16 или 17, где указанным соединением является 2-{2-[{2-[(1z}-3-(диметиламино)проп-1-енил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин; 2-{2-[{2-[(1E)-3-(диметиламино)проп-1-енил]пиридин-3ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. 19. Соединение имеющее формулу (Id) где R 0 -R 5 , X, Y и z имеют вышеуказанные значения, W означает О или CH 2 ; r равно 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, когда W означает CH 2 и, наиболее предпочтительно, когда W означает О; каждый из R 13 и R 14 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; либо R 13 и R 14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; где насыщенное гетероциклическое кольцо, является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N. 20. Соединение по п.19, где W означает О, X=N и Y=N. 21. Соединение по п.19, где r=t, W=СН 2 , X=N, Y=N, R 13 =R 11 и R 14 =R 12 ; где t, R 11 и R 12 имеют значения, указанные для формулы (Ic) по п.16. 22. Соединение по пп.19-21, где R 13 и R 14 оба означают метил. 23. Соединение по одному из пп.19-22, где указанным соединением является 2-{2-[(2-{[2-(диметиламино)этокси]метил}пиридин-3ил)окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил] пиразин или 2-{2-[{2-[3-(диметиламино)пропил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. 24. Соединение по одному из пп.1-23, для применения в терапии человека или животного. 25. Соединение по п.24, где терапия направлена на лечение вызываемого серотонином нарушения или состояния, связанного с рецептором 5-HT 2C . 26. Соединение по п.25, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 27. Применение соединения по одному из пп.1-23 при получении лекарственного средства для лечения или предупреждения вызываемого серотонином нарушения или состояния, связанного с рецептором 5-HT 2C . 28. Применение по п.27, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 29. Фармацевтическая композиция, включающая соединение по одному из пп.1-23 в качестве активного ингредиента вместе с фармацевтически приемлемым носителем. 30. Способ лечения вызываемого серотонином нарушения или состояния, в частности, связанного с рецептором 5-HT 2C , включающий введение нуждающемуся в таком лечении больному эффективного количества соединения по одному из пп.1-23. 31. Способ по п.30, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 32. Способ по одному из п.30 или 31, где больным является человек. 33. Способ по одному из п.30 или 31, где больным является животное. 34. Способ модуляции функции рецептора 5-HT 2C , включающих контактирование рецептора с эффективным стимулирующим или ингибирующим, предпочтительно стимулирующим, количеством соединения по одному из пп.1-23. 35. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (II) где X 1 выбран из F, Cl, Br и I, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) где X 1 и R 3 -R 5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, где m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, приводящее к соединению формулы (VIa) где R 3 -R 6 , m и n имеют вышеуказанные значения, с) обработку соединения формулы (VIa) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (VIIa) где R 3 -R 6 , m и n имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метилтрет-бутиловый эфир или толуол, где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ia), где X=N и Y=N: где R 0 -R 6 , m и n имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ia) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ia), где R 2 означает водород. 36. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (II) где X 1 выбран из F, Cl, Br и I, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) где X 1 и R 3 -R 5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, где о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил; приводящее к соединению формулы (VIb) где R 3 -R 5 и R 10 , о, р и q имеют вышеуказанные значения, с) обработку соединения формулы (VIb) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (VIIb) где R 3 -R 5 и R 10 , о, р и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метил-трет-бутиловый эфир или толуол, где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N: где R 0 -R 5 , R 10 , о, р и q имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ib) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R 2 означает водород. 37. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (X) где R 3 -R 5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (ХIа) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон где Х 2 означает галоген, OMs или OTs; m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, приводящее к соединению формулы (XIIа) где R 3 -R 6 , m и n имеют вышеуказанные значения; с) обработку соединения формулы (XIIа) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (ХIIIа) где R 3 -R 6 , m и n имеют вышеуказанные значения; d) взаимодействие соединения формулы (ХIIIа) с гидроксиэтилирующим агентом, таким как этиленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XIVa) где R 3 -R 6 , m и n имеют вышеуказанные значения; е) взаимодействие соединения формулы (XIVa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ia), где X=N и Y=N: где R 0 -R 6 , m и n имеют вышеуказанные значения; f) пo желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, g) если R 2 в формуле (Ia) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза получают соединение формулы (Ia), где R 2 означает водород. 38. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (X) где R 3 -R 5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (XIb) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон где Х 2 означает галоген, OMs или OTs; о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил; приводящее к соединению формулы (XIIb) где R 3 -R 5 , R 10 , о, р и q имеют вышеуказанные значения, с) обработку соединения формулы (ХIIb) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, приводящее к соединению формулы (XIIIb) где R 3 -R 5 , R 10 , о, р и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (XIIIb) с гидроксиэтилирующим агентом, таким как этиленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XIVb) R 3 -R 5 , R 1 0, о, р и q имеют вышеуказанные значения, е) взаимодействие соединения формулы (XIVb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 1 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N где R 0 -R 5 , R 10 , о, р и q имеют вышеуказанные значения, f) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, если R 2 в формуле (Ib) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R 2 означает водород. 39. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид где X 3 выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (XVI) где R 3 -R 5 , Х 3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид, где m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R 6 означает NR 7 R 8 или OR 9 , где каждый из R 7 и R 8 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 7 и R 8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R 9 означает амино-C 2 -C 4 -алкил или N,N-ди-C 1 -C 4 -алкиламино-C 2 -C 4 -алкил, приводящее к соединению формулы (XVIIа) где R 3 -R 6 , m, n и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIa) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (VIIa) где R 3 -R 6 , m, n и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид, где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ia), где X=N и Y=N где R 0 -R 6 , m, n и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ia) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ia), где R 2 означает водород. 40. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, где X 1 выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, приводящее к соединению формулы (XVI) где R 3 -R 5 , X 3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид, где о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R 10 означает Н или C 1 -C 4 -алкил, предпочтительно Н или метил; приводящее к соединению формулы (XVIIb) где R 3 -R 5 и R 10 , о, р, q и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIb) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (VIIb) где R 3 -R 5 и R 10 , о, р, q и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N где R 0 -R 5 , R 10 , о, р, q и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R 2 в формуле (Ib) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R 2 означает водород. 41. Способ получения соединения формулы (Ic) по одному из пп.16-18, указанный способ включает: а) взаимодействие соединения формулы (XVIII) где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород; z означает СН или N, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) где R 3 -R 5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XVI) в альдегидную функциональную группу в присутствии диметилсульфоксида и оксалилхлорида в дихлорметане, приводящее к соединению формулы (XX) где R 3 -R 5 и z имеют вышеуказанные значения, с) взаимодействие соединения формулы (XX) с соединением формулы (XXI) в присутствии основания, такого как трет-бутилат калия в смеси растворителей, состоящей из тетрагидрофурана и третбутанола где t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1 и каждый из R 11 и R 12 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 11 и R 12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXII) где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; ориентация относительно двойной связи может быть либо цис, либо транс; d) разделение с помощью препаративной ЖХВР и выделение цис- и транс-изомеров соединения формулы (XXII), приводящее к получению индивидуального цис-изомера формулы (XXIII) и индивидуального транс-изомера формулы (XXIV) где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; е) обработку соединений формулы (XXIII) и (XXIV), соответственно, водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединения формулы (XXV) и (XXVI), соответственно; где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; f) взаимодействие соединений формулы (XXV) и (XXVI) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид: где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединениям формулы (XXVII) и (XXVIII) где R 0 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; где соединения формул (XXVII) и (XXVIII) являются изомерами соединения формулы (Ic), где X=N и Y=N; d) если R 2 в формуле (Ic) после стадии f) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ic), где R 2 означает водород. 42. Способ получения соединения формулы (Id) по одному из пп.19 и 21-23, указанный способ включает: а) обработку соединения формулы (XXII) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (XXIX) где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород, z означает СН или N, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1; и каждый из R 11 и R 12 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 11 и R 12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; b) обработку соединения формулы (XXIX) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXX) где R 3 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; с) взаимодействие соединения формулы (XXX) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид или диоксан где каждый из R 0 и R 1 независимо означает Н или СН 3 ; R 2 выбран из группы, включающей C 1 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (XXXI) где R 0 -R 5 , R 11 , R 12 , t и z имеют вышеуказанные значения; где формула (XXXI) соответствует формуле (Id), в которой W=СН 2 , r=t, X=N, Y=N, R 13 =R 11 и R 14 =R 12 , d) если R 2 в формуле (Id) после стадии с) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R 2 означает водород. 43. Способ получения соединения формулы (Id) по одному из пп.19, 20, 22 или 23, указанный способ включает: а) взаимодействие соединения формулы (XVIII) где каждый из R 3 -R 5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R 3 -R 5 означает водород; z означает СН или N, с соединением формулы (III) где Y 1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) где R 3 -R 5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XIX) в подходящую удаляемую группу, например, путем обработки метансульфоновым ангидридом в присутствии триэтиламина в дихлорметане, приводящее к соединению формулы (XXXII) где R 3 -R 5 и z имеют вышеуказанные значения; Y 2 означает галоген, OMs или OTs; с) взаимодействие соединения формулы (XXXII) с соединением формулы (XXXIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как диоксан где W означает О; r равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 2; каждый из R 13 и R 14 независимо означает Н или линейный или разветвленный C 1 -C 4 -алкил; или R 13 и R 14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXXIV) где r, z, W, R 3 -R 5 и R 13 и R 14 имеют вышеуказанные значения; d) обработку соединения формулы (XXXIV) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXXV) где r, z, W, R 3 -R 5 и R 13 и R 14 имеют вышеуказанные значения; е) взаимодействие соединения формулы (XXXV) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как N,N-диметилформамид где каждый из R 0 и R 1 независимо означает Н или CH 3 ; R 2 выбран из группы, включающей C 2 -C 4 -алкоксикарбонил, бензил, тритил, C 1 -C 4 -алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C 1 -C 4 -ацил, R 15 означает галоген, такой как хлор, приводящее к соединению формулы (XXXVI) где R 0 -R 8 , R 13 , R 14 , r, W и z имеют вышеуказанные значения; где формула (XXXVI) отвечает формуле (Id), в которой X=N и Y=N, f) если R 2 в формуле (Id) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R 2 означает водород. 44. Способ лечения нарушения или состояния, включающий введение нуждающемуся в таком лечении больному эффективного количества соединения по одному из пп.1-23, где нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 45. Применение соединения по одному из пп.1-23 при получении лекарственного средства для лечения или предупреждения нарушения или заболевания, такого как нарушения памяти, такие как болезнь Альцгеймера; шизофрения; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическая зависимость и токсикомания; половые дисфункции, такие как эректильная дисфункция; эпилепсия; глаукома; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение.
008148 Родственные заявки По данной заявке испрашивается приоритет по заявке на патент Швеции 0201881-0, поданной 19 июня 2002 г., заявке на патент Швеции 0202516-1, поданной 26 августа 2002 г., заявке на предварительный патент США 60/406119, поданной 26 августа 2002 г., и заявке на предварительный патент США 60/416701, поданной 7 октября 2002 г., содержания которых включены здесь в качестве ссылки. Область изобретения Настоящее изобретение касается новых соединений, фармацевтических композиций, содержащих эти соединения, способов их получения, а также применения соединений для получения лекарственных средств, оказывающих, в частности, действие на центральную нервную систему. Предпосылки изобретения На многие нарушения и состояния центральной нервной системы оказывают влияния адренергиче-ская, допаминергическая и серотонинергическая нейромедиаторные системы. Например, серотонин вовлечен в ряд нарушений и состояний, возникающих в центральной нервной системе. Ряд фармакологических и генетических экспериментов, касающихся серотониновых рецепторов, убедительно доказывает вовлеченность подтипа рецептора 5-НТ2С в регуляцию потребления пищи (см., например, Obes. Res. 1995. 3, Suppl. 4, 449S-462S, Diabetes, Obesity and Metabolism 1999, 1, 207-214 и Drugs Future 2001, 26, 383-393). Подтип рецептора 5-HN2C воспроизводится и экспрессируется гипоталамическими структурами, связанными с регуляцией аппетита. Показано, что агонист рецептора 5-НТ2С м-хлорфенилпиперазин (mCPP), отдающий некоторое предпочтение рецептору 5-НТ^, снижает потребление пищи у мышей, экспрессирующих нормальный рецептор 5-НТ^, тогда как соединение не проявляет активности по отношению к мышам, экспрессирующим мутированную неактивную форму рецептора (Nature 1995, 374, 542-546). Согласно недавнему клиническому исследованию слабое, но устойчивое снижение массы тела наблюдается после 2-недельной обработки больных ожирением с помощью mCPP (Psychopharma-cology 1997, 133, 309-312). Недавно установлено, что ряд производных пирроло[3,2,1-у]хинолина является агонистами рецептора 5-НТ2 & проявляющими большую избирательность в отношении указанного рецептора, чем в отношении рецептора (Isaac M., et al., Bioorg. Med. Chem. Lett. 2000, 10, 919921). Отмечено, что соединения дают возможность нового подхода к лечению ожирения и эпилепсии. Сообщается также, на основании клинических исследований, о снижении массы тела под действием других "серотонинергических" средств (см., например, IDrugs 1998, 1, 456-470). Например, ингибитор обратного захвата 5-НТ флуоксетин и деблокирующий 5-НТ агент/ингибитор обратного захвата 5-НТ дексфенфлурамин обнаруживают способность к снижению массы в контролируемых исследованиях. Однако доступные в настоящее время лекарственные средства, усиливающие серотонинергическую передачу, видимо, оказывают только сдерживающее и, в некоторых случаях, преходящее действие на массу тела. Предполагается также, что подтип рецептора 5-HT2C вовлечен в нарушения ЦНС, такие как депрессия и состояние тревоги (Ехр. Opin. Invest. Drugs 1998. 7, 1587-1599; IDrugs. 1999,2, 109-120). Кроме того, предполагается, что подтип рецептора 5-HT2C вовлечен в заболевания мочевого пузыря, такие как недержание мочи (IDrugs, 1999, 2, 109-120). Соединения, обладающие избирательным действием в отношении рецептора 5-HT2C, могут также оказаться терапевтически эффективными в лечении нарушений, подобным указанным выше. Конечно, избирательность также снижает потенциальную возможность по отношению к другим серотониновым рецепторам. Описание имеющихся источников информации В US-A-3253989 описано применение mCPP в качестве анорексигенного средства. В ЕР-А1-863136 описаны производные азетидина и пирролидина, являющиеся избирательными агонистами рецептора 5-НТ^, обладающими антидепрессивной активностью, которые могут быть использованы для лечения или предупреждения связанных с серотонином заболеваний, включающих нарушения приема пищи и состояние тревоги. В ЕР-А-657426 описаны трициклические производные пиррола, обладающие активностью по отношению к рецептору 5-HT2C, которые могут быть использованы для лечения нарушений приема пищи. В ЕР-А-655440 описаны 1-аминоэтилиндолы, обладающие активностью по отношению к рецептору 5-HT2C, которые могут быть использованы для лечения нарушений приема пищи. В ЕР-А-572863 описаны пиразиноиндолы, обладающие активностью по отношению к рецептору 5-HT2C, которые могут быть использованы для лечения нарушений приема пищи. В J. Med. Chem. 1978, 21, 536-542 и US-A-4081542 описан ряд пиперазинилпиразинов, обладающих центральной серотонин-миметической активностью. В частности, US-A-4081542 описывает такие соединения в качестве анорексигенных средств. В J. Med. Chem. 1981, 24, 93-101 описан ряд пиперазинилхиноксалинов с центральной серотонин-миметической активностью. В WO 00/12475 описаны производные индолина как лиганды рецептора 5-НТ2Б и/или 5-HT2C, главным образом, для лечения ожирения. В WO 00/12510 описаны пирролоиндолы, пиридоиндолы и азепиноиндолы в качестве агонистов ре - 1 - 008148 цептора 5-HT2C, в частности, для лечения ожирения. В WO 00/12482 описаны производные индазола в качестве избирательных лигандов прямого действия для рецептора 5-HT2C, предпочтительно агонистов рецептора 5-HT2C, в частности, для применения в качестве средств против ожирения. В WO 00/12502 описаны пирролохинолины в качестве агонистов рецептора 5-HT2C, в частности, для применения в качестве средств против ожирения. В GB-B-1457005 описаны производные 1-пиперазинил-2-[2-(фенил)этенил]хиноксалина, обладающие противовоспалительной активностью. В Chem. Pharm. Bull. 1993, 41(10) 1832-1841 описаны антагонисты 5-HT3, включая 2-(4-метил-1-пиперазинил)-4-феноксихиноксалин. В GB-B-1440722 описаны соединения 2-(1'-пиперазинил)хиноксалина, обладающие фармацевтической противодепрессивной активностью. В WO 96/11920 описаны ЦНС-активные пиридинилкарбамидные производные. В WO 95/01976 описаны производные индолина, действующие как антагонисты 5-HT2C, которые могут использоваться для лечения расстройств ЦНС. В WO 97/14689 описаны арилпиперазиновые производные циклического амина, являющиеся избирательными антагонистами рецептора 5-HT1D. В WO 98/42692 описаны пиперазины, производные циклических аминов, являющиеся избирательными антагонистами рецепторов человека 5-HT1A, 5-HT1D и 5-HT1B. В GB-B-1465946 описаны замещенные пиридазинил-, пиримидинил-, пиразинил- и пиридил- производные, активные в качестве агентов, блокирующих в-рецептор. В ЕР-А-711757 описаны производные [3-(4-фенилпиперазин-1-ил)пропиламино]пиридина, пиримидина и бензола в качестве а-адреноблокирующих средств. В WO 99/03833 описаны производные арилпиперазина, являющиеся антагонистами 5-HT2 и агони-стами рецептора 5-HT1A, и которые могут использоваться в качестве средств для лечения или предупреждения психоневрозов. В WO 96/02525 описаны полученные из арилпиперазина производные пиперазида, обладающие антагонистической активностью в отношении рецептора 5-НТ. В WO 99/58490 описаны арилгидронафталиналканамины, способные частично или полностью блокировать серотонинергический рецепторы 5-HT2C в организме. В WO 00/35922 описаны 2, 3, 4, 4а-тетрагидро-1H-пиразино[1,2-а]хиноксалин-5(6H)оны в качестве агонистов 5-НТ2С, которые могут быть использованы для лечения ожирения. В WO 00/44737 описаны аминоалкилбензофураны в качестве антагонистов 5-HT2C, которые могут быть использованы для лечения ожирения. Кроме того, описаны соединения, являющиеся агонистами рецептора 5-HT2C, например индазолил-пропиламины, такие как описаны в WO 00/12481; индазолы, такие как описаны в WO 00/17170; пипера-зинилпиразины, такие как описаны в WO 00/76984, WO 02/40456 и WO 02/40457; гетероциклические конденсированные у-карболины, такие как описаны в WO 00/77001, WO 00/77002 и WO 00/77010; бензо-фурилпиперазины, такие как описаны в WO 01/09111 и WO 01/09123; бензофураны, такие как описаны в WO 01/09122; бензотиофены, такие как описаны в 01/09126; аминоалкилиндазолы, такие как описаны в WO 98/30548; индолы, такие как описаны в WO 01/12603; индолины, такие как описаны в WO 01/12602 и WO 02/44152; пиразино(аза)индолы, такие как описаны в WO 00/44753; диазациклопента[а]индены, такие как описаны в ЕР 1132389; производные пиперазина, такие как описаны в WO 02/10169; хиноксали-ноны, такие как описаны в США 6372745, и трициклические пирролы или пиразолы, такие как описаны в WO 98/56768. В WO 98/33504 описано новое медицинское применение 1-[6-хлор-5-(трифторметил)-2-пиридинил]пиперазина, в частности, для нового способа лечения недержания мочи. В WO 02/36596 описаны циклоалкил[Ъ][1,4]диазепино[6,7-Ы]индолы в качестве агонистов серото-нинового рецептора 5-HT2C, которые могут быть применены для лечения ожирения. В WO 03/00666 описаны [1,2']бипиразиниловые лиганды рецептора 5-НТ2, в частности, лиганды рецептора 5-НТ2С, предназначенные для лечения половой дисфункции. В WO 03/00663 описаны пиперазинилпиримидины в качестве лигандов рецептора 5-НТ2, в частности, лигандов рецептора 5-HT2C, предназначенные для лечения половых расстройств. В WO 02/51844 описаны конденсированные циклоалкильные производные индола и их применение в качестве лигандов рецептора 5-НТ2Ь и 5-HT2C. В WO 02/42304 описаны циклопента[Ъ][1,4]диазепино[6,7,1-Ы]индолы в качестве избирательных агонистов рецептора 5-HT2C. В WO 02/36596 описаны диазепинокарбазолы и родственные им соединения в качестве агонистов серотонинового рецептора 5-HT2C. В WO 02/48124 описаны производные пиперазина в качестве агонистов рецептора 5-HT2C, которые могут быть применены, например, при ожирении. - 2 - 008148 В WO 01/66548 описаны производные азаиндолила в качестве лигандов рецептора 5-НТ2Ь и 5-HT2C, преимущественно агонистов рецептора 5-HT2C, для применения в терапии, в особенности, для применения в качестве средств против ожирения. В WO 02/072584 описаны тетрагидропиразиноиндолы в качестве лигандов рецептора 5-НТ2Ь и 5-HT2C, преимущественно, агонисты рецептора 5-HT2C, для применения в терапии, в особенности, для применения в качестве средств против ожирения. В WO 00/76984 и WO 02/40457 описаны производные арилпиперазина, связывающие рецептор 5-HT2C (агонисты и антагонисты), которые могут использоваться для лечения связанных с серотонином нарушений. Однако избирательность в отношении рецептора 5-HT2C соединений по настоящему изобретению оказалась неожиданно высокой по сравнению с соединениями по WO 00/76984 и WO 02/40457. Отсутствие заметного сродства к некоторым другим подтипам рецепторов 5-НТ лежит в основе улучшенного терапевтического индекса в сравнении с обычной активацией всех различных подтипов рецепторов 5-НТ с помощью ингибиторов обратного захвата 5-НТ и/или деблокирующих 5-НТ средств. Средство против ожирения, дексфенфлурамин, ингибитор обратного захвата 5-НТ и деблокатор 5-НТ, был изъят из продажи в сентябре 1997 г. ввиду некоторых сообщений, предполагающих связь этого лекарства с риском развития первичной легочной гипертензии и нарушениями клапанов сердца (см., например, Kolanowski, J. A risk-benefit assessment of anti-obesity drugs. Drug Safety 1999, 20, 119-131). Ингибитор 5-НТ/норадреналинового обратного захвата, сибутрамин, поступающий в настоящее время в продажу для лечения ожирения, может повышать кровяное давление и сердечный ритм у некоторых пациентов. Применение сибутрамина было временно приостановлено в Италии в марте 2002 г. по причине двух смертельных исходов, вызванных сердечно-сосудистыми нарушениями, и его безопасность изучается в настоящее время в других европейских странах, где только в Великобритании и Франции было всего 103 сообщения о серьезных побочных реакциях у людей, использующих препарат, включая два смертельных исхода в Великобритании. Все вместе свидетельствует о необходимости разработки безопасных средств против ожирения. Важно свести к минимуму возможные побочные реакции, вызванные активацией подтипов рецепторов 5-НТ2А и 5-НТ2Б. Введение вещества, имеющего сродство к рецептору 5-НТ2А, может иметь отношение к сужению кровеносных сосудов, агрегации тромбоцитов и случаям галлюцинации, а введение вещества, имеющего сродство к рецептору 5-НТ2Б, может играть роль в патофизиологии мигрени. Стимуляция рецепторов 5-НТ2А и 5-НТ2Б может также быть связана с фиброзом миокарда. В следующих литературных ссылках показано, что случаи галлюцинации связаны с активацией рецептора 5-НТ2А: (a) Glennon, R.A. et al. Hallucinogens and Serotonergic Mechanisms. NBDA Res. Mongr. 1992, 119P, 131-135. (b) Egan, C.T. et al. Agonist Activity of LSD and Lisuride at cloned 5-HT2A and 5-HT2C receptors. Psy-chopharmacol. 1998, 136, 409-414. (c) Roth, B.L. et al. The multiplicity of serotonin receptors: Uselessly diverse molecules or an embarrassment of riches? Neuroscientist 2000, 6, 252-262. (d) Arvanov, V.L. et al. LSD and DOB: interaction with 5-HT2A receptors to inhibit NMDA receptor-mediated transmission in the rat prefrontal cortex. Eur. J. Neurosci. 1999, 11, 3064-3072. (e) Marek, G.J. et al. LSD and the phenethylamine hallucinogen DOI are potent partial agonists at 5-HT2A receptors on intemeurons in rat piriform cortex. J. Pharmacol. Exp. Ther. 1996, 278, 1373-1382. (f) Roth, B.L. et al. Activation is hallucinogenic and antagonism is therapeutic: role of 5-HT2A receptors in atypical antipsychotic drug actions. Neuroscientist 1999, 5, 254-262. (g) Aghajanian, G. K. et al. Serotonin and Hallucinogens. Neuropsychopharmacology 1999, 21, 16S-23S. (h) Aghajanian, G. K. et al. Serotonin model of schizophrenia: emerging role of glutamate mechanisms. Brain Res. Rev. 2000, 31, 302-312. В следующих литературных ссылках показано, что эффекты сужения кровеносных сосудов связаны с активацией рецептора 5-HT2A: (a) Roth, B. L. et al. 5-HT2-family receptors (5-HT2A, 5-HT2B, 5-HT2a): where structure meets function. Pharmacol. Ther. 1998, 79, 231-257. (b) Florian, J. A. et al. Integration of mitogen-activated protein kinase activation in vascular 5-hydroxytryptamine 2A receptor signal transduction. J. Pharmacol. Exp. Ther. 1998, 284, 346-355. (c) Saxena, P. R. Serotonin receptors: Subtypes, functional responses and therapeutic relevance. Pharmacol. Ther. 1995, 66, 339-368. (d) MacLennan, S. J. 5-HT receptors in the human cardiovascular system. ID Res. Alert 1997, 2, 207-213. (e) Nilsson, T. et al. Characterisation of 5-HT receptors in human coronary arteries by molecular and pharmacological techniques. Eur. J. Pharmacol. 1999, 372, 49-56. (f) MacLean, M.R. et al. 5-Hydroxytryptamine receptors mediating vasoconstriction in pulmonary arteries from control and pulmonary hypertensive rats. Br. J. Pharmacol. 1996, 119, 917-930. (g) Cortijo, J. et al. Characterization of 5-HT receptors on human pulmonary artery and vein: functional and binding studies. Br. J. Pharmacol. 1997, 122, 1455-1463. - 3 - 008148 (h) O'Connor, S. E. et al. Cardiovascular effects of SL65.0472, a 5-HT receptor antagonist. Bur. J. Pharmacol. 2001, 414, 259-269. (i) Galzin, A.-M. et al. Effects of SL 65.0472, a novel 5-HT receptor antagonist, on 5-HT receptor mediated vascular contraction. Eur. J. Pharmacol. 2000, 404, 361-368. В следующих литературных ссылках показано, что введение вещества, имеющего сродство к 5-НТ^, связано с агрегацией тромбоцитов и атеросклерозом: (a) Li, N. et al. Effects of serotonin on platelet activation in whole blood. Blood Coagul Fibrinolysis 1997, 8, 517-523. (b) Takano, S. Role of 5-hydroxytryptamine in platelet thrombus formation and mechanisms of inhibition of thrombus formation by 5-hydroxytryptamine 2A antagonists in rabbits. Arch. hit. Pharmacodyn. Ther. 1995, 330, 297-308. (c) de Clerck, F. The role of serotonin in thrombogenesis. Clin. Physiol. Biochem. 1990, 8 (Suppl. 3), 4049. Одним из инициирующих факторов атеросклероза является эндотелиальное повреждение с последующей агрегацией тромбоцитов. При атеросклерозе тромбоциты агрегируют значительно легче и большие количества серотонина высвобождаются тромбоцитами. Сосудистые реакции на высвобождение серотонина активированными тромбоцитами глубоко изменяются в направлении, благоприятствующем вазоконстрикции (артериальному спазму), что, в конечном счете, может приводить к тромбозу и полной закупорке сосудов. Считается, что пролиферация гладкомышечных клеток сосудов играет важную роль в патогенезе атеросклероза. Известно, что серотонин является митогеном для гладкомышечных клеток сосудов, вызывающим стимуляцию рецептора [предположительно, через активацию МАРК- (митоген-активированная протеинкиназа) и/или РКС- (протеинкиназа С) зависимых проводящих путей], см.: (a) Lee, S.-L. et al. Serotonin stimulates mitogen-activated protein kinase activity through the formation of superoxide anion. Am. J. PhysioL 1999, 277, (2Pt.1), L-282-L291. (b) Florian, J. A. et al. Integration of mitogen-activated protein kinase activation in vascular 5-hydroxytryptamine2A receptor signal transduction. J. Pharmacol. Exp. Ther. 1998, 284, 346-355. (c) Banes A. et al. Mechanisms of 5-hydroxytryptamine2A receptor activation of the mitogen-activated protein kinase pathway in vascular smooth muscle. J. Pharmacol. Exp. Ther. 1999, 291, 1179-1187. (d) Watanabe, T. et al. Lipid peroxidation product 4-hydroxy-2-nonenal acts synergistically with serotonin in inducing vascular smooth muscle cell proliferation. Atherosclerosis 2001, 155, 37-44. (e) Pakala, R. et al. Eicosapentaenoic Acid and Docosahexaenoic Acid Block Serotonin-Jnduced Smooth Muscle Cell Proliferation. Atherioscler. Thromb. Vase. Biol. 1999, 19, 2316-2322. Кроме того, выдвинуто предположение, что повышенная сосудосуживающая реакция на 5-НТ в атеросклеротических сосудах может быть обусловлена рецепторами с повышенной чувствитель- ностью, см.: Fujiwara, Т. et al. Augmented responses to 5-HT2-receptor-mediated vasoconstrictions in atherosclerotic rabbit common carotid arteries. J. Cardiovasc. Pharmacol. 1995, 26, 503-510. Подразумевается также, что 5-НТ-индуцированная повышающая регуляция экспрессии рецепторов тромбина в гладкомышечных клетках сосудов, посредством активации рецепторов 5-НТ^, играет определенную роль в атеросклерозе, см.: Schini-Kerth V.B. et al. Serotonin stimulates the expression of thrombin receptors in cultured vascular smooth muscle cells. Role of protein kinase С and protein tyrosine kinases. Circulation 1996, 93, 2170-2177. В следующих литературных ссылках показано, что введение вещества, имеющего сродство к 5-HT2B, связано с мигренью: (a) Schmuck, K. et al. Activation of meningeal 5-НТж receptors: an early step in the generation of migraine headache. Eur. J. Neurosci. 1996, 8, 959-967. (b) Johnson, K.W. et al. Serotonin in migraine: Theories, animal models and emerging therapies. Prog. Drug. Res. 1998, 51, 219-244. (c) Parsons, A. A. Prophylaxis of migraine. Curr. Opin. CPNS Invest. Drugs 2000, 2, 160-166. В следующей литературной ссылке показано, что легочная гипертензия связана с активацией рецептора 5-НТж: (a) Launay, J.-M. et al. Function of the serotonin 5-hydroxytryptamine 2B receptor in pulmonary hypertension. Nature Med. 2002, 8, 1129-1135. В следующих литературных ссылках показано, что введение вещества, имеющего сродство к 5-HT2A и, в особенности, к 5-НТж, связано с возникновением фиброза миокарда после терапии существующими в продаже препаратами против ожирения, такими как дексфенфлурамин: (a) Rothman, R.B. et al. Evidence for possible involvment of S-HT2B receptors in the cardiac valvulopathy associated with fenfluramine and other serotonergic medications. Circulation 2000, 102, 2836-2841. (b) Fitzgerald, L.W. et al. Possible role of valvular serotonin S-HT2B receptors in the cardiopathy associated with fenfluramine. Mol. Pharmacol. 2000, 57, 75-81. (c) Setola, V. et al. 3,4-Methylenedioxymethamphetamine (MDMA, "Ecstasy") induces fenfluramine-like proliferative actions on human cardiac valvular interstitial cells in vitro. Mol. Pharmacol. 2003, 63, 1223-1229. - 4 - 008148 Как указано ниже, настоящие соединения могут применяться в целях терапии вызываемых серото-нином состояний, таких как менопаузальные и постменопаузальные приливы. Berendsen H.H.G. "Hot flushes and serotonin". Journal of the British Menopause Society. 2002, 8, 30-34, указывает, что негормональное лечение либо антагонистами рецептора 5-НТ^, либо агонистами рецептора 5-HT2C может иметь некоторые преимущества перед гормональной терапией. Другим примером вызываемых серотонином нарушений является прибавление в весе, связанное с приемом нейролептических лекарственных средств. WO 02/19998 описывает, что применение атипичных нейролептических средств вызывает прибавление в весе у значительной доли из обследованной группы больных, до 50% больных. Piesla, M. J. et al. Atypical antipsychotic-like effects of 5-HT2C agonists. Schizophrenia Res. 2001, 49 (1-2; Sp Iss, Suppl.) 95, описывает, что агонисты 5-HT2C обладают нейролептической способностью. Кроме того, терапия с применением агонистов 5-HT2C будет вероятно препятствовать прибавлению в весе, вызываемому нейролептическими средствами, без противодействия нейролептическому эффекту. Естественно ожидать, что нейролептическое действие будет усиленным. Краткое описание изобретения Согласно настоящему изобретению, предложен класс новых соединений, связывающих рецептор 5-НТ2с:, указанные соединения могут являться агонистами, частичными агонистами или антагонистами данного рецептора, предпочтительно агонистами или частичными агонистами. Кроме того, настоящие соединения могут быть использованы для лечения вызываемых серотонином нарушений и состояний. К тому же показано, что избирательность настоящих соединений в отношении рецептора 5-HT2C неожиданно высока по сравнению с избирательностью соединений, известных из уровня техники. Согласно одному из аспектов, изобретение относится к новым соединениям общей формулы (I) Формула (I), где nx равно 2-4, предпочтительно 2; каждый из R0 и R1 независимо означает Н или CH3; R2 означает Н, Q-Q-алкил, 2-гидроксиэтил, 2-цианоэтил или тетрагидропиран-2-ил, Q-Q-ацил или C1-C4-алкоксикарбонил; каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород; каждый из X, Y и z независимо означает СН или N; A1 означает О, СН или СН2; А2 означает О, СН или (СН2)п2, где n2 равно целому числу 0-2; Связь между A1 и А2 является простой или двойной связью; A3 означает (СН2)п3, где n3 равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5; А4 означает (СМе^, где n4 равно целому числу 0-1; А5 означает N или О; каждый из А6 и А7 независимо означает Н, Q-Q-алкил, амино-С2-C4-алкил, N,N^-Q-C4-алкиламино-С^Огалкил, С3-С6-циклоалкил или вместе с A5 образует насыщенное гетероциклическое кольцо; А8 означает (CH2)n8, где n8 равно целому числу 0-2; А9 означает Н или СН2; или фармацевтически приемлемые соли, сольваты, гидраты, геометрические изомеры, таутомеры, оптические изомеры, N-оксиды и пролекарственные формы указанных соединений; при условии, что когда A5 означает N, то А5 замещен только двумя из А6, А7 и А8; когда А5 означает О, то А5 замещен только одним из А6, А7 и A8. В случае, когда соединения формулы (I) могут быть в форме оптических изомеров, изобретение включает рацемическую смесь, а также индивидуальные энантиомеры как таковые. Согласно другим аспектам, соединениями формулы (I) являются такие соединения, где в случае, когда по крайней мере одно из вышеуказанных целых чисел, n2, n3, n4 или n8, равно 0, то - 5 - 008148 соответствующая группа А2, A3, А4 или А8 означает простую связь. Однако, в случае, когда А9 означает Н, то А8 не может означать простую связь между А5 и А9. В случае, когда n8 равно 1 или 2, то А5 не может быть замещен А7. Когда A1 означает СН2, А2 означает 0 и А5 означает N, то как n3, так и n4, оба не равны 0. Когда один из A1 и А2 означает 0, другой из A1 и А2 не может означать 0. Когда один из A1 и А2 означает СН, то другой из A1 и А2 также означает СН, где связь между A1 и А2 означает двойную связь. Когда А5 означает 0, то А5 не может быть замещен А7 и А8, А9 означает Н и A6 означает амино-Q-Q-алкил или N, N-ди-C1-C4-алкиламино-C2-C4-алкил, и, кроме того, n3 и n4 оба предпочтительно равны 0. Когда А3, А4, А5, А8 и A9 вместе с атомом углерода между А3 и А9 образуют 4-7-членное насыщенное гетероциклическое кольцо (например, азациклическое кольцо), то A9 означает СН2, n4 равно 0 и сумма n3+n8 равна целому числу 1-4. Когда A9 означает СН2, то все, n3, n4 и n8, не равны 0. Когда A9 означает СН2 и А5 означает N, то n4 равно 0. Когда n4 равно 1, то A9 предпочтительно означает Н и A5 предпочтительно означает N. Когда А5 означает азот, каждый из A6 и A7 независимо означает Н, CrQ-алкил, C3-C6-циклоалкил или оба образуют вместе насыщенное гетероциклическое кольцо. В случае, когда R0 означает метил, предпочтительно, чтобы атом углерода, к которому присоединена указанная метильная группа R0, находился в ^-конфигурации. Предпочтительно, чтобы R1 означал водород. Также предпочтительно, чтобы X и Y оба означали азот. Кроме того, предпочтительно, чтобы R2 означал Н или метил. Также предпочтительно, чтобы все R3-R5 означали Н. Предпочтительно также, чтобы каждый из A6 и А7 независимо означал Н, метил, изопропил, 2-этиламин или образовывал вместе с A5 пирролидиновый или пиперазиновый цикл. По одному из предпочтительных вариантов изобретение касается соединения формулы (1а) где R0-R5, X, Y и z имеют вышеуказанные значения, предпочтительно, где z означает N, m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R6 означает NR7R5 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный CrQ-алкил; или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R9 означает амино-C2-C4-алкил или N,N-ди-C1-C4-алкиламино-С2-C4-алкил. Предпочтительно R7 и R8 выбран из группы, включающей Н, метил, изопропил, либо указанные группы образуют вместе с атомом азота, к которому присоединены, пирролидиновый или пиперазино-вый цикл. Предпочтительно также, чтобы R9 означал 2-аминоэтил. Характерными соединениями формулы (!а) являются N,N-диметил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2,]бипиразинил-3,-илокси)этокси]пири-дин-2-илокси)этил)амин; N,N-диизопропил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2,]бипиразинил-3,-илокси)эток-си]пиридин-2-илокси)этил)амин; N,N-диметил-2-[(3-{2-[(3-пиперазин-1-илпиразин-2-ил)окси]этокси}пиридин-2-ил)окси]этанамин; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2- {[2-(2-пирролидин-1-илэтокси)пиридин-3-ил]окси}это-кси)пиразин; N,N-диметил-4-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)бутан-1-амин; N-метил-N-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)этил]пропан-2-амин; Формула (1а), - 6 - 008148 диметил-3-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}ок-си)пропан-1 -амин; N,N-2-триметил-1-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил] пиразин-2-ил} окси)этокси] пиридин-2-ил} окси)пропан-2-амин; [2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}ок- си)этил]амин; №метил-2-( {3-[2-({3-[(2R)-2-метилпиперазин-1-ил] пиразин-2-ил} окси)этокси] пиридин-2-ил} окси)этанамин; 2-{2-[{2-[2-(диметиламино)этокси]пиридин-3-ил}окси]этокси}-3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин; 2-[2-(2-[2-(диметиламино)этокси]фенокси)этокси]-3-[(2R)-2-метилпиперазин-1-ил] пиразин; {2-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)это-кси]этил}амин; [6-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)гек-сил]амин; [5-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пен-тил]амин 5-({3-[2-({3 - [(2R)-2,4-диметилпиперазин-1-ил] пиразин-2-ил} окси)этокси] пиридин-2-ил} окси)-N,N-диметилпентан-1-амин; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2- {[2-(2-пиперазин-1 -илэтокси)пиридин-3-ил]окси}этокси)пи- разин. Согласно другому предпочтительному варианту выполнения изобретение касается соединения формулы (lb) где R0-R5, X, Y и z имеют вышеуказанные значения, o равно целому числу 0-2; p равно целому числу 0-2, где o и р предпочтительно не оба равны 0; q равно целому числу 0-1; R10 означает Н или CrQ-алкил, предпочтительно Н или метил. Характерными соединениями формулы (Ib) являются 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[(1-метилпиперидин-4-ил)окси]пиридин-3-ил}окси)это-кси]пиразин; 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[2-(1-метилпирролидин-2-ил)этокси]пиридин-3-ил}ок-си)этокси]пиразин; 2- [(2R)-2-метилпиперазин-1-ил]-3-(2- {[2-(пиперидин-3-илметокси)пиридин-3-ил] окси} этокси)пира- зин; 2-[(2R)-2-метилпиперазин-1-ил]-3-{2-[(2-{[(2S)-1-метилпирролидин-2-ил]метокси}пиридин-3-ил)окси]этокси}пиразин. Согласно еще одному предпочтительному варианту выполнения изобретение касается соединения Формула (lb) формулы (1с) - 7 - 008148 где R0-R5, X, Y и z имеют вышеуказанные значения, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, ориентация относительно двойной связи может быть либо цис, либо транс; каждый из R11 и R12 независимо означает Н или линейный или разветвленный C1-C4-алкил; либо R11 и R12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо. Предпочтительно, чтобы R11 и R12 оба означали метил. Характерными соединениями формулы (1с) являются 2-{2-[{2-[(lz)-3-(диметиламино)проп-1-енил]пиридин-3ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин; 2-{2-[{2-[(1E)-3-(диметиламино)проп-1-енил]пиридин-3ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. Согласно еще одному предпочтительному варианту выполнения изобретение касается соединения формулы (Id) Формула (Id), где R0-R5, X, Y и z имеют вышеуказанные значения, W означает О или CH2; г равно 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, когда W означает СН2 и, наиболее предпочтительно, когда W означает О; каждый из R13 и R14 независимо означает Н или линейный или разветвленный Q-Q-алкил; либо R13 и R14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо. В случае, когда W означает О, предпочтительно, чтобы X=N и Y=N. В случае, когда W означает CH2, предпочтительно, чтобы r=t, X=N, Y=N, R13=R11 и R14=R12, где t, R11 и R12 имеют значения, указанные для формулы (Ic). Предпочтительно, чтобы R13 и R14 оба означали метил. Характерными соединениями формулы (Id) являются 2-{2-[(2-{[2-(диметиламино)этокси]метил}пиридин-3-ил)окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин; 2-{2-[{2-[3-(диметиламино)пропил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пи-разин. Соединения, представленные любой из формул (I), (Ia), (Ib), (Ic) и (Id), носят общее название соединения формулы (I). В случае, когда соединения формулы (I) содержат группы, которые могут существовать в тауто-мерных формах, изобретение включает таутомерные формы соединений, а также их смеси. В случае, когда соединения формулы (I) могут быть в форме геометрических изомеров, изобретение включает геометрические изомеры, а также их смеси. Согласно другому аспекту, изобретение касается соединений вышеуказанной формулы (I) для применения в терапии человека или животного. Еще один аспект изобретения касается фармацевтической композиции, включающей соединение вышеуказанной формулы (I) в качестве активного ингредиента, предпочтительно вместе с фармацевтически приемлемым носителем и, по желанию, другими фармакологически активными агентами. Согласно еще одному аспекту изобретение касается способа лечения человека или животного, страдающего нарушением или заболеванием, вызываемым серотонином, в частности, связанным с рецептором 5-HT2C, таким как нарушения памяти, такие как болезнь Альцгеймера; шизофрения; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическая зависимость и токсикомания; половые дисфункции, такие как эректильная дисфункция; эпилепсия; глаукома; заболевания мочевого - 8 - 008148 пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. Другой аспект изобретения касается применения соединения вышеуказанной формулы (I) при получении лекарственного средства для лечения вызываемого серотонином нарушения или заболевания, в частности, связанного с рецептором 5-HT2C, такого как нарушения памяти, такие как болезнь Альцгей-мера; шизофрения; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическая зависимость и токсикомания; половые дисфункции, такие как эректильная дисфункция; эпилепсия; глаукома; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопау-зальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. Способ может включать введение нуждающемуся в таком лечении больному (например, человеку или животному) эффективного количества одного или более соединений формулы (I), солей указанных соединений или композиций, содержащих соединения или соли. Другой аспект изобретения касается способов модуляции функции рецептора 5-HT2C, включающих контактирование рецептора с эффективным стимулирующим или ингибирующим количеством соединения вышеуказанной формулы (I), предпочтительно с эффективным стимулирующим количеством указанного соединения. Описанные здесь способы могут также включать стадию, выявляющую, что больной нуждается в лечении вызванного серотонином нарушения или состояния. Идентификация больного в целях установления необходимости такого лечения может быть выполнена по обращению самого больного или по решению медицинского работника, и может являться субъективной (например, заключение специалиста) или объективной (например, оценка методом тестирования или диагностическим методом). Характерную особенность изобретения также составляет способ получения композиции. Способ включает объединение соединения формулы (I) с фармацевтически приемлемым носителем. Еще один аспект изобретения касается способов получения соединений вышеуказанной формулы (I). Другой аспект изобретения касается способа лечения нарушения или состояния, включающего введение нуждающемуся в этом больному эффективного количества соединения вышеуказанной формулы (I), где нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и по-стменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. Еще один аспект изобретения касается применения соединений вышеуказанной формулы (I) в целях промышленного получения лекарственного средства для лечения нарушений памяти, таких как болезнь Альцгеймера; шизофрении; расстройств настроения, таких как депрессия; состояний тревоги; боли; наркотической зависимости и токсикомании; половых дисфункций, таких как эректильная дисфункция; эпилепсии; глаукомы; заболеваний мочевого пузыря, таких как недержание мочи; менопаузальных и по-стменопаузальных приливов; диабета типа 2; нарушений приема пищи, таких как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавления в весе, вызванного приемом нейролептических средств, предменструального напряжения, нарушения сна и, особенно, ожирения. Подробное описание изобретения Во-первых, следует объяснить различные термины, используемые раздельно или в комбинациях в приведенном выше определении соединений общей формулы (I) (и каждой из формул (D). Q-Czj-алкил, который может быть линейным или разветвленным, означает алкильную группу с 1-4 атомами углерода. Характерные алкильные группы включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил и трет-бутил. Амино-C2-C4-алкил, который может быть линейным или разветвленным, означает C2-C4-алкильную группу, непосредственно соединенную с аминогруппой. Характерные аминоалкильные группы включают 2-аминоэтил, 3-амино-н-пропил и 4-амино-н-бутил. С3-C6-циклоалкил означает циклическую алкильную группу с 3-6 атомами углерода. Характерными циклоалкильными группами являются циклопропил, циклобутил, циклопентил и циклогексил. C1-C4-ацил, который может быть линейным или разветвленным, означает ацильную группу с 1-4 атомами углерода. Характерные ацильные группы включают формил, ацетил, пропионил, н-бутирил и изобутирил. Q-Czj-алкокси, который может быть линейным или разветвленным, означает алкоксигруппу с 1-4 атомами углерода. Характерные алкоксигруппы включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, втор-бутокси и трет-бутокси. - 9 - 008148 C1-C4-алкоксикарбонил означает C1-C4-алкоксигруппу, непосредственно соединенную с карбонильной группой. Характерной алкоксикарбонильной группой является трет-бутоксикарбонил (t-ВОС). DCM означает дихлорметан, DMSO (ДМСО) означает диметилсульфоксид, галоген означает фтор, хлор, бром или иод, НОАс означает уксусную кислоту, HPLC (ВЭЖХ) означает высокоэффективную жидкостную хроматографию, HRMS означает масс-спектрометрию высокого разрешения, "OTs" означает тозилат, т.е. паратолуолсульфонат, "OMs" означает мезилат, т.е. метансульфонат, TEA означает три-этиламин, ТФУ означает трифторуксусную кислоту, THF (ТГФ) означает тетрагидрофуран. Термин "насыщенный гетероциклический" означает гетероциклическое кольцо, которое является неароматическим (например, частично или полностью насыщенным) и содержит атомы углерода и один или два гетероатома, выбираемых из О, S и N (предпочтительно, из О и N, и, более предпочтительно, из N). Примерами служат насыщенные 4-7-членные гетероциклические кольца, включающие пиперидин, азетидин, морфолин, тиоморфолин, пирролидин и пиперазин. Катализатор гидрирования означает катализатор, подходящий для каталитического гидрирования с целью бензилирования. Примерами катализаторов гидрирования являются палладий на угле (Pd/C), никель Ренея, платина, оксид платины и оксид цинка. Источник гидрирования означает реагент, используемый для введения атома водорода по какому-либо атому соединения, включающему атом углерода или кислорода. Примерами источников водорода являются газообразный водород и формиат аммония. Гидроксиэтилирующий агент означает реагент, используемый для введения в соединение гидрокси-этильной группы по атому кислорода или азота. Примерами гидроксиэтилирующего агента являются этиленкарбонат, 2-бромэтанол, 2-хлорэтанол и этиленоксид. Для превращения спиртовой функциональности в альдегидную функциональную группу может быть использован способ, описанный в Swern et al., J. Org. Chem. 1978, 43, 2480-2482. Согласно указанному способу спирт подвергают взаимодействию с диметилсульфоксидом и оксалилхлоридом в дихлор-метане при температуре -78°С. Для превращения спиртовой функциональности в подходящую удаляемую группу спирт можно обработать метансульфоновым ангидридом в присутствии триэтиламина в дихлорметане при температуре 0°С, например, как описано в J. Org. Chem. 2000, 65, 7839-7846. Основание означает соединение, образующее отрицательный ион и определяющее наличие электронов для кислоты, если таковая присутствует. Термин "основание", как использован здесь, означает реагент, способный присоединять протоны в ходе взаимодействия. Примеры оснований включают карбонатные соли, такие как карбонат калия, бикарбонат калия, карбонат натрия, бикарбонат натрия и карбонат цезия; галогениды, такие как фторид цезия; фосфаты, такие как фосфат калия, дигидрофосфат калия и гидрофосфат калия; гидроксиды, такие как гидроксид лития, гидроксид натрия и гидроксид калия; алкоксиды, такие как трет-бутилат натрия, трет-бутилат калия и трет-бутилат лития; алкиламины, такие как триэтиламин, диизопропиламин и диизопропилэтиламин; гетероциклические амины, такие как 4-диметиламинопиридин, 2,6-лутидин, 1-метилимидазол, пиридин; бициклические амины, такие как 1,8-диазабицикло(4.3.0)ундец-7-ен; и гидриды, такие как гидрид лития, гидрид натрия и гидрид калия. Основание выбирано для конкретного превращения в зависимости от природы исходных материалов, растворителя или растворителей, в которых осуществляют взаимодействие, и температуры, при которой осуществляют взаимодействие. Термин "пролекарственные формы" означает фармакологически приемлемое производное, такое как сложный эфир или амид, указанное производное подвергается биопревращению в организме, образуя активное лекарственное средство. Ссылки могут быть сделаны на Goodman and Gilman's, The Pharmacological basis of Therapeutics, 8th ed. , McGraw-Hill, Int. Ed. 1992, "Biotransformation of Drugs, p. 13-15 и "The Organic Chemistry of Drug Design and Drug Action" by Richard B. Silverman. Chapter 8, p 352. (Academic Press, Inc. 1992. ISBN 0-12-643730-0). " Фармацевтически приемлемый" означает подходящий для применения в получении фармацевтической композиции, которая в целом является устойчивой, нетоксичной, не имеющей ни биологических, ни каких-либо других противопоказаний, и включает пригодность для применения в ветеринарии, а также в фармацевтическом производстве лекарственных средств для человека. Термин "фармацевтически приемлемые соли" означает соли, которые фармацевтически приемлемы согласно приведенному выше определению и обладают требуемой фармакологической активностью. Такие соли включают кислотно-аддитивные соли, образованные органическими и неорганическими кислотами, такими как хлористый водород, бромистый водород, йодистый водород, серная кислота, фосфорная кислота, уксусная кислота, гликолевая кислота, малеиновая кислота, малоновая кислота, яблочная кислота, щавелевая кислота, толуолсульфоновая кислота, метансульфоновая кислота, трифторуксус-ная кислота, фумаровая кислота, янтарная кислота, винная кислота, лимонная кислота, бензойная кислота, аскорбиновая кислота, изэтионовая кислота (т. е. 2-гидроксиэтилсульфоновая кислота) и т. п. "Лечение", как использовано здесь, означает профилактику указанного нарушения или состояния, либо улучшение или ликвидацию состояния или нарушения, после того, как указанное состояние или нарушение было установлено. - 10 - 008148 Следует отметить, что Е- и z-изомеры соединений, оптические изомеры, а также смеси указанных изомеров и все изотопы входят в объем изобретения и прилагаемой формулы изобретения. Е означает "против направления" (транс-изомер) и z означает "по направлению" (цис-изомер). Из числа соединений, представленных приведенной выше общей формулой (I), предпочтительными являются соединения по примерам 1-3 и 6-27; их фармацевтически приемлемые соли и сольваты. Как указано выше, соединения по настоящему изобретению могут быть использованы для лечения больного, человека или животного, страдающего нарушением или состоянием, вызываемым серотони-ном, в частности, связанным с рецептором 5-HT2C, таким как нарушения памяти, такие как болезнь Альц-геймера; шизофрения; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическая зависимость и токсикомания; половые дисфункции, такие как эректильная дисфункция; эпилепсия; глаукома; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постмено-паузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. Нарушение, связанное с рецептором 5-HT2C, включает любое нарушение или состояние, модулируемое рецептором 5-HT2C. Преимущественно соединения по настоящему изобретению могут быть использованы для лечения нарушений или состояний, где желателен или необходим агонист рецептора 5-НТ2о Соединения по настоящему изобретению в виде меченых соединений, например, меченные радиоактивными изотопами, могут быть использованы в качестве диагностических средств. Примеры таких меток известны из уровня техники и включают I, S, Р, 18F, 14C, 11С, 3Н и т.п. Другим объектом настоящего изобретения является способ получения соединения формулы (!а), включающий: а) взаимодействие соединения формулы (II) Формула (II), где X1 выбран из F, Cl, Br и I, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, с соединением формулы (III) Формула (III), где Y1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) Формула (IV), где X1 и R3-R5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, - 11 - 008148 Формула (Va) , где m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R6 означает NR7R8 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный C1-C4-алкил; или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R9 означает амино-С2-C4-алкил или N,N-ди-C1-C4-алкиламино-C2-C4-алкил, приводящее к соединению формулы (Via) Формула (Via), где R3-R6, m и n имеют вышеуказанные значения, с) обработку соединения формулы (VIa) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (Vila) Формула (Vila), где R3-R6, m и n имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метилтрет-бутиловый эфир или толуол, Формула (VIII), где каждый из R0 и R1 независимо означает Н или СН3; R2 выбран из группы, включающей Q-Q-алкоксикарбонил, бензил, тритил, Q-Q-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и Q-Q^im, R15 означает галоген, такой как хлор, приводящее к соединению формулы (!а), где X=N и Y=N - 12 - 008148 R, Re Формула (la), где R0-R6, m и n имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R2 в формуле (1а) после стадии d) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как осуществляемым в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ia), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (Ib), включающий: а) взаимодействие соединения формулы (II) Формула (II), где X1 выбран из F, Cl, Br и I, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, с соединением формулы (III) Формула (III), где Y1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) Формула (IV), где X1 и R3-R5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, НО. (СН2)у* Формула (Vb), - 13 - 008148 где о равно целому ЧИСЛУ 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R10 означает Н или Q-Q-алкил, предпочтительно Н или метил; приводящее к соединению формулы (VIb); Формула (VIb), где R3-R5 и R10, о, р и q имеют вышеуказанные значения, с) обработку соединения формулы (VIb) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (Vllb) 1?з Формула (VIlb), где R3-R5 и R10, о, р и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метилтрет-бутиловый эфир или толуол NR, Формула (VIII), где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей CrQ-алкоксикарбонил, бензил, тритил, C1-C4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и C1-C4-ацил, R15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N: - 14 - 008148 Формула (lb), где Ro-R5, Rio, о, р и q имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R2 в формуле (Ib) после стадии d) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (Ia), указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания Формула (IX), где каждый из R3-R5 независимо означает Н, галоген, метил и метокси, при условии, что по меньшей мере один из R3-R5 означает водород, приводящее к соединению формулы (X) Формула (X), где R3-R5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (Х!а) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон (СН,)т. 27 ^СМе2)п Формула (XIа), где Х2 означает галоген, OMs или OTs; m равно целому числу 0-10, предпочтительно, 0-7, более предпочтительно 0-5, n равно целому числу o или i, где сумма m+n предпочтительно равна по меньшей мере i, R6 означает NR7R8 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный C1-C4-алкил; или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R9 означает амино-C2-C4-алкил или N,N-ди-C1-C4-алкиламино-C2-C4-алкил, приводящее к соединению формулы (XIIa) - 15 - 008148 где R3-R6, m и n имеют вышеуказанные значения; с) обработку соединения формулы (ХПа) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (XIII) |СМе2)п Формула (XIНа) , где R3-R6, m и n имеют вышеуказанные значения; d) взаимодействие соединения формулы (ХШа) с гидроксиэтилирующим агентом, таким как эти-ленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XlVa) Формула (XlVa), где R3-R6, m и n имеют вышеуказанные значения; е) взаимодействие соединения формулы (XIVa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как г\Г,г\[-диметилформамид Формула (VIII), где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей CrQ-алкоксикарбонил, бензил, тритил, Q-Q-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и CrQ-ацил, R15 означает галоген, такой как хлор, приводящее к соединению формулы (!а), где X=N и Y=N - 16 - 008148 Формула (la), где Ro-Rs, m и n имеют вышеуказанные значения; f) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, g) если R2 в формуле (1а) после стадии е) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (1а), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (Ib), указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания Формула (IX), где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, приводящее к соединению формулы (X) где R3-R5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (XIb) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон где Х2 означает галоген, OMs или OTs; о равно целому числу o-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; Rio означает Н или Ci-C/галкил, предпочтительно Н или метил; приводящее к соединению формулы (XIIb) Формула (X) , Формула <Х1Ь), - 17 - 008148 где R3-R5, R10, о, p и q имеют вышеуказанные значения, с) обработку соединения формулы (XIIb) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, приводящее к соединению формулы (ХШЬ) где R3-R5, R10, о, p и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (ХШЬ) с гидроксиэтилирующим агентом, таким как эти-ленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XlVb) "ОН х|СН2)о (СН,)^ ^° ^(CH2)q Формула (XlVb), R3-R5, R10, о, р и q имеют вышеуказанные значения, е) взаимодействие соединения формулы (XlVb) С соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как 1Ч,]М-диметилформамид Формула (VIII), где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей CrQ-алкоксикарбонил, бензил, тритил, CrQ-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и Q-Сгацил, - 18 - 008148 Ris означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N 10 ^(CH2)q Формула (Ib), где R0-R5, Rio, о, р и q имеют вышеуказанные значения, f) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, g) если R2 в формуле (Ib) после стадии е) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (Ia), указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как 1Ч,]М-диметилформамид, Формула (XV), где Х3 выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород; приводящее к соединению формулы (XVI) ОВп *Г 2 хз Формула (XVI), где R3-R5, X3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как 1Ч,]М-диметилформамид, Формула (Va), где m равно целому числу 0-10, предпочтительно, 0-7, более предпочтительно 0-5, n равно целому числу 0 или i, где сумма m+n предпочтительно равна по меньшей мере i, R6 означает NR7R8 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный CrC/i-алкил; или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R9 означает амино-С2-C4-алкил или N,N-ди-C1-C4-алкиламино-С2-C4-алкил, приводящее к соединению формулы (XVIIa) - 19 - 008148 где R3-R6, m, n и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIa) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как ^^диметилформамид, приводящее к соединению формулы (Vila) где R3-R6, m, n и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как М,М-диметилформамид где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей CrC/галкоксикарбонил, бензил, тритил, CrC/галкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и CrC/гацил, Ri5 означает галоген, такой как хлор, приводящее к соединению формулы (1а), где X=N и Y=N Формула (1а), где R0-R6, m, n и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, Формула (VIII), - 20 - 008148 f) если R2 в формуле (Ia) после стадии d) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ia), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (Ib), указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как 1Ч,1ч[-диметилформамид Формула (XV) , где Xi выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, приводящее к соединению формулы (XVI) ОВп Формула (XVI), где R3-R5, X3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как 1ч[,1ч[-диметилформамид, НО. CH,)Q R10N 4CH2)q Формула (Vb), где о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-i; R10 означает Н или Q-Q-алкил, предпочтительно Н или метил; приводящее к соединению формулы (XVIIb) Формула (XVIIb), где R3-R5 и R10, о, р, q и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIb) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как ^^диметилформамид, приводящее к соединению формулы (VIIb) - 21 - 008148 Формула (VIIb), где R3-R5 и R10, о, р, q и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как М,М-диметилформамид Формула (VIII), где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей: С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ris означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N Формула (Ib), где R0-R5 и R10, о, р, q и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R2 в формуле (Ib) после стадии d) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (к), указанный способ включает: а) взаимодействие соединения формулы (XVIII) Формула (XVIII), - 22 - 008148 где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород; z означает СН или N, с соединением формулы (III) Формула (III), где Y1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) Формула (XIX), где R3-R5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XVI) в альдегидную функциональную группу в присутствии диметилсульфоксида и оксалилхлорида в дихлорметане, приводящее к соединению формулы (XX) где R3-R5 и z имеют вышеуказанные значения, с) взаимодействие соединения формулы (XX) с соединением формулы (XXI) в присутствии основания, такого как трет-бутилат калия в смеси растворителей, состоящей из тетрагидрофурана и третбутано-ла t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1 и каждый из R11 и R12 независимо означает Н или линейный или разветвленный С1-С4-алкил; или R11 и R12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXII) где - 23 - 008148 Формула (XXII), где R3-R5, R11, R12, t и z имеют вышеуказанные значения; ориентация относительно двойной связи может быть либо цис, либо транс; d) разделение с помощью препаративной ЖХВР и выделение цис-и транс- изомеров соединения формулы (XXII), приводящее к получению индивидуального цис-изомера формулы (XXIII) и индивидуального транс-изомера формулы (XXIV) Формула (XXIII), Формула (XXIV), где R3-R5, R11, R12, t и z имеют вышеуказанные значения; е) обработку соединений формулы (XXIII) и (XXIV), соответственно, водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединения формулы (XXV) и (XXVI), соответственно Формула (XXV), Формула (XXVI), где R3-R5, R11, R12, t и z имеют вышеуказанные значения; f) взаимодействие соединений формулы (XXV) и (XXVI) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как М,М-диметилформамид Формула (VIII) - 24 - 008148 где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей Q-Сгалкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ris означает галоген, такой как хлор, приводящее к соединениям формулы (XXVII) и (XXVIII) R12-4 R12\ Формула (XXVII), Формула (XXVIII), где R0-R5, R11, R12, t и z имеют вышеуказанные значения; где соединения формул (XXVII) и (XXVIII) являются изомерами соединения формулы (1с), где X=N и Y=N; g) если R2 в формуле (Ic) после стадии f) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ic), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (Id), указанный способ включает: а) обработку соединения формулы (XXII) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (XXIX) CH2)t Формула (XXIX) где каждый из R3-R5 независимо означает Н, галоген, метил и метокси, при условии, что по меньшей мере один из R3-R5 означает водород, z означает СН или N, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1; и каждый из R11 и R12 независимо означает Н или линейный, или разветвленный С1-С4-алкил; или R11 и R12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; b) обработку соединения формулы (XXIX) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXX) - 25 - 008148 R12^(CH2)t Формула (XXX) где R3-R5, Rn, R12, t и z имеют вышеуказанные значения; с) взаимодействие соединения формулы (XXX) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как ]^,]Ч-диметилформамид или диоксан: Формула (VIII), где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ri5 означает галоген, такой как хлор, приводящее к соединению формулы (XXXI) Формула (XXXI): где R0-R5, R11, R12, t и z имеют вышеуказанные значения, где формула (XXXI) отвечает формуле (Id), в которой W=OT2, r=t, X=N, Y=N, R13=R11 и R14=R12, d) если R2 в формуле (Id) после стадии с) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R2 означает водород. Другим объектом настоящего изобретения является способ получения соединения формулы (Id), указанный способ включает: а) взаимодействие соединения формулы (XVIII) Формула (XVIII), где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей - 26 - 008148 мере один из R3-R5 означает водород; z означает СН или N, с соединением формулы (III) Формула (III), где Yi означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) Формула (XIX), где R3-R5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XIX) в подходящую удаляемую группу, например, путем обработки метансульфоновым ангидридом в присутствии триэтиламина в дихлорметане, приводящее к соединению формулы (XXXII) Формула (XXXII), где R3-R-5 и z имеют вышеуказанные значения; Y2 означает галоген, OMs или OTs; с) взаимодействие соединения формулы (XXXII) с соединением формулы (XXXIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как диоксан: /R13 hw-(CH2)-|^ Формула (XXXIII), где W означает О; r равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 2; каждый из R13 и R14 независимо означает Н или линейный или разветвленный CrQ-алкил; или R13 и R14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXXIV) - 27 - 008148 L14 Формула (XXXIV) где r, z, W, R3-R5, R13 и R14 имеют вышеуказанные значения; d) обработку соединения формулы (XXXIV) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXXV) R13-N^(CH2)r Формула (XXXV), где r, z, W, R3-R5, R13 и R14 имеют вышеуказанные значения; е) взаимодействие соединения формулы (XXXV) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как 1Ч,1Ч-диметилформамид Формула (VIII) где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ri5 означает галоген, такой как хлор, приводящее к соединению формулы (XXXVI) NRj (CH2KN,R13 *1 < Формула (XXXVI): где R0-R5, R13, R14, r, W и z имеют вышеуказанные значения, где формула (XXXVI) отвечает формуле - 28 - 008148 (Id), в которой X=N и Y=N, f) если R2 в формуле (Id) после стадии е) означает азот-защитную группу, такую как t-BOC, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R2 означает водород. Химические реагенты, используемые в вышеуказанных способах синтеза, могут включать, например, растворители, реагенты, катализаторы, средства для защиты групп и для снятия защиты. Вышеуказанные способы могут также дополнительно включать стадии, либо до, либо после конкретных описанных здесь стадий, для введения или удаления подходящих защитных групп, обеспечивающие в конечном счете синтез соединений формулы (I). Кроме того, различные стадии синтеза могут быть выполнены в другой последовательности в целях получения требуемого соединения. Преобразования химических синтезов и методики применения защитных групп (защита и снятие защиты), используемые для синтеза соответствующих соединений, известны из уровня техники и включают, например, приемы, описанные в R. Larock, Comprehensive Organic Transformations, УСН Publishers (1989); T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis, 3rd Ed., John Wiley and Sons (1999); L. Fieser and M. Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994) и L. Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995) и их последующие издания. Примеры защитных групп по настоящему изобретению включают t-BOC (трет-бутоксикарбонил), тритил и бензил. Следует отметить, что соединение формулы (I) (включая любую из формул Ia, Ib, Ic и Id), полученное по настоящему изобретению, может быть преобразовано в другое соединение формулы (I) способами, хорошо известными из уровня техники. Например, стандартная реакция восстановительного алкили-рования иллюстрируется примером 17 применительно к получению соединения формулы (I), где R2 означает метил, из соответствующего соединения формулы (I), где R2 означает водород (ср. методику, описанную в J. Org. Chem. 1996, 61, 3849-3862). Вышеуказанные способы могут быть осуществлены для получения соединения по изобретению в виде свободного основания или в виде кислотно-аддитивной соли. Фармацевтически приемлемая кислотно-аддитивная соль может быть получена растворением свободного основания в подходящем органическом растворителе и обработкой раствора кислотой, согласно общепринятым методикам получения кислотно-аддитивных солей из соединений в форме оснований. Примерами кислот, образующих аддитивную соль, являются малеиновая кислота, фумаровая кислота, янтарная кислота, метансульфоновая кислота, трифторуксусная кислота, уксусная кислота, щавелевая кислота, бензойная кислота, яблочная кислота, хлористо-водородная кислота, серная кислота, фосфорная кислота, изэтионовая кислота и тому подобные. Соединения формул (I) могут обладать одним или более хиральными атомами углерода и поэтому могут быть получены в форме оптических изомеров, например, в виде чистого энантиомера или в виде смеси энантиомеров (рацемат), или в виде смеси, содержащей диастереомеры. Разделение смесей оптических изомеров с целью получения чистых энантиомеров хорошо известно из уровня техники и может, например, быть достигнуто фракционированной кристаллизацией солей с оптически активными (хираль-ными) кислотами или хроматографическим разделением на хиральных колонках. Необходимые исходные продукты для получения соединений формул (I) либо являются известными, либо могут быть получены по аналогии с получением известных соединений. Согласно настоящему изобретению соединения формулы (I) в виде свободных оснований или солей с физиологически приемлемыми кислотами могут быть представлены в подходящих галеновых формах, таких как композиции для перорального употребления, для инъекции, для введения в виде спрея через нос или тому подобные, согласно принятым фармацевтическим методикам. Такие фармацевтические композиции по изобретению включают эффективное количество соединений формулы (I) в совокупности с совместимыми фармацевтически приемлемыми носителями или разбавителями, хорошо известными из уровня техники. Носителями могут служить любые инертные вещества, органические или неорганические, подходящие для энтерального, чрескожного, подкожного или парентерального введения, такие как вода, желатин, гуммиарабик, лактоза, микрокристаллическая целлюлоза, крахмал, натрийкрахмалг-ликолят, кальцийгидрофосфат, стеарат магния, тальк, коллоидный диоксид кремния и т. п. Такие композиции могут также содержать другие фармакологически активные агенты и общепринятые добавки, такие как стабилизаторы, смачивающие средства, эмульгаторы, корригенты, буферы и т. п. Композиции по изобретению могут быть, например, изготовлены в твердой или жидкой форме для перорального приема, такой как таблетки, пилюли, капсулы, порошки, сиропы, эликсиры, диспергируемые гранулы, крахмальные облатки, суппозитории и т. п, и в форме стерильных растворов, суспензий или эмульсий для парентерального введения, спреев, например, спрея для носа, трансдермальных препаратов, например пластырей и т.п. Как указано выше, соединения по изобретению могут быть использованы для лечения больного, человека или животного, страдающего нарушением или состоянием, вызываемым серотонином, в частности, связанным с рецептором 5-HT2C, таким как нарушения памяти, такие как болезнь Альцгеймера; шизофрения; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическая за- 29 008148 висимость и токсикомания; половые дисфункции, такие как эректильная дисфункция; эпилепсия; глаукома; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. Данное изобретение также касается способа лечения или профилактики вызванного серотонином вышеуказанного нарушения или состояния. Способ включает введение нуждающемуся в таком лечении больному (например, человеку, лошади, собаке или кошке) эффективного количества одного или более соединений вышеуказанной формулы (I). Описанные здесь способы могут также включать стадию выявления того, что больной нуждается в лечении нарушения или состояния, вызываемого серотонином. Также в рамки объема настоящего изобретения и приложенных пунктов входит способ модуляции (например, стимуляции или блокирования) функции рецептора 5-HT2C. Способ включает контактирование рецептора со стимулирующим или ингибирующим количеством соединения вышеуказанной формулы (I), предпочтительно с эффективным стимулирующим количеством указанного соединения. Стадия контактирования может включать введение соединения, соли указанного соединения или композиции, содержащей указанное соединение или соль. "Эффективное количество" означает количество соединения, которое оказывает терапевтическое действие на излечиваемого больного. Терапевтический эффект может быть объективным (т.е. измеряемым некоторым тестом или маркером) или субъективным (т. е. субъект свидетельствует о том, что он чувствует эффект). Уровень доз и частота дозированного введения конкретного соединения изменяются в зависимости от факторов, включающих эффективность конкретного используемого соединения, метаболическую стабильность и длительность действия указанного соединения, возраст пациента, массу тела, общее состояние здоровья, пол, диету, способ и время введения, скорость выведения, комбинацию лекарственных средств, тяжесть излечиваемого состояния и переносимость пациентом терапии. Суточная доза может, например, изменяться в пределах приблизительно от 0,001 до 100 мг на килограмм массы тела, вводимая однократно или многократно в дозах, например, приблизительно от 0,01 до 25 мг каждая. Обычно такая дозировка вводится перорально, но может быть также выбрано парентеральное введение. Далее изобретение иллюстрируется следующими не ограничивающими примерами. Не вдаваясь в подробности, считается, что специалист в данной области может, на основании приведенного описания, использовать настоящее изобретение в наиболее полном объеме. Все цитируемые публикации полностью включены здесь в качестве ссылок. Примеры Общие положения За исключением особо оговоренных случаев, исходные продукты получают из промышленных источников и используют, не подвергая после получения какой-либо обработке. Спектры 1Н-ядерного магнитного резонанса (ЯМР) и 13С-ЯМР снимают на спектрометре Bruker Advance DPX 400 при 400,1 и 100,6 МГц, соответственно, или на спектрометре JEOL 270. Все спектры регистрируют, используя остаточный растворитель в качестве внутреннего стандарта. Температуру плавления определяют с помощью настольного измерительного прибора Koefler'a и используют без учета поправки. Спектр масс-спектроскопии с электрораспылением (МС) получают на масс-спектрометре Perkin-Elmer API 150EX. Точные измерения массы осуществляют с помощью двойного зонда Micromass LCT. Условия ЖХВР (жидкостной хроматографии высокого разрешения) для примера 1 и примера 2: Препаративную ЖХ осуществляют на приборе для препаративной ЖХ-МС Gilson-Finnigan'а с колонкой 120 А, 50x20 мм S 5 мкм. Используют расход 30 мл/мин и различные градиенты 0,1% уксусной кислоты в воде и ацетонитрила. Условия ЖХВР для примеров 3-16: Препаративную ЖХВР осуществляют на Gilson-системе, оборудованной колонкой YMC AQ С18, 5 мкм (20x50 мм), элюент: смесь вода/ацетонитрил + 0,1% трифторуксусная кислота. Аналитическую ЖХ-УФ выполняют на системе Agilent 1100 с колонкой АСЕ С8, 3 мкм (3x50 мм), элюент: вода/ацетонитрил + 0,1% трифторуксусная кислота. Аналитическую ЖХ-МС выполняют на системе Agilent 1100 с колонкой YMC AQ С18, 3 мкм (3х33 мм), элюент: смесь вода/ацетонитрил+0,1% трифторуксусная кислота. Условия ЖХВР для примеров 17-27: Препаративную ЖХВР/МС осуществляют на системе Wathers/Micromass Platform zQ, оборудованной системой А: колонкой АСЕ 5 С8 (19x50 мм), элюент: 0,1% ТФУ в воде MilliQ при различных градиентах и MeCN. Система В: колонка Xterra MS С18, 5 мкм (19x50 мм), элюент: 10 мМ буфер с рН 10 из смеси NH4HCO3/NH3 при различных градиентах в воде MilliQ и MeCN. Аналитическую ЖХВР выполняют на Agilent 1100, колонка: АСЕ 3 С8 (система А) или колонка: YMC-Pack (система В), элюенты: смесь MilliQ/0,1% ТФУ и MeCN. Препаративную флэш-хроматографию выполняют на силикагеле Merck 60 (230-400 меш). GC-MS анализ выполняют на газовом хроматографе Hewlett Packard 5890 с колонкой HP-5MS 15 мх0,25 ммх0,25 мкм, соединенной с детектором 5971 MS. Пример 1. N,N-Диметил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2Н-[1,2']бипиразинил-3'-илокси)этокси]пири - 30 - 008148 дин-2-илокси)этил)аминацетат. Стадия 1: 3-Бензилокси-2-бромпиридин* Смесь 2-бромпиридин-3-ола (50,4 г, 0,29 моль), бензилбромида (45,5 г, 0,28 моль) и карбоната калия (52 г, 0,38 моль) в сухом ^^диметилформамиде (ДМФА; 300 мл) нагревают до 110°С в течение 30 мин. Смесь фильтруют через подушку из Celite(r), растворитель удаляют при пониженном давлении и черный остаток распределяют между охлажденным льдом 0,5М водным NaOH и EtOAc. Органическую фазу промывают дважды насыщенным раствором соли, сушат (MgSO4), и концентрируют при пониженном давлении, получая 69,6 г (93%) указанного в заголовке соединения в виде коричневого масла. HRMS m/z: вычислено для C12H10BrNO (M)+, 263,9946, найдено 263,9939. *Ранее описанный в J. Med. Chem. 1996, 39, 5267-5275. Стадия 2. 2-{[3-(Бензилокси)пиридин-2-ил]окси}-^^диметилэтанамин. К смеси ^^диметиламиноэтанола (4,16 г, 46,7 ммоль) и (3-бензилокси)-2-бромпиридина (со стадии 1; 8,22 г, 31,1 ммоль) в сухом ДМФА (50 мл) добавляют одной порцией трет-бутилат натрия (5,98 г, 62,2 ммоль). Реакционную смесь перемешивают при 80°С в течение 1,5 ч, растворитель удаляют при пониженном давлении и маслянистый остаток распределяют между CHC^/вода. Водную фазу экстрагируют дважды СНС13 и объединенные органические слои промывают однократно насыщенным раствором соли, сушат (MgSO4) и концентрируют при пониженном давлении. Что дает 8,4 г (100%) указанного в заголовке соединения в виде светло-коричневого масла. Чистота 95% (ЖХВР). HRMS m/z: вычислено для C16H20N2O2 (М)+, 272,1525, найдено 272,1537. Стадия 3. 2-[2-(2-Диметиламиноэтокси)пиридин-3-илокси]этанол. К продутому N2 раствору 2-{[3-(бензилокси)пиридин-2-ил]окси}^^-диметилэтанамина (со стадии 2; 8,4 г, 31,1 ммоль) в МеОН (100 мл) добавляют 10% Pd/C (0,8 г) с последующим добавлением формиата аммония (6,3 г, 100 ммоль). Смесь перемешивают при 50°С в атмосфере азота в течение 2 ч. Реакционную смесь фильтруют через Celite(r) и растворитель удаляют при пониженном давлении, получая полукристаллический продукт, который используют без дополнительной очистки на следующей стадии синтеза. Сырой продукт растворяют в сухом ДМФА (50 мл), добавляют карбонат калия (6,0 г, 4 3 ммоль) и смесь нагревают до 150°С в течение 20 мин. Добавляют этиленкарбонат (4,1 г, 46 ммоль) и нагревание продолжают в течение еще 1,5 ч. Твердые вещества фильтруют и фильтрат концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с диоксидом кремния, используя смесь CHCl3/MeOH/NH4OH (95:5:0,2) в качестве элюента, получают 3,28 г (31%) указанного в заголовке продукта в виде светло-коричневого масла. HRMS m/z: вычислено для C11H18N2O3 (М)+, 226,1317, найдено 226,1323. Стадия 4. N,N-Диметил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2Н-[1,2']бипиразинил-3'-илок-си)этокси]пиридин-2-илокси)этил)аминацетат. К раствору 2-[2-(2-диметиламиноэтокси)пиридин-3-илокси]этанола (со стадии 3; 2,89 г, 12,8 ммоль) в ДМФА (50 мл) добавляют за одну порцию трет-бутилат натрия (1,84 г, 19,2 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 10 мин. К смеси добавляют (2R)-1-(3-хлор-2-пиразинил)-2-метилпиперазин* (2,81 г, 13,5 ммоль) и реакционную смесь перемешивают при 60°С в течение 30 мин. Добавляют диоксид кремния (-15 г) и смесь фильтруют через небольшой слой диоксида кремния. Растворитель выпаривают при пониженном давлении и остаток очищают хроматографией на колонке с диоксидом кремния, используя смесь CHCl3/MeOH/NH4OH (95:5:0,2 с последующим соотношением 90:10:0,2) в качестве элюента. Растворитель из очищенных объединенных фракций выпаривают при пониженном давлении и остаток растворяют в диэтиловом эфире и добавляют НОАс в диэтиловом эфире. После выдерживания в течение 15 ч в холодильнике белые кристаллы фильтруют и сушат (60°С, 1 мм Hg), получают 2,5 г (42%) указанного в заголовке соединения т.пл. 75°С. Предполагаемую структуру подтверждают фрагментирующим МС-анализом. HRMS m/z: вычислено для C20H30N6O3 (М)+, 402,2379, найдено 402,2383. *Получен, как описано в WO 00/76984, пример 192, стадия 2. Пример 2. N,N-Диизопропил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2']бипиразинил-3'-илокси)это-кси]пиридин-2-илокси)этил)аминацетат. Стадия 1: (2-{[3-(Бензилокси)пиридин-2-ил]окси}этил)диизопропиламин. К смеси ^^диизопропиламиноэтанола (4,07 г, 28,0 ммоль) и (3-бензилокси)-2-бромпиридина (по примеру 1, стадия 1; 6,16 г, 23,3 ммоль) в сухом ДМФА (50 мл) добавляют за одну порцию трет-бутилат натрия (3,36 г, 35,0 ммоль). Реакционную смесь перемешивают при 80°С в течение 1,5 ч. Добавляют диоксид кремния (- 15 г) и смесь фильтруют. Растворитель выпаривают при пониженном давлении и оставшееся масло очищают хроматографией на колонке с диоксидом кремния, используя смесь тoлyoл/Et3N (97:3) в качестве элюента, получают 5,8 г (76%) указанного в заголовке соединения в виде светло-коричневого масла. Чистота 85% (ЖХВР). Предполагаемую структуру подтверждают фрагменти-рующим МС-анализом. HRMS m/z: вычислено для C20H28N2O2 (М)+, 328,2151, найдено 328,2142. Стадия 2. 2-[2-(2-Диизопропиламиноэтокси)пиридин-3-илокси]этанол. Указанное в заголовке соединение получают, исходя из (2-{[3-(бензилокси)пиридин-2 - 31 - 008148 ил]окси}этил)диизопропиламина (со стадии 1; 5,0 г, 15,2 ммоль), используя методику, приведенную в пример 1, стадия 3. Что приводит к получению 1,8 г (42%) указанного в заголовке соединения в виде светло-коричневого масла. Чистота 91% (ЖХВР). Предполагаемую структуру подтверждают фрагменти-рующим МС-анализом. HRMS m/z: вычислено для C15H26N2O3 (М)+, 282,1943, найдено 282,1948. Стадия 3. N,N-Диизопропил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2Н-[1,2']бипиразинил-3'-илокси)этокси]пиридин-2-илокси)этил)аминацетат. Указанное в заголовке соединение получают, исходя из 2-[2-(2-диизопропиламиноэтокси)пиридин-3-илокси] этанола (1,52 г, 5,30 ммоль) и (2R)-1-(3-хлор-2-пиразинил)-2-метилпиперазина* (1,24 г, 5,83 ммоль), используя методику, приведенную в примере 1, стадия 4. Сырой продукт очищают хроматографией на колонке с диоксидом кремния, используя смесь СНС13/МеОН/водный концентрированный NH3 (90:10:0,2 с последующим соотношением 80:20:0,3) в качестве элюента. Растворитель из очищенных объединенных фракций выпаривают при пониженном давлении, остаток растворяют в диэтиловом эфире и добавляют НОАс в диэтиловом эфире. После выдерживания 15 ч в холодильнике белые кристаллы собирают фильтрованием и сушат (60°С, 1 мм Hg), получают 1,5 г (56%) указанного в заголовке соединения: т. пл. 87°С. Чистота 99% (ЖХВР). Предполагаемую структуру подтверждают фрагментирующим МС-анализом. HRMS m/z: вычислено для C24H38N6O3 (M)+, 458,3005, найдено 458,2988. *Получен, как описано в WO 00/76984, пример 192, стадия 2. Пример 3. N,N-Диметил-2-[(3-{2-[(3-пиперазин-1-илпиразин-2-ил)окси]этокси}пиридин-2-ил)окси]этанамин-трифторацетат. К раствору трет-бутил-4-(3-хлорпиразин-2-ил)пиперазин-1-карбоксилата* (45 мг, 0,15 ммоль) и 2-({2-[2-(диметиламино)этокси]пиридин-3-ил}окси)этанола (по примеру 1, стадия 3; 37 мг, 0,16 ммоль) в 4 мл сухого метилтрет-бутилового эфира добавляют 0,2 мл 1,0М трет-бутилата калия в третбутаноле и смесь перемешивают при комнатной температуре в течение одной недели. Реакционную смесь гасят 2 мл воды. Органическую фазу промывают 3х2 мл 1,0М NaOH и 2 мл насыщенного раствора соли, сушат (MgSO4) и концентрируют при пониженном давлении. Остаток очищают хроматографией с обращенной фазой. Очищенный продукт концентрируют, повторно растворяют в 3 мл хлороформа и обрабатывают 0,2 мл трифторуксусной кислоты в течение ночи. Растворитель удаляют при пониженном давлении, получают 46 мг (0,092 ммоль, 61%) указанного в заголовке соединения в виде масла. Чистота по ЖХ-УФ 100%. HRMS m/z: вычислено для Qtfl^NO (М)+, 388,2223, найдено 388,2217. *Получен, как описано в WO 00/76984, пример 52, стадия 1. Пример 4 (промежуточный продукт). 2-Хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин. Смесь 2-хлор-3-гидроксипиридина (5,00 г, 38,6 ммоль), 2-(2-бромэтокси)тетрагидро-2-пирана (5,85 мл, 38,6 ммоль) и карбоната калия (6,40 г, 46,3 ммоль) в 200 мл ацетонитрила нагревают до температуры кипения с обратным холодильником в течение ночи. Реакционную смесь фильтруют, концентрируют при пониженном давлении и повторно растворяют в 300 мл этилацетата. Органическую фазу промывают 3 х100 мл NaOH и 100 мл насыщенного раствора соли, сушат (MgSO4) и концентрируют при пониженном давлении. Остаток очищают флэш-хроматографией на колонке с диоксидом кремния, получают 7,21 г (28,0 ммоль, 73%) указанного в заголовке соединения в виде желтого масла. Чистота по ЖХ-УФ 100%. МС m/z 258 (М+1)+, выч. 258 (М+1)+. Пример 5 (промежуточный продукт). трет-Бутил-(3R)-4-(3 -хлорпиразин-2-ил)-3 -метилпиперазин-1-карбоксилат.* К раствору 2-хлор-3-[(2R)-2-метилпиперазин-1-ил]пиразина** (1,59 г, 7,48 ммоль) в 200 мл ацето-нитрила добавляют Ьос-ангидрид (1,63 г, 7,48 ммоль), порциями, за период 1 ч. Раствор перемешивают при комнатной температуре в течение ночи, гасят 10 мл воды и концентрируют. Остаток повторно растворяют в 200 мл этилацетата, промывают 100 мл 1,0М K2CO3, 100 мл воды и 100 мл насыщенного раствора соли, сушат (MgSO4) и концентрируют, получают 1,70 г (5,43 ммоль, 73%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 313 (М+1)+, выч. 313 (М+1)+. *Описан в WO 00/76984, пример 172, стадия 2. **Описан в WO 00/76984, пример 192, стадия 2. Пример 6. 2-[(2R)-2-Метилпиперазин-1-ил]-3-[2-({2-[( 1-метилпиперидин-4-ил)окси]пиридин-3-ил}окси)это-кси]пиразинтрифторацетат. Стадия 1: 2-({2-[(1-Метилпиперидин-4-ил)окси]пиридин-3-ил}окси)этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 4-гидрокси-^метилпиперидина (67 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в третбутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3x2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3x3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3x2 мл этилацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 62 мг (0,25 ммоль, 63%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС - 32 - 008148 m/z 253 (М+1)+, выч. 253 (М+1)+. Стадия 2. 2-[(R)-2-Метилпиперазин-1-ил]-3-[2-({2-[(1-метилпиперидин-4-ил)окси]пиридин-3-ил} окси)этокси]пиразинтрифторацетат. К раствору 2-({2-[(1-метилпиперидин-4-ил)окси]пиридин-3-ил}окси)этанола (со стадии 1; 30 мг, 0,12 ммоль) и 1,0М трет-бутилата калия в трет-бутаноле (0,15 мл, 0,15 ммоль) в 4 мл сухого толуола добавляют трет-бутил-(3R)-4-(3-хлорпиразин-2-ил)-3-метилпиперазин-1-карбоксилат (по примеру 5; 31 мг, 0,10 ммоль) в 1 мл толуола. Смесь встряхивают при комнатной температуре в течение 2 дней. Реакционную смесь гасят 2 мл воды. Органическую фазу промывают 3x2 мл воды и 2 мл насыщенного раствора соли и концентрируют при пониженном давлении. Остаток очищают хроматографией с обращенной фазой. Очищенный продукт концентрируют, повторно растворяют в 1 мл хлороформа и обрабатывают 0,2 мл трифторуксусной кислоты в течение 1 ч. Растворитель удаляют при пониженном давлении, получают 36 мг (0,066 ммоль, 66%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ- УФ 100%. HRMS m/z: вычислено для C22H32N6O3 (М)+, 428,2536, найдено 428,2546. Пример 7. 2-[(2R)-2-Метилпиперазин-1-ил]-3-(2-{ [2-(2-пирролидин-1-илэтокси)пиридин-3 -ил]окси}это-кси)пиразинтрифторацетат. Стадия 1: 2-{[2-(2-Пирролидин-1-илэтокси)пиридин-3-ил]окси}этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 1-(2-гидроксиэтил)пирролидина (68 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в трет-бутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3х2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3х3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3x2 мл этил-ацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 71 мг (0,28 ммоль, 72%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 253 (М+1)+, выч. 253 (М+1)+. Стадия 2. 2-[(2R)-2-Метилпиперазин-1-ил]-3-(2-{ [2-(2-пирролидин-1-илэтокси)пиридин-3 -ил]ок-си} этокси)пиразинтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-{[2-(2-пирролидин-1-илэтокси)пиридин-3-ил]окси}этанол (со стадии 1; 36 мг, 0,14 ммоль), получают 37 мг (0,069 ммоль, 69%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 100%. HRMS m/z: вычислено для C22H32N6O3 (М)+, 428,2536, найдено 428,2551. Пример 8. N,N-Диметил-4-({3-[2-({3-[(2R)-2-метилпиперазин-1ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)бутан-1-амин-трифторацетат. Стадия 1: 2-({2-[4-(Диметиламино)бутокси]пиридин-3-ил}окси)этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 4-(диметиламино)-1-бутанола (77 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в трет-бутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3x2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3x3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3x2 мл этилацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 55 мг (0,22 ммоль, 55%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 255 (М+1)+, выч. 255 (М+1)+. Стадия 2: N,N-Диметил-4-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пи-ридин-2-ил} окси)бутан-1-аминтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-({2-[4-(диметиламино)бутокси]пиридин-3-ил} окси)этанол (со стадии 1; 29 мг, 0,11 ммоль), получают 34 мг (0,062 ммоль, 62%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 100%. HRMS m/z: вычислено для C22H34N6O3 (M)+, 4 30,2 692, найдено 430,2695. Пример 9. 2-[(2R)-2-Метилпиперазин-1-ил]-3-[2-({2-[2-(1-метилпирролидин-2-ил)этокси]пиридин-3-ил}ок-си)этокси]пиразинтрифторацетат. Стадия 1: 2-({2-[2-(1-Метилпирролидин-2-ил)этокси]пиридин-3-ил}окси)этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 1-метил-2-пирролидинэтанола (79 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в трет-бутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3 х2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3x3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3х2 мл этилацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 55 мг (0,21 - 33 - 008148 ммоль, 53%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 267 (М+1)+, выч. 267 (М+1)+. Стадия 2. 2-[(2R)-2-Метилпиперазин-1 -ил]-3-[2-({2-[2-(1 -метилпирролидин-2-ил)этокси]пиридин-3 -ил} окси)этокси]пиразинтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-({2-[2-(1-метилпирролидин-2-ил)этокси]пиридин-3-ил}окси)этанол (со стадии 1; 28 мг, 0,11 ммоль), получают 33 мг (0,059 ммоль, 59%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 100%. HRMS m/z: вычислено для C23H34N6O3 (М)+, 442,2692, найдено 442,2681. Пример 10. N,N-Метил-N-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1 -ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)этил]пропан-2-аминтрифторацетат. Стадия 1: 2-[(2-{2-[Изопропил(метил)амино]этокси}пиридин-3-ил)окси]этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 2-(№метил^-изопропиламино)этанола (68 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в трет-бутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3х2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3x3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3x2 мл этил-ацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 75 мг (0,30 ммоль, 76%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 255 (М+1)+, выч. 255 (М+1)+. Стадия 2: N-Метил-N-[2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)эток-си]пиридин-2-ил}окси)этил]пропан-2-аминтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-[(2-{2-{изопропил(ме-тил)амино]этокси}пиридин-3-ил)окси]этанол (со стадии 1; 40 мг, 0,16 ммоль), получают 38 мг (0,070 ммоль, 70%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 100%. HRMS m/z: вычислено для C22H34N6O3 (М)+, 430,2692, найдено 430,2700. Пример 11. N,N-Диметил-3 -({3-[2-({3-[(2R)-2-метилпиперазин-1 -ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)пропан-1-амин-трифторацетат. Стадия 1: 2-({2-[3-(Диметиламино)пропокси]пиридин-3-ил}окси)этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4, 100 мг, 0,39 ммоль), 3-диметиламино-1-пропанола (69 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в третбутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3x2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3x3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3х2 мл этилацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 67 мг (0,28 ммоль, 71%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 241 (М+1)+, выч. 241 (М+1)+. Стадия 2: N,N-Диметил-3-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пи-ридин-2-ил} окси)пропан-1-аминтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-({2-[3-(диметиламино)пропокси]пиридин-3-ил}окси)этанол (со стадии 1; 31 мг, 0,13 ммоль), получают 38 мг (0,072 ммоль, 72%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 95%. HRMS m/z: вычислено для C21H32N6O3 (М)+, 416,2536, найдено 416,2523. Пример 12. 2-[(2R)-2-Метилпиперазин-1-ил]-3-(2-{[2-(пиперидин-3-илметокси)пиридин-3-ил]окси}этокси)пи-разинтрифторацетат. Стадия 1: 2-{[2-(Пиперидин-3-илметокси)пиридин-3-ил]окси}этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 3-пиперидинметанола (65 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в трет-бутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3х2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3x3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3x2 мл этилацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 52 мг (0,21 ммоль, 53%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 253 (М+1)+, выч. 253 (М+1)+. Стадия 2: 2-[(2R)-2-Метилпиперазин-1-ил]-3-(2-{[2-(пиперидин-3-илметокси)пиридин-3-ил]ок-си} этокси)пиразинтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-{[2-(пиперидин-3-илметокси)пиридин-3 - 34 - 008148 ил]окси}этанол (со стадии 1; 27 мг, 0,11 ммоль), получают 37 мг (0,069 ммоль, 69%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 95%. HRMS m/z: вычислено для C22H32N6O3 (М)+, 428,2536, найдено 428,2543. Пример 13. N,N,2-Триметил-1-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)пропан-2-аминтрифторацетат. Стадия 1: 2-({2-[2-(Диметиламино)-2-метилпропокси] пиридин-3-ил}окси)этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 2-(диметиламино)-2-метил-1-пропанола (68 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в трет-бутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3 х 2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3х3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3х2 мл этил-ацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 79 мг (0,31 ммоль, 80%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 255 (М+1)+, выч. 255 (М+1)+. Стадия 2: ^^2-Триметил-1 -({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)эток-си]пиридин-2-ил}окси)пропан-2-аминтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-({2-[2-(диметиламино)-2-метилпропокси]пиридин-3-ил}окси)этанол (со стадии 1; 38 мг, 0,15 ммоль), получают 47 мг (0,086 ммоль, 86%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 95%. HRMS m/z: вычислено для C22H34N6O3 (М)+, 430,2692, найдено 430,2700. Пример 14. 2-[(2R)-2-Метилпиперазин-1-ил]-3-{2-[(2-{[(2S)-1-метилпирролидин-2-ил]метокси}пиридин-3-ил)окси]этокси}пиразин, трифторацетат. Стадия 1: 2-[(2-{ [(2S)-1-Метилпирролидин-2-ил]метокси}пиридин-3-ил)окси]этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), ^)-(-)-2-гидроксиметил-1-метилпирролидина (69 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в третбутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3x2 мл воды и 2 мл насыщенного раствора соли. Органическую фазу встряхивают при 50°С с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3х3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3х2 мл этилацетата. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 78 мг (0,31 ммоль, 79%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 95%. МС m/z 253 (М+1)+, выч. 253 (М+1)+. Стадия 2: 2-[(2R)-2-Метилпиперазин-1 -mi]-3-{2-[(2-{[(2S)-1 -метилпирролидин-2-ил]метокси}пири-дин-3-ил)окси]этокси}пиразинтрифторацетат. Следуют методике примера 6, стадии 2, используя 2-[(2-{[(2S)-1-метилпирролидин-2-ил]метокси}пиридин-3-ил)окси]этанол (со стадии 1; 37 мг, 0,15 ммоль), получают 39 мг (0,071 ммоль, 71%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 95%. HRMS m/z: вычислено для C22H32N6O3 (М)+, 428,2536, найдено 428,2523. Пример 15. [2-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этил]амин-трифторацетат. Стадия 1: трет-Бутил-(2-{[3-(2-Гидроксиэтокси)пиридин-2-ил]окси}этил)карбамат. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 2-аминоэтанола (35 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в третбутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3х2 мл 1,0М NaOH и 1 мл насыщенного раствора соли. Добавляют дитрет-бутилдикарбонат (94 мг, 0,43 ммоль) и реакционную смесь встряхивают в течение 2 ч и промывают 2х2 мл NaOH и затем 2х2 мл воды. Органическую фазу встряхивают с 4 мл 2,0М уксусной кислоты в течение 1 недели, промывают 4х2 мл воды, 2х2 мл 1,0М NaOH и 2 мл насыщенного раствора соли, сушат (MgSO4) и концентрируют при пониженном давлении, получают 53 мг (0,18 ммоль, 46%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 90%. МС m/z 299 (М+1)+, выч. 299 (М+1)+. Стадия 2: [2-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)этил]аминтрифторацетат. К раствору трет-бутил-(2-{[3-(2-гидроксиэтокси)пиридин-2-ил]окси}этил)карбамата (со стадии 1; 4 4 мг, 0,15 ммоль) и 0,22 мл 1,0М трет-бутилата калия в трет-бутаноле в 4 мл сухого метил-трет-бутилового эфира добавляют трет-Бутил-(3R)-4-(3-хлорпиразин-2-ил)-3-метилпиперазин-1-карбоксилат (по примеру 5; 47 мг, 0,15 ммоль) и смесь встряхивают при комнатной температуре в течение 2 дней. Реакционную смесь гасят 2 мл воды. Органическую фазу промывают 3x2 мл воды и 2 мл насыщенного раствора соли и концентрируют при пониженном давлении. Остаток очищают хроматографией с обра - 35 - 008148 щенной фазой. Очищенный продукт концентрируют, повторно растворяют в 2 мл хлороформа и обрабатывают 0,2 мл трифторуксусной кислоты в течение 2 ч. Растворитель удаляют при пониженном давлении, получают 50 мг (0,10 ммоль, 67%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 100%. HRMS m/z: вычислено для C18H26N6O3 (M)+, 374,2066, найдено 374,2072. Пример 16. N,N-Метил-2-({3-[2-({3-[(2R)-2-метилпиперазин-1 -ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)этанаминтрифторацетат. Стадия 1: 2-({2-[2-(Метиламино)этокси)пиридин-3-ил}окси)этанол. Раствор 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 100 мг, 0,39 ммоль), 2-(метиламино)этанола (47 мкл, 0,58 ммоль) и 1,0М трет-бутилата калия в третбутаноле (0,8 мл, 0,80 ммоль) в 4 мл толуола нагревают до 100°С в течение 1 дня. Органическую фазу промывают 3х2 мл 1,0 М NaOH и 1 мл насыщенного раствора соли. Органическую фазу встряхивают с 4 мл 2,0М уксусной кислоты в течение 2 дней. Водную фазу промывают 3х3 мл этилацетата, делают основной путем добавления гидроксида калия, насыщают хлоридом натрия и экстрагируют 3x2 мл хлороформа. Органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении, получают 12 мг (0,056 ммоль, 14%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ 90%. МС m/z 213 (М+1)+, выч. 213 (М+1)+. Стадия 2: N,N-Meтил-2-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пири-дин-2-ил} окси)этанаминтрифторацетат. К раствору 2-({2-[2-(метиламино)этокси]пиридин-3-ил}окси)этанола (со стадии 1; 12 мг, 0,056 ммоль) и 0,15 мл 1,0М трет-бутилата калия в трет-бутаноле в 4 мл сухого метил-трет-бутилового эфира добавляют трет-Бутил-(3R)-4-(3-хлорпиразин-2-ил)-3-метилпиперазин-1-карбоксилат (по примеру 5; 18 мг, 0,056 ммоль) и смесь встряхивают при комнатной температуре в течение 3 дней. Реакционную смесь гасят 2 мл 1,0М NaOH. Органическую фазу промывают 3 х 2 мл 1,0М NaOH и 1 мл насыщенного раствора соли и концентрируют при пониженном давлении. Остаток очищают хроматографией с обращенной фазой. Очищенный продукт концентрируют, повторно растворяют в 1 мл хлороформа и обрабатывают 0,2 мл трифторуксусной кислоты в течение 1 ч. Растворитель удаляют при пониженном давлении, получают 32 мг (количественный выход) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ 100%. HRMS m/z: вычислено для C19H28N6O3 (M)+, 388,2223, найдено 388,2231. Пример 17. 2-{2-[{2-[2-(Диметиламино)этокси]пиридин-3-ил}окси]этокси}-3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин. К раствору 2-{2-[{2-[2-(диметиламино)этокси]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпи-перазин-1-ил]пиразина (по примеру 1; 0,48 г, 1,19 ммоль) в 1,2-дихлорэтане (4 мл) добавляют триацеток-сиборгидрид натрия (1,3 г, 6,2 ммоль) и 37% водный формальдегид (0,072 г, 2,4 ммоль), слабо экзотермическую реакционную смесь перемешивают при температуре окружающей среды в течение ночи. Добавляют воду и смесь делают основной (рН> 13) добавлением 8М NaOH. После перемешивания в течение 5 мин фазы разделяют и водную фазу экстрагируют дважды СНС13. Объединенные органические фазы сушат (MgSO4) и растворитель удаляют при пониженном давлении. Полученное масло очищают хроматографией на колонке с диоксидом кремния (80 мм, вн.д. = 30 мм), используя смесь СНС13/МеОН/№14ОН (95:5:0,2; 100 мл, с последующим соотношением 90:10:0,2) в качестве элюента, получают 0,33 г (67%) указанного в заголовке соединения в виде бесцветного масла. HRMS m/z: вычислено для C21H32N6O3 (М)+, 416,2536, найдено 416,2523. Пример 18. 2-[2-(2-[2-(Диметиламино)этокси]фенокси)этокси]-3-[(2R)-2-метилпиперазин-1-ил]пиразин. Стадия 1: №{2-[2-(Бензилокси)фенокси]этил}^^-диметиламингидрохлорид.* Смесь 2-(бензилокси)фенола (15,2 г, 75,9 ммоль), №(2-хлорэтил)-^^диметиламингидрохлорида (16,4 г, 114 ммоль) и карбоната калия (55 г, 0,40 моль) в сухом ацетоне (200 мл) нагревают до температуры кипения с обратным холодильником. Спустя 3 дня (50% конверсия по ЖХВР) твердые вещества фильтруют, растворитель удаляют при пониженном давлении и оставшееся масло распределяют между СНС13/0,5М NaOH. Органическую фазу промывают однократно водой и сушат. Органическую фазу (200 мл) фильтруют через слой диоксида кремния (60х60 мм), промывают СНС13 (100 мл) и затем СНС13/МеОН (95:5; 500 мл). Очищенные фракции упаривают при пониженном давлении, получают 7,7 г указанного в заголовке соединения, в форме свободного основания, в виде светло-коричневого масла. Данный продукт растворяют в диэтиловом эфире и добавляют смесь HCl/диэтиловый эфир для получения хлористо-водородной соли, что дает 2,28 г (47%) указанного в заголовке соединения в виде белых кристаллов: т.пл. 144°С. HRMS m/z: вычислено для C17H21NO2 (М)+, 271,1572, найдено 271,1569. *Описан в Bull. Soc. Chim. Fr. 1935, 1737-1741. Стадия 2: 2-[2-(Диметиламино)этокси]фенол.* К раствору №{2-[2-(бензилокси)фенокси]этил}^^-диметиламингидрохлорида (со стадии 1; 7,60 г, 28,0 ммоль) в МеОН (80 мл) добавляют 10% Pd/C (0,8 г) и смесь гидрируют при 70 фунт/кв. дюйм и комнатной температуре в течение 2 ч. Реакционную смесь фильтруют через подушку из Celite(r) и диоксида - 36 - 008148 кремния. Затем растворитель удаляют при пониженном давлении, получают 5,43 г (количественный выход) указанного в заголовке соединения в виде не совсем белых кристаллов: т. пл. 220°С. HRMS m/z: вычислено для C10H15NO2 (M)+, 181,1103 Найдено 181,1105. Соответствующая хлористо-водородная соль описана в Bull. Soc. Chim. Fr. 1935, 1737-1741. Стадия 3: 2-{2-[2-(диметиламино)этокси]фенокси}этанол. К сухому ДМФА (50 мл) добавляют 2-[2-(диметиламино)этокси]фенол (со стадии 1; 5,4 г, 28,0 ммоль), этиленкарбонат (3,20 г, 36,4 ммоль) и карбонат калия (3,9 г, 28 ммоль) и смесь нагревают до 155°С в течение 1 ч 30 мин. Растворитель из фильтрованного раствора выпаривают при пониженном давлении и полученный остаток растворяют в СНС13 (50 мл) и фильтруют через слой диоксида кремния (50х50 мм), используя СНС13 (50 мл) и затем смесь СНС13/МеОН (95:5) в качестве элюентов. Растворители из очищенных фракций удаляют при пониженном давлении, получают 4,8 г (76%) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C12H19NO3 (M)+, 225,1365, найдено 225,1363. Стадия 4: 2-[2-(2-[2-( Диметиламино)этокси] фенокси)этокси] -3-[(2R)-2-метилпиперазин-1-ил]пиразин. К раствору 2-{2-[2-(диметиламино)этокси]фенокси}этанола (со стадии 3; 0,82 г, 3,6 ммоль) в сухом ДМФА (25 мл) добавляют трет-бутилат калия (0,59 г, 5,3 ммоль) и смесь перемешивают при комнатной температуре в течение 10 мин. К смеси добавляют за одну порцию 2-хлор-3-[(2R)-2-метилпиперазин-1-ил]пиразин* (0,70 г, 3,3 ммоль) в ДМФА (5 мл) и реакционную смесь перемешивают при 55°С в течение 2 ч. Добавляют ложечку диоксида кремния, растворитель отделяют фильтрованием и выпаривают растворитель при пониженном давлении. Сырой продукт очищают на колонке с диоксидом кремния (100 мм, вн.д. =30 мм), используя смесь CHCl3/MeOH/NH4OH (95:5:0,2; 100 мл, с последующим соотношением 90:10:0,2) в качестве элюента, получают 0,80 г (60%) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C21H31N5O3 (M)+, 401,2427, найдено 401,2414. *Описан в WO 00/76984, пример 192, стадия 2. Пример 19. 2-{2-[(2-{[2-(Диметиламино)этокси]метил}пиридин-3-ил)окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. Стадия 1: {3-[2-(Тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}метанол. Суспензию 2-(гидроксиметил)пиридин-3-олгидрохлорида 85% чистоты (24,9 г, 130 ммоль) и карбоната калия (60 г, 434 ммоль) в ацетонитриле (200 мл) нагревают до температуры кипения с обратным холодильником в течение 15 мин, после чего добавляют за одну порцию 2-(2-бромэтокси)тетрагидро-2H-пиран (32,9 г, 160 ммоль) и продолжают нагревание в течение ночи. Твердые вещества фильтруют и растворитель удаляют при пониженном давлении, полученное масло очищают хроматографией на колонке с диоксидом кремния (100 мм, вн.д. = 60 мм), используя СНС13 в качестве элюента с последующим добавлением CHCl3/MeOH/NH4OH (95:5:0.2) получают 28,4 г (93%) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C13H19NO4 (М)+, 253,1314, найдено 253,1326. Стадия 2: {3-[2-(Тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}метилметансульфонат. К охлажденному льдом раствору {3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}метанола (со стадии 1; 3,39 г, 13,4 ммоль) и триэтиламина (1,95 г, 19,3 ммоль) в сухом DCM (25 мл) в атмосфере N2 добавляют раствор метансульфонового ангидрида в DCM (10 мл) за период 5 мин. Смесь перемешивают при 0°С в течение 1 ч при комнатной температуре. Добавляют воду (10 мл) и разделяют фазы. Органическую фазу промывают однократно насыщенным раствором соли, сушат (MgSO4) и растворитель удаляют при пониженном давлении, получают 4,50 г (количественный выход) слегка красноватого масла, которое темнеет при хранении. Сырой продукт используют непосредственно на следующей стадии без дополнительной очистки. Стадия 3: N-(2-{ [3-(2-(Тетрагидро-2H-пиран-2-илокси)этокси)пиридин-2-ил]метокси}этил)-N,N-диметиламин. К раствору 2-(^№диметиламино)этанола (0,84 г, 9,4 ммоль) в сухом диоксане (30 мл) добавляют трет-бутилат калия (0,92 г, 8,2 ммоль) и смесь перемешивают при комнатной температуре в течение 20 мин, по прошествии указанного времени добавляют раствор {3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}метилметансульфоната (со стадии 2; 2,1 г, 6,3 ммоль) в диоксане (10 мл). Реакционную смесь, вначале слабо экзотермическую, перемешивают при температуре окружающей среды в течение ночи. Растворитель из реакционной смеси выпаривают при пониженном давлении и полученное масло распределяют между СНС13/вода. Водную фазу экстрагируют однократно СНС13, объединенные органические фазы сушат (MgSO4) и растворитель вновь выпаривают. Полученное масло очищают хроматографией на колонке с диоксидом кремния (100 мм, вн.д. =30 мм), используя первоначально 100% СНС13 (100 мл) с последующим использованием смеси CHC13/MeOH/NH4OH (95:5:0,2; 100 мл, и затем 90:10:0,2), получают 0,74 г (36%) указанного в заголовке соединения в виде коричневого масла. HRMS m/z: вычислено для C17H28N2O4 (М)+, 324,2049, найдено 324,2042. - 37 - 008148 Стадия 4: 2-[(2-{[2-(Диметиламино)этокси]метил}пиридин-3-ил)окси]этанол. Раствор N-(2-{ [3 -(2-(тетрагидро-2H-пиран-2-илокси)этокси)пиридин-2-ил]метокси}этил)-N,N-диметиламина (со стадии 3; 0,69 г, 2,13 ммоль) в 2М НОАс (20 мл) перемешивают при 50°С в течение двух дней. Реакционную смесь промывают СНС13 (х3), насыщают хлоридом натрия, делают основной путем добавления 8 М NaOH и экстрагируют СНС13 (х3). Растворитель из объединенных органических фаз удаляют при пониженном давлении, получают 0,47 г (92%) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C12H20N2O3 (M)+, 240,1474, найдено 240,1476. Стадия 5: 2-{2-[(2-{[2-(Диметиламино)этокси]метил}пиридин-3-ил)окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. Следуют методике примера 18, стадии 4, исходя из 2-хлор-3-[(2R)-2-метилпиперазин-1-ил]пиразина* (0,27 г, 1,28 ммоль) и 2-[(2-{[2-(диметиламино)этокси]метил}пиридин-3-ил)окси]этанола (со стадии 4; 0,28 г, 1,16 ммоль). Сырой продукт очищают на колонке с диоксидом кремния (100 мм, вн.д. = 30 мм), используя смесь СНС13/МеОНЛМН4ОН (80:20:0,5; 200 мл, с последующим соотношением 60:40:1; 100 мл, и затем 50:50:1) в качестве элюента, получают 0,25 г (51%) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C21H32N6O3 (М)+, 417,2536, найдено 417,2541. *Описан в WO 00/76984, пример 192, стадия 2. Пример 20. 2-{2-[{2-[(1z)-3-(Диметиламино)проп-1-енил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпипе-разин-1-ил]пиразин. Стадия 1: 3-[2-(Тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-карбальдегид. В трехгорлую круглодонную колбу, содержащую сухой DCM (500 мл), охлажденный до -78°С в атмосфере N2, добавляют оксалилхлорид (20,0 мл, 157 ммоль) с последующим осторожным добавлением по каплям ДМСО (24,5 г, 315 ммоль). К охлажденной реакционной смеси осторожно добавляют {3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}метанол (по примеру 19, стадия 1; 21,0 г, 82,9 ммоль) в DCM (25 мл), температура не должна превышать -65°С. После добавления реакционную смесь перемешивают при -78°С в течение 1 ч, по прошествии указанного времени добавляют TEA (50,2 г, 4 97 ммоль) и смесь перемешивают еще 30 мин при температуре окружающей среды. К смеси добавляют ледяную воду (400 мл) и органическую фазу промывают Н^, насыщенный раствор соли сушат (MgSO4), коричневую органическую фазу фильтруют через подушку (60x40 мм) из диоксида кремния и окончательно растворитель удаляют при пониженном давлении, получают коричневое масло. Гидратированный альдегид растворяют в толуоле (150 мл) и нагревают в течение 3 ч в условиях Дина-Старка, получают 19,9 г (95%) указанного в заголовке соединения в виде черного масла. HRMS m/z: вычислено для C13H17NO4 (M)+, 251,1158, найдено 251,1153. Стадия 2: N,N-диметил-N-((2z)-3-{3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}проп-2-енил)амин. К суспензии [2-(диметиламино)этил](трифенил)фосфонийбромида (32,1 г, 77,4 ммоль) в сухом ТГФ (150 мл) добавляют раствор трет-бутилата калия (9,4 г, 83,7 ммоль) в сухом t-BuOH (100 мл). Суспензию обрабатывают ультразвуком в течение 15 мин, после чего к желтой суспензии добавляют раствор 3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-карбальдегида (со стадии 1; 18,3 г, 72,8 ммоль) в ТГФ (30 мл) и перемешивают при комнатной температуре в течение 1 ч, и затем еще один час при 60°С. Растворитель удаляют при пониженном давлении и остаток смешивают с водой (0,8 л) и доводят рН до 3-4 с помощью НОАс (-10 мл), после чего дважды экстрагируют СНС13. Водную фазу делают основной и экстрагируют СНС13 (х3), объединенные органические фазы сушат (MgSO4) и растворитель удаляют при пониженном давлении. Сырой продукт, содержащий цис- и транс-* изомеры разделяют с помощью ЖХВР на колонке YMC ODS-AQ (30х250 мм) при различных градиентах 0,1% ТФУ в смеси во-да/CH3CH. Цис-изомер выделяют в виде светло-желтого масла (2,33 г, 10%). HRMS m/z: вычислено для C17H26N2O3 (М)+, 306,1943, найдено 306,1942. * Соответствующий транс- изомер описан в примере 21, стадия 1. Стадия 3: 2-({2-[(1z)-3-(Диметиламино)проп-1-енил]пиридин-3-ил}окси)этанол. Следуют методике примера 19, стадия 4, используя N,N-диметил-N-((2z)-3-{3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}проп-2-енил)амин (со стадии 2; 1,3 г, 4,2 ммоль), получают 0,86 г (91%) указанного в заголовке соединения в виде бесцветного масла, кристаллизующегося при стоянии: т.пл. 71°С. HRMS m/z: вычислено для C12H18N2O2 (M)+, 222,1368, найдено 222,1363. Стадия 4: 2-{2-[{2-[(1z)-3-(Диметиламино)проп-1-енил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. Следуют методике примера 18, стадия 4, исходя из 2-хлор-3-[(2R)-2-метилпиперазин-1-ил]пиразина* (0,23 г, 1,0 ммоль) и 2-({2-[(1z)-3-(диметиламино)проп-1-енил]пиридин-3-ил}окси)этанола (со стадии 3; 0,24 г, 1,1 ммоль). Сырой продукт очищают на колонке с диоксидом кремния (100 мм, вн.д. = 30 мм), используя смесь CHC13/MeOH/NH4OH (80:20:0,5; 200 мл, с последующим соотношением 60:40:1) в качестве элюента, получают 0,050 г (12%) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C21H30N6O2 (М)+, 398,2430, найдено 398,2438. *Описан в WO 00/76984, пример 192, стадия 2. - 38 - 008148 Пример 21. 2-{2-[{2-[(1E)-3-(Диметиламино)проп-1-енил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпипера-зин-1-ил]пиразин. Стадия 1: NN-диметил-N-((2Е)-3-{3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}проп- 2- енил)амин. Указанное в заголовке транс-изомерное соединение выделяют в виде светло-желтого масла (1,2 г, 5,5%) из реакционной смеси, полученной по примеру 20, стадия 2. HRMS m/z: вычислено для C17H26N2O3 (М)+, 306,1943, найдено 306,1934. Стадия 2: 2-({2-[(1Е)-3-(Диметиламино)проп-1-енил]пиридин-3-ил}окси)этанол. Следуют методике примера 19, стадии 4, используя N,N-диметил-N-((2Е)-3-{3-[2-(тетрагидро-2H-пиран-2-илокси)-этокси]пиридин-2-ил}проп-2-енил)амин (со стадии 1; 1,0 г, 3,3 ммоль), получают 0,83 г (количественный выход) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C12H18N2O2 (M)+, 222,1368, найдено 222,1364. Стадия 3: 2-{2-[{2-[(1E)-3-(Диметиламино)проп-1-енил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. Следуют методике примера 18, стадии 4, исходя из 2-хлор-3-[(2R)-2-метилпиперазин-1-ил]пиразина* (0,30 г, 1,4 ммоль) и 2-({2-[(1Е)-3-(диметиламино)проп-1-енил]пиридин-3-ил}окси)этанола (со стадии 2; 0,32 г, 1,5 ммоль) . Сырой продукт очищают на колонке с диоксидом кремния (100 мм, вн.д. = 30 мм), используя смесь CHC13/MeOH/NH4OH (80:20:0,5; 200 мл, с последующим соотношением 60:40:1) в качестве элюента, получают 0,030 г (5,5%) указанного в заголовке соединения в виде светло-коричневого масла. HRMS m/z: вычислено для C21H30N6O2 (М)+, 398,2430, найдено 398,2433. *0писан в WO 00/76984, пример 192, стадия 2. Пример 22. 2-{2-[{2-[3-(Диметиламино)пропил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. Стадия 1: 2-({2-[3-(Диметиламино)пропил]пиридин-3-ил}окси)этанол. К смеси цис- и транс-изомеров ^№диметил-^((2Е и 2z)-3-{3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}проп-2-енил)амина (по примеру 20, стадия 2; 3,1 г, 10,1 ммоль) в МеОН (50 мл) добавляют 10% Pd/C (0,30 г) и смесь гидрируют в аппарате Парра при комнатной температуре, при 70 фунт/кв.дюйм H2, в течение ночи. Растворитель из фильтрованного раствора удаляют при пониженном давлении и тетрагидропиранил-защитную группу удаляют, используя методику, описанную в примере 19, стадия 4, получают 1,29 г (57%) указанного в заголовке соединения в виде коричневого масла. HRMS m/z: вычислено для C12H20N2O2 (М)+, 224,1525, найдено 224,1521. Стадия 2: 2-{2-[{2-[3-(Диметиламино)пропил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпипе-разин-1-ил]пиразин. Следуют методике примера 18, стадии 4, исходя из 2-хлор-3-[(2R)-2-метилпиперазин-1-ил]пиразина* (0,48 г, 2,28 ммоль) и 2-({2-[3-(диметиламино)пропил]пиридин-3-ил}окси)этанола (со стадии 1; 0,46 г, 2,07 ммоль). Сырой продукт очищают на колонке с диоксидом кремния (100 мм, вн.д. = 30 мм), используя смесь СНС13/МеОН/№г[4ОН (80:20:0,5; 200 мл, с последующим соотношением 60:40:1) в качестве элюента, получают 0,48 г (58%) указанного в заголовке соединения в виде бесцветного масла. HRMS m/z: вычислено для C21H32N6O2 (М)+, 400,2587, найдено 400,2571. *Описан в WO 00/76984 пример 192, стадия 2. Пример 23. {2-[2-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)эток-си]этил}амин-бис(трифторацетат). Стадия 1: трет-Бутил-{2-[2-({3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-ил}окси)это-кси]этил}карбамат. 2-(2-Аминоэтокси)этанол (0,45 г, 4,3 ммоль) и 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин (по примеру 4; 1,0 г, 3,9 ммоль) добавляют к раствору трет-бутилата калия (0,52 г, 4,7 ммоль) в сухом ДМСО (4 мл). Смесь нагревают до 90°С в течение 5 мин. По прошествии указанного времени реакционную смесь охлаждают до температуры окружающей среды. Добавляют ди-трет-бутилдикарбонат (1,1 г, 5,0 ммоль) и полученную смесь перемешивают в течение 1 ч при комнатной температуре. Добавляют пиридин (0,3 мл) и смесь оставляют на ночь при комнатной температуре. Реакционную смесь разбавляют водой (10 мл) и экстрагируют СНС13 (х3), объединенные органические фазы сушат (MgSO4) и растворитель удаляют при пониженном давлении. Оставшееся масло очищают хроматографией на колонке с диоксидом кремния, используя смесь DCM/MeOH (98:2) в качестве элюента, получают 0,76 г (46%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ: система (А) 96%. HRMS m/z: вычислено для C21H34N2O7 (М)+, 426,2366, найдено 426,2355. Стадия 2: трет-Бутил-(3R)-4-[3-(2-{ [2-(2-{2-[(трет-бутоксикарбонил)амино]этокси}этокси)пиридин- 3- ил] окси}этокси)пиразин-2-ил]-3 -метилпиперазин-1 -карбоксилат. трет-Бутил-{2-[2-({3-[2-(тетрагидро-2H-пиран-2-илокси)-этокси]пиридин-2-ил}окси)этокси]этил}ка-рбамат (со стадии 1; 0,74 г, 1,7 ммоль) суспендируют в 2 М НОАс (5 мл) и ацетонитриле (1 мл) и нагревают до - 39 - 008148 50°С в течение двух дней. Раствор нейтрализуют концентрированным водным аммиаком. Добавляют насыщенный раствор соли (3 мл) и смесь экстрагируют СНС13 (х3). Объединенные органические фазы сушат (MgSO4) и растворитель удаляют при пониженном давлении. Оставшееся масло растворяют в сухом ДМСО (10 мл), добавляют трет-бутилат калия (0,36 г, 3,2 ммоль) с последующим добавлением трет-бутил-(3R)-4-(3-хлорпиразин-2-ил)-3-метилпиперазин-1-карбоксилата (по примеру 5; 0,59 г, 1,9 ммоль) и смесь нагревают до 50°С в течение 20 мин. Реакционную смесь разбавляют смесью вода/насыщенный раствор соли (90:10) и экстрагируют СНС13 (х3). Объединенные органические фазы сушат (MgSO4), растворитель удаляют при пониженном давлении и оставшееся масло очищают хроматографией на колонке с диоксидом кремния, используя смесь гексан/EtOAc (70:30) в качестве элюента, получают 0,43 г (40%) указанного в заголовке соединения в виде бесцветного масла. Чистота по ЖХ-УФ: система (А) 100%. HRMS m/z: вычислено для C30H46N6O8 (M)+, 618,3377, найдено 618,3381. Стадия 3: {2-[2-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)этокси]этил}амин-бис-(трифторацетат). Раствор трет-бутил-(3R)-4-[3-(2-{[2-(2-{2-[(трет-бутоксикарбонил)амино]этокси}этокси)пиридин-3-ил]окси}этокси)пиразин-2-ил]-3-метилпиперазин-1-карбоксилата (со стадии 2; 0,405 г, 0,655 ммоль) в смеси DCM/ТФУ (1:1; 4 мл) перемешивают при комнатной температуре в течение ночи. Растворитель удаляют при пониженном давлении и оставшееся масло сушат (1 мм Hg, 40°С) в течение ночи, получают 0,424 г (100%) указанного в заголовке соединения в виде коричневого масла. Чистота по ЖХ-УФ: система (А) 99%, (В) 98%. HRMS m/z: вычислено для C20H30N6O4 (М)+, 418,2329, найдено 418,2337. Пример 24. [6-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)гек-сил]аминтрифторацетат. Стадия 1: трет-Бутиловый эфир (6-{3-[2-(тетрагидро-2Н-пиран-2-илокси)этокси]пиридин-2-илокси} гексил)карбаминовой кислоты. Указанное в заголовке соединение получают по методике примера 23, стадия 1, исходя из 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 1,0 г, 3,9 ммоль) и 6-амино-1-гексанола (0,50 г, 4,3 ммоль). Выход 1,0 г (58%). Стадия 2: [6-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил} окси)гексил]аминтрифторацетат. Указанное в заголовке соединение получают, исходя из трет-бутилового эфира (6-{3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридин-2-илокси}гексил)карбаминовой кислоты (со стадии 1; 1,0 г, 2,3 ммоль), первоначальным удалением тетрагидропиранил-защитной группы и последующим осуществлением взаимодействия с трет-бутил-(3R)-4-(3-хлорпиразин-2-ил)-3-метилпиперазин-1-карбоксилатом (по примеру 5; 0,73 г, 2,3 ммоль) по методике примера 23, стадии 2, с последующим снятием N-Boc-защиты по методике примера 23, стадии 3. Выход 62 мг (6%) . Чистота по ЖХ-УФ: система (А) 97%, (В) 97%. HRMS m/z: вычислено для C22H34N6O3 (М)+, 430,2692, найдено 430,2676. Пример 25. [5-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пен-тил]амин-бис(трифторацетат). Указанное в заголовке соединение получают аналогично примеру 24 путем замены 6-амино-1-гексанола на 5-амино-1-пентанол (1,76 г, 17,0 ммоль). Выход 0,126 г (3%). Чистота по ЖХ-УФ: система (А) 98%, (В) 97%. HRMS m/z: вычислено для C21H32N6O3 (М)+, 416,2536, найдено 416,2547. Пример 26. 5-({3-[2-({3-[(2R)-2,4-Диметилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)-N,N-диметилпентан-1-амин. [5-({3-[2-({3-[(2R)-2-Метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пен-тил]амин-бис(трифторацетат) (по примеру 25; 0,17 г, 0,26 ммоль), 1,2-дихлорэтан (5 мл), 37% водный формальдегид (0,13 г, 1,6 ммоль) и триацетоксиборгидрид натрия (0,66 г, 3,1 ммоль) смешивают и смесь перемешивают при 50°С в течение ночи. Реакционную смесь гасят несколькими каплями 8М NaOH, разбавляют водой и экстрагируют дважды СНС13. Объединенные органические фазы сушат (Hydromatrix) и упаривают при пониженном давлении. Сырое масло очищают, используя препаративную ЖХ-МС-систему (В), получают 36 мг (30%) целевого соединения в виде светло-коричневого масла. Чистота по ЖХ-УФ: система (А) 100%, (В) 100%. HRMS m/z: вычислено для С-ДТ^НА (М)+, 458,3005, найдено 458,3013. Пример 27. 2-[(2R)-2-Метилпиперазин-1-ил]-3-(2-{ [2-(2-пиперазин-1 -илэтокси)пиридин-3 -ил]окси}этокси)пи-разинтрифторацетат. Стадия 1: трет-Бутиловый эфир 4-{2-[3-(2-гидроксиэтокси)пиридин-2-илокси]этил}пиперазин-1-карбоновой кислоты. Указанное в заголовке соединение получают, исходя из 2-хлор-3-[2-(тетрагидро-2H-пиран-2-илокси)этокси]пиридина (по примеру 4; 0,67 г, 2,6 ммоль) и трет-Бутил-4-(2-гидроксиэтил)пиперазин-1-карбоксилата (0,66 г, 2,9 ммоль) по методике примера 23, стадии 1, с последующим удалением тетрагид - 40 - 008148 ропиранил-защитной группы по методике, приведенной в примере 23, стадия 2. Выход 0,36 г (38%). МС (ESI+) для C18H29N3O5 m/z 368,0 (М+Н)+ Стадия 2: 2-[(2R)-2-Метиллиперазин-1-ил]-3-(2-{[2-(2-пиперазин-1-илэтокси)пиридин-3-ил]ок-си}этокси)пиразинтрифторацетат. Указанное в заголовке соединение получают, осуществляя взаимодействие трет-бутилового эфира 4-{2-[3-(2-гидроксиэтокси)пиридин-2-илокси]этил}пиперазин-1-карбоновой кислоты (со стадии 1; 0,367 г, 1,00 ммоль) с трет-бутил-(3R)-4-(3-хлорпиразин-2-ил)-3-метилпиперазин-1-карбоксилатом (по примеру 5; 0,313 г, 1,00 ммоль) по методике примера 23, стадии 2, с последующим удалением N-Boc-защитной группы по методике примера 23, стадии 3. Выход 12 мг (2%). Чистота по ЖХ-УФ: система (А) 80%, (В) 85%. HRMS m/z: вычислено для C22H33N7O3 (М)+, 443,2645 найдено 443,2646. Получение фармацевтической композиции Пример: Получение таблеток Ингредиенты мг/таблетка 1. Активное соединение формулы (I) 10,0 2. Целлюлоза, микрокристаллическая 57,0 3. Кальцийгидрофосфат 15,0 4. Натрийкрахмалгликолят 5,0 5. Диоксид кремния, коллоидный 0,25 6. Стеарат магния 0,75 Активный ингредиент 1 перемешивают с ингредиентами 2, 3, 4 и 5 около 10 мин. Затем добавляют стеарат магния, полученную смесь перемешивают около 5 мин и прессуют в форме таблеток с пленочным покрытием, либо без покрытия. Фармакологические испытания Способность соединения по изобретению связывать или воздействовать на специфические подтипы рецептора 5-НТ может быть определена на основании известных из уровня техники испытаний in vitro и in vivo. Биологическая активность полученных согласно примерам соединений проверена с помощью различных испытаний. Испытания на сродство Сродство к рецептору полученных согласно примерам соединений установлено в конкурентных экспериментах, где способность каждого соединения при последовательном разведении вытеснять 3Н-меченный 5-НТ, связанный с мембранами, полученными из трансфицированной клеточной линии НЕK293, устойчиво экспрессирующей белок рецептора 5-HT2C человека, контролируют с помощью приборов по Scintillation Proximity методике анализа. Неспецифическое связывание определяют, используя 5 мкМ миансерина. Результаты, полученные для типичных соединений по изобретению, представлены ниже. Сродство к связыванию соединениями рецепторов 5-HT2A и 5-HT2B человека в клеточных линиях СНО определяют, используя в качестве радиолигандов 3Н-меченный диэтиламид лизергиновой кислоты (LSD) и 5-НТ, соответственно. Сродство к связыванию соединениями рецепторов 5-HT1A и 5-HT1B человека в клеточных линиях СНО определяют подобным образом, используя в качестве радиолигандов 3Н-меченный 8-гидрокси-2-(ди-н-пропиламино)тетралин (8-OH-DPAT) и 5-НТ, соответственно. Функциональные анализы in vitro Эффективность в качестве агонистов рецептора 5-HT2C для полученных согласно примерам соединений определяют по способности каждого из соединений к мобилизации внутриклеточного кальция в трансфицированных клетках НЕ1С293, стабильно экспрессирующих 5-HT2C рецепторный белок человека, используя образующий хелатные соединения с кальцием флуоресцентный краситель FLUO-3 (Sigma, St. Louis, МО, USA). Способность соединений к мобилизации внутриклеточного кальция на рецепторах 5HT2A и 5-HT2B определяют подобным образом, используя клетки СНО, экспрессирующие рецепторы 5-НТ^ или 5-HT2B. Максимальные функциональные реакции соединений, при 1 мкМ, на рецепторы 5-НТ2а, 5-HT2B и 5-HT2C выражены относительно максимальной реакции 5-НТ (серотонин) при концентрации 1 мкМ. Пример 28. Испытуемым соединением является соединение по примеру 1. Сродство (Ki) определяют, используя три отдельных весовых обработки данных, анализируемых двумя различными приемами, за исключением значений для 5-HT2C, основанных на трех отдельных весовых обработках данных, анализируемых тремя различными приемами (12 индивидуальных значений Ki). EC50 (концентрация, при которой наблюдается половинный максимальный эффект) и эффективность в % определяют из 2-5 измерений. 5-НТ2А 5-НТ2в 5-НТ2с 5-HTiA 5-НТ1в К±(нМ) > 1000 > 1000 800 > 1000 ЕС50 (нМ) 1200 1940 4,2 Эффективность 117 Пример 29. Испытуемым соединением является соединение по примеру 2. Сродство (Ki) определяют, исполь- - 41 - 008148 зуя три отдельных весовых обработки данных. ЕС50 и эффективность в % определяют из 3-4 измерений. 5-НТ2А 5-НТ2в 5-НТ2с 5-НТ1в Ki (нМ) > 1000 > 1000 380 200 ЕС50 (нМ) 260 900 3,9 Эффективность 111 Сродство к рецептору некоторых соединений, описанных в WO 00/76984, приведено ниже. Пример 177 по WO 00/76984 5-НТгд 5-НТ2в 5-НТ2с 5-HTiA 5-НТ1в Ki (нМ) 177 530 517 1548 Эффективность Пример 193 по WO 00/76984 5-НТ2А 5-НТ2в 5-НТ2с 5-НТ1в Ki (нМ) 498 267 155 507 Эффективность 112 Пример 194 по WO 00/76984 5-НТ2А 5-НТ2в 5-НТ2с 5-НТ1А 5-НТ1в Ki (нМ) 234 334 567 > 1000 Эффективность Как следует из сравнения приведенных выше данных, избирательность по отношению к рецептору 5-HT2c (т.е. Ki в отношении 5-HT2c по сравнению с 5-HT2A и 5-НТ2В) соединений по настоящему изобретению неожиданно высока по сравнению с соединениями по WO 00/76984. Сродство к рецептору некоторых соединений, описанных в WO 02/40457, приведено ниже. Пример 2 по WO 02/40457 5-НТ2А 5-НТ2в 5-НТ2с 5-НТ1А 5-НТ1в Ki (нМ) 787 107 Эффективность Пример 5 по WO 02/40457 5-НТ2А 5-НТ2в 5-НТ2с 5-НТ1А 5-НТ1в Ki (нМ) > 1000 2,4 Эффективность Как следует из сравнения приведенных выше данных, избирательность по отношению к рецептору 5-HT2C (т.е. Ki в отношении 5-HT2C по сравнению с 5-НТж, 5-HT1A и 5-HT1B) соединений по настоящему изобретению неожиданно высока по сравнению с соединениями по WO 02/40457. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) Формула (I) , где ПХ равно 2-4, предпочтительно 2; каждый из R и R1 независимо означает Н или СН3; R2 означает Н, Q-Q^Kmi, 2-гидроксиэтил, 2-цианоэтил или тетрагидропиран-2-ил, C1-C4-ацил или C1-C4-алкоксикарбонил; каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород; - 42 - 008148 каждый из X, Y и z независимо означает СН или N; Ai означает О, СН или СН2; A2 означает О, СН или (CH2)n2, где n2 равно целому числу 0-2; Связь между A1 и А2 является простой или двойной связью; A3 означает (СН2)п3, где n3 равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5; А4 означает (СМе2)п4, где п4 равно целому числу 0-1; A5 означает N или О; при условии, что когда A5 представляет собой азот, то А5 замещен только двумя из A6, А7 и A5; когда A5 представляет собой O, то A5 замещен только одним из A6, А7 и A8; каждый из A6 и А7 независимо означает Н, C1-C4-алкил, амино-C2-C4-алкил, N,N^^CrC4-алкиламино-C2-C4-алкил, C3-C6-циклоалкил или вместе с A5 образует насыщенное гетероциклическое кольцо; где насыщенное гетероциклическое кольцо является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N; A8 означает (СН2)п8, где n8 равно целому числу 0-2; A9 означает CH2; или фармацевтически приемлемые соли, сольваты, гидраты, геометрические изомеры, таутомеры, оптические изомеры, N-оксиды и пролекарственные формы указанных соединений. 2. Соединение по п.1, где R0 означает метил. 3. Соединение по одному из пп.1-2, где атом углерода, к которому присоединена указанная метиль-ная группа R0, находится в ^-конфигурации. 4. Соединение по п.1, где R0 означает водород. 5. Соединение по одному из пп.1-4, где R1 означает водород. 6. Соединение по одному из пп.1-5, где X и Y оба означают азот. 7. Соединение по одному из пп.1-6, где R2 означает Н или метил. 8. Соединение по одному из пп.1-7, где все R3-R5 означают Н. 9. Соединение по одному из пп.1-8, где каждый из A6 и А7 независимо означает Н, метил, изопро-пил, 2-этиламин или взятые вместе образуют пирролидиновое или пиперазиновое кольцо. 10. Соединение имеющее формулу (1а) где R0-R5, X, Y и z имеют вышеуказанные значения по одному из пп.1-8, предпочтительно, где z означает N, m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R6 означает NR7R8 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный C1-C4-алкил; или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, где насыщенное гетероциклическое кольцо является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N; R9 означает амино-C2-C4-алкил или N,N-ди-C1-C4-алкиламино-C2-C4-алкил. 11. Соединение по п.10, где R7 и R8 выбраны из группы, включающей Н, метил, изопропил, либо указанные группы образуют вместе с атомом азота, к которому присоединены, пирролидиновый или пи-перазиновый цикл. 12. Соединение по одному из пп.10 или 11, где R9 означает 2-аминоэтил. 13. Соединение по одному из пп.10-12, где указанным соединением является N,N-диметил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2']бипиразинил-3'-илокси)этокси]пири-дин-2-илокси)этил)амин; N,N-диизопропил-(2-(3-[2-(2-(R)-метил-3,4,5,6-тетрагидро-2H-[1,2']бипиразинил-3'-илокси)эток-си]пиридин-2-илокси)этил)-амин; N,N-диметил-2-[(3-{2-[(3-пиперазин-1-илпиразин-2-ил)окси]этокси}пиридин-2-ил)окси]этанамин; Формула (1а) , - 43 - 008148 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(2-пирролидин-1-илэтокси)пиридин-3-ил]окси}этокси)пи-разин; ^^диметил-4-( {3-[2-({3-[(2R)-2-метилпиперазин-1 -ил]пиразин-2-ил} окси)этокси]пиридин-2-ил}окси)бутан-1-амин; N-метил-N- [2-({3-[2-({3-[(2R)-2-метилпиперазин-1 -ил]пиразин-2-ил} окси)этокси]пиридин-2-ил}окси)этил]пропан-2-амин; ^^диметил-3-( {3-[2-({3-[(2R)-2-метилпиперазин-1 -ил]пиразин-2-ил} окси)этокси]пиридин-2-ил}окси)пропан-1-амин; N,N,2-триметил-1-( {3-[2-({3-[(2R)-2-метилпиперазин-1-ил] пиразин-2-ил} окси)этокси]пиридин-2-ил}окси)пропан-2-амин; [2-( {3-[2-({3- [(2R)-2-метилпиперазин-1 -ил] пиразин-2-ил} окси)этокси]пиридин-2-ил} окси)этил]амин; N-метил-2-( {3-[2-( {3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил} окси)этокси]пиридин-2-ил}окси)этанамин; 2-{2-[{2-[2-(диметиламино)этокси]пиридин-3-ил}окси]этокси}-3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин; 2-[2-(2-[2-(диметиламино)этокси]фенокси)этокси]-3-[(2R)-2-метилпиперазин-1-ил]пиразин; {2-[2-({3-[2-( {3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил} окси)этокси]пиридин-2-ил} окси)это-кси]этил}амин; [6-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)гек-сил]амин; [5-({3-[2-({3-[(2R)-2-метилпиперазин-1-ил]пиразин-2-ил}окси)этокси]пиридин-2-ил}окси)пен-тил]амин 5-({3-[2-({3-[(2R)-2,4-диметилпиперазин-1-ил]пиразин-2-ил} окси)этокси]пиридин-2-ил} окси)-N,N-диметилпентан-1-амин; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(2-пиперазин-1-илэтокси)пиридин-3-ил]окси}эток-си)пиразин. 14. Соединение по одному из пп.1-9, имеющее формулу (Ib) R0-R5, X, Y и z имеют значения по одному из пп.1-8, о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R10 означает Н или C1-C4-алкил, предпочтительно Н или метил. 15. Соединение по п.14, где указанным соединением является 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[(1-метилпиперидин-4-ил)окси]пиридин-3-ил}окси)это-кси]пиразинтрифторацетат; 2-[(2R)-2-метилпиперазин-1-ил]-3-[2-({2-[2-(1-метилпирролидин-2-ил)этокси]пиридин-3-ил}ок-си)этокси]пиразинтрифторацета ; 2-[(2R)-2-метилпиперазин-1-ил]-3-(2-{[2-(пиперидин-3-илметокси)пиридин-3-ил}окси}этокси)пи-разинтрифторацетат; 2-[(2R)-2-метилпиперазин-1-ил]-3-{2-[(2-{[(2S)-1-метилпирролидин-2-ил]метокси}пиридин-3-ил)окси]этокси}пиразинтрифторацетат. 16. Соединение имеющее формулу (Ic) Формула (Ib) , где - 44 - 008148 где R0-R5, X, Y и z имеют вышеуказанные значения, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, ориентация относительно двойной связи может быть либо цис, либо транс; каждый из R11 и R12 независимо означает Н или линейный или разветвленный С1-С4-алкил; либо R11 и R12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, где насыщенное гетероциклическое кольцо, является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N. 17. Соединение по п.16, где R11 и R12 оба означают метил. 18. Соединение по одному из пп.16 или 17, где указанным соединением является 2-{2-[{2-[(^}-3-(диметиламино)проп-1 -енил]пиридин-3-ил} окси]этокси}-3-[(2R)-2-метилпипе- разин-1 -ил] пиразин; 2-{2-[{2-[(1E)-3-(диметиламино)проп-1-енил]пиридин-3ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. 19. Соединение имеющее формулу (Id) где R0-R5, X, Y и z имеют вышеуказанные значения, W означает О или CH2; r равно 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1, когда W означает CH2 и, наиболее предпочтительно, когда W означает О; каждый из R13 и R14 независимо означает Н или линейный или разветвленный CrC/галкил; либо R13 и R14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; где насыщенное гетероциклическое кольцо, является неароматическим 4-7-членным кольцом, содержащим атомы углерода и один или два гетероатома, выбираемых из О, S и N. 20. Соединение по п.19, где W означает О, X=N и Y=N. 21. Соединение по п.19, где r=t, W=Qi2, X=N, Y=N, R13=R11 и R14=R12; где t, R11 и R12 имеют значения, указанные для формулы (Ic) по п.16. 22. Соединение по пп.19-21, где R13 и R14 оба означают метил. 23. Соединение по одному из пп.19-22, где указанным соединением является 2-{2-[(2-{ [2-( диметиламино)этокси] метил} пиридин-3 ил)окси] этокси}-3- [(2R)-2-метилпиперазин-1-ил] пиразин или 2-{2-[{2-[3-(диметиламино)пропил]пиридин-3-ил}окси]этокси}-3-[(2R)-2-метилпиперазин-1-ил]пиразин. 24. Соединение по одному из пп.1-23, для применения в терапии человека или животного. 25. Соединение по п.24, где терапия направлена на лечение вызываемого серотонином нарушения или состояния, связанного с рецептором 5-HT2C. 26. Соединение по п.25, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства на Формула (Id), - 45 - 008148 строения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 27. Применение соединения по одному из пп.1-23 при получении лекарственного средства для лечения или предупреждения вызываемого серотонином нарушения или состояния, связанного с рецептором 5-HT2C. 28. Применение по п.27, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 29. Фармацевтическая композиция, включающая соединение по одному из пп.1-23 в качестве активного ингредиента вместе с фармацевтически приемлемым носителем. 30. Способ лечения вызываемого серотонином нарушения или состояния, в частности, связанного с рецептором 5-HT2C, включающий введение нуждающемуся в таком лечении больному эффективного количества соединения по одному из пп.1-23. 31. Способ по п.30, где вызываемое серотонином нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и бу-лимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 32. Способ по одному из п.30 или 31, где больным является человек. 33. Способ по одному из п.30 или 31, где больным является животное. 34. Способ модуляции функции рецептора 5-HT2C, включающих контактирование рецептора с эффективным стимулирующим или ингибирующим, предпочтительно стимулирующим, количеством соединения по одному из пп.1-23. 35. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (II) "ОН R5 N Формула (II), где X1 выбран из F, Cl, Br и I, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, с соединением формулы (III) Формула (III), где Y1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) - 46 - 008148 Формула (IV), где X1 и R3-R5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, НО, (СН2)т. ^СМе2)п Re Формула (Va) , где m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R6 означает NR7R8 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный CrC/галкил; или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R9 означает амино-C2-C4-алкил или N,N-ди-C1-C4-алкиламино-C2-C4-алкил, приводящее к соединению формулы (Via) Формула (Via), где R3-R6, m и n имеют вышеуказанные значения, с) обработку соединения формулы (VIa) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (Vila) Формула (Vila), где R3-R6, m и n имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метилтрет-бутиловый эфир или толуол, - 47 - 008148 Формула (VIII), где каждый из R0 и R1 независимо означает Н или СН3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ris означает галоген, такой как хлор, приводящее к соединению формулы (1а), где X=N и Y=N: Формула (Ia) , где R0-R6, m и n имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R2 в формуле (Ia) после стадии d) означает азотзащитную группу, такую как t-ВОС, тритил и бензил, удалением указанной азот-защитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ia), где R2 означает водород. 36. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (II) Формула (II), где X1 выбран из F, Cl, Br и I, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, с соединением формулы (III) Формула (III), где Y1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (IV) - 48 - 008148 Формула (IV) , где Xl и R3-R5 имеют вышеуказанные значения; b) взаимодействие соединения формулы (IV) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как толуол, где о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; Rl0 означает Н или С1-С4-алкил, предпочтительно Н или метил; приводящее к соединению формулы (VIb) Формула (VIb), где R3-R5 и Rl0, о, р и q имеют вышеуказанные значения, с) обработку соединения формулы (VIb) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (Vllb) где R3-R5 и Rl0, о, р и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как метил-трет-бутиловый эфир или толуол, Формула (Vb), Формула (VIIb), Формула (VIII), - 49 - 008148 где каждый из Ro и Ri независимо означает Н или CH3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ris означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N: Формула (Ib), где R0-R5, R10, о, р и q имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R2 в формуле (Ib) после стадии d) означает азотзащитную группу, такую как t-ВОС, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R2 означает водород. 37. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания Формула (IX), где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, приводящее к соединению формулы (X) Формула (X) , где R3-R5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (Х!а) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон Формула (Х1а), где Х2 означает галоген, OMs или OTs; m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или 1, где сумма m+n предпочтительно равна по меньшей мере 1, R6 означает NR7R8 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный С1-С4-алкил; - 50 - 008148 или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R9 означает амино-С2-С4-алкил или ^^ди-СгС^алкиламино-С^С^алкил, приводящее к соединению формулы (ХПа) Формула (ХПа), где R3-R6, m и n имеют вышеуказанные значения; с) обработку соединения формулы (XIte) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (ХШа) <СН*)П> Мвг)п Формула (ХШа) , где R3-R6, m и n имеют вышеуказанные значения; d) взаимодействие соединения формулы (ХШа) с гидроксиэтилирующим агентом, таким как эти-ленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XlVa) R4)6c° <СН> -(СМвг)п Формула (XIVa), где R3-R6, m и n имеют вышеуказанные значения; e) взаимодействие соединения формулы (XIVa) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как 1Ч,1Ч-диметилформамид N N Формула (VIII) где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, R15 означает галоген, такой как хлор, приводящее к соединению формулы (Ia), где X=N и Y=N: - 51 - 008148 Формула (Ia), где Ro-R6, m и n имеют вышеуказанные значения; f) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, g) если R2 в формуле (Ia) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза получают соединение формулы (Ia), где R2 означает водород. 38. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (IX) с бензилирующим агентом, таким как бензилхлорид, бензилбромид или бензилтозилат, в присутствии основания Формула (IX), где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, приводящее к соединению формулы (X) Формула (X), где R3-R5 имеют вышеуказанные значения, b) взаимодействие соединения формулы (X) с соединением формулы (XIb) в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетон Формула (Xlb), где Х2 означает галоген, OMs или OTs; о равно целому числу o-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу o-1; Rio означает Н или Q-C/i-алкил, предпочтительно Н или метил; приводящее к соединению формулы (XIIb) - 52 - 008148 Формула (XIIb): где R3-R5, Rio, о, р и q имеют вышеуказанные значения, с) обработку соединения формулы (XIIb) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, приводящее к соединению формулы (ХШЬ) Формула (ХШЬ) : где R3-R5, R10, о, р и q имеют вышеуказанные значения, d) взаимодействие соединения формулы (XIIIb) с гидроксиэтилирующим агентом, таким как эти-ленкарбонат, в присутствии основания, такого как карбонат калия, в растворителе, таком как N,N-диметилформамид, приводящее к соединению формулы (XlVb) Формула (XlVb), R3-R5, R10, о, р и q имеют вышеуказанные значения, е) взаимодействие соединения формулы (XIVb) С соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как ]^,]Ч-диметилформамид Формула (VIII), где каждый из R0 и R1 независимо означает Н или СН3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С1-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, R15 означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N - 53 - 008148 Формула (Ib), где R0-R5, Rio, о, р и q имеют вышеуказанные значения, f) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, если R2 в формуле (Ib) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R2 означает водород. 39. Способ получения соединения формулы (Ia) по одному из пп.10-13, указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как 1Ч,1Ч-диметилформамид R <\ /L ^он К v -х3 Формула (XV) , где X3 выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, приводящее к соединению формулы (XVI) "ОВп к ^ % Формула (XVI), где R3-R5, Х3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Va) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как 1Ч,1Ч-диметилформамид, Формула (Va), где m равно целому числу 0-10, предпочтительно 0-7, более предпочтительно 0-5, n равно целому числу 0 или i, где сумма m+n предпочтительно равна по меньшей мере i, R6 означает NR7R8 или OR9, где каждый из R7 и R8 независимо означает Н или линейный или разветвленный C1-C4-алкил; или R7 и R8 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; R9 означает амино-C2-C4-алкил или N,N-ди-C1-C4-алкиламино-C2-C4-алкил, приводящее к соединению формулы (XVIte) - 54 - 008148 Формула (XVIIa), где R3-R5, m, n и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIa) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как К,К-диметилформамид, приводящее к соединению формулы (Vila) Формула (Vila), где R3-R <5, m, n и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (Vila) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как ТЧДЧ-диметилформамид, Формула (VIII), где каждый из Ro и Ri независимо означает Н или CH3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и Q-Q-ацил, R15 означает галоген, такой как хлор, приводящее к соединению формулы (1а), где X=N и Y=N Формула (1а) , где R0-R6, m, n и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R2 в формуле (Ia) после стадии d) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, триф-торуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия - 55 - 008148 гидрогенолиза, получают соединение формулы (Ia), где R2 означает водород. 40. Способ получения соединения формулы (Ib) по одному из пп.14 или 15, указанный способ включает: а) взаимодействие соединения формулы (XV) с соединением, выбираемым из группы, включающей бензилхлорид, бензилбромид, бензилиодид, бензилтозилат и бензилмезилат, в присутствии основания, такого как карбонат калия, в растворителе, таком как 1Ч,1Ч-диметилформамид, Формула (XV), где X1 выбран из группы, включающей Cl, Br и I, z означает СН или N, каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, приводящее к соединению формулы (XVI) Формула (XVI), где R3-R5, X3 и z имеют вышеуказанные значения; b) взаимодействие соединения формулы (XVI) с соединением формулы (Vb) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как 1Ч,1Ч-диметилформамид, (СН2)р R"%H2)q Формула (Vb), где о равно целому числу 0-2; р равно целому числу 0-2, где о и р предпочтительно не оба равны 0; q равно целому числу 0-1; R10 означает Н или C1-C4-алкил, предпочтительно Н или метил; приводящее к соединению формулы (XVIIb) 5 > Н2)о (СН2)р' Формула (XVIIb), где R3-R5 и R10, о, р, q и z имеют вышеуказанные значения, с) обработку соединения формулы (XVIIb) в присутствии катализатора гидрирования с использованием подходящего источника водорода, такого как формиат аммония, и последующее нагревание в присутствии гидроксиэтилирующего агента, предпочтительно этиленкарбоната, и основания, такого как карбонат калия, в растворителе, таком как ^^диметилформамид, приводящее к соединению формулы (VIIb) - 56 - 008148 Формула (VIIb), где R3-R5 и R10, о, р, q и z имеют вышеуказанные значения, d) взаимодействие соединения формулы (VIIb) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат натрия, в растворителе, таком как ]^,]^-диметилформамид Формула (VIII), где каждый из R0 и Ri независимо означает Н или СН3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ris означает галоген, такой как хлор, приводящее к соединению формулы (Ib), где X=N и Y=N Формула (Ib), где R0-R5, R10, о, р, q и z имеют вышеуказанные значения; e) по желанию, разделение полученного рацемата на оптические изомеры и/или получение кислотно-аддитивной соли с органической или неорганической кислотой, f) если R2 в формуле (Ib) после стадии d) означает азотзащитную группу, такую как t-ВОС, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ib), где R2 означает водород. 41. Способ получения соединения формулы (Ic) по одному из пп.16-18, указанный способ включает: а) взаимодействие соединения формулы (XVIII) Формула (XVIII), где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей - 57 - 008148 мере один из R3-R5 означает водород; z означает СН или N, с соединением формулы (III) Формула (III) , где Y1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) Формула (XIX), где R3-R5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XVI) в альдегидную функциональную группу в присутствии диметилсульфоксида и оксалилхлорида в дихлорметане, приводящее к соединению формулы (XX) Формула (XX) , где R3-R5 и z имеют вышеуказанные значения, с) взаимодействие соединения формулы (XX) с соединением формулы (XXI) в присутствии основания, такого как трет-бутилат калия в смеси растворителей, состоящей из тетрагидрофурана и третбутано-ла Ri2\N-(CH2)t R-11 Формула (XXI), где t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1 и каждый из R11 и R12 независимо означает Н или линейный или разветвленный С1-С4-алкил; или R11 и R12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXII) Формула (XXII), - 58 - 008148 где R3-R5, Rii, R12, t и z имеют вышеуказанные значения; ориентация относительно двойной связи может быть либо цис, либо транс; d) разделение с помощью препаративной ЖХВР и выделение цис- и транс-изомеров соединения формулы (XXII), приводящее к получению индивидуального цис-изомера формулы (XXIII) и индивидуального транс-изомера формулы (XXIV) R12-N R,2^N/(CH2)t Формула (XXIII), Формула (XXIV), где R3-R5, R11, R12, t и z имеют вышеуказанные значения; е) обработку соединений формулы (XXIII) и (XXIV), соответственно, водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединения формулы (XXV) и (XXVI), соответственно; где R3-R5, R11, R12, t и z имеют вышеуказанные значения; f) взаимодействие соединений формулы (XXV) и (XXVI) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как]^,]^-диметилформамид: NR, Формула (VIII), где каждый из R0 и R1 независимо означает Н или CH3; R2 выбран из группы, включающей С1-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ris означает галоген, такой как хлор, приводящее к соединениям формулы (XXVII) и (XXVIII) (CH2)t R12-N R < < Формула (XXVII), R N R11 Формула (XXVIII), - 59 - 008148 где Ro-R5, Ян, R12, t и z имеют вышеуказанные значения; где соединения формул (XXVII) и (XXVIII) являются изомерами соединения формулы (Ic), где X=N и Y=N; d) если R2 в формуле (Ic) после стадии f) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Ic), где R2 означает водород. 42. Способ получения соединения формулы (Id) по одному из пп.19 и 21-23, указанный способ включает: а) обработку соединения формулы (XXII) водородом в присутствии катализатора гидрирования, такого как палладий на угле, в растворителе, таком как метанол, дающую соединение формулы (XXIX) -(CH2)t R11 Формула (XXIX), где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород, z означает СН или N, t равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 1; и каждый из R11 и R12 независимо означает Н или линейный или разветвленный C1-C4-алкил; или R11 и R12 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо; b) обработку соединения формулы (XXIX) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXX) R12\M/(CH2)t V Формула (XXX) где R3-R5, R11, R12, t и z имеют вышеуказанные значения; с) взаимодействие соединения формулы (XXX) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как М,М-диметилформамид или диоксан N^R,5 Формула (VIII), где каждый из R0 и R1 независимо означает Н или СН3; R2 выбран из группы, включающей Q-Gi-алкоксикарбонил, бензил, тритил, Q-Gi-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и Q-Czi-ацил, R15 означает галоген, такой как хлор, приводящее к соединению формулы (XXXI) - 60 - 008148 Формула (XXXI): где Ro-R5, Ян, R12, t и z имеют вышеуказанные значения; где формула (XXXI) соответствует формуле (Id), в которой \?=СН2, r=t, X=N, Y=N, Ris=Rn и Ri4=Ri2, d) если R2 в формуле (Id) после стадии с) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R2 означает водород. 43. Способ получения соединения формулы (Id) по одному из пп.19, 20, 22 или 23, указанный способ включает: а) взаимодействие соединения формулы (XVIII) Формула (XVIII), где каждый из R3-R5 независимо означает Н, галоген, метил или метокси, при условии, что по меньшей мере один из R3-R5 означает водород; z означает СН или N, с соединением формулы (III) Формула (III), где Y1 означает подходящую удаляемую группу, выбранную из Cl, Br, I, OTs или OMs; в присутствии основания, такого как карбонат калия, триэтиламин или пиридин, в растворителе, таком как ацетонитрил, приводящее к соединению формулы (XIX) Формула (XIX), где R3-R5 и z имеют вышеуказанные значения, b) превращение спиртовой функциональности соединения формулы (XIX) в подходящую удаляемую группу, например, путем обработки метансульфоновым ангидридом в присутствии триэтиламина в дихлорметане, приводящее к соединению формулы (XXXII) - 61 - 008148 Формула (XXXII), где R3-R5 и z имеют вышеуказанные значения; Y2 означает галоген, OMs или OTs; с) взаимодействие соединения формулы (XXXII) с соединением формулы (XXXIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как диоксан /R13 HW-(CH2)- Формула (XXXIII), где W означает О; г равно целому числу 1-11, предпочтительно 1-8, более предпочтительно 1-6, наиболее предпочтительно 2; каждый из R13 и R14 независимо означает Н или линейный или разветвленный CrQ-алкил; или R13 и R14 образуют вместе с атомом азота, к которому присоединены, насыщенное гетероциклическое кольцо, приводящее к соединению формулы (XXXIV) Формула (XXXIV), где r, z, W, R3-R5 и R13 и R14 имеют вышеуказанные значения; d) обработку соединения формулы (XXXIV) водной кислотой, такой как водная уксусная кислота или водная соляная кислота, дающую соединение формулы (XXXV) Формула (XXXV), где r, z, W, R3-R5 и R13 и R14 имеют вышеуказанные значения; е) взаимодействие соединения формулы (XXXV) с соединением формулы (VIII) в присутствии основания, такого как трет-бутилат калия, в растворителе, таком как ^^диметилформамид - 62 - 008148 где каждый из Ro и R1 независимо означает Н или CH3; R2 выбран из группы, включающей С2-С4-алкоксикарбонил, бензил, тритил, С1-С4-алкил, 2-гидроксиэтил, 2-цианоэтил, тетрагидропиран-2-ил и С1-С4-ацил, Ri5 означает галоген, такой как хлор, приводящее к соединению формулы (XXXVI) R0-R8, R13, R14, r, W и z имеют вышеуказанные значения; где формула (XXXVI) отвечает формуле (Id), в которой X=N и Y=N, f) если R2 в формуле (Id) после стадии е) означает азотзащитную группу, такую как t-BOC, тритил и бензил, удалением указанной азотзащитной группы, таким как в кислотных условиях (например, трифторуксусная кислота в растворителе, таком как хлороформ), в условиях гидрогенолиза или отсутствия гидрогенолиза, получают соединение формулы (Id), где R2 означает водород. 44. Способ лечения нарушения или состояния, включающий введение нуждающемуся в таком лечении больному эффективного количества соединения по одному из пп.1-23, где нарушение или состояние выбрано из группы, включающей нарушения памяти, такие как болезнь Альцгеймера; шизофрению; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическую зависимость и токсикоманию; половые дисфункции, такие как эректильная дисфункция; эпилепсию; глаукому; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постменопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. 45. Применение соединения по одному из пп.1-23 при получении лекарственного средства для лечения или предупреждения нарушения или заболевания, такого как нарушения памяти, такие как болезнь Альцгеймера; шизофрения; расстройства настроения, такие как депрессия; состояния тревоги; боль; наркотическая зависимость и токсикомания; половые дисфункции, такие как эректильная дисфункция; эпилепсия; глаукома; заболевания мочевого пузыря, такие как недержание мочи; менопаузальные и постме-нопаузальные приливы; диабет типа 2; нарушения приема пищи, такие как нарушения приема пищи по причине пьянства, нервная анорексия и булимия; прибавление в весе, вызванное приемом нейролептических средств, предменструальное напряжение, нарушения сна и, особенно, ожирение. Формула (XXXVI): где Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6 - 63 - 
|