|
Патентная документация ЕАПВ |
|
||
| Запрос: | ea200601816a*\id |
|
Термины запроса в документе Реферат В заявке описаны дигидратная и безводная кристаллические формы 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6H-дипиридо[3,2-b:2',3'-e][1,4]диазепин-6-она.
Полный текст патента (57) Реферат / Формула:
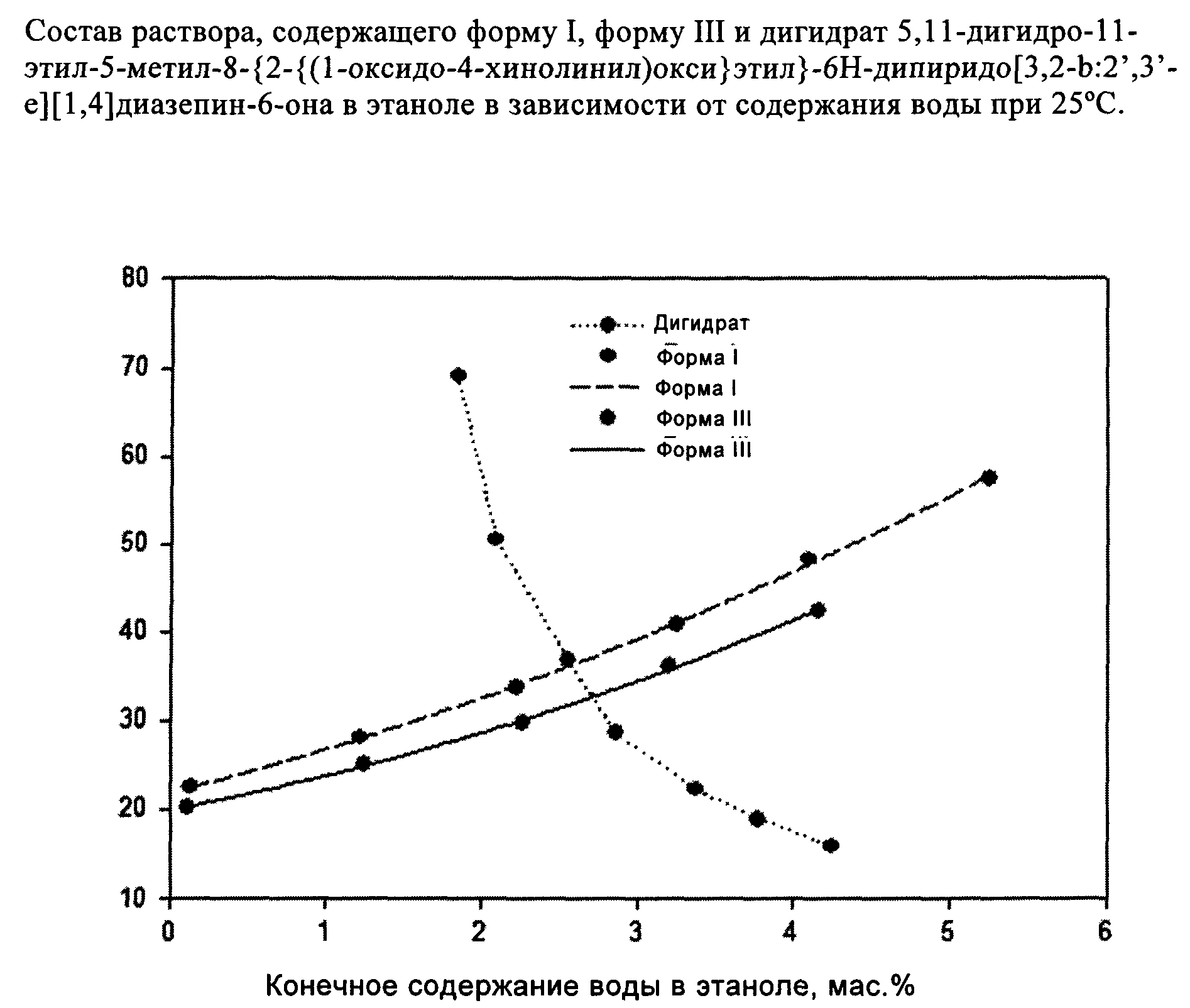
Заявка № 200601816 Заявитель Бёрингер Ингельхайм Интернациональ ГмбХ, DE КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 5,11-ДИГИДРО-11-ЭТИЛ-5-МЕТИЛ-8-{2-{(1-ОКСИ ДО-4-ХИНО ЛИНИЛ)ОКСИ } ЭТИЛ} -6Н-ДИПИРИ ДО [3,2-Ь: 2' ,3' - е] [ 1,4] ДИАЗЕПИН-6-ОН А ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ По настоящей заявке испрашивается приоритет по предварительной заявке 60/559354, поданной 2 апреля 2004 г. ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ 1. ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ Настоящее изобретение относится к дигидратным и безводным кристаллическим формам 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. 2. УРОВЕНЬ ТЕХНИКИ 5,11 -Дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси}этил } -6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-он является ненуклеозидным - 2 - ингибитором обратной транскриптазы ВИЧ-1 (вируса иммунодефицита человека). Его химическая структура приведена ниже. Синтез 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-5 хинолинил)окси} этил} -бН-дипиридо[3,2-Ь:2' ,3'-е] [ 1,4]диазепин-6-она, его применение для борьбы с инфекцией ВИЧ и фармацевтические композиции, включающие это соединение и пригодные для такого применения, описаны в патенте U.S. 6420359 и соответствующей заявке WO0196338. КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ 10 Согласно изобретению мы установили, что, когда 5,11-дигидро-11-этил-5- метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-он получают по методике, описанной в патенте U.S. 6420359, полученное вещество является тригидратом, обладающим плохой кристалличностью. Мы также установили, что тригидрат не является самой 15 желательной формой этого лекарственного вещества для применения при приготовлении лекарственного препарата. Первым объектом настоящего изобретения является дигидратная кристаллическая форма 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е] [ 1,4]диазепин-6-она. Эта 20 дигидратная кристаллическая форма является термодинамически или кинетически выгодной при температурах и влажностях, которые наиболее вероятны во время хранения лекарственного вещества или лекарственного препарата, и поэтому фармацевтически предпочтительной по сравнению с тригидратом, который описан в предшествующем уровне техники. Настоящее 25 изобретение также включает способы получения этой дигидратной кристаллической формы. Мы также установили, что при соответствующих условиях могут образоваться различные безводные полиморфные формы 5,11-дигидро-11-этил- - 3 - 5- метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. Одна из них, которую мы обозначаем, как безводную форму III (БФ III), при некоторых использованных при исследованиях условиях окружающей среды обнаружила фазовую стабильность, что указывает на то, что 5 она является фармацевтически приемлемой, и биологические исследования показали, что она приводит к более высоким уровням в плазме, чем те, которых можно добиться при использовании других кристаллических форм этого лекарственного средства. Таким образом, настоящее изобретение также включает безводную форму III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-10 хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она и способы ее получения. КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ На фиг. 1 представлена ПРРГ дигидрата 5,11-дигидро-11-этил-5-метил-8-{2- {(1 -оксидо-4-хинолинил)окси} этил} -6Н-дипиридо[3,2-Ь :2' ,3 '-е] [ 1,4] диазепин-15 6-она. На фиг. 2 представлена полученная с помощью ДСК (дифференциальная сканирующая калориметрия) термограмма дигидрата 5,11-дигидро-11-этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь :2' ,3' -е] [ 1,4] диазепин-6-она. 20 На фиг. 3 представлена ПРРГ безводной формы III 5,11-дигидро-11-этил-5- метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь :2' ,3' -е] [ 1,4] диазепин-6-она. На фиг. 4 представлена полученная с помощью ДСК термограмма безводной формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-25 хинолинил)окси} этил } -бН-дипиридо [3,2-Ь :2' ,3' -е] [ 1,4] диазепин-6-она. На фиг. 5 представлена фазовая диаграмма 5,11-дигидро-11-этил-5-метил-8-{2- {(1 -оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь :2' ,3 '-е] [ 1,4] диазепин- 6- она. ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ 30 1. Идентификация по характеристическим порошковым рентгенограммам Как отмечено выше, настоящее изобретение включает 2 новые кристаллические формы 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она, -4- дигидратную и безводную форму III. Их можно идентифицировать и отличить друг от друга и от других кристаллических форм, которые не являются частью настоящего изобретения, по характеристическим порошковым рентгенограммам (ПРРГ). 5 Дигидратная кристаллическая форма 5,11-дигидро-11-этил-5-метил-8-{2- {(1 -оксидо-4-хинолинил)окси} этил } -бН-дипиридо [3,2-Ь:2' ,3' -е] [ 1,4] диазепин-6-она согласно настоящему изобретению характеризуется порошковой рентгенограммой, которая включает пик при 23,4° 29 (± 0,2° 20), и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 10 Предпочтительно, если дигидрат, предлагаемый в настоящем изобретении, характеризуется порошковой рентгенограммой, которая включает пики при 23,4 и 24,9° 20 (± 0,2° 20) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. Более предпочтительно, если дигидрат, предлагаемый в настоящем 15 изобретении, характеризуется порошковой рентгенограммой, которая включает пики при 23,4, 24,9 и 17,3° 20 (± 0,2° 20) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. Еще более предпочтительно, если дигидрат, предлагаемый в настоящем изобретении, характеризуется порошковой рентгенограммой, которая включает 20 пики при 23,4, 24,9, 17,3, 24,3, 12,1, 18,5 и 17,6° 20 (± 0,2° 20) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. Более предпочтительно, если дигидрат, предлагаемый в настоящем изобретении, характеризуется порошковой рентгенограммой, полученной с использованием излучения СиКа, которая является в основном такой же, как и 25 представленная на фиг. 1. Безводная кристаллическая форма III 5,11-дигидро-11-этил-5-метил-8-{2-{(1 -оксидо-4-хино линил)окси} этил} -бН-дипиридо [3,2-Ь:2',3'-е][1,4] диазепин-6-она, предлагаемая в настоящем изобретении, характеризуется порошковой рентгенограммой, которая включает пик при 11,6° 20 (± 0,2° 20), и указанная 30 порошковая рентгенограмма получена с использованием излучения СиКн. Предпочтительно, если безводная кристаллическая форма III, предлагаемая в настоящем изобретении, характеризуется порошковой рентгенограммой, которая включает пики при 11,6, 22,5 и 8,3° 20 (± 0,2° 20), и указанная порошковая рентгенограмма получена с использованием излучения СиКа. Более предпочтительно, если безводная кристаллическая форма III, предлагаемая в настоящем изобретении, характеризуется порошковой 5 рентгенограммой, которая включает пики при 11,6, 22,5, 8,3, 12,0, 12,4 и 5,8° 20 (± 0,2° 20), и указанная порошковая рентгенограмма получена с использованием излучения СиКа. Еще более предпочтительно, если безводная кристаллическая форма III, предлагаемая в настоящем изобретении, характеризуется порошковой 10 рентгенограммой, которая включает пики при 11,6, 22,5, 8,3, 12,0, 12,4, 5,8 и 20,8° 20 (± 0,2° 20), и указанная порошковая рентгенограмма получена с использованием излучения СиКа. Более предпочтительно, если безводная кристаллическая форма III, предлагаемая в настоящем изобретении, характеризуется порошковой 15 рентгенограммой, полученной с использованием излучения СиКа, которая является в основном такой же, как и представленная на фиг. 3. Для учета возможной экспериментальной погрешности описанные выше значения 20 следует считать точными с погрешностью ± 0,2° 20. Это означает, что при установлении того, является ли данный образец 5,11-дигидро-11-этил-5- 20 метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь: 2' ,3' - е][1,4]диазепин-6-она дигидратной или безводной кристаллической формой III, предлагаемой в настоящем изобретении, значение 20, которое экспериментально получено для образца, следует считать идентичным характеристическому значению, описанному выше, если оно совпадает с характеристическим 25 значением с точностью ± 0,2° 20. Кристаллические формы, предлагаемые в настоящем изобретении, предпочтительно применять в качестве активных лекарственных веществ в форме, которая является в основном чистой, т. е. в основном не содержащей других кристаллических форм 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4- 30 хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. Тем не менее, настоящее изобретение также включает дигидратную кристаллическую форму или безводную кристаллическую форму III в смеси с другой кристаллической формой или формами. Если активное лекарственное вещество является смесью кристаллических форм, то предпочтительно, чтобы это вещество содержало по меньшей мере 50% или дигидратной, или безводной кристаллической формы III, описанной в настоящем изобретении. 2. Синтез 5 Настоящее изобретение также относится к способам синтеза дигидратной и безводной формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь: 2' ,3' -е] [ 1,4] диазепин-6-она. (А) Общие методики синтеза, предлагаемые в настоящем изобретении (i) Общая методика синтеза для получения дигидратной кристаллической 10 формы 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она При описании в самом общем виде дигидратную кристаллическую форму получают путем перекристаллизации 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хино линил)окси } этил } -бН-дипиридо [3,2-Ь: 2' ,3' -е] [ 1,4] диазепин-6-она, 15 находящегося в неочищенном виде и полученного по любой методике синтеза (включая, но не ограничиваясь теми, которые описаны в патенте U.S. 6420359 или в соответствующей заявке WO0196338), проводимой из воды. Это выполняют путем суспендирования 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси } этил } -6Н-дипиридо[3,2-Ь :2' ,3' -е] [ 1,4] диазепин-6-она 20 в смеси воды с растворителем, который и смешивается с водой, и является жидким при температуре, близкой к температуре окружающей среды. Подходящие растворители включают низш. алкилнитрилы (например, ацетонитрил и пропионитрил), низш. алкилспирты (С1-С7, например, метанол, этанол и изопропанол), циклические и ациклические простые эфиры, включая 25 простые полиэфиры (например, тетрагидрофуран, диоксан и диметиловый эфир диэтиленгликоля), амиды (например, диметилформамид, N-метилпирролидон и диметилацетамид), сульфоксиды (например, ДМСО (диметилсульфоксид)), сульфоны (например, сульфолан), низш. алкилкетоны (например, ацетон) и низш. алкилнитроалканы (например, нитрометан). Суспензию нагревают до 30 получения прозрачного раствора, который является насыщенным или почти насыщенным. Количество воды должно быть по меньшей мере таким, чтобы образовать стехиометрический дигидрат с используемым 5,11-дигидро-11-этил-5 -метил-8 - {2- {(1 -оксидо-4-хинолинил )окси } этил} -6Н-дипиридо [3,2-Ь:2',3' е][1,4]диазепин-6-оном, и составлять менее примерно 90% от всей смеси растворителей. Если раствор не образуется, то при повышенной температуре прибавляют дополнительные объемы растворителя до получения прозрачного раствора. Затем раствору дают медленно охладиться до более низкой 5 температуры до первого обнаружения кристаллического осадка. После этого взвесь выдерживают при этой температуре, пока осаждение в основном не прекратится. Затем осадок удаляют из раствора, например, фильтрованием. После этого твердое вещество сушат, пока не будут удалены все находящиеся на поверхности растворители, и получают дигидрат 5,11-дигидро-11-этил-5-метил- 10 8-{2-{(1 -оксидо-4-хинолинил)окси} этил } -6Н-дипиридо[3,2-Ь :2' ,3' -е] [ 1,4] диазепин-6-она. (ii) Общая методика синтеза для получения безводной формы III 5,11-дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси}этил} -6Н-дипиридо [3,2-Ь: 2' ,3' -е] [ 1,4] диазепин-6-она 15 Дигидрат или тригидрат 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4- хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она (полученный по любой методике) сушат для удаления НгО. Сушку можно проводить любым способом, например, проводить сушку в сушильном шкафу при 23°С или более высокой температуре и при атмосферном давлении или в 20 вакууме. Можно сушить путем пропускания над твердым веществом сильного потока сухого инертного газа в течение длительных периодов времени или можно сушить химическим путем, например, путем перегонки с удалением воды с каким-либо растворителем, который может образовать с водой азеотропную смесь. Типичными растворителями являются низш. алкилнитрилы (такие как 25 ацетонитрил), низш. алкилспирты (такие как этанол и изопропанол) и простые эфиры (такие как диоксан и ТГФ (тетрагидрофуран)). Сушку проводят до тех пор, пока анализ не покажет, что осталось <1% воды. Затем это сухое вещество растворяют в безводном растворителе, в котором растворим 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'- 30 е][1,4]диазепин-6-он (таком как, например, этанол), при повышенной температуре, так чтобы получить раствор, который является насыщенным или почти насыщенным по 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-ону. Затем - 8 - этому раствору дают медленно охладиться до более низкой температуры до первого обнаружения кристаллического осадка или к исходному раствору можно необязательно прибавить затравочные кристаллы безводной формы III 5,11-дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -6Н-5 дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она (если они имеются). После этого взвесь выдерживают при этой температуре, пока происходит отчетливое осаждение, и после этого ее фильтруют или дополнительно охлаждают и затем фильтруют. Затем твердое вещество сушат, пока не будут удалены все находящиеся на поверхности растворители, и получают безводную форму III 10 5,11 -дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил } -6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. (В) Примеры конкретных синтезов, предлагаемые в настоящем изобретении. Конкретные синтезы этих двух кристаллических форм 5,11-дигидро-1115 этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она, предлагаемых в настоящем изобретении, описаны в приведенных ниже примерах. Пример 1: Получение дигидрата 5.11-дигидро-11-этил-5-метил-8-(2-1(1-оксидо-4-хинолинил)окси} этил) -бН-дипиридо \ 3.2-Ь :2' .3 '-е] \ 1,4] диазепин-6-она. 20 29,1 кг Неочищенного 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4- хинолинил)окси}этил} -бН-дипиридо[3,2-Ь:2',3'-е] [ 1,4]диазепин-6-она в виде влажного осадка на фильтре помещали в продутый инертным газом реактор объемом 400 л. Реактор повторно продували инертным газом, затем прибавляли 105 кг MeCN и 8,3 кг 0,002 М НС1 и смесь нагревали до 70°С в темноте и при 25 этих условиях выдерживали в течение 30 мин. Затем раствор в течение 1 ч охлаждали до 22°С, выдерживали в течение 1 ч и полученную таким образом взвесь центрифугировали, осадок промывали с помощью 35 кг смеси 8:1 MeCN:H20. Затем перекристаллизованный влажный осадок 5,11-дигидро-11-этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил } -бН-дипиридо [3,2-Ь :2' ,3' -30 е][1,4]диазепин-6-она (18,55 кг) выгружали и повторно возвращали в реактор. Реактор продували инертным газом, затем прибавляли 12,6 кг НгО и 77,7 кг EtOH (SDA-2B) и смесь нагревали до 70°С в темноте. Еще представляющую собой раствор смесь в горячем виде переносили во второй реактор через - 9 - встроенный в технологическую линию фильтр тонкой очистки с использованием 22,1 кг смеси 8:1 ЕЮН:Н20 для облегчения переноса и промывки реактора. Затем примерно 22 л удаляли путем отгонки при атмосферном давлении. После этого к полученному раствору прибавляли 300 г 6 н. НС1 для протонирования 5 примеси (-2%) простого эфира 5,11-дигидро-11-этил-5-метил-8-{2-{(4- хинолинил)окси}этил} -6Н-дипиридо[3,2-Ь:2',3'-е][ 1,4]диазепин-6-она. Затем раствор охлаждали до 50°С в течение 1 ч и в качестве затравки вносили 100 г дигидрата 5,11 -дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси}этил}-бН-дипиридо[3,2-Ь:2',3 '-е][ 1,4]диазепин-6-она. После 10 этого смесь охлаждали до 22°С, снижая температуру в линейном режиме в течение 8 ч. Полученную таким образом взвесь затем центрифугировали, осадок промывали с помощью 15 кг смеси 8:1 ЕЮН:Н20. Твердое вещество сушили с помощью центрифуги, пока анализ содержания воды методом Карла Фишера не приводил к значению, равному 7,5%, и получали 14,45 кг дигидрата 5,1115 дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -6Н- дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она (суммарный выход 67% в пересчете на промежуточный продукт - простой эфир 5,11-дигидро-11-этил-5-метил-8-{2-{(4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2'> 3'-е][1,4]диазепин-6-она С1) в виде бесцветного твердого вещества, чистота которого по данным ВЭЖХ 20 (высокоэффективная жидкостная хроматография) составляла 99,1%. Т. пл. 199°С; !Н ЯМР (400 МГц, CDC13) 5: 8,69 (d, J= 7,0 Гц, 1Н,), 8,62 (d, J= 8,7 Гц, 1H), 8,39 (d, J= 2,4 Гц, 1H), 8,21 (d, J= 8,4 Гц, 1H), 8,18 (dd, J= 4,7, 1,6 Гц, 1H), 7,8 (dd, J= 5,4, 5,4 Гц, 1H), 7,70 (dd, J= 7,2, 7,2 Гц, 1H), 7,47 (dd, J= 8,0, 1,6 Гц, 1H), 7,07 (dd, J= 7,9, 4,7 Гц, 1H), 6,78 (d, J= 7,0 Гц, 1H), 4,42 (dd, J= 6,2, 6,2 Гц, 25 2H), 4,18 (q, J= 6,9 Гц, 2H), 3,50 (s, 3H), 3,22 (dd, J= 6,2, 6,2 Гц, 2H), 1,24 (t, J = 7,0 Гц, ЗН). 13C ЯМР (125 МГц, d6^MCO) 5: 166,25 (C6), 157,68 (C15), 153,95 (C12), 151,31 (C21), 151,13 (C9), 144,02 (C2), 141,21 (C7), 140,47 (C30), 135,36 (C23), 131,70 (C4), 131,11 (C13), 130,58 (C26), 128,86 (C8), 128,02 (C27), 122,28 (C28), 122,07 (C29), 120,24 (C3 + C14), 119,24 (C25), 101,92 (C22), 68,87 (C20), 30 40,36 (C17), 36,71 (C16), 30,59 (C19), 13,40 (C18). Анализ: Рассчитано для C25H27N5O5: С, 62,88; Н, 5,70; N, 14,67. Найдено С, 62,86; Н, 5,72; N, 14,54. - 10 - Пример 2: Получение безводной формы III 5.11-дигидро-11-этил-5-метил-8-(2- Щ -оксидо-4-хинолинил)окси| этил} -бН-дипиридоГ 3,2-Ь :2 ' .3' -е] \ 1.41 диазепин-6-она. 22,5 кг Дигидрата 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-5 хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-он сушили в вакуумном сушильном шкафу (40°С/44 мм рт. ст.) до постоянной массы, для чего потребовалось примерно 60 ч, и получали 20,4 кг (выход 98%) безводного 5,11-дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси } этил} -6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. Затем это твердое вещество 10 помещали в продутый инертным газом реактор объемом 200 л, защищенный от воздействия света. Затем прибавляли 82 л безводного этанола и полученную взвесь кипятили с обратным холодильником. После этого прибавляли дополнительное количество этанола (10 л) и получали прозрачный раствор. Затем этот раствор охлаждали до 67°С, снижая температуру в линейном режиме 15 в течение 1 ч, и после этого в качестве затравки в виде взвеси в 2 л абсолютного этанола под поверхности вносили 205 г безводной формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. После этого партию вещества охлаждали до 35°С, снижая температуру в линейном режиме в течение 4 ч, затем охлаждали до 30°С, снижая 20 температуру в линейном режиме в течение 12 ч. После этого партию вещества охлаждали до 10°С в течение 1 ч и получали взвесь. Затем эту смесь перегоняли в вакууме (30°С/400 мм рт. ст.), и собирали 32 л этанола. Полученную взвесь затем охлаждали до 10°С в течение 1 ч, после этого фильтровали, осадок на фильтре промывали с помощью 6 л этанола. После этого твердое вещество 25 сушили (42°С/51 мм рт. ст.) в течение 20 ч и получали 19,2 кг (94%) безводной формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-ОКСИДО-4-хинолинил)окси}этил}-бН-дипиридо[3,2-Ь:2',3 '-е] [ 1,4]диазепин-6-она в виде почти белого твердого вещества. Пример 3: Получение дигидрата 5,11-дигидро-11-этил-5-метил-8-12-(П- 30 оксидо-4-хинолинил)окси)этил)-6Н-дипиридо[3,2-Ь:2,.3,-е]|"1.4]диазепин-6-она. В продутый инертным газом реактор объемом 400 л помещали 11,2 кг 5,11-дигидро-11 -этил-5-метил-8- {2- {(4-хинолинил)окси} этил} -6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она-НС1 (24,0 моль, 1 экв.) и 9,9 кг Na3P04 (60,0 моль, -11 - 2,5 экв.) и реактор повторно продували инертным газом. После этого прибавляли 3,75 кг МеОН и 53,7 кг CH2CI2, а затем 125 кг Н2О. Смесь перемешивали при 100 оборотов/мин в течение 15 мин при 22°С, затем в течение 10 мин прибавляли 34,5 кг смеси 32% надуксусная кислота/НОАс (146 моль, 6,1 экв.). Полученную 5 смесь энергично перемешивали в темноте в течение 2,5 ч при 22°С, затем охлаждали до 5°С. Затем к этой холодной смеси в течение 45 мин медленно прибавляли 91,9 кг 2 М ЫагЗгОз, поддерживая внутреннюю температуру ниже 15°С. После этого смесь перемешивали при 22°С в течение 1 ч, затем органические растворители удаляли отгонкой при 45°С/50 мм рт. ст. и собирали 10 31л дистиллята. После этого содержимое перемешивали в течение 4 ч при 22°С и полученную взвесь центрифугировали и осадок промывали с помощью 75 кг Н2О. Затем полученный влажный осадок (15,5 кг) выгружали и возвращали в реактор. После этого загружали еще 13,6 кг влажного осадка 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'- 15 е][1,4]диазепин-6-она из другой партии вещества, т. е. всего 29,1 кг влажного осадка. Реактор продували инертным газом, затем прибавляли 105 кг MeCN и 8,3 кг 0,002 М НС1 и смесь нагревали до 70°С в темноте и при этих условиях выдерживали в течение 30 мин. Затем раствор охлаждали до 22°С в течение 1 ч, 20 выдерживали в течение 1 ч и полученную таким образом взвесь центрифугировали и осадок промывали с помощью 35 кг смеси 8:1 MeCN:H20. После этого перекристаллизованный влажный осадок 5,11-дигидро-11-этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси } этил } -6Н-дипиридо[3,2-Ь :2' ,3' -е][1,4]диазепин-6-она (18,55 кг) выгружали и повторно возвращали в реактор. 25 Реактор продували инертным газом, затем прибавляли 12,6 кг Н2О и 77,7 кг EtOH (SDA-2B) и смесь нагревали до 70°С в темноте. Еще представляющую собой раствор смесь в горячем виде переносили во второй реактор через встроенный в технологическую линию фильтр тонкой очистки с использованием 22,1 кг смеси 8:1 EtOH:H20 для облегчения переноса и промывки реактора. 30 Затем примерно 22 л удаляли путем отгонки при атмосферном давлении. После этого к полученному раствору прибавляли 300 г 6 н. НС1 для протонирования примеси (~2%) простого эфира 5,11-дигидро-11-этил-5-метил-8-{2-{(4 - 12 - хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е] [ 1,4]диазешш-6-она. Т Затем раствор охлаждали до 50°С в течение 1 ч и в качестве затравки вносили 100 г 5,11 -дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси}этил} -6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она-2 НгО. После этого смесь охлаждали 5 до 22°С, снижая температуру в линейном режиме в течение 8 ч. Полученную таким образом взвесь затем центрифугировали, осадок промывали с помощью 15 кг смеси 8:1 EtOH:H20. Твердое вещество сушили с помощью центрифуги, пока анализ содержания воды методом Карла Фишера не приводил к значению, равному 7,5%, и получали 14,45 кг дигидрата 5,11-дигидро-11-этил-5-метил-8- 10 {2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она (67% overall yield from 5,11-дигидро-11-этил-5-метил-8-{2-{(4-хинолинил)окси}этил}-бН-дипиридо[3,2-Ь:2' ,3'-е] [ 1,4]диазепин-6-она-С1) в виде бесцветного твердого вещества, чистота которого по данным ВЭЖХ составляла 99,1%. Т. пл. 199°С; *Н ЯМР (400 МГц, CDC13) 6: 8,69 (d, J= 7,0 Гц, 1Н,), 8,62 (d, 15 J= 8,7 Гц, 1H), 8,39 (d, J= 2,4 Гц, 1H), 8,21 (d, J= 8,4 Гц, 1H), 8,18 (dd, J= 4,7, 1,6 Гц, 1H), 7,8 (dd, J= 5,4, 5,4 Гц, 1H), 7,70 (dd, J= 7,2, 7,2 Гц, 1H), 7,47 (dd, J= 8,0, 1,6 Гц, 1H), 7,07 (dd, J= 7,9, 4,7 Гц, 1H), 6,78 (d, J= 7,0 Гц, 1H), 4,42 (dd, J= 6,2, 6,2 Гц, 2H), 4,18 (q, J= 6,9 Гц, 2H), 3,50 (s, 3H), 3,22 (dd, J= 6,2, 6,2 Гц, 2H), 1,24 (t, J = 7,0 Гц, ЗН). 13C ЯМР (125 МГц, d6-flMCO) 6: 166,25 (C6), 157,68 (C15), 20 153,95 (C12), 151,31 (C21), 151,13 (C9), 144,02 (C2), 141,21 (C7), 140,47 (C30), 135,36 (C23), 131,70 (C4), 131,11 (C13), 130,58 (C26), 128,86 (C8), 128,02 (C27), 122,28 (C28), 122,07 (C29), 120,24 (C3 + C14), 119,24 (C25), 101,92 (C22), 68,87 (C20), 40,36 (C17), 36,71 (C16), 30,59 (C19), 13,40 (C18). Анализ: Рассчитано для C25H27N505: С, 62,88; H, 5,70; N, 14,67. Найдено С, 62,86; Н, 5,72; N, 14,54. 25 Пример 4: Лабораторный синтез безводной формы III 5.11 -дигидро-11 -этил- 5-метил-8-(2-1(1-oкcидo-4-xинoлинил')oкcи|этилl-6H-дипиpидo[3.2-b:2^3,-е] |" 1,4] диазепин-6-она. 2,05 г Дигидрата 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-бН-дипиридо[3,2-Ь :2 ',3 '-е] [ 1,4]диазепин-6-она сушили в 30 вакуумном сушильном шкафу при 85°С до постоянной массы. Затем полученное твердое вещество перекристаллизовывали из 8 мл абсолютного этанола при 70°С и ему в течение 18ч давали охладиться до температуры окружающей среды. - 13 - Затем полученную взвесь фильтровали и промывали небольшим количеством абсолютного этанола, кратковременно сушили на воздухе, затем сушили в токе азота до постоянной массы и получали 1,67 г (88%). ПРРГ показывала, что образец представляет собой безводную форму III 5,11-дигидро-11-этил-5-метил-5 8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е] [ 1,4] диазепин-6-она. Пример 5: Получение безводной формы III 5,11-дигидро-11-этил-5-метил-8-(2- ((1 -оксидо-4-хинолинил)окси} этил I -бН-дипиридо [3,2-Ь :2' ,3' -е] [" 1.41 диазепин-6-она. 10 22 кг Дигидрата 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4- хинолинил)окси}этил}-бН-дипиридо[3,2-Ь:2',3'-е] [ 1,4]диазепин-6-она (46,1 моль, 1 экв.) помещали в лотковую сушилку и сушили в вакууме при 40 мм рт. ст. и 60°С, пока анализ содержания НгО методом Карла Фишера не приводил к значению < 0,2% (48 ч). Затем твердое вещество (19,5 кг) загружали в продутый 15 инертным газом реактор объемом 200 л, который после этого повторно продували инертным газом. После этого прибавляли 80 л абсолютного этанола (SDA-2B) и смесь перемешивали при 100 оборотов/мин, при этом температуру повышали до 82°С. Отбор аликвоты из реактора показывал, что образовался прозрачный раствор. Затем смесь охлаждали до 72°С и под поверхность в 20 качестве затравки вносили 200 г безводной формы III 5,11-дигидро-11-этил-5-метил- 8- {2- {(1 -оксидо-4-хино линил)окси} этил} -бН-дипиридо [3,2-Ь: 2', 3' -е][1,4]диазепин-6-она в виде взвеси в этаноле. После этого содержимое реактора охлаждали до температуры окружающей среды, снижая температуру в линейном режиме в течение 18 ч, затем дополнительно охлаждали до 14°С и выдерживали 25 при этой температуре в течение 1 ч, затем фильтровали. Полученный осадок на фильтре затем сушили до постоянной массы в вакуумном сушильном шкафу при 60°С в течение 24 ч и получали 19,2 кг безводной формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е1[1,4]диазепин-6-она (95%) в виде почти белого твердого вещества. Анализ 30 этого вещества с помощью ПРРГ и сопоставление с аутентичным стандартом показывало, что оно представляет собой полиморфную форму безводной формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. По данным ВЭЖХ чистота - 14 - составляла 99,2%. Т. пл. 198,2°С; !Н ЯМР (400 МГц, CDC13) 5: 8,69 (d, J= 7,0 Гц, Ш,), 8,62 (d, J= 8,7 Гц, 1H), 8,39 (d, J= 2,4 Гц, 1H), 8,21 (d, J= 8,4 Гц, 1H), 8,18 (dd, J= 4,7, 1,6 Гц, 1H), 7,8 (dd, J= 5,4, 5,4 Гц, 1H), 7,70 (dd, J= 7,2, 7,2 Гц, 1H), 7,47 (dd, J= 8,0, 1,6 Гц, 1H), 7,07 (dd, J= 7,9, 4,7 Гц, 1H), 6,78 (d, J= 7,0 Гц, 1H), 5 4,42 (dd, J= 6,2, 6,2 Гц, 2H), 4,18 (q, J= 6,9 Гц, 2H), 3,50 (s, 3H), 3,22 (dd, J= 6,2, 6,2 Гц, 2H), 1,24 (t, J = 7,0 Гц, ЗН). 13C ЯМР (125 МГц, d6-HMCO) 8: 166,25 (C6), 157,68 (C15), 153,95 (C12), 151,31 (C21), 151,13 (C9), 144,02 (C2), 141,21 (C7), 140,47 (C30), 135,36 (C23), 131,70 (C4), 131,11 (C13), 130,58 (C26), 128,86 (C8), 128,02 (C27), 122,28 (C28), 122,07 (C29), 120,24 (C3 + C14), 119,24 (C25), 101,92 10 (C22), 68,87 (C20), 40,36 (C17), 36,71 (C16), 30,59 (C19), 13,40 (C18). Анализ: Рассчитано для C25H23N503: С, 62,92; H, 5,30; N, 15,77. Найдено С, 62,76; Н, 4,97; N, 15,72. 3. Методика порошковой рентгенографии Для того, чтобы различить разные кристаллические формы 5,11-дигидро- 15 11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она, можно использовать высококачественный порошковый дифрактометр. Типичные ПРРГ дигидратной и безводной III кристаллических форм, предлагаемых в настоящем изобретении, получены на порошковом 20 дифрактометре Bruker AXS X-Ray Powder Diffractometer, Model D8 Advance. Прибор снабжен длинной рентгеновской трубкой с тонкой фокусировкой. Электропитание трубки установлено на 40 кВ и 40 мА. Прибор работал в режиме параксиальной фокусировки с использованием щели расхождения шириной 1,0 мм, щели для устранения рассеяния шириной 1,0 мм, щели детектора шириной 25 0,2 мм, щели монохроматора шириной 0,6 мм, графитового монохроматора и сцинтилляционного детектора Nal. Шаговое сканирование выполняли в диапазоне от 2 до 35° 29 с шагом 0,05°, с длительностью шага, равной 4 с. Для проверки юстировки прибора использовали эталонный кварцевый стандарт. Образцы для анализа готовили путем настройка на кремниевый держатель с 30 нулевым фоном. Полученные ПРРГ приведены на фиг. 1 и 3. 4. Дополнительные методики характеризации Кристаллические формы, предлагаемые в настоящем изобретении, можно оптимально дополнительно охарактеризовать с помощью дифференциальной - 15 - сканирующей калориметрии (ДСК). Полученные с помощью ДСК термограммы для дигидратной и безводной III кристаллических форм, предлагаемых в настоящем изобретении, приведены на фиг. 2 и 4 соответственно. Дополнительным способом характеризации является термомикроскопия. 5 При исследовании с помощью термомикроскопии (скорость нагрева = 10°С/мин) с использованием поляризационного оптического микроскопа дигидрат характеризуется следующими термическими проявлениями: 1. Помутнение кристалла и выделение летучих веществ указывает на протекание дегидратации в диапазоне ~75-112°С, что приводит к 10 дегидратированной фазе. 2. Плавление дегидратированной фазы в диапазоне ~155-162°С. 3. Перекристаллизация в диапазоне ~162-188°С. 4. Конечное плавление в диапазоне ~195-203°С. Кроме того, с помощью термогравиметрического анализа/инфракрасной 15 Фурье-спектроскопии (ТГА/ИКФС) или аналогичных методик можно подтвердить, что дигидрат является стехиометрическим дигидратом. 5. Термодинамическая предпочтительность дигидратной и безводной формы III Для получения однозначной фазовой диаграммы для различных форм 5,1120 дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -6Н- дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она, приведенной на фиг. 5, использовали исследования растворимости. Фазовая диаграмма показывает, что при 25°С безводная форма III термодинамически предпочтительнее безводной формы I. Кроме того, безводная форма III термодинамически предпочтительнее дигидрата 25 и безводной формы I при 25°С при взаимодействии с этанольными растворами, содержащими < -2,7 ± 0,5 мас.% воды. Напротив, дигидрат термодинамически предпочтительнее безводной формы I и формы III при взаимодействии с этанольными растворами, содержащими > ~2,7 мас.% воды и насыщенными 5,11 -дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -6Н-30 дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-оном. 6. Применение Дигидратную и безводную форму III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6 -16 - она, предлагаемые в настоящем изобретении, можно применять для борьбы с инфекцией ВИЧ у людей способом, описанным в патенте U.S. 6420359 и соответствующей заявке WO0196338. Соединение в любой из этих двух кристаллических форм можно включать в фармацевтические препаративные 5 формы и вводить в соответствии с дозировочными режимами, описанными в патенте U.S. 6420359 и соответствующей заявке WO0196338. - 17 - ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Кристаллическая форма дигидрата 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она, обладающая порошковой рентгенограммой, которая включает пик при 23,4° 28 (± 0,2° 29), и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 2. Кристаллическое вещество по п. 1, такое что порошковая рентгенограмма указанного вещества дополнительно включает пик при 24,9° 29 (± 0,2° 29) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 3. Кристаллическое вещество по п. 1 или 2, такое что порошковая рентгенограмма указанного вещества дополнительно включает пик при 17,3° 29 (± 0,2° 29) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 4. Кристаллическое вещество по п. 1,2 или 3, такое что порошковая рентгенограмма указанного вещества включает пики при 24,3, 12,1, 18,5 и 17,6° 29 (± 0,2° 29) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 5. Кристаллическая форма дигидрата 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она, обладающая порошковой рентгенограммой, полученной с использованием излучения СиКа, которая является в основном такой же, как и представленная на фиг. 1. 6. 5,11-Дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-он, в котором по меньшей мере 50% - 18 - указанного вещества находится в форме кристаллического дигидрата по п. 1,2, 3, 4 или 5. 7. Фармацевтическая композиция, включающая кристаллическое вещество по п. 1, 2, 3, 4 или 5 и фармацевтически приемлемый носитель или разбавитель. 8. Кристаллическая форма III безводного 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она, обладающая порошковой рентгенограммой, которая включает пик при 11,6° 26 (± 0,2° 26), и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 9. Кристаллическое вещество по п. 8, такое что порошковая рентгенограмма указанного вещества дополнительно включает пики при 22,5 и 8,3° 26 (± 0,2° 26) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 10. Кристаллическое вещество по п. 8 или 9, такое что порошковая рентгенограмма указанного вещества дополнительно включает пики при 12,0, 12,4 и 5,8° 26 (± 0,2° 26) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 11. Вещество по п. 8, 9 или 10, такое что порошковая рентгенограмма указанного вещества включает пик при 20,8° 26 (± 0,2° 26) и указанная порошковая рентгенограмма получена с использованием излучения СиКа. 12. Кристаллическая форма III безводного 5,11-дигидро-11-этил-5-метил-8-{2- {(1 -оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь :2' ,3' -е] [ 1,4] диазепин-6-она, обладающая порошковой рентгенограммой, полученной с использованием излучения СиКа, которая является в основном такой же, как и представленная на фиг. 3. - 19 - 13. 5,11 -Дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-он, в котором по меньшей мере 50% указанного вещества находится в виде безводной кристаллической формы III по п. 8, 9, 10, 11 или 12. 14. Фармацевтическая композиция, включающая кристаллическое вещество по п. 8, 9, 10, 11 или 12 и фармацевтически приемлемый носитель или разбавитель. 10 15. Способ получения кристаллической формы дигидрата 5,11-дигидро-11- этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она по п. 1, 2, 3, 4, 5 или 6, указанный способ включает следующие стадии: (а) растворения 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-15 хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она в смеси НгО со смешивающимся с водой растворителем с получением насыщенного или почти насыщенного раствора, при условии, что количество H20 должно быть по меньшей мере равно количеству, необходимому для образования стехиометрического дигидрата; 20 (Ь) охлаждения раствора для осаждения дигидрата 5,11-дигидро-11-этил-5- метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'- е][1,4]диазепин-6-она из раствора; (c) удаления осадка из раствора; и (d) сушки твердого вещества, пока не будут удалены все находящиеся на 25 поверхности растворители. 16. Способ получения безводной кристаллической формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она по п. 8, 9, 10, 11 или 12, и способ включает 30 следующие стадии: (а) сушки дигидрата или тригидрата 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь :2' ,3' -е] [ 1,4] диазепин-6-она для удаления воды и получения безводного вещества; -20- (b) растворения безводного твердого вещества в безводном растворителе с получением насыщенного или почти насыщенного раствора; (c) охлаждения раствора для осаждения безводной кристаллической формы III 5,11 -дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил } -6Н- 5 дипиридо[3,2-Ь :2' ,3 '-е] [ 1,4] диазепин-6-она; (d) отделения осадка от раствора; и (e) сушки твердого вещества, пока не будут удалены все находящиеся на поверхности растворители. ФИГ. 1. ПРРГ дигидрата 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4- хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. Данные получены с использованием излучения Си Ка. ДСК ФИГ. 2. Полученная с помощью ДСК термограмма дигидрата 5,11-дигидро-11-этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. ФИГ. 3. ПРРГ безводной формы III 5,11-дигидро-11-этил-5-метил-8-{2-{(1- оксидо-4-хино лини л)окси } этил } -бН-дипири до [3,2-Ь: 2' ,3' -е] [ 1,4] диазепин-6-она. Данные получены с использованием излучения Си Ка. 4 - ДСК DSC Экзо до Температура (°С) ФИГ. 4. Полученная с помощью ДСК термограмма безводной формы III 5,11-дигидро-11 -этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси}этил} -6Н-дипиридо[3,2-Ь:2' ,3' -е] [ 1,4] диазепин-6-она. - 5 - Состав раствора, содержащего форму I, форму III и дигидрат 5,11-дигидро-11-этил-5-метил-8- {2- {(1 -оксидо-4-хинолинил)окси} этил} -бН-дипиридо [3,2-Ь:2' ,3 '-е][1,4]диазепин-6-она в этаноле в зависимости от содержания воды при 25°С. ФИГ. 5. Фазовая диаграмма 5,11-дигидро-11-этил-5-метил-8-{2-{(1-оксидо-4-хинолинил)окси}этил}-6Н-дипиридо[3,2-Ь:2',3'-е][1,4]диазепин-6-она. 
|