|
Патентная документация ЕАПВ |
|
||
| Запрос: | ea200601798a*\id |
|
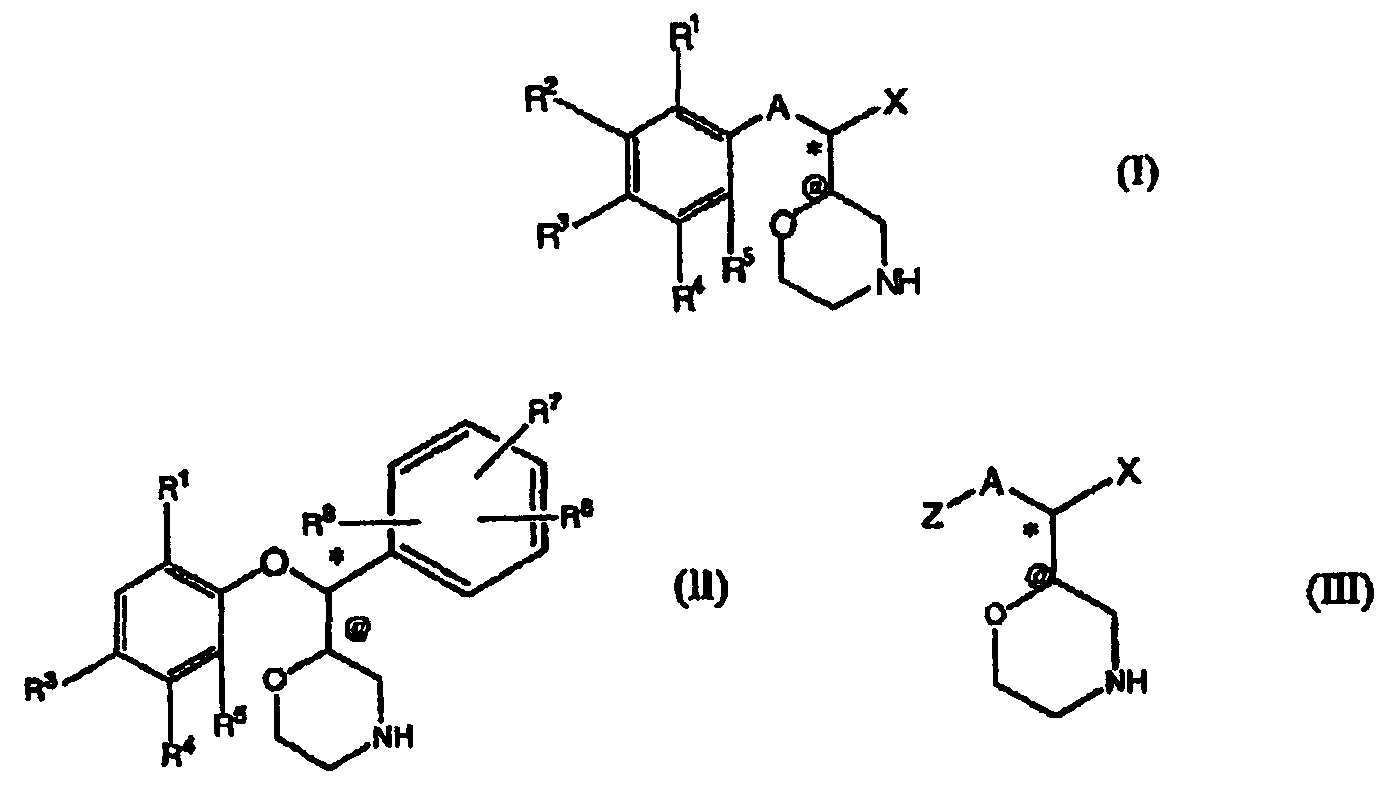
Термины запроса в документе Реферат Это изобретение относится к соединениям формул (I), (II), (III) где R 1 -R c , A, X и Z определены в описании, фармацевтическим композициям, содержащим данные соединения, и их применению для лечения расстройств центральной нервной системы.
Полный текст патента (57) Реферат / Формула: где R 1 -R c , A, X и Z определены в описании, фармацевтическим композициям, содержащим данные соединения, и их применению для лечения расстройств центральной нервной системы.
2420-139842ЕА/071 ЗАМЕЩЕННЫЕ СОЕДИНЕНИЯ МОРФОЛИНА ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ Это изобретение касается материалов и способов профилактики или лечения расстройства центральной нервной системы или состояния и, в частности, способа лечения и профилактики синдрома дефицита внимания с гиперактивностью (СДВГ) с помощью введения соединения, ингибирующего обратный захват норэпинефрина. На такие соединения также имеются ссылки в литературе как на селективные ингибиторы обратного захвата норэпинефрина (ИОЗН). Уровень техники данного изобретения Синдром дефицита внимания с гиперактивностью (СДВГ) имеет определенную частоту заболеваний среди детей школьного возраста, составляющую 3-5%, и характеризуется основными симптомами гиперактивности, импульсивности и/или невнимания. Симптомы СДВГ, связанные со вниманием, могут успешно лечиться такими психомоторными стимуляторами, как метилфенидат (Риталин). Клонидин, агонист а2-адренорецепторов, предназначен для лечения симптомов агрессии и оппозиционных симптомов. Существуют потенциальные побочные эффекты как для метилфенидата, так и для клонидина, поэтому представляется важным идентифицировать другие лекарства, имеющие подобную или лучшую эффективность с минимальными побочными эффектами и склонностью к привыканию. СДВГ является одним из наиболее распространенных детских психических расстройств, а также, проявляется как обычное часто диагносцируемое психическое заболевание и у взрослых (Т. Spencer, et al., J Clin Psychiatry, 1998, 59 (Suppl. 7), 759768). Это расстройство, возникающее в детстве, которое может продолжаться на протяжении жизни с проявлением симптомов (например, невнимания и/или импульсивности) (J.B. Schweitzer, et al., Med Clin North Am, May 2001, 85: 3, 757-777). СДВГ может изменять свои проявления на протяжении жизни начиная с дошкольного возраста (D.P. Cantwell, J Am Acad Child Adolesc Psychiatry, Aug. 1996, 35 (8), 978-987; J. Elia, et al. N Eng J Med, Mar. 1999, 340(10), 780-788; E.E. Nolan, et al., J Am Acad Child Adolesc Psychaitry, Feb. 2001, 40(2), 241-249). Диагноз СДВГ ставят на основании клинических анализов (М. Dulcan, et al. М, J Am Acad Child Adolesc Psychaitry, Oct. 1997, 36 (10 Suppl), 85S-121S; National Institutes of Health, 1998). "The essential feature of ADHD is a persistent pattern of inattention and/or hyperactivity-impulsivity that is more frequent and severe than is typically observed in individuals at a comparative level of development" (Diagnostic and Statistical Manual of Mental Disorders (DSM-IV), American Psychiatric Association, Washington, D. C, 1994). Для того, чтобы диагносцировать СДВГ у пациентов, они должны демонстрировать симптомы СДВГ, вызывающие ухудшение состояния до достижения семилетнего возраста, и симптомы должны продолжаться дольше шести месяцев в, по крайней мере, двух местах (например, школе [или работе] и дома). (Смотри DSM-IV). Известно несколько соединений ИОЗН. Атомексетин, в настоящее время доступный коммерчески, (Strattera (r), Eli Lilly) и находящийся в начале интенсивного использования для клинического лечения СДВГ у детей и взрослых. Атомексетин представляет собой лекарственный препарат для нестимулирующего лечения СДВГ. Предполагается, что число вылеченных пациентов с СДВГ будет повышаться как в результате введения атомексетина, так и в результате улучшенных образовательных проектов. Следовательно, существует непосредственная потребность в подходах к лечению СДВГ, обеспечивающих большую эффективность, чем те, что доступны в настоящее время. Сущность изобретения Настоящее изобретение касается соединений I: и фармацевтически приемлемых солей или производных, где: А представляет собой О или S; X представляет собой арил, гетероцикл, бензоконденсированный бицикличес кий, - Ci - Сюалкил, - С2 - С8алкенил, -С5-С8циклоалкенил, - (СН2) пСз-С9циклоалкил, конденсированный циклоалкил, Н, SCF3, гидрокси-С1-С6алкил, -С1-С6алкокси, -С1-С6алкоксиС1-С6алкокси, - (СН2) nS-Ci-Сбалкил, -(CH2)nS02- С1-С6алкил; где каждая группа необязательно замещена одним или более заместителями, независимо выбранными из Сд.-С6алкила, -С3-С8циклоалкила, -С1-Сбалкокси, арила, гетероцикла, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON(H) С1-С6алкила, -CON (Сх-С6алкил) 2, гидрокси-С1-С6алкила, -С1-4алкокси, -SCF3, S02, -С1-С4алкил-3-С1-С4алкила, -С1-С4алкил-3-, -Cl-C4aлкилNR,Rn, NR'R", при условии, что когда X является фенилом, замещенным фенилом, Сд^замещенным алкилом, гало-замещенным С1-С4алкилом, незамещенным С3-С8Циклоал килом, или гало-замещенным С3-С8циклоалкилом, тогда * и @ являются либо (R, S) или (S, R) ; R1-R5 выбирают независимо из Н, С1-С6алкила, арила, -С3-С8циклоалкила, -С1-Сбалкенила, -С5-С8циклоалкенила, - (СН2)пС3-С8циклоалкила, -С1-С6алкокси, -О-арила, гетероцикла, S02, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, - CON (H) Ci - Свал кил a, -CON (С1-С6алкил) 2, гидрокси-С!-С6алкила, С1-С4алкоксиС1-Сбалкила, -SCF3, -С1-С6алкил-S02, С1-С4алкил-3-С1-С4алкила, С1-С4алкил-Б-, -С1-С4алкшгёШ' R", и NR'R", и где две группы из групп R1-R5, связанные с кольцом, могут образовывать бензоконденсированное бициклическое кольцо, содержащее фенильную группу, конденсированную с 5-6-членным карбоциклическим кольцом, или фенильную группу, конденсированную с 5-6-членным гетероциклическим кольцом, содержащим, по меньшей мере, один из гетероатомов N, О или S, и где каждая из групп С!-Сбалкил, арил, -С3-С8циклоалкил, -С2-С8алкенил, -С5-С8циклоалкенил, -С!-С6алкокси, гетероцикл может быть необязательно замещена одной или более из следующих групп: арильной, гетероциклильной, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3/ -CN, -CONH2, -CON (H) С1-С6алкильной, - CON (Ci - Свалкил) 2, гидрокси-Ci- С6алкильной, -Сх-Сбалкокси, -С1-С6алкильной, -SCF3, -Ci-СбалкилЗС> 2, С1-С4алкил-8-С1-С4алкильной, С^-Сиалкил-Б-, -Ci-С4алкилШ^" и NR'R"; R' и R" независимо представляют собой С!-С6алкил или Н; п представляет собой значение от 1 до 5; * обозначает первый хиральный центр; и @ обозначает второй хиральный центр. Дополнительный аспект этого изобретения касается соединений формулы I, где R1 представляет собой С1-С6алкил, галоген, ОН, CN, -SCi-Свалкил, СН2ОС1-С6алкил, -С3-С8циклоалкил, Ci-Сбалкокси, фенил, замещенный фенил, или пиридил. Дополнительный аспект данного изобретения касается соединений, где R1 является С1-Сбалкокси, F, С1-С6алкилом или CN. Другие аспекты касаются соединений, где R3, R4 и R5 не могут быть одновременно замещены. Еще дополнительный аспект данного изобретения касается соединений, где, по меньшей мере, два из R3, R4 и R5 являются водородом. Еще дополнительный аспект данного изобретения касается соединений, где R3, R4 и R5 независимо выбирают из Н, F, С1 и -OCi-Сбалкила. Еще дополнительный аспект данного изобретения касается соединений, где X является гетероциклом. Еще дополнительный аспект данного изобретения касается соединений, где гетероциклом является пиридил, тиазолил, пиразол, оксазол, бензофуран или дигидробензофуран. Еще дополнительный аспект данного изобретения касается соединений, где пиридил является 2-пиридильной группой. Еще дополнительный аспект данного изобретения касается соединений, где R2 является водородом. Еще дополнительный аспект данного изобретения касается соединений, где конформация @ и * является S,S. Дополнительный аспект данного изобретения касается соединений формулы II и его фармацевтически приемлемых солей или производных, где: R1 и R6, R7 и R8 независимо выбирают из Н, С1-С6алкила, арила, -С3-С8циклоалкила, -С2-С6алкенила, -С5-С8циклоалкенила, - (СН2)пС3-С9циклоалкила, -С1-С6алкокси, -О-арила, гетероцикла, S02, ОН, гало, -CF3, -CHF2/ -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON(H) С1-Сбалкила, -CON (С1-Сбалкил) 2, гидрокси-С1-С6алкила, -С1-С4алкоксиС1-С6алкила, -SCF3, -С1-Сбалкил-302, -С1-С4алкил-3-С1-С4алкила, -С:.-С4алкил-3, -Cl-C4aлкилNR, R" и NR'R", и где каждая из групп -С1-Сбалкил, арил, -С3-С8циклоалкил, -С2-С8алкенил, -С5-С8циклоалкенил, -Ci-С6алкокси, арил, гетероцикл может быть необязательно замещена одной или более из следующих групп: -С1-Сбалкильной, арильной, гетероциклильной, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON (H) С1-Сбал киль ной, -CON (С1-С6алкил) 2, гидрокси-С1-С6алкильной, -С].-С4алкокси- С1-С6алкильной, -С1-С6алкокси, -SCF3, -С1-С6алкил302, -С1-С4алкил-3-С1-С4-алкильной, -С1-С4алкил-3-, -Cl-C4aлкилNR'R" и NR'R"; R' и R" независимо представляют собой С1-С6алкил или Н; п представляет собой значение от 1 до 5; R3 представляет собой Н или F; R4 представляет собой Н или F, однако когда R3 является F, R4 не является F; R5 представляет собой Н, галоген, Сх-С6алкил, С1-С6алкокси, -S-Ci-Сбалкил, - (СН2) п-0-(СН2) п-, -OCF3 или -SCF3; и * обозначает первый хиральный центр; и @ обозначает второй хиральный центр при условии что, когда R1 представляет собой метил, -О-метил, -О-этил, С1 и R3-R6 представляет собой Н, тогда * и @ являются либо (S,R) или (R,S) и, кроме того, когда R1 представляет собой -О-метил и R6-R8 представляют собой Н, -О-метил, С1 или метил, тогда * и @ являются либо (S,R) или (R,S). Дополнительный аспект данного изобретения касается соединений формулы I, где R1 представляет собой Сг-Сбалкил, галоген, ОН, -CN, -SCi-Сбалкил, -СН2ОСд.-С6алкил, -С3-С8циклоалкил, С1-С6алкокси, пиридил, фенил или замещенный фенил. Дополнительный аспект данного изобретения касается соединений, где R1 является -С1-С6алкокси, F, Сх-Сбалкилом или CN. Другие аспекты касаются соединений, где R3, R4 и R5 не могут быть одновременно замещены. Еще дополнительный аспект данного изобретения касается соединений, где, по меньшей мере, два из R3, R4 и R5 являются водородом. Еще дополнительный аспект данного изобретения касается соединений, где конформация @ и * является S,S. Дополнительный аспект данного изобретения касается соединений формулы III и фармацевтически и/или его ветеринарно приемлемых солей или производных, где: А представляет собой О; Z представляет собой нефенильный гетероарил, выбранный из пиридина, фурана, тиофена, нафталина, нафтиридина, пиразола, пиразина, пиримидина, тиазола, оксазола, изоксазола, триазола, тетразола; или фенильное кольцо, конденсированное с гетероциклом, содержащим N, О, или S; где каждый из гетероарилов может быть необязательно замещен одним или более заместителями, независимо выбранными из гетероцикла, -С3-С8Циклоалкила, фенила, -С2-С8алкенила, -С5-С8циклоалкенила, -(СН2) пС3-С9циклоалкила, -С5-Сконденсированного циклоалкила, арила, Н, -SCF3, гидрокси-С1-С6алкила, -С1-С6алкокси, -О-арила, -(СН2)пЗ-С1-С6алкила, -С1-С6алкил-802, - (СН2) п802-С1-С6алкила, -Ci-Сбалкил-S-, С1-С4алкилЫК'Н", или NR'R", где любая из предшествующих групп необязательно замещена одним или более заместителями, независимо выбранными из -С1-С6алкила, -С3-С8циклоалкила, -С1-С6алкокси, замещенных или незамещенных арилом, гетероциклом, ОН, гало, -CF3l -CHF2, -CH2F, -OCF3, OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON (H) Сх-С6алкилом, -CON (С1-С6алкил) 2, гидрокси-С1-С6алкилом, -SCF3, -С1-С6алкил802, -С1-С4алкил-3-С1-С4алкилом, -Сх-^алкил-Б-, -Cl-C4aлкилNR' R" и NR'R"; X представляет собой гетероцикл, арил, -С1-С8алкил, -С2-С8алкенил, -С5-С8циклоалкенил, бензоконденсированный бициклический, -С3-С8циклоалкил, - (СН2) пС3-С8циклоалкил, -С5-С9конденсированный циклоалкил, Н, -SCF3, гидрокси-С!-С6алкил, -Сх-Сбалкокси, С1-С6алкил, - (СН2) nS-Ci-Сбалкил, -(CH2)nS02-Ci-Сбалкил, где любая из групп необязательно замещена одним или более заместителями, независимо выбранными из -С1-С6алкила, -С3-С8циклоалкила, -С1-С6алкокси, арила, гетероцикла, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON (H) Ci-Сбалкила, -CON (Ci-Сбалкил) 2, гидрокси-С1-С6алкила, -SCF3, -С1-С6алкил802, -С1-С4алкил-8-С1-С4алкила, -С1-С4алкил-8-, - Ci - С4ал килЖ' R" и NR'R"; R' и R" независимо представляют собой С1-Сбалкил или Н; п представляет собой значение от 1 до 5; * обозначает первый хиральный центр; и @ обозначает второй хиральный центр. Дополнительный аспект данного изобретения касается соединений, где Z представляет собой пиридил. Еще дополнительный аспект данного изобретения касается соединений, где конформация @ и * является S,S. Соединения данного изобретения включают следующие соединения и их фармацевтически приемлемые соли, энантиомеры и диастереомеры: 2-[фенил-(2-трифторметокси-фенокси)-метил]-морфолин; 2-[(2-этилсульфанил-фенокси)-фенил-метил]-морфолин; 2-[(2-изобутил-фенокси)-фенил-метил]-морфолин; 2- [ (2-бром-фенокси)-фенил-метил]-морфолин; 2-[фенил-(2-винил-фенокси)-метил]-морфолин; 2- [ (2-хлор-фенокси)-фенил-метил]-морфолин; 2-[(2-метоксиметил-фенокси)-фенил-метил]-морфолин; 2-[фенил-(2-трифторметил-фенокси)-метил]-морфолин; 2- [ (2-бензил-фенокси)-фенил-метил]-морфолин; 2-[фенил-(2-пиридин-4-ил-фенокси)-метил]-морфолин; 2-[(2-циклопропил-фенокси)-фенил-метил]-морфолин; 2-[(нафталин-1-илокси)-фенокси)-метил]-морфолин; 2-[фенил-(2-пиридин-З-ил-фенокси)-метил]-морфолин; 2-[(2-фенокси-фенокси)-фенил-метил]-морфолин; этиловый эфир 2-(морфолин-2-ил-фенил-метокси)-бензойной кислоты; 2- [ (41-хлор-бифенил-2-илокси)-фенил-метил]-морфолин; 2-(2-этокси-феноксиметил)-морфолин; 2- [ (2-фтор-фенокси)-фенил-метил]-морфолин; 2-[(2-хлор-4-фтор-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин; 2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил; 2- [ (2-фторфенокси)-пиридин-3-ил-метил]-морфолин; 2-(морфолин-2-ил-пиридин-З-ил-метокси)-бензонитрил; 2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[пиридин-3-ил(2-трифторметокси-фенокси)-метил]-морфолин; 2-[(2,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[(1-окси-пиридин-2-илокси)-фенил-метил]-морфолин; 2-[(2'-хлор-бифенил-2-илокси)-фенил-метил]-морфолин; (2-фтор-6-метокси-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[(2-фтор-б-метокси-фенокси)-пиридин-3-ил-метил]-морфолин; 2- [2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин; 2-{[2-(4-фтор-фенил)-пиридин-3-илокси]-фенил-метил}-морфолин; 2- [ (2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; 2-[(2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; 2-[(2,6-дифтор-фенокси)-фенил-метил]-морфолин; 2-[2-циклогексил-1-(2-этокси-фенокси)-этил]-морфолин; 2-[1-(2-этокси-фенокси)-3-метил-бутил]-морфолин; 2-[(2-аллил-фенокси)-фенил-метил]-морфолин; 2-[фенил-(пиридин-3-илокси)-метил]-морфолин; 2-[(2-бром-пиридин-З-илокси)-фенил-метил]-морфолин 2-[фенил-(2-п-толил-пиридин-3-илокси)-метил]-морфолин; 2-[(2-хлор-фенокси)-фенил-метил]-морфолин; 2-[(2-изопропил-фенокси)-фенил-метил]-морфолин; 2-[(бензофуран-6-илокси)-фенил-метил]-морфолин; 2-[(2-изопропокси-фенокси)-фенил-метил]-морфолин; 2-[(2-бром-фенокси)-(4-фтор-фенил)-метил]-морфолин; 2-[(бензофуран-5-илокси)-фенил-метил]-морфолин; 2-(фенил-о-толилокси-метил)-морфолин; 2-(морфолин-2-ил-фенил-метокси)-фенол; 2-[циклогексил-(2-этокси-фенокси)-метил]-морфолин; 2-[фенил-(2-пиперазин-1-ил-фенокси)-метил]-морфолин; 2-[(2-метилсульфанил-фенокси)-фенил-метил]-морфолин; 2-[(2-метансульфонил-фенокси)-фенил-метил]-морфолин; 2-[(2-циклопентил-фенокси)-фенил-метил]-морфолин; 2-[(2-циклогексил-фенокси)-фенил-метил]-морфолин; 2-[(2-дифторметокси-фенокси)-фенил-метил]-морфолин; 2-{[2-(2-фтор-этокси)-фенокси]-фенил-метил}-морфолин; 2-[(4-фтор-2-изобутил-фенокси)-фенил-метил]-морфолин; 2- [ (2-хлор-6-фтор-фенокси)-фенил-метил]-морфолин; 2-[(2-циклопропилметил-фенокси)-фенил-метил]-морфолин; 2-[(2,6-дихлор-фенокси)-фенил-метил]-морфолин; 2-[(2-этоксиметил-фенокси)-фенил-метил]-морфолин; диметил-[2-(морфолин-2-ил-фенил-метокси)-фенил]-амин; 2-{[2-(4-фтор-фенокси)-пиридин-3-илокси]-фенил-метил}-морфолин; 2-[(2,6-дифтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; 2-[(2-бром-фенокси)-фенил-метил]-морфолин; 2-[(2,4-дифтор-фенокси)-фенил-метил]-морфолин; 2-[(4-фтор-фенокси)-фенил-метил]-морфолин; 2-[(2-этокси-фенокси)-(3-фтор-фенил)-метил]-морфолин; 2-[(2-циклопропил-фенокси)-фенил-метил]-морфолин; 2-(2-фенокси-феноксиметил)-морфолин; 2-(2'-хлор-бифенил-2-илоксиметил)-морфолин; 2-(2'-метокси-бифенил-2-илоксиметил)-морфолин; 2-(5-фтор-41-метил-бифенил-2-илоксиметил)-морфолин; 2-(5,4'-дифтор-бифенил-2-илоксиметил)-морфолин; 2-(2-фенокси-пиридин-З-илоксиметил)-морфолин; 2-[3-(4-фтор-фенокси)-пиразин-2-илоксиметил]-морфолин; 2-[2-(3,4-дифтор-фенокси)-пиридин-3-илоксиметил]-морфолин; 2-(фенокси-фенил-метил)-морфолин; 2- [ (4'-фтор-бифенил-2-илокси)-фенил-метил]-морфолин; 2-[(4'-метил-бифенил-2-илокси)-фенил-метил]-морфолин; 2-[(2-бензилокси-фенокси)-фенил-метил]-морфолин; 2-[(2-фтор-фенокси)-фенил-метил]-морфолин; [2-(морфолин-2-ил-фенил-метокси)-фенил]-метанол; 2- [ (2'-фтор-бифенил-2-илокси)-фенил-метил]-морфолин; 2- [ (2,4-дифтор-фенокси)-пиридин-2-ил-метил]-морфолин; 2-(2'-метил-бифенил-2-илоксиметил)-морфолин; 2- [2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин; 2- [ (2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; 2- [ (2-этокси-фенокси)-фенил-метил]-морфолин; 2-[(2-этокси-фенокси)-фенил-метил]-морфолин; 2-[морфолин-2-ил(фенил)метокси]бензонитрил; 2-[(2-хлор-5-фторфенокси)(фенил)метил]морфолин; 2-[(2-фтор-6-метоксифенокси)(фенил)метил]морфолин; 2-[(2,5-дифторфенокси)(фенил)метил]морфолин; 2-[фенил(2-пропилфенокси)метил]морфолин; 2- [ (2-этилфенокси) (фенил)метил]морфолин; 2-[циклопропил(2,4-дифторфенокси)метил]морфолин; 2-[(2-этоксифенокси)(1-оксидопиридин-2-ил)метил]морфолин; 2-[1-(2,6-дифторфенокси)-2-фенилэтил]морфолин; 2- [ [2-(бензилокси)фенокси] (пиридин-2-ил)метил]морфолин; 2-[(2-изопропилфенокси)(пиридин-2-ил)метил]морфолин; 2- [1-(2-этоксифенокси)бутил]морфолин; 2- [1-(2-этоксифенокси)-3-метилбутил]морфолин; 2-[(2 , 3-дифторфенокси) (3-хлорфенил)метил]морфолин; 2-[(2-этоксифенокси)(б-метилпиридин-2-ил)метил]морфолин; 2-[(2-этоксифенокси)(б-метоксипиридин-2-ил)метил]морфолин 2-{(6-метоксипиридин-2-ил) [2- .... - (трифторметокси)фенокси]метил}морфолин; 2-[(2,3-дигидро-1Н-инден-4-илокси)(пиридин-2-ил)метил]морфолин; 2-[(2,б-дифторфенокси)(4-фторфенил)метил]морфолин; 2-[(2-бромфенокси)(фенил)метил]морфолин; 2-[(2-хлор-б-фторфенокси)(фенил)метил]морфолин; 2-[(2-циклопропилфенокси)(фенил)метил]морфолин; N,N,КГ-триметил-2- [морфолин-2-ил(фенил)метокси]бензоламиний; 2-[{[2-(4-фторфенокси)пиридин-3-ил]окси}(фенил)метил]-морфолин; 2-[(2-бром-4-фторфенокси)(фенил)метил]морфолин; 2-[циклопропил(2-этоксифенокси)метил]морфолин; 2-[(2-циклопропил-4-фторфенокси)(фенил)метил]морфолин; 2-[[2-фторфенокси)](пиридин-2-ил)метил]морфолин; 2-[(2-циклопропил-4,6-дифторфенокси)(фенил)метил]морфолин 2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-[[(2-этилпиридин-З-ил)окси](фенил)метил]морфолин; 2-[морфолин-2-ил(пиридин-2-ил)метокси]бензонитрил; 2-[(2-изопропоксифенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-пропилфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-бензилфенокси)(пиридин-2-ил)метил]морфолин; 2-{пиридин-2-ил[2-(трифторметокси)фенокси]метил}морфолин; 2-[(2-изопропил-5-метилфенокси)(пиридин-2-ил)метил]морфолин; 2-[[(2-метилпиридин-З-ил)окси](фенил)метил]морфолин; 2-[(2-циклопентилфенокси)(пиридин-2-ил)метил]морфолин; 2-{пиридин-2-ил[2-(трифторметил)фенокси]метил]морфолин; 2 -[(2,6-дифторфенокси) (4-метил-1,3-оксазол-2-ил)метил]морфолин; 2-{фенил[(2-пропилпиридин-З-ил)окси]метил}морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]пропил}морфолин; 2-[[(2-этоксипиридин-З-ил)окси](фенил)метил]морфолин; 2-[(2-этоксифенокси)(З-метилпиридин-2-ил)метил]морфолин; 2-{(З-метилпиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; 2-[(2-изопропоксифенокси)(6-метоксипиридин-2-ил)метил]морфолин; 2-[(4-этилпиридин-2-ил)(2-фтор-6-метоксифенокси)метил]морфолин; 2-[(2-этоксифенокси)(4-этилпиридин-2-ил)метил]морфолин; 2-[1-бензофуран-2-ил(2,б-дифторфенокси)метил]морфолин; 2-{l-[(2-этоксипиридин-З-ил)окси]этил}морфолин; 2-[[2-(3-фторпропил)фенокси)(фенил)метил]морфолин; 2-[циклопент-1-ен-1-ил(2,б-дифторфенокси)метил]морфолин; 2-[(2,6-диметоксифенокси)(фенил)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]-3-метилбутил}морфолин; 2-[[(2-циклопропилпиридин-З-ил)окси](фенил)метил]морфолин; 2-{1-[2-(4-фторфенокси)фенокси]этил}морфолин; 2-[(2-хлор-5-фторфенокси)(пиридин-2-ил)метил]морфолин; 2-[(бифенил-2-илокси)(пиридин-2-ил)метил]морфолин; 2-[(2-циклопропилфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-бромфенокси)(пиридин-2-ил)метил]морфолин; 2-[[2-(фторметил)фенокси](фенил)метил]морфолин; 2-[(2-этокси-6-фторфенокси)(фенил)метил]морфолин; 2-[(2-фтор-6-метоксифенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-этокси-6-фторфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2,б-дифторфенокси)(пиридин-2-ил)метил]морфолин; 2-[[2-(3-фторпропокси)фенокси)(фенил)метил]-морфолин; 2-{2-циклогексил)-1-[(2-этоксипиридин-З-ил) окси]этил}морфолин; 2-[(2,6-дифторфенокси)(2,3-дигидро-1-бензофуран-7-ил)метил]морфолин; 2-[(2-циклопропил-5-фторфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-фтор-6-изопропоксифенокси)(фенил)метил]морфолин; 2-[[(2-метоксипиридин-З-ил)окси](фенил)метил]морфолин; 2-[(5-фтор-2-метоксифенокси)(фенил)метил]морфолин; 2-[(З-фтор-2-метоксифенокси)(фенил)метил]морфолин; 2-[(2-этокси-5-фторфенокси)(фенил)метил]морфолин; 2-[(2-этокси-З-фторфенокси)(фенил)метил]морфолин; 2-[(2-фтор-б-пропоксифенокси)(фенил)метил]морфолин; 2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-[(2,6-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-{(4-метил-1,З-оксазол-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; 2-[(2,6-дифторфенокси)(1,З-тиазол-2-ил)метил]морфолин; 2-{l-[(2-этоксипиридин-З-ил)окси]пентил}морфолин; 2-[(2-бромфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-[(2-фтор-6-метилфенокси)(фенил)метил]морфолин; 2-[[(2-изопропилпиридин-З-ил)окси](фенил)метил]морфолин; 2-[(2-этоксифенокси)(1,З-тиазол-2-ил)метил]морфолин; 2-[(2-этоксифенокси)(пиридин-2-ил)метил]морфолин; 2-[[(2-изобутилпиридин-З-ил)окси](фенил)метил]морфолин; 2- [ (2-фтор-6-изопропилфенокси) (фенил)метил]морфолин; 2-[(2-циклопропил-6-фторфенокси)(фенил)метил]морфолин; 2-[(2-бром-б-фторфенокси)(б-метоксипиридин-г-ил) метил] морфолин; 2-[(2-бром-б-фторфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-бромфенокси)(б-метоксипиридин-2-ил)метил]морфолин; 2-[(2-фтор-б-метоксифенокси)(6-метоксипиридин-2-ил)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]-2-метилпропил}морфолин; 2-[(2-циклопропилфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]бутил}морфолин; 2- [{ [2-(циклопропилметокси)пиридин-3-ил]окси}(фенил)метил]морфолин; 2-[ [2-фтор-6-(трифторметил)фенокси] (фенил)метил]морфолин; 2- [ [2-фтор-б-(трифторметокси)фенокси)(фенил)метил]морфолин; 2-[(2-этоксифенокси)(1,З-оксазол-2-ил)метил]морфолин; 2-[(2,б-дифторфенокси)(1,3-оксазол-2-ил)метил]морфолин; 2-{l-[(2-этоксипиридин-З-ил)окси]-2-фенилэтил}морфолин; 2-[[4-фтор-2-(метилтио)фенокси](фенил)метил]морфолин; 2- [ (2,6-дифторфенокси) (6-метоксипиридин-2-ил)метил]морфолин; 2,21 -[пиразин-2,3-диилбис(оксиметилен)]диморфолин; 2- [2-этокси-пиридин-3-илоксиметил]морфолин; и 2-[(2-фтор-6-метоксифенокси)(пиридин-3-ил)метил]морфолин. Соединения данного изобретения также включают следующие соединения и их фармацевтически приемлемые соли, энантиомеры и диастереомеры: (S)-2-[(S)-фенил-(2-трифторметокси-фенокси)-метил]-морфолин; (S)-2-[(S)-2-этилсульфанил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-(2-изобутил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-(2-бром-фенокси)-фенил-метил]-морфолин; (S)-2- [ (S)-фенил-(2-винил-фенокси)-метил]-морфолин; (S)-2-[(S)-(2-хлор-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-(2-метоксиметил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-фенил-(2-трифторметил-фенокси)-метил]-морфолин; (S)-2-[(S)-(2-бензил-фенокси)-фенил-метил]-морфолин; (S)-2- [ (S)-фенил-(2-пиридин-4-ил-фенокси)-метил]-морфолин; (S)-2-[(S)-(2-циклопропил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-(нафталин-1-илокси)-фенил-метил]-морфолин; (S)-2- [ (S)-фенил-(2-пиридин-З-ил-фенокси)-метил]-морфолин; (S)-2- [ (S)-(2-фенокси-фенокси)-фенил-метил]-морфолин; этиловый эфир (2S,3S)-2-(морфолин-2-ил-фенил-метокси)-бензойной кислоты; (S)-2-[((S)-4'-хлор-бифенил-2-илокси)-фенил-метил]-морфолин; (S)-2-(2-этокси-феноксиметил)-морфолин; (R)-2-[(S)-(2-фтор-фенокси)-фенил-метил]-морфолин; (S)-2-[(R)-(2-хлор-4-фтор-фенокси)-пиридин-3-ил-метил]-морфолин; (S)-2-[(R)-(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин; (S)-2-[(S)-(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин; (2S,3S)-2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил; (2S,3R)-2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил; (S)-2-[(S)-(2-фторфенокси)-пиридин-3-ил-метил]-морфолин; (2S,3R)-2-(морфолин-2-ил-пиридин-З-ил-метокси)-бензонитрил; (2R,3R)-2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; (2S,3R)-2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(S)-пиридин-3-ил(2-трифторметокси-фенокси)-метил]-морфолин; (R)-2-[(S)-(2-,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(R)-(2-,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин; (S)-2-[((S)-1-окси-пиридин-2-илокси)-фенил-метил]-морфолин; (S)-2- [ (S)-(2'-хлор-бифенил-2-илокси)-фенил-метил]-морфолин; (2R,3R)-(2-фтор-б-метокси-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(S)-(2-фтор-6-метокси-фенокси)-пиридин-3-ил-метил]-морфолин; (S)-2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин; (S)-2-{(S)-[2-(4-фтор-фенил)-пиридин-3-илокси]-фенил-метил }-морфолин; (R)-2-[(S)-(2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; (R)-2-[(S)-(2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; (S)-2-[(S)-(2,б-дифтор-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-2-циклогексил-1-(2-этокси-фенокси)-этил] морфолин; (2S, 3R) морфолин; (S) - 2- [ (S) - 2- [ (S) - 2- [ (S) - 2- [ морфолин; (S) - 2- [ морфолин; (S) - 2- [ (S) - 2- [ (R) - 2- [ (S) - 2- [ (R)- 2- [ морфолин; (S) - 2- [ (S) - 2- ( (2S, 3S) (S) - 2- [ (S) - 2- [ морфолин; (S) - 2- [ морфолин; (S) - 2- [ морфолин; (S) - 2- [ (S) - 2- [ (S) - 2- [ морфолин; (S) - 2-{ морфолин; (S) - 2- [ морфолин; (S) - 2- [ (S) - 2- [ [2-циклогексил-1-(2-этокси-фенокси)-этил]- -1-(2-этокси-фенокси)-3-метил-бутил]-морфолин; -(2-аллил-фенокси)-фенил-метил]-морфолин; -фенил-(пиридин-3-илокси)-метил]-морфолин; -(2-бром-пиридин-З-илокси)-фенил-метил]- -фенил-(2-п-толил-пиридин-3-илокси)-метил]- -(2-хлор-фенокси)-фенил-метил]-морфолин; -(2-изопропил-фенокси)-фенил-метил]-морфолин; -(бензофуран-6-илокси)-фенил-метил]-морфолин; -(2-изопропокси-фенокси)-фенил-метил]-морфолин; -(2-бром-фенокси)-(4-фтор-фенил)-метил]- -(бензофуран-5-илокси)-фенил-метил]-морфолин; -фенил-о-толилокси-метил)-морфолин; (морфолин-2-ил-фенил-метокси)-фенол; -циклогексил-(2-этокси-фенокси)-метил]-морфолин; -фенил-(2-пиперазин-1-ил-фенокси)-метил]- -(2-метилсульфанил-фенокси)-фенил-метил]- -(2-метансульфонил-фенокси)-фенил-метил]- -(2-циклопентил-фенокси)-фенил-метил]-морфолин; -(2-циклогексил-фенокси)-фенил-метил]-морфолин; -(2-дифторметокси-фенокси)-фенил-метил]- - [2-(2-фтор-этокси)-фенокси]-фенил-метил}- -(4-фтор-2-изобутил-фенокси)-фенил-метил]- -(2-хлор-6-фтор-фенокси)-фенил-метил]-морфолин; -(2-циклопропилметил-фенокси)-фенил-метил]- морфолин; (S (S (2S,3S)-диметил-[2-(морфолин-2-ил-фенил-метокси)-фенил]- амин; (S)-2-{(S)-[2-(4-фтор-фенокси)-пиридин-3-илокси]-фенил-метил} -морфолин; (R)-2-[(S)-(2,6-дифтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; (R) -2- [ (S) - (2- (S) -2- [ (S) -(2, (S) -2- [ (S) -(4- (R) -2- [ (S) - (2- морфолин (R (S (R (S (R (S (R (S (S морфолин; (S (S морфолин; (S морфолин; -2-[(S)-(2,6-дихлор-фенокси)-фенил-метил]-морфолин; -2-[(S)-(2-этоксиметил-фенокси)-фенил-метил]-морфолин; 2222222 2222-2- (S) - :(s) (S) - :(s) (2S, 3S) - [2 (S) - :(s) (S)-(2-циклопропил-фенокси)-фенил-метил]-морфолин; 2-фенокси-феноксиметил)-морфолин; 5-фтор-4'-метил-бифенил-2-илоксиметил)-морфолин; 5-фтор-41-метил-бифенил-2-илоксиметил)-морфолин; 5,4'-дифтор-бифенил-2-илоксиметил)-морфолин; 5,4'-дифтор-бифенил-2-илоксиметил)-морфолин; 2- фенокси-пиридин-3-илоксиметил)-морфолин; 3- (4-фтор-фенокси)-пиразин-2-илоксиметил]-морфолин 2-(3,4-дифтор-фенокси)-пиридин-3-илоксиметил]- (S)-фенокси-фенил-метил)-морфолин; (S)-(41-фтор-бифенил-2-илокси)-фенил-метил]- (S)-(4'-метил-бифенил-2-илокси)-фенил-метил]- морфолин; (2R,3R)-2-[(2,4-дифтор-фенокси)-пиридин-2-ил-метил] морфолин; (2R)-2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин; (2R)-2-[(R)-(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(S)-(2-этокси-фенокси)-фенил-метил]-морфолин; (S)-2-[(R)-(2-этокси-фенокси)-фенил-метил]-морфолин; 2-[(S)-(2S)-морфолин-2-ил(фенил)метокси]бензонитрил; (2S)-2-[(2-хлор-5-фторфенокси)(фенил)метил]-морфолин; (2S)-2-[(2-фтор-6-метоксифенокси)(фенил)метил]-морфолин; (2S)-2-[(S)-(2,5-дифторфенокси)(фенил)метил]-морфолин; (2S)-2- [ (S)-фенил(2-пропилфенокси)метил]-морфолин; (2S)-2-[(S)-(2-этилфенокси)(фенил)метил]-морфолин; (2S)-2-[циклопропил(2,4-дифторфенокси)метил]-морфолин; (2S)-2-[(S)-(2-этоксифенокси)(1-оксидопиридин-2-ил)метил]морфолин; (2S)-2- [1-(2,6-дифторфенокси)-2-фенилэтил]морфолин; (2S)-2- [ (S)- [2-(бензилокси)фенокси] (пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-изопропилфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(IS)-1-(2-этоксифенокси)бутил]морфолин; (2S)-2-[(IS)-1-(2-этоксифенокси)-3-метилбутил]морфолин; (2S)-2- [ (S)-(2,3-дифторфенокси) (3-фторфенил)метил]морфолин; (2S)-2-[(R)-(2,3-дифторфенокси)(3-фторфенил)метил]морфолин; (2S)-2- [ (S)-(2-этоксифенокси) (б-метилпиридин-г-ил) метил] морфолин; (2S)-2-[(S)-(2-этоксифенокси)(б-метоксипиридин-г-ил) метил] морфолин; (2S)-2-{(S)-(6-метоксипиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; (2S)-2-[(S)-(2,3-дигидро-1Н-инден-4-илокси)(пиридин-2-ил)метил]морфолин; (2R)-2-[(2,6-дифторфенокси)(4-фторфенил)метил]морфолин; (2R)-2-[(2-бромфенокси)(фенил)метил]морфолин; (2S)-2-[(S)-(2-хлор-6-фторфенокси)(фенил)метил]морфолин/ (2R)-2-[(2-циклопропилфенокси)(фенил)метил]морфолин; Ы,Ы,Ы-триметил-2-[(S)-(2S)-морфолин-2-ил(фенил)метокси]бензоламиний; (2S)-2-[(S)-{[2-(4-фторфенокси)пиридин-3-ил]окси}(фенил)метил]морфолин; (2S)-2-[(S)-(2-бром-4-фторфенокси)(фенил)метил]морфолин; (2S)-2-[циклопропил(2-этоксифенокси)метил]морфолин; (2S)-2- [ (S)-(2-циклопропил-4-фторфенокси)(фенил)метил]морфолин; (2S)-2- [ (S)- [2-фторфенокси)] (пиридин-2-ил)метил]морфолин; (2S)-2-[(R)-[2-фторфенокси)](пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-циклопропил-4,6-дифторфенокси)(фенил)метил]морфолин; (2S)-2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; (2S)-2-[(S)-[(2-этилпиридин-З-ил)окси](фенил)метил]морфолин; 2-[(S)-(2S)-морфолин-2-ил(пиридин-2-ил)метокси]бензонитрил; (2S)-2- [ (S)-(2-изопропоксифенокси) (пиридин-2-ил)метил]морфолин; (2S)-2- [ (S)-(2-пропилфенокси) (пиридин-2-ил)метил]морфолин (2S)-2-[(S)-(2-бензилфенокси)(пиридин-2-ил)метил]морфолин (2S)-2-{(S)-пиридин-2-ил[2-(трифторметокси)фенокси]метил}морфолин; (2S)-2- [ (S)-(2-изопропил-5-метилфенокси) (пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-[(2-метилпиридин-З-ил)окси](фенил)метил]морфолин; (2S)-2- [ (S)-(2-циклопентилфенокси) (пиридин-2-ил)метил]морфолин; (2S)-2-{(S)-пиридин-2-ил[2-(трифторметил)фенокси]метил]морфолин; (2S)-2-[(2,б-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; (2S)-2-{(S)-фенил[(2-пропилпиридин-З-ил)окси]метил}морфолин; (2S)-2-{l-[(2-этоксипиридин-З-ил)окси]пропил}морфолин; (2S)-2- [ (S)- [ (2-этоксипиридин-З-ил) окси] (фенил)метил]морфолин; (2S)-2-[(S)-(2-этоксифенокси)(З-метилпиридин-г-ил ) метил] морфолин; (2S)-2-{(S)-(З-метилпиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; (2S)-2-[(S)-(2-изопропоксифенокси)(6-метоксипиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(4-этилпиридин-2-ил)(2-фтор-б-метоксифенокси)метил]морфолин; (2S)-2-[(S)-(2-этоксифенокси)(4-этилпиридин-2-ил)метил]морфолин; (2S)-2- [1-бензофуран-2-ил(2,6-дифторфенокси)метил]морфолин; (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]этил}морфолин; (2S)-2- [ (S)- [2- (3-фторпропил)фенокси](фенил)метил]морфолин; (2S)-2-[(S)-циклопент-1-ен-1-ил(2,6-дифторфенокси)метил]морфолин; (2S)-2-[(R)-циклопент-1-ен-1-ил(2,6-дифторфенокси)метил]морфолин; (2S)-2-[(2,6-диметоксифенокси)(фенил)метил]-морфолин; (2S)-2-{1- [ (2-этоксипиридин-З-ил)окси]-3-метилбутил}морфолин; (2S)-2-[(S)-[(2-циклопропилпиридин-З-ил)окси](фенил)метил]морфолин; (2S)-2-{1-[2-(4-фторфенокси)фенокси]этил}морфолин; (2S)-2- [ (S)-(2-хлор-5-фторфенокси) (пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(бифенил-2-илокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-циклопропилфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-бромфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2- [ [2-(фторметил)фенокси] (фенил)метил]морфолин; (2S)-2-[(2-этокси-6-фторфенокси)(фенил)метил]морфолин; (2S)-2- [ (S)-(2-фтор-6-метоксифенокси) (пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-этокси-6-фторфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2,6-дифторфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-[2-(3-фторпропокси)фенокси](фенил)метил]морфолин; (2S)-2-{(1S)-2-циклогексил-1-[(2-этоксипиридин-З-ил) окси]этил}морфолин; (2S)-2-[(2,6-дифторфенокси)(2,3-дигидро-1-бензофуран-7-ил)ме тил]морфолин; (2S)-2- [ (S)-(2-циклопропил-5-фторфенокси) (пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-фтор-6-изопропоксифенокси)(фенил)метил]морфолин; (2S)-2-[(S)-[(2-метоксипиридин-З-ил)окси](фенил)метил]морфолин; (2S)-2-[(5-фтор-2-метоксифенокси)(фенил)метил]морфолин; (2S)-2-[(З-фтор-2-метоксифенокси)(фенил)метил]морфолин; (2S)-2-[(2-этокси-5-фторфенокси)(фенил)метил]морфолин; (2S)-2- [ (2-этокси-З-фторфенокси) (фенил)метил]морфолин; (2S)-2-[(S)-(2-фтор-6-пропоксифенокси)(фенил)метил]морфолин; (2S)-2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; (2S)-2-[(2,6-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; (2S)-2-{(4-метил-1,З-оксазол-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; (2S)-2- [ (2,6-дифторфенокси) (1,З-тиазол-2-ил)метил]морфолин; (2S)-2-{(IS)-1- [ (2-этоксипиридин-З ил)окси]пентил}морфолин; (2S)-2-[(2-бромфенокси)(4-метил-1,З-оксазол-2-ил)метил]-морфолин; (2S)-2-[(S)-(2-фтор-6-метилфенокси)(фенил)метил]-морфолин; (2S)-2- [ (S)-[(2-изопропилпиридин-З-ил)окси](фенил)метил]морфолин; (2S)-2-[(2-этоксифенокси)(1,3-тиазол-2-ил)метил]морфолин; (2R)-2-[(R)-(2-этоксифенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-[(2-изобутилпиридин-З-ил)окси](фенил)метил]морфолин; (2S)-2- [ (S)-(2-фтор-б-изопропилфенокси)(фенил)метил]морфолин; (2S)-2- [ (S)-(2-циклопропил-6-фторфенокси)(фенил)метил]морфолин; (2S) -2-[(S)-(2 -бром-6-фторфенокси)(6-метоксипиридин-2- ил)метил] морфолин; (2S) -2-[(S)-(2 -бром-6-фторфенокси)(пиридин-2- ил)метил] морфолин; (2S) -2- [(S)-(2 -бромфенокси)(6-метоксипиридин-2- ил)метил] морфолин; (2S) -2-[(S)-(2 -фтор-6-метоксифенокси)(6-метоксипиридин ил)метил] -морфолин; (2S) -2-{1- [(2-1 этоксипиридин-3-ил)окси]-2- метилпропил}морфолин; (2S)-2-[(2-циклопропилфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]бутил}морфолин; (2S)-2-[(S)-{[2-(циклопропилметокси)пиридин-Зил) окси} (фенил)метил]морфолин; (2S)-2- [ (S)- [2-фтор-6-(трифторметил)фенокси](фенил)метил]морфолин; (2S)-2- [ (S)-[2-фтор-6-(трифторметокси)фенокси)(фенил)метил]морфолин; (S)-2-[(2-этоксифенокси)(1,З-оксазол-2-ил)метил]морфолин; (S)-2-[(2,6-дифторфенокси)(1,З-оксазол-2-ил)метил]морфолин; (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]-2-фенилэтил}морфолин; (2S)-2-[(S)-[4-фтор-2-(метилтио)фенокси)(фенил)метил]морфолин; (2S)-2-[(S)-(2,6-дифторфенокси)(б-метоксипиридин-2-ил)метил]-морфолин; (2R,21R)-2,21 -[пиразин-2,3-диилбис(оксиметилен)]диморфолин; (S)-2-[2-этокси-пиридин-3-илоксиметил]морфолин; и (2R)-2-[(2-фтор-6-метоксифенокси)(пиридин-Зил )метил]морфолин. Настоящее изобретение касается способа лечения синдрома дефицита внимания с гиперактивностью, расстройств мочеиспускания, боли, тревожности, депрессии, преждевременной эякуляции или фибромиалгии, который включает введение терапевтически эффективного количества соединения, как это определено в любой из формул I, II, III. Соответственно, один аспект настоящего изобретения направлен на способ селективного ингибирования обратного захвата норэпинефрина и используемые для этого соединения, способ, включающий стадию введения пациенту терапевтически эффективного количества соединения или композиции, соединение или композицию, содержащую соединение, имеющее фармакологическую селективность по отношению к серотонину (Ki)/норэпинефрину (Ki), равную, по меньшей мере, 25, предпочтительно, по меньшей мере, примерно, 50, и более предпочтительно, по меньшей мере, примерно 200. Другой аспект настоящего изобретения направлен на способ лечения страдания человека от состояния или профилактики состояния, где ингибирование обратного захвата норэпинефрина приносит пользу, способ, включающий стадию введения терапевтически эффективного количества композиции, содержащей соединение, имеющее фармакологическую селективность по отношению к серотонину (Ki)/норэпинефрину (Ki), равную, по меньшей мере, 25, предпочтительно, по меньшей мере, примерно, 50, и более предпочтительно, по меньшей мере, примерно 200. Это изобретение также касается способа лечения нарушения или состояния, выбранного из группы, состоящей из норэпинефриновой дисфункции, единичных эпизодических или регулярных основных депрессивных состояний, дистимических нарушений, депрессивного невроза и невротической депрессии, меланхолической депрессии, включая анорексию, потерю веса, бессонницу, раннее утреннее пробуждение или психомоторную заторможенность, атипичную депрессию (или реактивную депрессию) включая повышенный аппетит, сонливость, психомоторное возбуждение или возбудимость, зимнюю депрессию и детскую депрессию; биполярных расстройств или маниакальной депрессии, включая биполярное расстройство 1-го типа, биполярное расстройство 11-го типа и циклотимическое расстройство; расстройства поведения; расстройства, связанного с агрессивным поведением; расстройств поведения, связанных с умственной отсталостью, аутизмом и поведенческих расстройств; таких тревожных расстройств, как паническое расстройство с или без агорафобии, агорафобия без истории панического расстройства, определенные фобии, например, боязни животных, социальная тревожность, социофобия, (включая социальную тревожность), навязчивые состояния, и связанные с ними обширные расстройства, стрессовые нарушения, включающие посттравматическое стрессовое нарушение, острое стрессовое нарушение и хроническое стрессовое нарушение, и генерализованные состояния тревожности; пограничных личностных расстройств; шизофрении и других психотических расстройств, например, шизофреноподобных расстройств; шизоаффективных нарушений, бредовых расстройств, кратковременных психотических расстройств, общих психотических расстройств, психотических расстройств с бредом и галлюцинациями, психотических приступов тревожности, психоза связанного с тревожностью, психотических расстройств настроения, включая острое основное депрессивное состояние; расстройств настроения, связанных с психотическими нарушениями, включающими острую манию и депрессию, связанную с биполярным расстройством; расстройств настроения, связанных с шизофренией; делирия, деменции, и амнестического и других когнитивных или нейродегенеративных расстройств, включающих болезнь Паркинсона (БП), болезнь Хантингтона, болезнь Альцгеймера, старческое слабоумие, деменцию по типу болезни Альцгеймера, нарушения памяти, потерю дееспособности, мультиинфарктную деменцию и другие деменции, включающие, относящихся к заболеванию ВИЧ, травме головы, болезни Паркинсона, болезни Хантингтона, болезни Пика, болезни Крейтцфельда-Якоба, или относящихся к множественной этиологии; расстройств движений, включающих акинезии, дискинезии, включая семейные пароксизмальные дискинезии, спазмы, синдром де ла Туретта, синдром Скотта, параличи и акинетический ригидный синдром; экстрапирамидальные двигательные расстройства, включая двигательные расстройства, вызванные лечением, включая паркинсонизм, индуцированный нейролептиками, злокачественный нейролептический синдром, острую дистонию, индуцированную нейролептиками, острую акатизию, индуцированную нейролептиками, отсроченную дискинезию, индуцированную нейролептиками и индуцированный лечением постуральный тремор; расстройств связанных с привыканием и абстинентного синдрома, химических зависимостей и привыкания (включающих зависимости от алкоголя, героина, кокаина, бензодиазепинов, психоактивных веществ, никотина, или фенобарбитала) и поведенческих привычек, включающих привычку к игре; нарушений зрения, включающих глаукому и ишемическую ретинопатию (включая те, что возникают благодаря привыканию к алкоголю, никотину и другим психоактивным веществам) и абстинентного синдрома, нарушения адаптации (включая подавленное состояние, тревожность, сочетание тревожности и подавленного состояния, расстройство поведения и сочетание расстройства поведения и настроения); возрастных нарушений обучаемости и психических расстройств (включая болезнь Альцгеймера); нервно-психических анорексий; апатии; нарушений внимания (или других когнитивных нарушений), обусловленных основными клиническими состояниями, включающими синдром дефицита внимания (СДВ) и синдром дефицита внимания с гиперактивностью (СДВГ) и его узнаваемые подтипы; нейрогенной булимии; синдрома хронической усталости; боли; хронической боли; циклотимического нарушения; депрессии (включающей пубертатную депрессию и малую депрессию); фибромиалгии и других соматических нарушений (включая соматизацию; конверсионные расстройства; болевые расстройства; ипохондрии; дизморфизм, недифференцированное соматоформное расстройство и соматоподобные NOS); недержания (то есть стрессовое недержание; истинное недержания мочи при напряжении и смешанное недержание); расстройств мочеиспускания; преждевременной эякуляции; расстройств дыхания; интоксикаций (включающих алкогольную зависимость); мании; мигреней; ожирения (то есть снижение веса у пациентов с ожирением или избыточным весом); оппозиционно-вызывающего расстройства; периферической нейропатии; диабетической нейропатии; постгерпетической невралгии; предменструального дисфорического расстройства (то есть предменструальный синдром дисфорического расстройства поздней стадии лютеинизации); нарушений сна (то есть нарколепсию, бессонницу, и энурез); определенных нарушений развития; ингибирования селективного обратного захвата серотонина (СОЗС) синдрома "выхода из игры" (то есть в случае, когда пациент перестает проявлять удовлетворительную реакцию на терапию после начального периода удовлетворительной реакции); и судорожных нарушений (например, болезнь Туретта) у млекопитающих, включая человека, включающего введение животному, нуждающемуся в таком лечении количества соединения формулы I, II или III, или его фармацевтически приемлемой соли, эффективного в лечении такого расстройства или состояния. Другой аспект настоящего изобретения направлен на получение лекарственного препарата из композиции, содержащей соединение с фармакологической селективностью по отношению к серотонину (Ki)/норэпинефрину (Ki), равную, по меньшей мере, 25, предпочтительно, по меньшей мере, примерно, 50, и более предпочтительно, по меньшей мере, примерно 200 для лечения или профилактики, по меньшей мере, ранее упомянутых расстройств центральной нервной системы. Это изобретение также касается фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы I, II или III, или его фармацевтически приемлемой соли, и фармацевтически приемлемый носитель. Это изобретение также касается фармацевтической композиции для лечения расстройства или состояния, выбранного из норэпинефриновой дисфункции, единичных эпизодических или регулярных основных депрессивных состояний, дистимических нарушений, депрессивного невроза и невротической депрессии, меланхолической депрессии, включая анорексию, потерю веса, бессонницу, раннее утреннее пробуждение или психомоторную заторможенность, атипичную депрессию (или реактивную депрессию), включая повышенный аппетит, сонливость, психомоторное возбуждение или возбудимость, зимнюю депрессию и детскую депрессию; биполярных расстройств или маниакальной депрессии, включая биполярное расстройство 1-го типа, биполярное расстройство II-го типа и циклотимическое расстройство; расстройства поведения; расстройства, связанного с агрессивным поведением; расстройствповедения, связанных с умственной отсталостью, аутизмом и расстройством поведения; тревожных расстройств, таких как паническое расстройство с или без агорафобии, агорафобия без истории панического расстройства, определенные фобии, например, боязни животных, социальная тревожность, социофобия, (включая социальную тревожность), навязчивые состояния и связанные с ними обширные расстройства, стрессовые нарушения, включающие посттравматическое стрессовое нарушение, острое стрессовое нарушение и хроническое стрессовое нарушение, и генерализованные состояния тревожности; пограничных личностных расстройств; шизофрении и других психотических расстройств, например, шизофреноподобных расстройств; шизоаффективных нарушений, бредовых расстройств, кратковременных психотических расстройств, общих психотических расстройств, психотических расстройств с бредом и галлюцинациями, психотических приступов тревожности, психоза, связанного с тревожностью, психотических расстройств настроения, включая острое основное депрессивное состояние; расстройств настроения, связанных с психотическими нарушениями, включающими острую манию и депрессию, связанную с биполярным расстройством; расстройств настроения, связанных с шизофренией; делирия, деменции, и амнестического и других когнитивных или нейродегенеративных расстройств, включающих болезнь Паркинсона (БП), болезнь Хантингтона, болезнь Альцгеймера, старческое слабоумие, деменцию по типу болезни Альцгеймера, нарушения памяти, потерю дееспособности, мультиинфарктную деменцию и другие деменции, включающие, относящихся к заболеванию ВИЧ, травме головы, болезни Паркинсона, болезни Хантингтона, болезни Пика, болезни Крейтцфельда-Якоба, или относящихся к множественной этиологии; расстройств движений, включающих акинезии, дискинезии, включая семейные пароксизмальные дискинезии, спазмы, синдром де ла Туретта, синдром Скотта, параличи и акинетический ригидный синдром; экстрапирамидальные двигательные расстройства, включая двигательные расстройства, вызванные лечением, включая паркинсонизм, индуцированный нейролептиками, злокачественный нейролептический синдром, острую дистонию, индуцированную нейролептиками, острую акатизию, индуцированную нейролептиками, отсроченную дискинезию, индуцированную нейролептиками и индуцированный лечением постуральный тремор; расстройств, связанных с привыканием, и абстинентного синдрома, химических зависимостей и привыкания (включающих зависимости от алкоголя, героина, кокаина, бензодиазепинов, психоактивных веществ, никотина, или фенобарбитала) и поведенческих привычек, включающих привычку к игре; нарушений зрения, включающих глаукому и ишемическую ретинопатию (включая те, что возникают благодаря привыканию к алкоголю, никотину и другим психоактивным веществам) и абстинентного синдрома, нарушения адаптации (включая подавленное состояние, тревожность, сочетание тревожности и подавленного состояния, расстройство поведения и сочетание расстройства поведения и настроения); возрастных нарушений обучаемости и психических расстройств (включая болезнь Альцгеймера); нервно-психических анорексий; апатии; нарушений внимания (или других когнитивных нарушений), обусловленных основными клиническими состояниями, включающими синдром дефицита внимания (СДВ) и синдром дефицита внимания с гиперактивностью (СДВГ) и его узнаваемые подтипы; нейрогенной булимии; синдрома хронической усталости; боли; хронической боли; циклотимического нарушения; депрессии (включающей пубертатную депрессию и малую депрессию); фибромиалгии и других соматических нарушений (включая соматизацию; конверсионные расстройства; болевые расстройства; ипохондрии; дизморфизм; недифференцированное соматоформное расстройство и соматоподобные NOS); недержания (то есть стрессовое недержание; истинного недержания мочи при напряжении и смешанного недержания); расстройств мочеиспускания; преждевременной эякуляции; расстройств дыхания; интоксикаций (включающих алкогольную зависимость); мании; мигреней; ожирения (то есть снижение веса у пациентов с ожирением или избыточным весом); оппозиционно-вызывающего расстройства; периферической нейропатии; диабетической нейропатии; постгерпетической невралгии; предменструального дисфорического расстройства (то есть предменструальный синдром дисфорического расстройства поздней стадии лютеинизации); нарушений сна (то есть нарколепсию, бессонницу и энурез); определенных нарушений развития; ингибирования селективного обратного захвата серотонина (СОЗС) синдрома "выхода из игры" (то есть в случае, когда пациент перестает проявлять удовлетворительную реакцию на терапию после начального периода удовлетворительной реакции); и судорожных нарушений (например, болезнь Туретта) у млекопитающих, включая человека, включающего введение животному, нуждающемуся в таком лечении количества соединения формулы I, II или III, или его фармацевтически приемлемой соли, эффективной в лечении такого расстройства или состояния, и фармацевтически приемлемого носителя. Другой специфический аспект этого изобретения касается вышеуказанного способа, где соединение формулы I, II или III, вводят человеку для лечения любых двух или более сопутствующих расстройств или состояний, выбранных из тех расстройств и состояний, на которые ссылаются в каких либо приведенных ранее способах. Для лечения СДВГ, депрессии, тревожности, шизофрении или любых других расстройств, на которые ссылаются в описаниях способов и фармацевтических композиций этого изобретения, новые соединения этого изобретения могут использоваться в связи с одним или большим числом дополнительных активных агентов, включающих антидепрессанты, антипсихотические средства (антипсихотики), или противотревожные средства. Примеры классов антидепрессантов, которые могут использоваться в комбинации с активными соединениями этого изобретения, включают ингибиторы обратного захвата норэпинефрина (ИОЗН), селективные ингибиторы обратного захвата серотонина (ИОЗС), антагонисты рецепторов НК-1, ингибиторы моноаминооксидазы (ИМАО), обратимые ингибиторы моноаминооксидазы (ОИМАО), ингибиторы обратного захвата серотонина и норэпинефрина, антагонисты кортикотропин-рилизинг фактора (КРФ), антагонисты а-адренорецепторов, альфа-2-дельта лиганды (А2Д), и атипичные антидепрессанты. Другим типом агента, который может быть использован в комбинации с новыми соединениями этого изобретения, являются агонисты или антагонисты никотиновых рецепторов. ИОЗС, применяемые в способах и фармацевтических композициях настоящего изобретения, включают, но не ограничиваются, сертралином (Золофтом(r)), метаболитом сертралина, диметилсертралином, флуоксетином (Прозаком(r)), норфлуоксетином (десметиловым метаболитом флуоксетина), флувоксамином (Лувоксом(r)), пароксетином (Сероксатом(r), Паксилом(r)) и его альтернативной формой Паксилом-CR(r), циталопрамом (Целексой(r)), метаболитом циталопрама десметилциталопрамом, эсциталопрамом (Лексапро(r)), фенфлурамином (Пондимином(r)), фемоксетином, ифоксетином, цианодотиепином, литоксетином, церикламином, дапоксетином, нефазаодоном (Серксоне(r)), и тразодоном (Дезирелом(r)) или любым их пролекарством или любой фармацевтически приемлемой солью или пролекарством ИОЗС. ИОЗН, применяемые в способах и фармацевтических композициях настоящего изобретения, включают, но не ограничиваются, ребоксетином (Эдронаксом(r)) и всеми изомерами ребоксетина, например, (R/R,S/S,R/S,S/R) , дезипрамином (Норпрамином(r)), мапротилином (Людиомилом(r)), лофепрамином (Гаманилом(r)), миртазепином (Ремероном(r)), оксапротилином, фезоламином, атомексетином (Стратерра(r)) и бупроприоном (Велбутрином(r)), метаболитом бупроприона - гидроксибупроприоном, номифензином (Мериталом(r)), вилоксазином (Виваланом(r)), или миансерином (Болвидоном(r)) или любым их пролекарством или любой фармацевтически приемлемой солью или пролекарством ИОЗН. Фармацевтические агенты, которые ингибируют обратный захват серотонина и норэпинефрина включают венлафаксин (Еффексор(r)), метаболит венлафаксина О-десметилвенлафаксин, кломипрамин (Анафранил(r)), метаболит кломипрамина десметилкломипрамин, дулоксетин (Кимбальта(r)), милнаципран и имипрамин (Тофранил(r) или Жанимин(r)). Примерами предпочтительных А2Д лигандов для использования в настоящем изобретении являются те, что раскрыты в патенте США 4024175, особенно, габапентин, ЕР641330, особенно, прегабалин, в патенте США 5563175, W09733858, W09733859, WO9931057, WO9931074, WO9729101, WO02085839, особенно, [(1R,5R,6S)-6- (аминометил)бицикло[3.2.0]гепт-6-ил]уксусная кислота, W09931075, особенно, 3-(1-аминометил-циклогексилметил)-4Н- [1,2,4]оксадиазол-5-он и С- [1-(1Н-тетразол-5-илметил)- циклогептил]-метиламин, W09921824, особенно, (3S,4S)-(1-аминометил-3,4 -диметил-циклопентил)-уксусная кислота, WO0190052, W00128978, особенно, (1а,За,5а)(3-аминометил-бицикло[3.2.0]гепт-3-ил)-уксусная кислота, ЕР0641330, W09817627, WO0076958, особенно, (3S,5R)-З-аминометил-5-метил-октановая кислота, USSN 10/401,060, особенно, (3S,5R)-3-амино-5-метил-гептановая кислота, USSN 10/401,060, (3S,5R)-3-амино-5-метил-нонановая кислота, и (3S,5R)-З-аминометил-5-метил-октановая кислота, ЕР1178034, ЕР1201240, WO9931074, WO03000642, WO0222568, WO0230871, WO0230881 WO02100392, WO02100347, WO0242414, WO0232736 и WO0228881, и их фармацевтически приемлемые соли и сольваты. Подходящие антагонисты КРФ включают соединения, описанные в международных заявках Ш WO 94/13643, WO 94/13644, WO 94/13661, WO 94/13676 и WO 94/13677. Подходящие атипичные антидепрессанты включают бупроприон, литий, нефазодон, тразодон и вилоксазин. Подходяще антагонисты рецепторов НК-1 включают те, на которые имеется ссылка в публикации международной заявки W0 01/77100. Подходящие классы противотревожных агентов, которые могут быть использованы в комбинации с активными соединениями этого изобретения, включают бензодиазепины и агонисты или антагонисты серотонина IA (5-HTiA) , особенно, частичные агонисты 5-НТ1А, и антагонисты кортикотропин-рилизинг фактора (КРФ). Подходящие бензодиазепины включают алпразолам, . хлордиазопоксид, клоназепам, хлоразепат, диазепам, галазепам, лоразепам, оксазепам и празепам. Подходящие агонисты или антагонисты рецепторов 5-НТ1А включают буспирон, флезиноксан, гепирон и ипзапирон. Подходящие антипсихотические агенты включают обычные и атипичные антипсихотики. Обычные антипсихотики являются антагонистами допаминовых рецепторов (D2). Атипичные антипсихотики также имеют антагонистические свойства в отношении D2, но обладают отличной кинетикой связывания с этими рецепторами и активностью в отношении других рецепторов, особенно, 5-НТ2А, 5-НТ2с и 5-HT2d (Schmidt В et al, Soc. Neurosci. Abstr. 24: 2177, 1998). Примеры лигандов допаминовых рецепторов (D4) описаны в патентах США 6548502, 5852031, 5883094, 5889010 и WO 98/08835. Примеры агонистов и антагонистов никотиновых рецепторов включают: варениклин, производные азаиндол-этиламина, как это описано в патенте США 5977131, и аналоги, производные, пролекарства, фармацевтически приемлемые соли и пролекарства агонистов или антагонистов никотиновых рецепторов. Особенно предпочтительным агонистом никотиновых рецепторов является варениклин, 7,8,9,10-тетрагидро-6,10-метано-бН- пиразино[2,З-h][3]бензапин(2R,3R)-2,3-дигидроксибутандиоат, или любая его фармацевтически приемлемая соль, включая любую его полиморфную форму или пролекарство, или любую фармацевтически приемлемую соль такого пролекарства. Предпочтительной солью варениклина является варениклина тартрат. Варениклин является частичным никотиновым агонистом с аффинностью к некоторым, но не ко всем, подтипам никотиновых рецепторов. Синтез варениклина тартрата описан в W0 99/35131, патенте США № 6410550, заявках №№ 1997070245, 2002072524, 2002072525, 2002111350, и 2002132824. Класс атипичных антипсихотиков включает клозапин (Клозарил(r)), 8-хлор-11-(4-метил-1-пиперазинил)-5Н- дибензо[b,е][1,4]диазепин (патент США № 3539573); рисперидон (Риспердал(r)), 3- [2- [4- (6-фтор-1,2-бензизоксазол-З- ил)пиперидино]этил]-2-метил-6,7,8,9-тетрагидро-4Н-пиридо-[1,2- a] пиримидин-4-он (патент США № 4804663); оланзапин (Зипрекса(r)), 2-метил-4-(4-метил-1-пиперазинил)-10Н-тиено[2,3- b] [1,5]бензодиазепин (патент США № 5229382); квитиапин (Сероквель(r)), 5-[2-(4-дибензо[b,f][1,4]тиазепин-11-ил-1-пиперазинил)этокси]этанол (патент США № 4879288); арипипразол (Абилифай(r)), 7-{4- [4-(2,3-дихлорфенил)-1-пиперазинил]-бутокси}-3,4-дигидрокарбостирил и 7-{4- [4-(2,3-дихлорфенил)-1-пиперазинил]-бутокси}-3,4-дигидро-2(1Н)-хинолинон (патенты США №№ 4734416 и 5006528); сертиндол, 1-[2-[4-[5-хлор-1-(4-фторфенил)-1Н-индол-3-ил]-1-пиперидинил]этил]имидазолидин-2-он (патент США № 4710500); амисулприд (патент США № 4410822); ципразидон (Геодон(r)) гидрат гидрохлорида 5-[2-[4-(1,2-бензизотиазол-3-ил)пиперазин-3-ил]этил]-6-хлориндолин-2-она (патент США № 4831031); и азенапин транс-5-хлор-2-метил-2,3,За,12Ь-тетрагидро-1Н-дибенз[2,3:6,7]оксепино[4,5-с]пиррол (патенты США №№ 4145434 и 5763476). Это изобретение также касается способа лечения расстройства или состояния, выбранного из расстройств связанных с привыканием (включающих зависимости от алкоголя, никотина и других психоактивных веществ) и абстинентного синдрома, нарушений адаптации (включая подавленное состояние, тревожность, сочетание тревожности и подавленного состояния, расстройство поведения и сочетание расстройства поведения и настроения); возрастных нарушений обучаемости и психических расстройств (включая болезнь Альцгеймера); нервно-психических анорексий; апатии; нарушений внимания (или других когнитивных нарушений) обусловленных основными клиническими состояниями, включающими синдром дефицита внимания (СДВ) и синдром дефицита внимания с гиперактивностью (СДВГ) и его узнаваемые подтипы; нейрогенной булимии; синдрома хронической усталости; боли; хронической боли; циклотимического нарушения; депрессии (включающей пубертатную депрессию и малую депрессию); фибромиалгии и других соматоподобных нарушений (включая соматизацию; конверсионные расстройства; болевые расстройства; ипохондрии; дизморфизм; недифференцированное соматоформное расстройство; и соматоподобные NOS); недержания (то есть стрессового недержания; истинного недержания мочи при напряжении и смешанного недержания); расстройств мочеиспускания; преждевременной эякуляции; расстройств дыхания; интоксикаций (включающих алкогольную зависимость); мании; мигреней; ожирения (то есть снижения веса у пациентов с ожирением или избыточным весом); оппозиционно-вызывающего расстройства; периферической нейропатии; диабетической нейропатии; постгерпетической невралгии; предменструального дисфорического расстройства (то есть предменструального синдрома дисфорического расстройства поздней стадии лютеинизации); нарушений сна (то есть нарколепсии, бессонницы и энуреза); определенных нарушений развития; селективного ингибирования обратного захвата серотонина (СОЗС) синдрома "выхода из игры" (то есть в случае, когда пациент перестает проявлять удовлетворительную реакцию на терапию после начального периода удовлетворительной реакции); и судорожных нарушений (например, болезнь Туретта) у млекопитающих, включая человека, включающего введение животному, нуждающемуся в таком лечении: (a) соединения формулы I, II или III, или его фармацевтически приемлемой соли; и (b) другого фармацевтически активного соединения, являющегося антидепрессантом, антипсихотиком или противотревожным агентом, или его фармацевтически приемлемой солью; где активные соединения "а" и "Ь" присутствуют в количествах, делающих комбинацию эффективной в лечении такого расстройства или состояния. Другой более специфический аспект настоящего изобретения касается вышеуказанного способа, где соединения формулы I, II или III, и дополнительный фармацевтический агент, включая антидепрессант, противотревожный агент или антипсихотический агент, вводят человеку для лечения одного или более сопутствующих расстройств или состояний, выбранных из тех расстройств и состояний, на которые ссылаются в любых из вышеуказанных способов. Это изобретение также касается фармацевтической композиции для лечения расстройства или состояния, выбранных из расстройств, связанных с привыканием (включающих зависимости от алкоголя, никотина и других психоактивных веществ), и абстинентного синдрома, нарушений адаптации (включая подавленное состояние, тревожность, сочетание тревожности и подавленного состояния, расстройство поведения и сочетание расстройства поведения и настроения); возрастных нарушений обучаемости и психических расстройств (включая болезнь Альцгеймера); нервно-психических анорексий; апатии; нарушений внимания (или других когнитивных нарушений), обусловленных основными клиническими состояниями, включающими синдром дефицита внимания (СДВ) и синдром дефицита внимания с гиперактивностью (СДВГ) и его узнаваемые подтипы; нейрогенной булимии; синдрома хронической усталости; боли; хронической боли; циклотимического нарушения; депрессии (включающей пубертатную депрессию и малую депрессию); фибромиалгии и других соматоподобных нарушений (включая соматизацию; конверсионные расстройства; болевые расстройства; ипохондрии; дизморфизм; недифференцированное соматоформное расстройство; и соматоподобные NOS); недержания (то есть стрессового недержания; истинного недержания мочи при напряжении и смешанного недержания); расстройств мочеиспускания; преждевременной эякуляции; расстройств дыхания; интоксикаций (включающих алкогольную зависимость); мании; мигреней; ожирения (то есть снижения веса у пациентов с ожирением или избыточным весом); оппозиционно-вызывающего расстройства; периферической нейропатии; диабетической нейропатии; постгерпетической невралгии; предменструального дисфорического расстройства (то есть предменструального синдрома дисфорического расстройства поздней стадии лютеинизации); нарушений сна (то есть нарколепсии, бессонницы и энуреза); определенных нарушений развития; селективного ингибирования обратного захвата серотонина (СОЗС) синдрома "выхода из игры" (то есть в случае, когда пациент перестает проявлять удовлетворительную реакцию на терапию после начального периода удовлетворительной реакции); и судорожных нарушений (например, болезнь Туретта) у млекопитающего, включая человека, включающей: (a) соединение формулы I, II или III, или его фармацевтически приемлемую соль; и (b) другое фармацевтически активное соединение, включая антидепрессант или противотревожный агент, или его фармацевтически приемлемую соль; и (c) фармацевтически приемлемый носитель; где активные соединения "а" и "Ь" присутствуют в количествах, делающих комбинацию эффективной в лечении такого расстройства или состояния. Другой аспект настоящего изобретения направлен на использование композиции, содержащей соединение формулы I, II, или III, имеющей фармакологическую селективность по отношению к серотонину (Ki)/норэпинефрину (Ki), равную, по меньшей мере, 25, предпочтительно, по меньшей мере, примерно, 50, и более предпочтительно, по меньшей мере, примерно 200 в производстве леакрственного препарата для лечения или профилактики, по меньшей мере, одного из ранее упомянутых расстройств центральной нервной системы. Это изобретение также касается фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы I, II или III, или его фармацевтически приемлемой соли, и фармацевтически приемлемого носителя. Соединения формул I, II или III могут содержать хиральные центры и, следовательно, могут существовать в различных энантиомерных и диастереомерных формах. Это изобретение касается всех оптических изомеров и всех стереоизомеров соединений формул I, II или III, как рацемических смесей, так и индивидуальных энантиомеров и диастереомеров таких соединений, и их смесей и всех фармацевтических композиций и способов лечения, определенных выше, которые их содержат или используют, соответственно. Индивидуальные изомеры могут быть получены такими известными способами, как классическое разделение, стереоселективное взаимодействие или хроматографическое разделение с получением конечного продукта или промежуточного соединения. Индивидуальные энантиомеры соединений формул I, II или III могут иметь, по сравнению с рацемическими смесями этих соединений, преимущества в лечении различных расстройств и состояний. Когда в молекуле есть два хиральных центра, они способствуют образованию четырех возможных стереоизомеров: (R, R) , (S,S), (R,S) и (S,R) . Из этих, (R, R) и (S, S) являются примером пары энантиомеров (зеркальные отражения друг друга), которые обычно имеют общие химические свойства и температуры плавления как и любая другая пара энантиомеров. Зеркальные отражения (R,R) и (S,S), однако, не могут быть совмещены с (R,S) и (S,R). Это называется диастереоизомерией, и (S,S) молекула является диастереоизомером (R,S) молекулы, в то время как (R,R) молекула является диастереоизомером (S,R) молекулы. Поскольку соединения формул I, II или III этого изобретения являются основными соединениями, все они способны образовывать широкий спектр различных солей с различными органическими и неорганическими кислотами. Несмотря на то, что такие соли должны быть фармацевтически приемлемыми для введения животным, часто желательно на практике сначала выделить основное соединение из реакционной смеси как фармацевтически неприемлемую соль и затем просто перевести в состояние свободного основания обработкой щелочным реагентом и, после этого, перевести свободное основание в фармацевтически приемлемую аддитивную соль кислоты. Аддитивные соли кислоты основных соединений этого изобретения легко получают обработкой основного соединения в наибольшей степени эквивалентным количеством выбранной минеральной или органической кислоты в водном растворителе или в таком подходящем органическом растворителе, как метанол или этанол. После осторожного выпаривания растворителя легко получают требуемую твердую соль. Кислоты, используемые для получения фармацевтически приемлемых солей присоединения кислоты, упомянутых выше основных соединений этого изобретения, являются теми, что образуют нетоксичные соли присоединения кислоты, например, соли, содержащие фармацевтически приемлемые анионы/ такие соли как гидрохлорид, гидробромид, гидроиодид, нитрат, сульфат или бисульфат, фосфат или кислый фосфат, ацетат, лактат, цитрат или кислый цитрат, тартрат или битартрат, сукцинат, малеат, фумарат, глюконат, сахарат, бензоат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат и памоат (а именно, 1,1'-метилен-бис-(2-гидрокси-З-нафтоат)). Настоящее изобретение также включает соединения, меченные изотопами, идентичные приведенным в формулах I, II или III, за исключением того, что один или более атомов замещены атомом, имеющим значение атомной массы или массовое число, отличное от таковых, обычно обнаруживаемых в природе. Примеры изотопов, которые могут входить в состав соединений настоящего изобретения, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора или хлора, такие как 2Н, 3Н, 13С, г1С, 14С, 15N, 180, 170, 31Р, 32Р, 35S, 18F и 36С1, соответственно. Соединения настоящего изобретения, их пролекарства и фармацевтически приемлемые соли указанных соединений или указанных пролекарств, которые содержат ранее упомянутые изотопы и/или другие изотопы других атомов, находятся в объеме этого изобретения. Определенные соединения, меченные изотопами настоящего изобретения, например, те, в состав которых входят радиоактивные изотопы, такие как 3Н, 18F, 1гС и 14С, применимы в анализах распределения лекарства в ткани и/или в субстрате, и другие, такие как 11С и 18F, применимы для визуализации исследований, а именно, в позитронно-эмиссионной томографии (ПЭТ), ЯМР, и т.д. Дополнительно замещение более тяжелыми изотопами, такими как дейтерий, а именно, 2Н, может обеспечить определенные терапевтические преимущества, из-за большей метаболитической стабильности, например, увеличенный период полувыведения in vivo или сниженная необходимая доза и, поэтому, они могут быть предпочтительными при некоторых обстоятельствах. Соединения формул I, II или III этого изобретения, меченные изотопами, и их пролекарства могут быть, в основном, получены при осуществлении методик, описанных в схемах и/или в примерах ниже, замещением легко доступного изотопномеченного реагента неизотопоно меченным реагентом. Термин "алкил", используемый в данном описании, если иначе не определено, включает насыщенные углеводородные радикалы, имеющие прямые, разветвленные или циклические участки или их комбинации. Примеры "алкильных" групп включают, но не ограничиваются ими, метил, этил, пропил, изопропил, бутил, изо-, сек- и трет-бутил, пентил, гексил, гептил, 3-этилбутил, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, норборнил и подобные. Термин "арил" включает замещенные или незамещенные группы, включающие 5- и 6-членные ароматические группы с одним кольцом, которые могут включать от 0 до четырех гетероатомов, например, бензол, фенил, пиррол, фуран, тиофен, тиазол, изотиазол, имидазол, триазол, тетразол, пиразол, оксазол, изооксазол, пиридин, пиразин, пиридазин, и пиримидин и подобные. Более того, термин "арил" включает полициклические арильные группы, например, трициклическую, бициклическую, например, нафталин, бензоксазол, бензодиоксазол, бензотиазол, бензоимидазол, бензотиофен, метилендиоксифенил, хинолин, изохинолин, нафтридин, индол, бензофуран, пурин, бензофуран, деазапурин или индолизин. Арильные группы могут быть замещены, например, алкильными группами, алкинильными группами, галогенами, гидроксилом, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилатом, алкилкарбонилом, арилкарбонилом, алкоксикарбонилом, аминокарбонилом, алкиламинокарбонилом, диалкиламинокарбонилом, алкилтиокарбонилом, алкоксилом, фосфатом, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилатом, сульфатом, алкилсульфинилом, сульфонато, сульфмоилом, сульфонамидом, нитро, трифторметилом, циано, азидо, гетероциклилом, алкиларилом или ароматическим или гетероароматическим участком. Арильные группы, имеющие гетероатомы в структуре кольца, могут также быть названы "арильные гетероциклы", "гетероциклы", "гетероарилы" или "гетероароматики". Ароматическое кольцо может быть замещено по одному или более положениям такими заместителями, как описано выше, как например, галогеном, гидроксилом, алкилом, алкокси, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилатом, алкилкарбонилом, алкиламинокарбонилом, арилалкиламинокарбонилом, алкениламикарбонилом, алкилкарбонилом, арилкарбонилом, арилалкилкарбонилом, алкенилкарбонилом, алкоксикарбонилом, аминокарбонилом, алкилтиокарбонилом, фосфатом, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрилом, алкилтио, арилтио, тиокарбоксилатом, сульфатами, алкилсульфинилом, сульфонато, сульфмоилом, сульфонамидо, нитро, трифторметилом, циано, азидо, гетероциклилом, алкиларилом или ароматическим или гетероароматическим участком. Арильные группы могут быть также конденсированы или соединены мостиками с алициклическими или гетероциклическими кольцами, которые не являются ароматическими для образования полицикла (например, тетралина). В сущности, гетероароматическая группа представляет собой 2- или 3-тиенил, 2- или 3-фуранил, 2- или 3-пирролил, 2-, 3- или 4-пиридинил, 2-пиразинил, 2-, 4- или 5-пиримидинил, 3-или 4-пиридазинил, или 2-, 3-, 4-, 5-, 6- или 7-индолил. Термин "фенил" включает ароматические кольца из шести атомов углерода. Фенил может быть незамещенным (или замещенным водородом) по одной или более позициям заместителем, таким как, но не ограничиваясь, алкил, галоген, гидроксил, алкокси, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, алкиламинокарбонил, арилалкиламинокарбонил, алкениламинокарбонил, алкилкарбонил, арилкарбонил, арилалкилкарбонил, алкенилкарбонил, алкоксикарбонил, аминокарбонил, алкилтиокарбонил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, циано, азидо, гетероциклил, алкиларил или ароматический или гетероароматический участок. Считается, что термин "арил" включает замещенные и незамещенные фенильные группы. Термин "арилокси" или "-О-арил" включает замещенные и незамещенные арильные группы, ковалентно связанные с атомом кислорода. Примеры арилокси групп включают фенокси и бензокси. Термин "алкокси" включает замещенные и незамещенные алкильные, алкенильные и алкинильные группы, ковалентно связанные с атомом кислорода. Примеры алкокси групп включают метокси, этокси, изопропокси, пропокси, бутокси и пентокси группы. Примеры замещенных алкокси групп включают галогенированные алкокси группы. Алкокси группы могут быть замещены группами, такими как алкенил, алкинил, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, циано, азидо, гетероциклил, алкиларил или ароматический или гетероароматический участки. Примеры галоген-замещенных алкокси групп включают, но не ограничиваются, фторметокси, дифторметокси, трифторметокси, хлорметокси, дихлорметокси, трихлорметокси, и т.д. Термин "гетероарил", используемый в данном описании, если иначе не определено, включает моноциклические ароматические гетероциклы, содержащие от пяти до семи членов в кольце, из которых от 1 до 4 могут быть гетероатомами, независимо выбранными из N, S и О, и бициклические ароматические гетероциклы, содержащие от шести до 10 членов, из которых от 1 до 4 могут быть гетероатомами, независимо выбранными из N, S и О. Термин "гетероцикл", используемый в данном описании, если иначе не определено, включает замещенное или незамещенное 4, 5 или б-членное кольцо, содержащее, по меньшей мере, гетероатом N, О или S, которое включает как ароматическую, так и неароматическую систему колец и включает конденсацию с 5 или 6-ти членным ароматическим, гетероароматическим, неароматическим карбоциклом или неароматическим гетероциклом. Примеры гетероциклов включают, но не ограничиваются, фуран, тетрагидрофуран, тиофен, пиррол, пирролидин, оксазол, тиазол, имидазол, пиразол, изоксазол, изотиазол, триазол, тетразол, пиран, пиридин, пиперидин, морфолин, пиридазин, пиримидин, пиразин, пиперазин и конденсированные бициклические гетероциклы: индолизин, индол, изоиндол, индолин, бензофуран, бензотиофен, индазол, бензимидазол, бензтиазол, хинолин, изохинолин, хиназолин, ацетидин, оксэтан и этилендиоксибензол. Термин "алкенил" включает незамещенные аналоги алифатических групп по длине и возможное замещение алкилов, описанных выше, но содержащих, по меньшей мере, одну двойную связь. Например, термин "алкенил" включает алкенильные группы с прямой цепью (например, этиленил, пропенил, бутенил, пентенил, гексенил, гептенил, октенил, ноненил, деценил и т.д.), алкенильные группы с разветвленной цепью, циклоалкенильные (алициклические) группы (циклопропенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил), циклоалкенильные группы, замещенные алкилом или алкенилом, и алкенильные группы, замещенные циклоалкилом или циклоалкенилом. Термин алкенил дополнительно включает алкенильные группы, которые содержат атомы кислорода, азота, серы или фосфора, замещающие один или более углеродных атомов углеводородного скелета. В определенных аспектах, алкенильная группа с прямой или разветвленной цепью имеет 6 или более атомов углерода в своем скелете (например, С2-С6 для прямой цепи, С3-С6 для разветвленной цепи). Таким образом, циклоалкенильные группы могут иметь 3-8 атомов углерода в своей кольцевой структуре и, более предпочтительно, 5 или б атомов углерода в кольцевой структуре. Термин С2-С6 включает алкенильные группы, содержащие 2-6 атомов углерода. Более того, термин алкенил включает как "незамещенные алкенилы" так и "замещенные алкенилы", из которых последние относятся к алкенильным участкам, имеющим заместители, замещающие водород по одному или более атомам углерода углеводородного скелета. Такие заместители могут включать, например, алкильные группы, алкинильные группы, галогены, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфмоил, сульфонамид, нитро, трифторметил, циано, азидо, гетероциклил, алкиларил или ароматический или гетероароматический участки. Термин "один или более заместителей", используемый в данном описании, касается числа заместителей, которое соответствует одному заместителю до максимального возможного числа заместителей в зависимости от доступных сайтов связывания. Термины "гало" и "галоген", используемые в данном описании, если иначе не определено, включают фтор, хлор, бром и иод. Следует отметить, что структура некоторых соединений этого изобретения включает асимметрические атомы углерода. Следует понимать, что в соответствии с тем, что изомеры, получаемые исходя из такой асимметрии (например, все энантиомеры и диастереомеры), если иначе не определено, входят в объем этого изобретения. Такие изомеры могут быть получены в значительной мере в чистой форме с помощью классических методик разделения и стереохимически контролируемого синтеза. Более того, структуры и другие соединения, и участки, обсуждаемые в этой заявке, также включают все их таутомеры. Термин "лечение", используемый в данном описании, касается регресса заболевания, облегчения, ингибирования прогрессирования или профилактики расстройства или состояния, к которому применяется такой термин или предотвращения развития одного или более симптомов такого состояния или расстройства. Термин "терапия", используемый в данном описании, касается действия лечения, в то время как "лечение" является тем, что определено выше. Термин "терапия" также включает снижение выраженности или облегчение, по меньшей мере, одного симптома, связанного с или обусловленного вылечиваемым расстройством. Например, терапией может быть уменьшение выраженности нескольких симптомов расстройства или полное устранение расстройства. Соединения формул I, II или III и их фармацевтически приемлемые соли, также совместно упоминаются в данном документе как "новые соединения этого изобретения" и "активные соединения этого изобретения". Дополнительные преимущества и черты настоящего изобретения станут очевидными для квалифицированного специалиста в этой области из обзора следующего подробного описания, рассматриваемого в связи с примером и прилагаемой формулой изобретения. Следует отметить, однако, что в то время как данное изобретение рассмотрено с различных точек зрения в различных формах, описанные здесь и далее аспекты являются особенно предпочтительными аспектами изобретения, при этом следует понимать, что настоящее описание носит иллюстративный характер и не стремится ограничить данное изобретение описанными здесь и далее конкретными аспектами. Подробное описание изобретения Соединения формул I, II или III настоящего изобретения могут быть получены как описано в следующих схемах реакций. Если иначе не определено, R1-!?8 в схемах реакций и последующем обсуждении являются такими, как определено выше. Если иначе не определено, в данном документе: TMS = хлортриметилсилан; Red-Al = натрийбис(2-метокси)алюминий; IBX = 1,2-бензиодоксол-З(1Н)-он, 1-гидрокси, 1-оксид; DIAD = диизопропилазодикарбоксилат; ВОС = бутилоксикарбонил; TFA = трифторуксусная кислота; и DPPP = 1,3-бис-дифенилфосфинопропан. Схема А: Общая методика синтеза производных морфолина из бензилглицидола (Общая методика А). 10 11 Общая методика синтеза производных морфолина (Схема А) Получение диола 3 К 1 М раствору гидроксида натрия добавляли соответствующий фенол (1,05 экв) и перемешивали при комнатной температуре в течение 30 мин. Затем одной порцией добавляли (2R,3R)-3-фенилглицидол 2 (1,0 экв) и реакционную смесь нагревали при 70°С в течение 2 ч. Реакционную смесь охлаждали до комнатной температуры и продукт экстрагировали эфиром. Объединенный органический экстракт промывали 1 М раствором гидроксида натрия, насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении и продукт очищали на колонке с силикагелем для получения чистого диола. Получение мезилата 6 К раствору диола 3 в этилацетате, добавляли триэтиламин (избыток). Смесь охлаждали до 0°С, затем по каплям добавляли хлортриметилсилан (1,0 экв) в этилацетате в течение 30 мин. После 1 ч, если ТСХ-анализ показывал, что осталось небольшое количество исходного диола, добавляли дополнительное количество хлортриметилсилана (0,26 мл, 1,83 ммоль) и реакционную смесь перемешивали при 0°С в течение 45 мин. Когда ТСХ-анализ показал, что диол 3 превратился в TMS-производное 4, к реакционной смеси добавляли триэтиламин (1,0 экв) и метансульфонилхлорид (1,1 экв, который добавляли по каплям). Реакционную смесь оставляли до достижения комнатной температуры и перемешивали в течение 12 ч. Когда ТСХ-анализ показал, что TMS-производное 4 превратилось в соединение 5, добавляли 1 М раствор соляной кислоты и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь разбавляли водой и органический слой отделяли и водный слой экстрагировали этилацетатом. Объединенный органический экстракт промывали раствором бикарбоната натрия, насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении с получением мезилата 6 в виде бесцветной жидкости. Получение эпоксида 7 К раствору мезилата 6 в толуоле, добавляли 1 М раствор гидроксида натрия (3 экв основания) и метилтрибутиламмонийхлорид (75% по массе в воде). Реакционную смесь перемешивали при комнатной температуре в течение 4 8 ч и при 50°С в течение 18 ч. Слои разделяли и водный слой экстрагировали толуолом. Объединенный органический экстракт промывали раствором бикарбоната натрия, насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении и продукт очищали на колонке с силикагелем с получением эпоксида 7. Получение аминоспирта 8 К концентрированному раствору гидроксида аммония добавляли равный объем метанола. Раствор эпоксида 7 в метаноле добавляли по каплям более 3 ч. Реакционную смесь перемешивали при комнатной температуре в течение 18 ч. Продукт экстрагировали дихлорметаном. Объединенный органический экстракт промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении. Очистка на колонке с силикагелем давала соединение 8. Получение хлорацетамида 9 К смеси аминоспирта 8 и триэтиламина (1,5 экв) в ТГФ, по каплям добавляли раствор хлорацетилхлорида (1 экв) в ТГФ. После перемешивания в течение 1,5 ч, растворитель и летучие компоненты удаляли при пониженном давлении, остаток растворяли в этилацетате, промывали водой, насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении с получением хлорацетамида 9. Получение морфолина 10 Хлорацетамид 9 растворяли в смеси изопропилового спирта и толуола. Добавляли по каплям раствор трет-бутоксида калия (4 экв) в изопропиловом спирте в атмосфере азота. Реакционную смесь перемешивали при комнатной температуре в течение 4 ч. Значение рН смеси доводили до 6,5 добавлением раствора 2 М НС1 и летучие компоненты удаляли при пониженном давлении. Остаток разделяли между толуолом и водой. Водный слой экстрагировали толуолом. Объединенный органический экстракт промывали раствором бикарбоната натрия, насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении и продукт растирали со смесью этилацетата и гексана с получением морфолина 10, обычно в виде твердого вещества белого цвета. Получение 11 К раствору морфолина 10 в толуоле добавляли по каплям Red-А1 (75% раствор в толуоле) при 0°С. Реакционную смесь перемешивали при температуре образования льда в течение 3 ч. Избыток Red-Al удаляли добавлением по каплям 2 М раствора NaOH. Слои разделяли и водный слой разбавляли водой и экстрагировали толуолом. Объединенный органический экстракт промывали насыщенным солевым раствором и сушили над безводным Na2S04. Растворитель удаляли при пониженном давлении и продукт очищали на колонке с силикагелем (этилацетат: метанол) с получением соединения морфолина 11 обычно в виде бесцветной жидкости. Схема В Палладиевое присоединение бромпроизводного (Общая методика Получение морфолина 13: К раствору арилбромида 12 в бензоле добавляли тетракис(трифенилфосфин)палладий (0) и карбонат калия. Затем добавляли раствор соответствующей борной кислоты в ТГФ. Реакционную смесь нагревали в течение 18 ч с обратным холодильником (80°С) и затем охлаждали до комнатной температуры, разбавляли толуолом и промывали водой и насыщенным солевым раствором. Органическую фазу сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении и остаток очищали на колонке с силикагелем (EtOAc/гексан) с получением соединения морфолина 13. Получение соединения морфолина 11 Восстановление морфолинона до морфолина проводили как это описано в общей методике А. Схема С: Общая методика получения соединения морфолина 7 из спиртов морфолина 1 или 2 (Общая методика С). Синтез соединений морфолина "S" (формула I, II). XMgBr.XU 1. DiAD.PhCCOH 2. КОН очистка хроматографией DUO, толуол Синтез соединений морфолина "R" (формула I, II). Альтернативный общий путь синтеза соединений морфолина (формула I, II, III). 1.М*а,ВД ШиО№олуол Z-OH Н 7 Х"Гетероарил Схема С, продолжение Синтез "2-S, 3-R" соединений морфолина (формула I, II) ИЛИ || Синтез "2-R, 3-S" соединений морфолина (формула I, II). Общая методика синтеза (2-S, 3-S)-, (2-R, 3-R)-соединений морфолина (формула I, II или III) и (2-S, 3-R)-, (2-R, 3-S)-соединений морфолина (формула I, II или III). Окисление N-BOC-морфолинового спирта Соответствующий S или R хиральный морфолиновый спирт (1 или 2) растворяли в подходящем количестве EtOAc (0,2М) в круглодонной колбе с подсоединенным обратным холодильником и магнитной мешалкой, и этот раствор с IBX (2,0 экв) осторожно кипятили с обратным холодильником в течение 3 часов при перемешивании. Реакционную смесь охлаждали до комнатной температуры, разбавляли гексаном (40% по объему) и фильтровали через средний фарфоровый фильтр. Собранное твердое вщество промывали дважды смесью EtOAc и гексана 1:1 и объединенные фильтраты концентрировали до получения бесцветного масла, которое без дополнительной очистки использовали в следующей реакции. Смотри Org Lett, 2002, 3002. Предварительный анализ ЯМР показывает пик СНО и следы ( <3%) иодобензойной кислоты. Альдегид, полученный таким образом, дает хороший результат в реакции последующего алкилирования. Альдегидный продукт 3 является, в некоторой степени, не стабильным и должен быть использован сразу после получения. Алкилирование N-BOC-морфолинового альдегида Неочищенный альдегид (3) полученный на предыдущей стадии растворяли в безводном ТГФ (0,6 М) в сухой колбе в инертной атмосфере и полученный раствор охлаждали до -4 0°С. Добавляли по каплям раствор соответствующего литийалкила или реактива Гриньяра (1,5-3,0 экв.) в ТГФ или диэтилэфире в течение 15 минут с помощью пипетки при тщательном перемешивании реакционной смеси. Когда добавление было завершено, охлаждение убирали и реакционную смесь оставляли для нагревания до температуры окружающей среды. После перемешивания в течение 4 часов при этой температуре, было установлено, что реакция прошла (с помощью ТСХ-анализа и использования EtOAC в гексане в качестве элюента) и реакционную смесь выливали в химический стакан, содержащий насыщенный водный раствор NH4CI и лед. Полученную смесь экстрагировали EtOAc и объединенные органические экстракты промывали насыщенным водным раствором NaCl и концентрировали досуха. Полученное неочищенное масло адсорбировали на силикагель и очищали колоночной хроматографией (кремний, Biotage prepack, EtOAc в гексане) для получения продуктов 4 и 5 в виде бесцветного масла (60-75% общий выход двух стадий исходного N-BOC-морфолинового спирта 1 или 2) . Н ЯМР и МС (масс-спектральный) анализы соответствовали продукту. Инверсия вторичного спирта: Эта методика была применена для инверсии стереохимии нежелательного спирта (например, 4) в желательный спирт (например, 5) во время проведения синтеза (2-S, 3-S)- и (2-R, 3-R)-производных морфолина, таких как 7, 8, или 10. Эту методику также применяли для превращения нежелательного (например, 5) в желательный спирт (например, 4) во время проведения синтеза (2-S, 3-R)- и (2-R, 3-S)-производных морфолина, таких как 12, 12а, 13 или 14. Однако, спирты 4 и 5 могут быть превращены один в другой, создавая, таким образом, путь синтеза, применимый к любым из четырех возможных стереоизомеров. Образование бензоата Исходный спирт (5), трифенилфосин (3,0 экв), и исходный фенол (5,0 экв) растворяли в толуоле (0,4 М) в круглодонной колбе с магнитной мешалкой и мембраной прокладкой, и смесь охлаждали до 0°С и перемешивали в течение 10 минут при этой температуре. DIAD (2,9 экв) добавляли по каплям в течение 10 минут при 0°С. Реакционную смесь подогревали до температуры окружающей среды и перемешивали в течение 24-48 часов. Результат взаимодействия оценивали с помощью ТСХ (4 0% EtOAc в гексане в качестве элюента) и МС. После завершения реакции, растворитель удаляли в вакууме с получением масла, которое растворяли в дихлорметане (0,1 М). Этот раствор переносили в делительную воронку и промывали дважды 1 М водным раствором КОН. Органическую фазу сушили над Na2S04, концентрировали досуха, адсорбировали на силикагеле и подвергали колоночной хроматографии (кремний марки, Biotage prepack, EtOAc в гексане) с получением продукта бензоата, обычно в виде пенообразного полутвердого вещества с 95-99% выходом. Н ЯМР и МС анализы соответствовали продукту. Расщепление бензоата Исходный бензоат растворяли в МеОН (0,1 М) и добавляли NaOH (10 экв, 5% водный раствор). Реакционную смесь подогревали до 60°С и перемешивали при этой температуре в течение 0,5 ч. МеОН удаляли в вакууме и водный слой экстрагировали СН2С12 (4 раза). Объединенные органические слои сушили над Na2S04 и концентрировали с получением масла, которое очищали колоночной хроматографией (кремний, Biotage prepack, EtOAc/гексан) с получением желаемого спирта 5 с выходом, изменяющимся от хорошего до отличного. Н ЯМР и МС анализы соответствовали продукту. Образование эфира с помощью реакции Митсунобу Исходный спирт (5), трифенилфосин (2,0 экв), и исходный фенол (5,0 экв) растворяли в толуоле (0,4 М) в круглодонной колбе с магнитной мешалкой и мембраной прокладкой, и смесь охлаждали до 0°С и перемешивали в течение 10 минут при этой температуре. В некоторых случаях немного фенола или спирта оставалось нерастворенным и небольшое количество (5-10% общего объема растворителя) ТГФ добавляли для повышения растворимости. DIAD (1,9 экв) добавляли по каплям в течение 10 минут при 0°С. Реакционную смесь подогревали до температуры окружающей среды и перемешивали в течение 24-48 часов. Результат взаимодействия оценивали с помощью ТСХ (4 0% EtOAc в гексане в качестве элюента) и МС. После завершения реакции, растворитель удаляли в вакууме с получением масла, которое растворяли в дихлорметане (0,1 М). Этот раствор переносили в делительную воронку и промывали дважды 1 М водным раствором КОН. Органическую фазу сушили над Na2S04, концентрировали досуха, адсорбировали на силикагеле и подвергали колоночной хроматографии (кремний, Biotage prepack, 10 до 25% EtOAc в гексане) с получением продукта б в виде твердого вещества или пены с умеренным выходом. Удаление ВОС-группы Исходное вещество б растворяли в минимальном количестве диоксана в круглодонной колбе с магнитной мешалкой и смесь охлаждали до 0°С. Раствор НС1 (4,0 экв, 4,0 М в диоксане) добавляли по каплям с помощью пипетки и реакционную смесь перемешивали в течение 0,5 ч, при этом смесь нагревалась до комнатной температуры. Перемешивание продолжали, при необходимости, в течение дополнительных 0,5 часов. Когда все исходное вещество было израсходовано (это оценивалось с помощью ТСХ с использованием EtOAc в гексане), реакционную смесь концентрировали досуха в вакууме и помещали в минимальное количество 5% (об./об.) раствора НОАс в МеОН. Этот раствор помещали на ионообменную колонку (Varian SCX) и очищали с использованием МеОН и элюировали 1 М NH3 в МеОН) с получением продукта амина 7 или 8 (в виде свободного амина) в виде бесцветного твердого вещества или масла, которое по данным ЯМР и ВЭЖХ было чистым. Образование соли фумаровой кислоты Свободный амин растворяли в минимальном количестве изопропанола в круглодонной колбе соответствующего размера с магнитной мешалкой. Раствор фумаровой кислоты (0,96 экв, 0,205 М в изопропаноле) добавляли и реакционную смесь тщательно перемешивали в течение 15 минут. Часть растворителя (30-40%) оставляли для испарения в потоке азота для получения твердого вещества или смолистого твердого вещества. Остаток растворителя удаляли в вакууме и добавляли MeCN (0,1 М) . Полученную реакционную смесь тщательно перемешивали в течение нескольких часов, в течение этого периода времени образовывалось твердое вещество белого цвета. Реакционную смесь нагревали до тех пор, пока все твердое вещество не растворилось, и оставляли охлаждаться (медленно) в течение 1 ч до температуры окружающей среды на масляной бане. Реакционную смесь фильтровали через фильтровальную бумагу, и кристаллы продукта собирали и сушили в вакууме. Образование эфира посредством замещения мезилата (методика, альтернативная реакции Митсунобу). Исходный спирт 5 растворяли в СН2С12 (0,4М) и добавляли Et3N (1,3 экв) . Реакционную смесь охлаждали до 0°С и по каплям добавляли метансульфонилхлорид (1,2 экв). Смесь перемешивали при 0°С в течение 2 ч. Реакцию гасили добавлением насыщенного водного раствора NH4C1, разбавляли дополнительным объемом СН2С12 и выливали в делительную воронку. 1,5М водный раствор НС1 использовали для двукратного промывания органического слоя. Органическую фазу сушили над Na2S04, фильтровали и концентрировали в вакууме для получения продукта мезилата, который использовали на следующей стадии без дополнительной очистки. Это вещество растворяли в подходящем растворителе, таком как ацетонитрил или толуол и наряду с соответствующим фенолом (1,3 экв) добавляли К2С03 (3,0 экв). Реакционную смесь нагревали до температуры близкой к температуре кипения растворителя либо в микроволновом реакторе или на масляной бане. После нагревания в течение 12-60 часов, реакционную смесь фильтровали и концентрировали для получения смолистого остатка, который очищали флэш-колоночной хроматографией для получения желаемого эфирного продукта 6 или 9 со средним выходом. Схема D: Альтернативная методика синтеза биарил и пиридил-замещенных производных морфолина (формула III) . Основная методика D. Этерификация с помощью реакции Митсунобу К перемешиваемой при комнатной температуре смеси либо (R) или (S)-2-гидроксиметил-морфолин-4-карбоновой кислоты, трет-бутилового эфира (1) , соответствующего фенола (например, 2-бромфенола, 2-бром-З-пиридинола, или замещенного аналога), и трифенилфосфина, в ДМЭ по каплям добавляли диизопропилазодикарбоксилат. Раствор перемешивали и нагревали при 40°С в течение 24 ч, концентрировали (для удаления большего количества ДМЭ), затем суспендировали в диэтиловом эфире. Образованное твердое вещество отфильтровывали. Фильтрат концентрировали и хроматографировали (MPLC, силикагель, EtOAc в дихлорметане) для получения продукта (2), обычно в виде желтого или бесцветного масла. Образование диарилового эфира К перемешиваемому раствору арилбромида 2 и соответствующего фенола в ДМЭ добавляли третбутоксид и комплекс трифлатбензола меди (I) . Смесь перемешивали и нагревали при 100°С в течение 24 часов. Реакционную смесь затем концентрировали (для удаления большего количества ДМЭ), и суспендировали в диэтиловом эфире и воде. Эту смесь фильтровали через целит и целит промывали дополнительным количеством диэтилового эфира. Слои разделяли и органический слой промывали 2 Н раствором NaOH (2 х) , насыщенным КН2Р04, и насыщенными солевыми растворами. Органический экстракт сушили с помощью Na2S04, фильтровали, концентрировали и хроматографировали (MPLC, силикагель, EtOAc в гексане) для получения продукта (3), обычно в виде жидкого масла. Образование соли фумарата Раствор ВОС-защищенного производного морфолина 3 в СН2С12 обрабатывали 2 мл трифторуксусной кислоты. Раствор перемешивали при комнатной температуре в атмосфере N2 в течение 3 ч, концентрировали, затем фракционировали между СН2С12 и 10% водным раствором NH4OH. Слои разделяли и органический экстракт сушили (Na2S04) , фильтровали и концентрировали. Образец превращали в соль фумаровой кислоты в 2-пропаноле, из которого ее кристаллизовали для получения продукта 4 в виде соли фумарата (твердое вещество белого цветв). Дополнительное дебензилирование и альтернативная этерификация для образования дифенилового эфира без пиридинового кольца: (W=C) Дополнительная реакция дебензилирования: К раствору (S)-2-(2-бензилокси-феноксиметил)морфолин-4 -карбоновой кислоты, трет-бутилового эфира (полученного как указано выше, общая методика D) в этаноле добавляли 10% Pd/C. Образец при комнатной температуре гидрогенизировали при давлении газа из баллона в течение 2 ч, фильтровали и концентрировали. Образец растворяли в EtOAc, промывали насыщенным раствором КН2Р04 и насыщенными солевыми растворами, сушили (MgS04) , фильтровали и концентрировали для получения трет-бутилового эфира (S)-2-(2-гидрокси-феноксиметил)-морфолин-4-карбоновой кислоты, в виде масла светложелтого цвета. Альтернативное образование дифенилового эфира: была осуществлена методика David Evans, et al., Tetrahedron Letters 1998, 39, 2937-2940. Смесь, состоящую из 2, арилборной кислоты, ацетата меди (II), пиридина, и активированные порошковые Вое молекулярные сита 4А в СН2С12 перемешивали при комнатной температуре в атмосфере окружающей среды в течение 5 дней. Образец разбавляли EtOAc, перемешивали при комнатной температуре в течение 2 ч, затем фильтровали через целит. Фильтрат промывали 1 Н раствором NaOH (2 х) , насыщенным КН2Р04 и насыщенными солевыми растворами, сушили (MgS04) , фильтровали и концентрировали. Неочищенный образец хроматографировали (MPLC, силикагель, EtOAc в гексане) для получения продукта дифенилового эфира 3. Бифенильная версия общей методики D К смеси арилбромида 2, в дегазированном этаноле, добавляли тетракис(трифенилфосфин)палладий(0), карбонат калия и соответствующую борную кислоту. Реакционную смесь нагревали с обратным холодильником в течение 18 ч, охлаждали до коматной температуры, содержимое фильтровали и фильтрат концентрировали. Остаток растворяли в этилацетате (100 мл), промывали водой и насыщенным солевым раствором. Растворитель удаляли при пониженном давлении и продукт очищали на колонке с силикагелем с применением этилацетата в гексане для получения соединений 5, с которых защита была снята обычным способом. Общая методика Е: Схема Е. Общая методика синтеза хиральных производных морфолина. t-B иОН/толуол, 100-120 С, 12 ч 6 7 " Окисление N-BOC-морфолинового спирта Соответствующий S-хиральный морфолиновый спирт 1 (15 г) растворяли в подходящем количестве дихлорметана и, TEMPO (160 мг) , КВг (650 мг) , и ТВАС1 (1 г) растворяли в смеси DCM (950 мл) и 40 мл 1 М NaHC03. Реакционную смесь охлаждали до 0°С и по каплям добавляли раствор NaOCl (13%, 300 мл), 300 мл насыщенного NaCl, и 180 мл NaHC03 в течение 45 минут. После перемешивания полученной смеси в течение дополнительных 1,5 часов, ее промывали СН2С12 (4x500 мл) . Водный слой осторожно подкисляли до рН 2 с помощью 1 М НС1 и экстрагировали СН2С12. Объединенные органические экстракты сушили и концентрировали для получения твердого вещества белого цвета. Полученная таким образом кислота дает хороший результат в последующей реакции присоединения. Получение амида Вайнреба: Кислоту 15, (32 г) растворяли в 400 мл дихлорметана наряду с амингидрохлоридом (15,1 г), триэтиламином (35 г), и этот раствор охлаждали до 0-5°С. К этой реакционной смеси добавляли циклический ангидрид фосфорной кислоты (97 г) в течение 90 минут при 0-5°С. Реакционную смесь перемешивали в течение 1,5 часов и реакцию гасили 250 мл 20% раствора К2С03 при <15°С. Органическую фазу разделяли и промывали 2Х 400 мл 10% К2С03 для получения, после удаления растворителя, 35,7 г желаемого амида 16 в виде бесцветного масла (94%) . Получение кетона: Получение трет-бутилового эфира 2-(пиридин-2-карбонил)-морфолин-4-карбоновой кислоты в качестве характерного примера. 2-пиридилиодид (5,5 г) растворяли в ТГФ и охлаждали до -20°С. EtMgBr (3,3 г) по каплям добавляли в течение 10 минут в качестве раствора в ТГФ и перемешивание продолжали в течение 30 минут при -20°С. Раствор становился темножелтого цвета. Амид 16 (4 г) добавляли к этому раствору в качестве раствора в ТГФ (8 мл) и реакционную смесь выдерживали при -30°С и перемешивали в течение 30 минут. В реакционную смесь, пока она оставалась холодной, выливали воду (100 мл) и гасили NH4C1 (водн.) (50 мл) . Экстракция в EtOAc (3x7 5 мл) и концентрирование давало твердое вещество, которое очищали на 4 0 г колонке Biotage prepack (15% EtOAc в гексане) для получения желаемого продукта в виде воскообразного твердого вещества слегка желтого цвета. Восстановление: Получение трет-бутилового эфира 2-(гидрокси-пиридин-2-ил-метил)-морфолин-4-карбоновой кислоты в качестве характерного примера. В камере с перчатками в запаянной пробирке наряду с 0,001 г Ru(S) кат (0,02 моль% экв) растворяли в ТГФ и изопропаноле реактивы (1,15 г кетона, 0,1 г K2C03) (Strem cat #44-0211 lot # В7081103). Смесь перемешивали при давлении 50 фунтов/кв. дюйм Н2 при комнатной температуре в течение ночи. Реакционную смесь вынимали из камеры с перчатками, фильтровали (твердый К2С03) через микрофильтр, содержащий 3 г кремния, и концентрировали досуха при пониженном давлении для получения масла желтого цвета, которое было чистым по оценке ЯМР. После отстаивания, масло затвердевало в рыхлое твердое вещество, которое использовали на следующих стадиях без дополнительной очистки. ЯМР анализ может быть использован для оценки соотношения диастереомеров, присутствующих в неочищенной восстановленной смеси. Образование и замещение мезилата или реакция Митсунобу: Трет-бутиловый эфир 2- [ (2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин-4-карбоновой кислоты получали в соответствии с протоколами, изложенными для общей методики С. Удаление Вое-группы и образование соли: 2-[(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолинфумарат получали в соответствии с протоколами, изложенными для общей методики С. Получение соли янтарной кислоты: Свободный морфолин 7 растворяли в минимальном количестве Et20. Периодически добавляли небольшое количество изопропанола для полного растворения морфолина. Медленно по каплям при перемешивании добавляли 0,25 М раствор янтарной кислоты в изопропаноле (1,0 экв кислоты). После нескольких минут в реакционной смеси начинали осаждаться кристаллы твердого вещества. После отстаивания в течение 2 часов, осадок отфильтровывали и сушили для получения продукта присоединения янтарной кислоты и производного морфолина в соотношении 1:1. Схема F (Общая методика F) {2Чморфолин-2-и1> ч1)^ил-мвто1(Си)-фвнил]-мвтанол трет-бутиловый эфир 2-[(2-гидроксиметил- фенокси)-фенил-метил]-морфолин-4 карбоновой кислоты трет-бутиловый эфир 4-[(2-этокси-фенокси)-фенил-2-[(2-метоксиметил-фенокси)-фенил-метил]- метил]-пиперидин морфолин-4-карбоновой кислоты Общая методика F: Получение этилового эфира 2-[ (5-оксо-морфолин-2-ил)-фенил-метокси]-бензойной кислоты. 6- [ (2-бром-фенокси)-фенил-метил]-морфолин-3-он (0,82 г) переводили в этанол (40 мл). Добавляли ацетат палладия (0,051 г), DPPP (0,112 г) и TEA (0,63 мл), и реакционную смесь помещали в атмосферу СО и нагревали при 100"С. Вторую порцию катализатора добавляли на 60-м часу, и опять добавляли на 74-м часу. После 88 ч, смесь охлаждали, фильтровали и концентрировали для получения масла тёмнокрасного цвета. Масло переводили в DCM, концентрировали на кремнеземе и очищали хроматографией на кремнеземе (гексан/EtOAc 95:5 до 40:60). Фракции, содержащие желаемый продукт, объединяли и концентрировали для получения 0,66 г этилового эфира 2-[(5-оксо-морфолин-2-ил)-фенил-метокси]-бензойной кислоты в виде масла оранжевого цвета (выход 83%, М+1=356,1). Получение [2-(морфолин-2-ил-фенил-метокси)-фенил]-метанола Этиловый эфир 2-[(5-оксо-морфолин-2-ил)-фенил-метокси]-бензойной кислоты (0,66 г) переводили в 10 мл толуола, и охлаждали до 0°С для добавления Red-Al (2,8 мл, 5 экв). Смесь оставляли для нагревания до комнатной температуры. После 12 ч, добавляли 2 мл 2Н NaOH и смесь перемешивали при комнатной температуре в течение 30 мин, экстрагировали толуолом (2x5 мл). Органические экстракты объединяли, сушили над MgS04, фильтровали и концентрировали. Остаточное масло переводили в DCM, наносили на кремнезем, и очищали MPLC в DCM/MeOH+0, 1NH40H. Фракции, содержащие желаемый продукт, объединяли и концентрировали. 0,287 г [2-(морфолин-2-ил-фенил-метокси)-фенил]-метанола в виде масла бледножелтого цвета (выход 51%, М+1=300,1). Получение трет-бутилового эфира 2-[(2-гидроксиметил-фенокси)-фенил-метил]-морфолин-4-карбоновой кислоты [2-(морфолин-2-ил-фенил-метокси)-фенил]-метанол (0,287 г) переводили в ТГФ, и после ди-т-бутилдикарбоната (0,23 г, 1,1 экв.) добавляли NaOH (1,2 мл, 1М, 1,1 экв.). Данную смесь перемешивали при комнатной температуре в течение 12 ч. ТГФ выпаривали на роторном испарителе, и оставшееся масло разделяли между водой и эфиром. Слои разделяли и водный слой экстрагировали эфиром (2x15 мл) . Органические экстракты объединяли и сушили над MgS04, фильтровали и концентрировали для получения 0,44 г трет-бутилового эфира 2-[(2-гидроксиметил-фенокси)-фенил-метил]-морфолин-4-карбоновой кислоты (выход неочищенного продукта 114%). Получение трет-бутилового эфира 2-[(2-метоксиметил-фенокси)-фенил-метил]-морфолин-4-карбоновой кислоты Трет-бутиловый эфир 2-[(2-гидроксиметил-фенокси)-фенил-метил] -морфолин-4 -карбоновой кислоты (0,44 г) переводили в ТГФ (10 мл) и помещали на баню комнатной температуры для добавления NaH (0,05 г). Данную смесь перемешивали в течение 10 мин, и затем добавляли Mel (0,17 г) и перемешивали при комнатной температуре в течение 3 ч. Данную смесь снова обрабатывали NaH и Mel и перемешивали при комнатной температуре в течение 4 8 ч. Исходное вещество все еще присутствовало, поэтому данную смесь обрабатывали NaH. Mel пропускали через патрон оксида алюминия и затем добавляли. После 3 ч, реакцию осторожно гасили добавлением воды. Данную смесь экстрагировали эфиром (3x30 мл), и органические экстракты объединяли, промывали насыщенным солевым раствором (1x20 мл), сушили над MgS04, фильтровали и концентрировали. Бесцветное масло переводили в DCM и наносили на кремнезем, затем очищали MPLC (гексан:EtOAc 95:5 до 40:60). Фракции, содержащие желаемый продукт, объединяли и концентрировали для получения 0,317 г препарата трет-бутилового эфира 2-[(2-метоксиметил-фенокси)-фенил-метил]-морфолин-4- карбоновой кислоты (выход 70%). Получение 4-[(2-этокси-фенокси)-фенил-метил]-пиперидина Трет-бутиловый эфир 2-[ (2-метоксиметил-фенокси)-фенил-метил] -морфолин-4-карбоновой кислоты (0,761 г) брали в 1М НС1 в диоксане (7,4 мл), перемешивали при комнатной температуре в течение 12 ч. Диоксан удаляли, оставшееся клейкое твердое вещество переводили в DCM, промывали 1М NaOH, сушили над MgS04, фильтровали и концентрировали на кремнеземе. Данный материал очищали с помощью MPLC (DCM/MeOH+l%NH4OH 95:5 до 75:25). Собранный продукт не был чистым, поэтому его очищали препаративной ВЭЖХ для получения 0,077 г 4-[(2-этокси-фенокси)-фенил-метил]-пиперидина (выход 21%, М+1=312,2). Соединения формул I, II, или III и их фармацевтически приемлемых солей могут быть введены млекопитающим либо перорально, парентерально (например, подкожно, внутривенно, внутримышечно, надчревно и инфузионно) , ректально, буккально или интраназально. В общем, эти соединения наиболее предпочтительно вводить в дозах, варьирующих от, примерно, 0,1 мг до, примерно, 1000 мг в день, в единой или разделенных дозах (а именно, от 1 до 4 доз в день), хотя, несомненно, будут существовать различные варианты в зависимости от вида, веса и состояния пациента, подвергаемого лечению и индивидуального ответа пациента на указанный препарат, так же как и от типа выбранной технологии получения лекарственного средства и временного периода и интервала, в течение которого осуществляют такое введение. Однако, наиболее желательно применять уровень дозировки в интервале от, примерно, 25 мг до, примерно, 100 мг в день. В некоторых случаях, уровни дозировки ниже нижнего предела вышеуказанного интервала могут быть более чем достаточны, при этом в других случаях еще большие дозы могут быть применены, не вызывая каких-либо вредных побочных эффектов, при условии, что такие большие дозы сначала разделяют на несколько малых доз для введения в течение дня. Соединения настоящего изобретения могут быть введены самостоятельно или в комбинации с фармацевтически приемлемыми носителями или разбавителями, с помощью ранее обозначенных способов, и такое введение может быть осуществлено в одной или нескольких дозах. Более конкректно, новые терапевтические агенты этого изобретения могут быть введены в виде широкого спектра различных лекарственных форм, а именно, они могут быть объединены с различными фармацевтически приемлемыми инертными носителями в виде таблеток, капсул, пастилок, подушечек, карамели, суппозиториев, желе, гелей, паст, мазей, водных суспензий, инъекционных растворов, эликсиров, сиропов и подобных. Такие носители включают твердые разбавители или наполнители, стерильную водную среду и различные нетоксичные органические растворители, и т.д. Более того, пероральные фармацевтические композиции могут быть подходящим образом подслащены и/или ароматизированы. В общем, отношение масс новых соединений этого изобретения к массе фармацевтически приемлемого носителя будет варьировать от, примерно, 1:6 до, примерно, 2:1, и, предпочтительно, от, примерно, 1:4 до, примерно, 1:1. Для перорального введения могут применяться таблетки, содержащие такие различные эксципиенты, как микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, фосфат дикальция и глицин наряду с такими различными дезинтегрантами, как крахмал (и предпочтительно кукурузный, картофельный или маниока крахмал), альгиновая кислота и определенный комплекс силикатов, совместно с такими гранулированными связующими веществами, как поливинилпирролидон, сахароза, желатин и камедь. Дополнительно очень часто применяются для таблетирования такие смазывающие агенты, как стеарат магния, лаурилсульфат натрия и тальк. Твердые композиции похожего типа могут также применяться в качестве наполнителей в желатиновых капсулах; в связи с этим, предпочтительные материалы также включают лактозу или молочный сахар, так же как и высокомолекулярные полиэтиленгликоли. Когда для перорального введения предпочтительны суспензии и/или эликсиры, активный ингредиент может быть комбинирован с различными подсластителями или ароматизаторами, пигментами или красителями, и, если это предпочтительно, так же эмульгирующими и/или суспендирующими агентами, совместно с таким разбавителями, как вода, этанол, пропиленгликоль, глицерин и различными подобными их комбинациями. Для парентерального введения могут применяться растворы соединения настоящего изобретения либо в кунжутном или в арахисовом масле или в водном пропиленгликоле. Водные растворы должны быть подходящим образом забуферены (предпочтительное значение рН более 8) если необходимо, и жидкий разбавитель изначально доведен до изотоничности. Эти водные растворы подходят для внутривенных инъекций. Масляные растворы подходят для внутрисуставных и подкожных инъекций. Получение всех этих растворов в стерильных условиях легко осуществимо с помощью стандартных фармацевтических методик, хорошо известных квалифицированному специалисту в этой области. Это изобретение касается способов лечения расстройств центральной нервной системы или состояния, такого как СДВГ, тревожность, депрессия, шизофрения и других расстройств, упоминаемых в описании способов настоящего изобретения, где новое соединение этого изобретения и один или более другие активные агенты, упоминаемые выше (например, антагонист, NKi рецептора, анксиолитический антипсихотический агент, трициклический антидепрессант, антагонист рецептора БИТдВ или ингибитор обратного захвата серотонина), вводят совместно в виде части этой же фармацевтической композиции, так же как и способов введения таких активных агентов раздельно в качестве части подходящего режима дозирования, созданного для получения полезных эффектов комбинированной терапии. Подходящий режим дозирования, количество каждой дозы вводимого активного агента и определенные интервалы межу дозами каждого активного агента зависят от субъекта, подвергаемого лечению, конкретного вводимого активного агента и природы и выраженности конкретного расстройства, подвергаемого лечению, или состояния. В общем, новые соединения этого изобретения при использовании в виде отдельного активного агента или в комбинации с другим активным агентом вводят взрослому человеку в количестве от, примерно, 3 мг до, примерно, 300 мг в день, в единой или разделенной дозах, предпочтительно от, примерно, 25 до, примерно, 100 мг в день. Такие соединения могут быть введены в режиме до б раз в день, предпочтительно от 1 до 4 раз в день, особенно, 2 раза в день и наиболее особенно, раз в день. Вариации, тем не менее, могут существовать в зависимости от вида животного, подвергаемого лечению, и его индивидуального ответа на указанный препарат, так же как и от типа выбранной технологии получения лекарственного средства и временного периода и интервала, в течение которого осуществляют такое введение. В некоторых случаях, уровни дозировки ниже нижнего предела вышеуказанного интервала могут быть более чем достаточны, при этом в других случаях еще большие дозы могут быть применены, не вызывая каких-либо вредных побочных эффектов, при условии, что такие большие дозы сначала разделяют на несколько малых доз для введения в течение дня. Предполагаемая суточная доза атипичного антипсихотика, предпочтительно, пипразидона, в способах комбинирования и композициях этого изобретения, для перорального, парентарального или буккального введения среднему взрослому человеку для лечения состояний, упоминаемых выше, составляет от, примерно, 0,1 мг до, примерно, 2000 мг, предпочтительно от, примерно, 1 мг до, примерно, 200 мг атипичного антипсихотика на единицу дозы, которая может быть введена, например, от 1 до 4 раз в день. Предполагаемая суточная доза антагониста 5HTiB рецептора в способах комбинирования и композициях этого изобретения, для перорального, парентарального, ректального или буккального введения среднему взрослому человеку для лечения состояний, упоминаемых выше, составляет от, примерно, 0,1 мг до, примерно, 2000 мг, предпочтительно от, примерно, 0,1 мг до, примерно, 200 мг антагониста 5HTjB рецептора на единицу дозы, которая может быть введена, например, от 1 до 4 раз в день. Для интраназального введения или введения с помощью ингаляции, новые соединения данного изобретения удобно доставляются в форме раствора или суспензии из баллончика с пульверизатором, который сжимается или нажимается пациентом или в виде подачи аэрозольной струи из контейнера под давлением или небулайзера с применением подходящего пропеллента, например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа. В случае аэрозоля под давлением, единица дозирования может быть определена с помощью распределителя для доставки дозированного количества. Контейнер под давлением или небулайзер может содержать раствор или суспензию активного соединения. Капсулы и картриджи (сделанные, например, из желатина) для применения в ингаляторе или распылителе могут содержать порошковую смесь соединения данного изобретения и подходящую порошковую основу, такую как лактоза или крахмал. Лекарственные формы активных соединений этого изобретения для лечения состояний у среднего взрослого человека, указанных выше, предпочтительно создаются таким образом, что каждая отмеренная доза или "вдох" аэрозоля содержит от 20 мкг до 1000 мг активного соединения. Общая суточная доза с применением аэрозоля будет находиться в пределах от 100 мкг до 10 мг. Введение может быть осуществлено несколько раз в день, например, 2, 3, 4 или 8 раз с введением, например, 1, 2 или 3 доз каждый раз. Способность соединений этого изобретения связываться с hNET рецептором к серотонину SERT может быть определена с использованием обычного радиологического анализа и анализа связывания с рецептором. Рецепторы могут различным образом экспрессироваться в клеточных линиях и экспериментах, проводимых в препаратах мембран клеточных линий с использованием методик, указанных ниже. Концентрации IC50 могут быть определены с помощью нелинейной регрессии концентрационно-зависимого восстановления в конкретном связывании. Для перевода IC50 концентраций в Ki концентрации может быть использовано уравнение Cheng-Prussoff. Связывание с рецептором hNET: Массы НЕК-293 клеток, трансфицированных переносчиком человеческого норэпинефрина, поставлялись группой Pfizer Ann Arbor Protein Expression and Production. Осадки ресуспендировали в объеме от 400 до 700 мл буфера для анализа Krebs-HEPES (25 мМ HEPES, 122 мМ NaCl, 3 мМ KCI, 1,2 мМ MgS04, 1,3 мМ СаС12, и 11 мМ глюкоза, рН 7,4) с помощью гомогенизатора Polytron с установленным временем от 7 до 30 сек. Аликвоты мембран (5 мг/мл белка) до использования хранили в жидком азоте. Анализ связывания проводили в полипропиленовых планшетах с глубокими лунками (Beckman) с общим объемом 250 мкл, содержащих: лекарство (10"5 М до 10"12 М) , клеточные мембраны, и 50 пМ [125I]-RTI-55 (Perkin Elmer, NEX-272; специфическая активность 2200 Ки/ммоль). Реакционную смесь инкубировали при осторожном взбалтывании в течение 90 мин при комнатной температуре и завершали фильтрацией через плоские фильтры Whatman GF/C с использованием 96-луночного Brandel коллектора. В каждую лунку добавляли сцинтилляционную жидкость (100 мкл I), и связывание [125I] -RTI-55 определяли с использованием счетчика Wallac Trilux Beta Plate. Тестируемые соединения оценивались в двойном экземпляре, и специфическое связывание определялось как разница между связыванием в присутствии и отсутствии 10 мкл М дезипрамина. Приложения Excel и GraphPad Prism использовались для обсчета данных и анализа. Значения IC50 переводили в значения Ki с использованием уравнения Cheng-Prusoff. Связывание с рецептором hSERT: Массы НЕК-2 93 клеток, трансфицированных переносчиком человеческого серотонина, поставлялись группой Pfizer Ann Arbor Protein Expression and Production. Осадки ресуспендировали в объеме от 4 00 до 700 мл буфера для анализа Krebs-HEPES (25 мМ HEPES, 122 мМ NaCl, 3 мМ КС1, 1,2 мМ MgS04, 1,3 мМ СаС12, и 11 мМ глюкоза, рН 7,4) с помощью гомогенизатора Polytron с установленным временем от 7 до 30 сек. Аликвоты мембран (5 мг/мл белка) до использования хранили в жидком азоте. Анализ связывания проводили в полипропиленовых планшетах с глубокими лунками (Beckman) с общим объемом 250 мкл, содержащих: лекарство (10"5 М до 10"12 М) , клеточные мембраны, и 50 пМ [1251] -RTI-55 (Perkin Elmer, NEX-272; специфическая активность 2200 Ки/ммоль). Реакционную смесь инкубировали при осторожном взбалтывании в течение 90 мин при комнатной температуре и завершали фильтрацией через плоские фильтры Whatman GF/C с использованием 96-луночного Brandel коллектора. В каждую лунку добавляли сцинтилляционную жидкость (100 мкл I), и связывание [125I] -RTI-55 определяли с использованием счетчика Wallac Trilux Beta Plate. Тестируемые соединения оценивались в двойном экземпляре, и специфическое связывание определялось как разница между связыванием в присутствии и отсутствии 10 мкл М циталопрама. Приложения Excel и GraphPad Prism использовались для обсчета данных и анализа. Значения IC50 переводили в значения Ki с использованием уравнения Cheng-Prusoff. Активности hNET и hSERT соединений настоящего изобретения представлены ниже в таблице 1. Таблица 1 Пример hNET (Ki) SERT (Ki) 9,9 3942 6,3 564 1581 1,6 708 1176 3227 6610 4,2 4713 967 689 10000 1,8 452 6,7 6,4 4097 10000 3772 4505 133 1015 593 10000 6,8 2500 22 (2S,3R) 4816 6671 22 (2S,3S) 10000 2629 210 7722 124 10000 359 2437 7903 412 8414 1409 154 10000 10000 348 10000 2410 141 184 605 3,7 471 163 517 4099 3,7 475 317 828 4941 172 5,3 1359 6,5 5632 8,4 8,9 729 5,2 6260 10000 1617 1351 5,9 259 1306 10000 2244 2463 7,4 965 206 6603 2538 119 10000 1195 176 660 1894 818 595 10000 10000 849 349 3163 10000 7974 10000 9646 7,5 3669 9,6 4320 2609 3,9 3116 7,3 4865 869 8085 2893 953 633 10000 4110 10000 211 5045 2289 1452 5603 811 3410 4447 471 1140 880 1271 100 152 10000 101 912 102 5740 103 6073 104 2386 9786 105 1500 5587 106 10000 107 3675 108 676 109 364 110 8, 57 356 111 105 237 112 105 113 114 116 1333 118 1137 10000 119 120 10000 121 470 10000 122 123 935 4116 124 346 125 10000 126 10000 127 6280 128 3325 129 4473 130 457 7057 131 388 132 6117 133 1457 9059 134 10000 135 4483 136 102 6135 137 1813 138 1609 3822 139 1189 1139 140 763 141 2745 142 4538 143 896 3319 144 304 7221 145 4138 146 3704 147 2568 2533 148 10000 149 2311 150 2025 151 3290 152 1938 153 6319 154 2524 155 768 156 801 157 2573 158 10000 159 7368 160 6503 161 3877 162 263 163 446 164 3067 165 351 166 1349 167 2554 168 791 169 2982 170 4934 171 1039 172 9341 173 10000 174 7517 175 7640 176 3417 177 1961 178 179 2553 180 8234 181 225 4904 182 7084 183 5344 184 460 185 201 186 1255 187 224 188 2212 189 147 5218 190 4338 191 5832 192 1880 193 707 194 2560 195 7057 196 10000 197 811 198 199 2942 200 9546 10000 201 171 10000 202 722 ПРИМЕРЫ Пример 1 (S)-2-[(S)-фенил-(2-трифторметокси-фенокси)-метил]-морфолин синтезировали из бензилглицидола и 2-трифторметоксифенола в соответствии с общей методикой А (Схема А) и выделяли в виде смолистого масла. 1Н ЯМР (CDC13) 5 7,22 (м, 5Н), 7,07 (д, 1Н), 6,91 (дт, 1Н) , 6,72 (м, 2Н) , 5,04 (д, 1Н) , 3,82 (м, 2Н) , 3,51 (м, 1Н), 2,65 (м, 2Н) , 2,53 (м, 1Н) , 2,46 (т, 1Н), 1,61 (с, 1Н). МС (ЭИ) : подсчитано: [Ci8Hi803F3N] 353, обнаружено: [М+Н] : 354. Элементный анализ: подсчитано: С 61,19%, Н 5,10%, N 3,97%, обнаружено: С 60,33%, Н 5,04%, N 3,82%. Пример 2 Хиральный (S)-2- [ (S)-(2-этилсульфанил-фенокси)-фенил-метил]-морфолин синтезировали из 2-этилсульфанилфенола в соответствии с общей методикой А (Схема А) и выделяли в виде смолистого масла. МС (APCI) : 330 [М+Н] +. Пример 3 -jHj Хиральный (S)-2-[(S)-(2-изобутил-фенокси)-фенил-метил]-морфолин синтезировали из 2-изобутилфенола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI) : 326 [М+Н] +. Пример 4 Хиральный (S)-2-[(S)-(2-бром-фенокси)-фенил-метил]-морфолин синтезировали из 2-бромфенола в соответствии с общей методикой А со следующей модификацией последней реакции восстановления. Схема: Получение соединения морфолина 2: К раствору бромморфолина (1,0 г, 2,7 6 ммоль) в 20 мл ТГФ добавляли 10 мл 1,0 М боргидрида в ТГФ и реакционную смесь перемешивали при комнатной температуре в течение 18 ч. Затем реакционную смесь гасили добавлением 3 мл 3,0 М раствора соляной кислоты и нагревали при 80 °С в течение 10 минут. Реакционную смесь охлаждали до комнатной температуры и подщелачивали добавлением 2,0 М раствором гидроксида натрия. Продукт экстрагировали этилацетатом (2x30 мл). Объединенные органические экстракты промывали насыщенным солевым раствором и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении, и продукт очищали на колонке с силикагелем (EtOAc:МеОН=9:1) с получением 2-[ (2-бром-фенокси)-фенил-метил]-морфолина (2) в виде вязкого масла (0,650 г, 67,6%). гН ЯМР (CDC13) 5: 7,50 (д, 1Н), 7,40-7,20 (м, 5Н), 7,06 (м, 1Н), 6,76 (м, 2Н), 5,20 (д, 1Н), 3,94 (м, 1Н) , 3,70 (м, 1Н) , 2,90-2,50 (м, 4Н) . МС (ЭС) m/z 347,96 [Ci7H18BrN02+H]+. Анализ: подсчитано для Ci7Hi8BrN02: С, 58,63; Н, 5,21; N, 4,02, обнаружено: С, 58,20; Н, 5,12; N, 4,37. (S)-2- [ (S)-фенил-(2-винил-фенокси)-метил]-морфолин синтезировали из 6-[(2-бром-фенокси)-фенил-метил]-морфолин-3-она в соответствии с общей методикой А и общей методикой В, как это продемонстрировано ниже. Пример 5 Синтез соединения 2: К смеси 1, (1,0 г, 2,76 ммоль) в дегазированном этаноле (25 мл), добавляли тетракис(трифенилфосфин)палладий (0) (0,319 г, 0,276 ммоль), карбонат калия (1,14 г, 8,28 г ммоль), дибутиловый эфир винилборной кислоты (1,22 мл, 5,52 ммоль). Реакционную смесь нагревали с обратным холодильником в течение 18 ч, охлаждали до комнатной температуры, содержимое фильтровали и фильтрат концентрировали. Остаток растворяли в этилацетате (100 мл), промывали водой и насыщенным солевым раствором. Растворитель удаляли при пониженном давлении и продукт очищали на колонке с силикагелем с использованием 70% этилацетата в гексане с получением соединения 2 в виде бесцветного масла (0,351 г, 47%). ХН ЯМР (CDC13) 5: 7,46 (дд, 1Н) , 7, 40-7,28 (м, 5Н), 7,16 (дд, 1Н) , 7,03 (м, 1Н) , 6,89 (т, 1Н), 6,67 (д, 1Н), 6,45 (ушир.с, 1Н), 5,78 (дд, 1Н), 5,31 (дд, 1Н) , 5,25 (д, 1Н) , 4,30 (АВкв., 2Н) , 4,18 (м, 1Н) , 3,34 (т, 1Н), 3,05 (тд, 1Н) ; МС (ЭС) 310,2 [Ci9H19N03+H]+. Получение соединения 3 (2-[фенил-(2-винил-фенокси)-метил]-морфолина К раствору морфолина 2 (0,255 г, 0,825 ммоль) в толуоле (10 мл), по каплям добавляли Red-Al (65% раствор в толуоле (0,8 мл, 2,55 ммоль), при 0°С в течение 20 мин. Реакционную смесь перемешивали при 0-5°С в течение 2,5 ч. Избыток Red-Al удаляли добавлением по каплям 2 М раствора NaOH (2,7 мл). Слои разделяли, и водный слой разбавляли водой (20 мл) и экстрагировали толуолом (2x15 мл) . Объединенный органический экстракт промывали насыщенным солевым раствором и сушили над безводным Na2S04. Растворитель удаляли при пониженном давлении и продукт очищали на колонке с силикагелем с использованием 10% метилового спирта в этилацетате с получением морфолинового соединения 3 (2-[фенил-(2-винил-фенокси)-метил]-морфолина) в виде вязкого бесцветного масла (0,154 г, 63%). 1Н ЯМР (CDC13) 5: 7,46-7,18 (м, 7Н), 7,01 (м, 1Н) , 6,84 (т, 1Н) , 6,68 (д, 1Н) , 5,78 (дд, 1Н), 5,29 (дд, 1Н), 5,12 (д, 1Н), 3,98-3,86 (м, 2Н), 3,64 (дт,1Н), 2, 86-2,72 (м, 2Н) , 2, 66-2, 54 (м, 2Н) ; МС (ЭС) 296,1 [C19H2iN02+H]+. ВЭЖХ чистота (94,3%) Анализ: подсчитано Ci9H2iN02.0, 5Н20: С, 74,91, Н, 7,23; N, 4,60. Обнаружено: С, 75,41, Н, 7,09; N, 4,95. синтезировали из 2-хлорфенола в соответствии с общей методикой А и выделяли в виде бесцветной жидкости (Выход 0,325 мг, 51%). ХН ЯМР (CDC13) 5: 7,40-7,35 (м, 6Н), 7,00 (м, 1Н), 6,80 (м, 2Н), 5,20 (д, 1Н), 3,90 (м, 2Н), 3,65 (м, 1Н) , 2, 90-2, 80 (м, 2Н) , 2,70-2,60 (м, 2Н), 1,65 (с, 1Н). МС(ЭС) m/z 304,06 [Ci7Hi8ClN02+H]+. Анализ: подсчитано для С, 67,21; Н, 5,91; N, 4,61. Обнаружено: С, 66,51; Н, 6,19; N, 5, 51. Пример 6 (S)-2- [ (S)-(2-хлор-фенокси)-фенил-метил]-морфолин Пример 7 (S)-2-[(S)-(2-метоксиметил-фенокси)-фенил-метил]-морфолин синтезировали из 2-бромфенола через образование б-[(2-бромфенокси) -фенил-метил]-морфолин-3-она в соответствии с общими методиками А и F и выделяли в виде смолистого масла. МС (APCI): 314 [М+Н]+. Пример 8 (S)-2-[(S)-фенил-(2-трифторметил-фенокси)-метил]-морфолин синтезировали из 2-трифторметилфенола в соответствии с общей методикой А и выделяли в виде бесцветной жидкости (Выход 0,36 мг, 65%). ХН ЯМР (CDC13) 5: 7,55 (м, 1Н) , 7, 40-7,25 (м, 6Н) , 6,90 (м, 1Н) , 6,78 (д, 1Н) , 5,25 (д, 1Н) , 3,90 (м, 2Н) , 3,62 (м, 1Н), 2,80-2,73 (м, ЗН), 2,55-2,50 (м, 1Н), 1,60 (ушир. с, 1Н) . МС(ЭС) m/z 338,07 [C17H18CINO2+H]+. Анализ: подсчитано для Ci8H18F3N02: С, 64,09; Н, 5,38; N, 4,54. Обнаружено: С, 63,52; Н, 5,44; N, 4,66. Пример 9 (S)-2- [ (S)-(2-бензил-фенокси)-фенил-метил]-морфолин синтезировали из 2-бензилфенола в соответствии с общей методикой А и выделяли в виде густого масла. 1Н ЯМР (4 00 МГц, CDCI3) 6: 7,16 (м, 11Н), 7,00 (м, 1Н) , 6,80 (м, 1Н) , 6,64 (м, 1Н), 5,10 (д, 1Н), 4,10 (м, 2Н), 3,92 (д, 1Н) , 3,78 (м, 1Н) , 3,62 (м, 1Н) , 2,78 (м, 2Н) , 2,44 (м, 2Н) , 1,76 (ушир. с, 1Н) . ЭС m/z 360,18 [C24H25NO2+H4 . Пример 10 Хиральный (S)-2- [ (S)-фенил-(2-пиридин-4-ил-фенокси)-метил]-морфолин синтезировали из б-[(2-бром-фенокси)-фенил-метил]-морфолин-3-она и 4-пиридинборной кислоты в соответствии с общими методиками А и В и выделяли в виде густой вязкой смолы. 1Н ЯМР (CDC13) 5: 8,65 (д, 2Н), 7,60 (д, 2Н) , 7,32-7,18 (м, 7Н) , 6,96 (м, 1Н), 6,90 (д, 1Н), 5,10 (д, 1Н), 3,93 (д, 1Н) , 3,80 (м, 1Н) , 3,60 (м, 1Н) , 2,75 (м, 2Н) , 2,48 (м, 2Н) , 1,80 (ушир. с, 1Н) . МС (ЕС) m/z 347,08 [СггИгг^Ог+Н]+. Анализ: подсчитано для C22H22N2O2:0,5Н20: С, 74,34; Н, 6,52; N, 7,88. Обнаружено: С, 74,15; Н, 6,84; N, 7,37. (S)-2-[(S)-(2-циклопропил-фенокси)-фенил-метил]-морфолин синтезировали из 6-[(2-бром-фенокси)-фенил-метил]-морфолин-3-она и циклопропилборной кислоты в соответствии с общими методиками А и В и выделяли в виде густого бесцветного масла. 1Н ЯМР (CDCI3) : 5 7,40-7,24 (м, 5Н), 6,91 (м, 1Н), 6,80 (м, 2Н), 6,66 (д, 1Н), 5,15 (д, 1Н), 3,94 (м, 2Н), 3,65 (дт, 1Н), 2,852,59 (м, 4Н) , 2,32 (м, 1Н) , 0, 99-0, 89 (м, 2Н) , 0,74-0, 59 (м, 2Н) ; МС(ЭС) 310,1 [C20H23NO2+H]+; ВЭЖХ чистота (98,6%); Анализ: подсчитано для C2oH23N02: С 77,64, Н 7,49, N 4,53. Обнаружено: С 76,61, Н 7,58, N 4,37. Пример 11 Хиральный Пример 12 Хиральный (S)-2-[(S)-(нафталин-1-илокси)-фенил-метил]-морфолин синтезировали из нафтола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI): 320 [М+Н]+. Пример 13 Хиральный (S)-2- [ (S)-фенил-(2-пиридин-З-ил-фенокси)-метил]-морфолин синтезировали из б-[(2-бром-фенокси)-фенил-метил]-морфолин-3-она и 4-пиридинборной кислоты в соответствии с общими методиками А и В и выделяли в виде смолистого масла. MS (APCI): 347 [М+Н] +. Пример 14 (S)-2-[(S)-(2-фенокси-фенокси)-фенил-метил]-морфолин синтезировали из 2-феноксифенола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI): 362 [М+Н]+. Пример 15 Qof> Этиловый эфир (2S,3S)-2-(морфолин-2-ил-фенил-метокси)-бензойной кислоты синтезировали из 6-[(2-бром-фенокси)-фенил метил]-морфолин-3-она в соответствии с общими методиками А и F и выделяли в виде смолистого масла. МС (APCI): 342 [М+Н]+. Пример 16 (S)-2-[((S)-4'-хлор-бифенил-2-илокси)-фенил-метил]-морфолин синтезировали из 2-бромфенола в соответствии с общими методиками А и В и выделяли в виде смолистого масла. МС (APCI): 381 [М+Н]+. Пример 17 сн. (S)-2-(2-этокси-феноксиметил)-морфолин синтезировали из третбутилового эфира (S)-2-гидроксиметилморфолин-4-карбоновой кислоты и 2-этоксифенола в соответствии со следующей методикой: Стадия 1. К перемешиваемой при комнатной температуре смеси третбутилового эфира (S)-2-гидроксиметилморфолин-4-карбоновой кислоты, 2-этоксифенола и трифенилфосфина в ДМЭ по каплям добавляли азодикарбоксилат. Раствор перемешивали при комнатной температуре в течение 24 ч, концентрировали (для удаления большей части ДМЭ), затем суспендировали в гексане. Образовавшееся твердое вещество отфильтровывали. Фильтрат концентрировали, повторно растворяли в диэтиловом эфире, затем промывали 1 Н NaOH (2 х) , насыщенным КН2Р04 и насыщенным солевым раствором. Органический экстракт сушили (MgS04) , фильтровали, концентрировали и хроматографировали (MPLC, силикагель, 20% EtOAc в гексане) для получения третбутилового эфира (S)-2-(2-этокси-феноксиметил)морфолин-4-карбоновой кислоты в виде бесцветного масла. Стадия 2. (S)-2-(2-этокси-феноксиметил)морфолинфумарат. Раствор третбутилового эфира (S)-2-(2-этокси- феноксиметил) морфолин-4 -карбоновой кислоты в СН2С12 обрабатывали трифторуксусной кислотой. Раствор перемешивали при комнатной температуре в атмосфере N2 в течение 2 ч, концентрировали и разделяли между СНС13 и 10% водным раствором NH4OH. Органический экстракт промывали насыщенным солевым раствором, сушили (MgS04) , фильтровали и концентрировали. Образец переводили в соль фумаровой кислоты в 2-пропаноле и осаждали из ацетонитрила для получения (S)-2-(2-этокси-феноксиметил)морфолинфумарата в виде твердого вещества белого цвета, т.пл. 12б-127°С. Анализ: подсчитано для Ci3H19N03 х С4Н404 (353,375): С, 57,78; Н, 6,56; N, 3,96. Обнаружено: С, 57,61; Н, 6,50; N, 3,93. (R)-2-[(S)-(2-фтор-фенокси)-фенил-метил]-морфолин синтезировали из 2-фторфенола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI): 288 [М+Н]+. Пример 19 (S)-2-[(R)-(2-хлор-4-фтор-фенокси)-пиридин-3-ил-метил]-морфолин синтезировали из морфолин-2-ил-пиридин-З-ил-метанола в соответствии с общей методикой С и выделяли в виде смолистой пены. МС (APCI): 324[М+Н]+. Пример 18 Пример 20 (S)-2-[(R)-(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин синтезировали из 2-бромпиридина и 2-этоксифенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 315 [М+Н]+. Пример 21 (S)-2-[(S)-(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин синтезировали из 2-бромпиридина и 2-этоксифенола в соответствии с общей методикой Е и выделяли в виде сукцината. МС (APCI): 315 [М+Н] +. Пример 22 (2S,3R)2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил) и (2S,3S)2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил независимо синтезировали из 2-бромпиридина и 2-цианофенола в соответствии с общей методикой С и выделяли в виде смолистых масел, которые, как это было показано с помощью Н ЯМР, представляют собой смесь диастереомеров. Разделение этих изомеров приводило к получению смолистой пены. МС (APCI): 296 [М+Н] +. Пример 23 (S)-2-[(S)-(2-фторфенокси)-пиридин-3-ил-метил]-морфолин синтезировали посредством морфолин-2-ил-пиридин-З-ил-метанола из 3-бромпиридина и 2-фторфенола в соответствии с общей методикой С и выделяли в виде смолистого масла (смесь диастереомеров). МС (APCI): 289 [М+Н]+. Пример 24 (2S,3R)-2-(морфолин-2-ил-пиридин-З-ил-метокси)-бензонитрил синтезировали посредством морфолин-2-ил-пиридин-З-ил-метанола из 3-бромпиридина и 2-цианофенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI) : 296 [М+Н] +. Пример 25 HJC'"vO (2R,3R)-2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин и (2S,3R)-2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин независимо синтезировали посредством морфолин-2-ил-пиридин-3-ил-метанола из 3-бромпиридина и 2-этоксифенола в соответствйи с общей методикой С и выделяли в виде масел. МС (APCI) : 315 [М+Н] +. Пример 26 (R)-2-[(S)-пиридин-3-ил-(2-трифторметокси-фенокси)-метил]-морфолин синтезировали посредством морфолин-2-ил-пиридин-3-ил-метанола из 3-бромпиридина и 2-трифторметоксифенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 355 [М+Н]+. (R)-2-[(S)-(2-,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин синтезировали посредством морфолин-2-ил-пиридин-З-ил-метанола из 2-бромпиридина и 2,4-дифторфенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 307 [М+Н]+. (R)-2-[(R)-(2-,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин синтезировали посредством морфолин-2-ил-пиридин-3-ил-метанола из 2-бромпиридина и 2,4-дифторфенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 3 07 [М+Н]+. Пример 27 Пример 28 Пример 29 Хиральный (S)-2-[((S)-1-окси-пиридин-2-илокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде бледножелтого густого масла (0, 095 г, 35%). ^"Н ЯМР (CDC13) 5: 7,55 (дд, 1Н) , 7,45-7,31 (м, 6Н) , 6,54 (дд, 1Н) , 6,07 (дт, 1Н) , 5,48 (д, 1Н), 4,08 (м, 1Н) , 3,90 (дт, 1Н) , 3,62 (м, 1Н) , 2,76 (м, 2Н), 2,56 (дд, 1Н) , 2,41 (дд, 1Н) ; МС(ЭС) 287,0 (Ci6H18N203+H)+; ВЭЖХ чистота (98%); CHN анализ: подсчитано для C16Hi8N203: С 66,65, Н 6,99, N 9,72, обнаружено: С 66,67, Н 6,70, N 9,32. (S)-2-[(S)-(2'-хлор-бифенил-2-илокси)-фенил-метил]-морфолин синтезировали из 2-бромфенола с применением 2-хлорборной кислоты в общих методиках А и В и выделяли в виде густой вязкой смолы. ХН ЯМР (CDC13) 5: 7,48 (м, 1Н), 7,40-7,10 (м, ЮН), 6,96 (м, 1Н) , 6,80 (д, 1Н) , 5,04 (д, 1Н) , 3,84 (м, 1Н), 3,64 (м, 1Н), 3,50 (м, 1Н), 2,68 (м, 2Н) , 2,42 (м, 1Н) , 2,30 (м, 1Н) . МС(ЭС) m/z 380,03 [C23H22C1N02+H]+. Анализ: подсчитано C23H22C1N02: С, 72,72, Н, 5,84; N, 3,69. Обнаружено: С, 72,41, Н, 5,90; N, 3,80. Пример 3 0 Пример 31 (2R, 3R) и (R)-2-[(S)-(2-фтор-б-метокси-фенокси)-пиридин-3-ил-метил]-морфолин независимо синтезировали посредством морфолин-2-ил-пиридин-3-ил-метанола из 3-бромпиридина и 2-фтор-6-метоксифенола в соответствии с общей методикой В с модификацией С и выделяли в виде смолистого масла. МС (APCI): 319 [М+Н] + . Пример 32 (S)-2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин синтезировали посредством общий методики D и выделяли в виде смолистого масла. МС (APCI): 305 [М+Н]+. Пример 33 Хиральный (S)-2-{(S)-[2-(4-фтор-фенил)-пиридин-3-илокси]-метил}-морфолин синтезировали в соответствии со следующей схемой и методикой (которая является вариантом общих методик А и В): Схема G: Синтез соединений пиридилморфолина. Red-Al PhCHs Получение соединения 3 Раствор 2-бромпиридинола 1 (7,6 г, 44 ммоль) в 1 Н водном растворе гидроксида натрия (44 мл, 44 ммоль) перемешивали при комнатной температуре в течение 30 минут. Фенилглицидол 2 (5,0 г, 33 ммоль) добавляли в одну порцию и реакционную смесь нагревали при 75°С в течение 5 ч. Реакционную смесь оставляли до достижения ею комнатной температуры и экстрагировали этилацетатом. Объединенные органические экстракты сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Продукт реакции очищали на силикагеле (элюент 1:1 гексан/этилацетат) с получением диола 3 (7,5 г, 69%) в виде желтого масла. гЯ ЯМР (400 МГц, CDC13) 5: 7,90 (м, 1Н), 7,36 (м, 5Н) , 7,00 (м, 1Н) , 6,92 (м, 1Н) , 5,32 (д, 1Н) , 4,00 (м, 2Н), 3,84 (м, 1Н), 2,94 (м, 1Н), 2,60 (м, 1Н). Получение соединения 4 К раствору диола 3 (5,0 г, 15,4 ммоль) в этилацетате (120 мл) при 0°С в атмосфере азота добавляли триэтиламин (3,2 мл, 23,0 ммоль). Хлортриметилсилан (2,5 мл, 19,7 ммоль) добавляли посредством пипетки и реакционную смесь оставляли до нагрева до комнатной температуры в течение 1 часа. ТСХ анализ показал отсутствие диола. Добавляли дополнительное количество триэтиламина (3,2 мл, 23,0 ммоль), затем метансульфонилхлорид (1,6 мл, 20,7 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч, обрабатывали 1 Н НС1, и перемешивали при комнатной температуре в течение 2 часов. Водную фазу отделяли и экстрагировали этилацетатом. Объединенные органические экстракты сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении для получения 3,5 г мезилата 4 (56%), который использовали без очистки. ХН ЯМР (400 МГц, CDC13) 5: 7,96 (м, 1Н) , 7,40 (м, 5Н) , 7,04 (м, 1Н) , 6,94 (м, 1Н), 5,58 (д, 1Н) , 5,00 (м, 1Н) , 4,24 (м, 1Н), 4,04 (м,1Н), 2,76 (с, ЗН). Получение соединения 5 К раствору соединения 4 (5,5 г, 13,7 ммоль) в толуоле (25 мл) добавляли 1Н гидроксид натрия (41 мл, 41 ммоль), затем трибутилметиламмоний хлорид (75 масс.% в воде, 0,5 мл). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов, затем нагревали при 75°С в течение 4 часов. ТСХ анализ показал отсутствие мезилата. Реакционную смесь доводили до комнатной температуры и слои разделяли. Водную фазу экстрагировали толуолом, и объединенные органические экстракты промывали насыщенным солевым раствором и сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Хроматография продукта на колонке с силикагелем (в качестве элюента 7:3 гексан/этилацетат) давала 4,0 г эпоксида 5 (96%) . гИ ЯМР (400 МГц, CDCI3) 5 7, 96 (м, 1Н) , 7,40 (м, 5Н) , 7,06 (м, 2Н), 4,92 (д, 1Н) , 3,50 (м, 1Н) , 2,88 (м, 1Н) , 2,82 (м, 1Н) . Получение соединения 6 К раствору концентрированного аммиака (60 мл) в метаноле (60 мл) добавляли раствор соединения 5 (4,0 г, 13,1 ммоль) в метаноле (50 мл) в течение 1 ч. Реакционную смесь перемешивали при комнатной температуре в течение 24 ч. ТСХ анализ показал отсутствие исходного вещества. Реакционную смесь концентрировали при пониженном давлении и остаток разделяли между водой и этилацетатом. Водную фазу отделяли и дополнительно экстрагировали этилацетатом. Объединенные органические экстракты сушили над сульфатом натрия, фильтровали, и растворитель удаляли при пониженном давлении с получением 4,0 г (95%) аминоспирта 6 в виде масла желтого цвета, который использовали без очистки. ХН ЯМР (400 МГц, CDC13) 5 7, 92 (м, 1Н) , 7,36 (м, 5Н) , 6,96 (м, 2Н) , 5,16 (д, 1Н) , 4,00 (м, 1Н), 2,72 (м, 2Н), 2,20 (ушир. с, ЗН). Получение соединения 7 К перемешиваемому раствору соединения 6 (4,0 г, 12,4 ммоль) в тетрагидрофуране (80 мл) в атмосфере азота, добавляли триэтиламин (2,3 мл, 16,5 ммоль). Реакционную смесь охлаждали до 0°С. Добавляли по каплям хлорацетилхлорид (1,2 мл, 15,1 ммоль) и реакционную смесь нагревали до комнатной температуры в течение 2 ч. ТСХ анализ показал отсутствие исходного вещества. Реакционную смесь концентрировали при пониженном давлении и остаток разделяли между насыщенным водным раствором бикарбоната натрия и этилацетатом. Органическую фазу отделяли, промывали водой, сушили над сульфатом натрия и фильтровали. Удаление растворителя при пониженном давлении давало хлорацетамид 7 (4,4 г, 8 9%) в виде твердого вещества грязно-белого цвета, которое использовали без очистки. ХН ЯМР (400 МГц, CDC13) 5 7, 96 (м, 1Н) , 7,40 (м, 5Н) , 7,24 (м, 1Н), 6,90 (м, 1Н) , 5,04 (д, 1Н), 4,20 (м, 1Н) , 4,04 (с, 2Н), 3,44 (м, 2Н). Получение соединения 8 К перемешиваемому раствору соединения 7 (4,4 г, 11,0 ммоль) в смеси изопропиловый спирт/толуол (90 мл/30 мл) в атмосфере азота добавляли раствор третбутоксида калия (3,9 г, 33,0 ммоль) в изопропиловом спирте (50 мл). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов, на этой стадии ТСХ анализ показал, что реакция завершена. Значение рН реакционной смеси доводили до, примерно, 6,5 добавлением 2Н соляной кислоты. Реакционную смесь концентрировали при пониженном давлении и остаток разделяли между этилацетатом и водой. Водную фазу отделяли, подщелачивали добавлением 2Н NaOH, экстрагировали этилацетатом и объединенные органические экстракты сушили над сульфатом натрия, фильтровали, и растворитель удаляли при пониженном давлении. Продукт очищали на колонке с силикагелем (3:1 этилацетат/гексан) для получения морфолинона 8 (2,4 г, 60%) в виде твердого вещества бледножелтого цвета. ХН ЯМР (400 МГц, CDC13) 5 7, 95 (м, 1Н) , 7,37 (м, 5Н) , 7,03 (м, 1Н) , 6,97 (м, 1Н) , 6,00 (ушир. с, 1Н) , 5,30 (д, 1Н) , 4,32 (м, 2Н), 4,26 (м, 1Н), 3,37 (м, 1Н), 3,13 (м, 1Н). Получение соединения 9 К раствору соединения 8 (0,526 г, 1,45 ммоль) в тетрагидрофуране (10 мл) добавляли водный раствор карбоната натрия (2М, 7 мл, 14 ммоль), 4-фторфенилборной кислоты (0,683 г, 4,88 ммоль), и тетракис(трифенилфосфин)палладий (0) (0,093 г, 0,080 ммоль). Темную реакционную смесь нагревали при 75-80°С в течение 3 ч. Проверка с помощью ЯМР показала отсутствие исходного вещества. Реакционную смесь доводили до комнатной температуры, концентрировали при пониженном давлении и остаток разделяли между водой и этилацетатом. Водную фазу отделяли и дополнительно экстрагировали этилацетатом, объединенные органические экстракты сушили над сульфатом натрия, фильтровали, и растворитель удаляли при пониженном давлении. Начальная хроматография продукта реакции давала 0,4 г желаемого продукта в виде пенистого твердого вещества желтого цвета. Продукт дополнительно хроматографировали на силикагеле (элюент 1:1 дихлорметан/ацетонитрил) для получения 0,37 г соединения 9. гН ЯМР (400 МГц, CDCI3) 5 8,26 (м, 1Н) , 7,96 (м, 2Н) , 7,32 (м, 5Н), 7,12 (м, ЗН) , 7,04 (м, 1Н) , 5,96 (ушир. с, 1Н) , 5,20 (д, 1Н), 4,28 (м, 2Н), 4,12 (м, 1Н), 3,28 (м, 1Н), 2,86 (м, 1Н) 19F ЯМР (376 МГц, CDC13) 5 -113, 770 (с, 1F) Получение соединения 10 Раствор соединения 9 (0,95 г, 2,90 ммоль) в безводном толуоле (25 мл) помещали в атмосферу азота и охлаждали до 0°С. По каплям добавляли коммерческий раствор Red-Al в толуоле (65 масс.%, 3,0 мл, 10,0 ммоль) с помощью пипетки. Реакционную смесь нагревали до комнатной температуры в течение 1,5 ч, на этом этапе ТСХ анализ показал присутствие исходного вещества. Добавляли дополнительное количество Red-Al (0,3 мл, 1,0 ммоль) и реакционную смесь перемешивали в течение дополнительных 1,5 ч до момента завершения реакции, оцениваемого с помощью ТСХ. Реакционную смесь опять охлаждали до 0°С и реакцию гасили капельным добавлением 2Н гидроксида натрия. Данную смесь разбавляли водой, и водную фазу отделяли и экстрагировали толуолом. Объединенные органические экстракты промывали насыщенным солевым раствором и сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении для получения 0,21 г мутного масла. Это масло подвергали колоночной хроматографии (силикагель, элюент 4:1 этилацетат/метанол) для получения 2-{[2-(4-фтор-фенил)-пиридин-3-илокси]-фенил-метил}-морфолина (10) (0,16 г, 66%) в виде густого масла. 1Н ЯМР (400 МГц, CDCI3) 5 8,24 (м, 1Н), 8,06 (м, 2Н) , 7,28 (м, 5Н) , 7,14 (м, ЗН), 7,02 (м, 1Н), 5,10 (д, 1Н) , 3,96 (м, 1Н) , 3,86 (м, 1Н), 3,64 (м, 1Н), 2,80 (м, 2Н), 2,50 (м, 2Н) . 19F ЯМР (376 МГц, CDCI3) 5 -114, 394 (м, IF) ; (МС) m/z 364,97 [C22H2iFN202+H+] ; CHN -C22H2iFN202. Подсчитано: С 72,51%, Н 5,81%, N 7,69%. Обнаружено: С 72,39%, Н 6,07%, N 8,04%. Пример 34 (R)-2-[(S)-(2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин синтезировали из 3-фторфенилбромида магния и 2-фторфенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 306 [М+Н]+. Пример 35 (R)-2-[(S)-(2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин синтезировали из 4-фторфенилбромида магния и 2-этоксифенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 332 [М+Н]+. Пример 36 Хиральный (S)-2- [ (S)-(2,6-дифтор-фенокси)-фенил-метил]-морфолин синтезировали из 2,6-дифторфенола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI): 306 [М+Н]+. Пример 37 (S)-2-[(S)-2-циклогексил-1-(2-этокси-фенокси)-этил]-морфолин и (2S,3R)-2-[2-циклогексил-1-(2-этокси-фенокси)-этил]-морфолин синтезировали из метиленциклогексилбромида магния в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 334 [М+Н]+. Пример 38 сн, (S)-2-[(S)-1-(2-этокси-фенокси)-3-метил-бутил]-морфолин синтезировали из изобутилбромида магния в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 294 [М+Н]+. (S)-2- [ (S)-(2-аллил-фенокси)-фенил-метил]-морфолин синтезировали из 2-аллилфенола в соответствии с общими методиками А и В и выделяли в виде вязкого бесцветного масла (0,415 г, 79%). ХН ЯМР (CDCI3) : 5 7,38-7,24 (м, 5Н) , 7,10 (дд, 1Н), 6,98 (дт, 1Н), 6,81 (дт, 1Н), 6,65 (д, 1Н), 6,04 (м, 1Н) , 5,18-5,04 (м, ЗН) , 3, 98-3, 86 (м, 2Н) , 3,65 (дт, 1Н) , 3,50 (м, 2Н), 2,86-2,74 (м, 2Н), 2,70-2,54 (м, 2Н), МС(ЭС) 310,0 [C20H23NO2+H]+; ВЭЖХ чистота (98,2%); Анализ: подсчитано для C20H23NO2: С 77,64, Н 7,49, N 4,53. Обнаружено: С 76,94, Н 7,48, N 5,43. (S)-2-[(S)-фенил-(пиридин-3-илокси)-метил]-морфолин синтезировали из соответствующего амида (6-[фенил-(пиридин-3-илокси)-метил]-морфолин-3-она) (смотри Схему G, соединение 8) с использованием следующей методики: А раствор соединения 1 (0,30 г, 0,85 ммоль) в безводном толуоле (3,0 мл) помещали в Пример 39 Пример 40 Хиральный атмосферу азота, охлаждали до 0°С и по каплям добавляли коммерческий раствор Red-Al (65 масс.% в толуоле, 1,0 мл, 3,3 ммоль) с помощью пипетки. Реакционную смесь нагревали до комнатной температуры в течение 4 ч. ТСХ анализ показал отсутствие исходного вещества. Реакционную смесь снова охлаждали до 0°С и гасили капельным добавлением 2Н гидроксида натрия. Реакционную смесь разбавляли толуолом, водную фазу отделяли и дополнительно экстрагировали толуолом. Объединенные органические экстракты сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении для получения 0,30 г светлокоричневого масла. Две хроматографии продукта реакции на силикагеле (элюент - 3:1 этилацетат/метанол второй) давали 0,080 г (35%) желаемого продукта. ХН ЯМР (400 МГц, CDC13) 6 8, 32 (м, 1Н), 8,12 (м, 1Н), 7,24 (м, 5Н), 7,10 (м, 2Н) , 5,10 (д, 1Н) , 3,96 (м, 2Н), 3,68 (м, 1Н), 2,84 (м, 2Н) , 2,66 (м, 2Н), 1,84 (ушир. с, 1Н) . (МС) m/z 271,05 tC16Hi8N202+H+] ; CHN -Ci6Hi8N202. Подсчитано: С 71,09%, Н 6,71% N 10,36%. Обнаружено: С 70,49%, Н 6,70%, N 9,83%. Пример 41 Хиральный (S)-2-[(S)-(2-бром-пиридин-З-илокси)-фенил-метил]-морфолин синтезировали из соответствующего амида (6-[фенил-(пиридин-3-илокси)-метил]-морфолин-3-она) с использованием следующей методики: К раствору соединения 1 (0,4 г, 1,1 ммоль) в безводном тетрагидрофуране (10 мл) в атмосфере азота добавляли коммерческий раствор комплекса бор-тетрагидрофуран (1,0 М в тетрагидрофуране, 3,4 мл, 3,4 ммоль) с помощью пипетки. Реакционную смесь перемешивали при комнатной температуре в течение 20 ч. ТСХ анализ показал, что реакция не прошла. Добавляли дополнительное количество комплекса бор-тетрагидрофуран (3,0 мл, 3,0 ммоль) и реакционную смесь нагревали с обратным холодильником в течение 2,5 ч. ТСХ анализ показал отсутствие исходного вещества. Реакционную смесь доводили до комнатной температуры, обрабатывали 1Н НС1, перемешивали в течение 30 минут, подщелачивали добавлением 2Н гидроксида натрия и экстрагировали этилацетатом. Объединенные органические экстракты сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Две хроматографии продукта реакции на силикагеле (элюент - 3:1 этилацетат/метанол для первой хроматографии, 10:1 дихорметан/метанол для второй) давали 0,063 г (16%) желаемого продукта. ХН ЯМР (400 МГц, CDC13) 6 7,90 (м, 1Н), 7,36 (м, 5Н), 7,00 (м, 2Н), 5,16 (д, 1Н) , 3,96 (м, 2Н) , 3,68 (м, 1Н) , 2,82 (м, 2Н) , 2,64 (м, 2Н) , 1,80 (ушир. с, 1Н) . (МС) m/z 350,92 [C16Hi7BrN202+H+] ВЭЖХ - 91,49% CHN - C22H21FN2O2. Подсчитано: С 55,03%, Н 4,91%, N 8,02%. Обнаружено: С 55,01%, Н 4,97%, N 8,60%. Пример 42 (S)-2-[(S)-фенил-(2-п-толил-пиридин-3-илокси)-метил]-морфолин синтезировали из соответствующего амида ((6-[фенил- (пиридин-3-илокси)-метил]-морфолин-3-она) с использованием общей методики В (применяя 4-метилфенилборную кислоту на стадии присоединения) и получали 0,20 г светлокоричневого масла. Две хроматографии продукта реакции на силикагеле (элюент - 3:1 этилацетат/метанол) давали 0,080 г (35%) желаемого продукта. ХН ЯМР (400 МГц, CDCI3) 5 8,24 (м, 1Н) , 7,96 (д, 2Н) , 7,27 (м, 7Н), 7,07 (м, 1Н) , 6,98 (м, 1Н) , 5,13 (д, 1Н) , 3,96 (м, 1Н) , 3,87 (м, 1Н) , 3,64 (м, 1Н) , 2,80 (м, 2Н) , 2,53 (м, 2Н) , 2,44 (с, ЗН) . (МС) m/z 361,07 [С2зН24^02+Н+] . 100 Пример 43 (S)-2-[(S)-2-хлор-фенокси)-фенил-метил]-морфолин синтезировали из 2-хлорфенола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI): 3 05 [М+Н]+. Пример 44 (S)-2-[(S)-(2-изопропил-фенокси)-фенил-метил]-морфолин синтезировали из 2-изопропилфенола в соответствии с общей методикой А и выделяли в виде смолистого масла. 1Н ЯМР (CDC13) 5: 7,40-7,30 (м, 5Н), 7,19 (д, 1Н), 6,90 (м, 1Н), 6,82 (м, 1Н), 6,70 (д, 1Н), 5,13 (д, 1Н), 3,90 (м, 2Н) , 3,70 (м, 1Н) , 3,50 (м, 1Н) , 2,80 (м, 2Н), 2,75 (м, 1Н), 2,60 (м, 1Н), 1,70 (ушир. с, 1Н), 1,32 (д, ЗН), 1,30 (д, ЗН). МС (ЕС) m/z 312,06 [C20H25NO2+H]+. Анализ: подсчитано для C20H25NO2: С, 77,14; Н, 8,09; N, 4,50. Обнаружено: С, 75,62; Н, 8,47; N, 5,09. (R)-2-[(S)-(бензофуран-6-илокси)-фенил-метил]-морфолин синтезировали из третбутилового эфира 2-(гидрокси-фенил-метил)-морфолин-4-карбоновой кислоты и 6-гидроксибензофурана в соответствии с общей методикой С, применяя последовательность альтернативной этерификации (с помощью мезилата) , и выделяли в Хиральный Пример 45 виде масла. МС (APCI): 310 [М+Н]+. 101 Пример 46 Хиральный (S)-2-[(S)-2-изопропокси-фенокси)-фенил-метил]-морфолин синтезировали из 2-изопропоксифенола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI) : 328 [М+Н] +. Пример 47 (R)-2- [ (S)-(2-бром-фенокси)-(4-фтор-фенил)-метил]-морфолин синтезировали из 4-фторфенолбромида магния и бромфенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 367 [М+Н]+. Пример 48 (S)-2-[(S)-(бензофуран-5-илокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой С, применяя последовательность альтернативной этерификации (с помощью мезилата), и выделяли в виде масла. МС (APCI): 310 [М+Н]+. Пример 49 Хиральный (S)-2-[(S)-фенил-о-толилокси-метил)-морфолин синтезировали из 2-метилфенола в соответствии с общей методикой А и выделяли 102 в виде смолистого масла. МС (APCI): 284 [М+Н]+. Пример 50 Хиральный (2S,3S)-2-(морфолин-2-ил-фенил-метокси)-фенол синтезировали из 2-бензилоксифенола в соответствии с общей методикой А со следующей модификацией: Схема: Экспериментально: Стадия 1: Получение соединения 2 Смесь 1 (0,61 г, 1, 568 ммоль) и 10% Pd-C (0,22 г) в метаноле: тетрагидрофуран (50 мл: 20 мл) встряхивали в атмосфере азота (40 фунтов/кв. дюйм) в течение 18 часов. Смесь фильтровали через колонку с целитом и концентрировали при пониженном давлении для получения фенола 2 в виде густой вязкой смолы (Выход: 0,224 г, 47,8%). гН ЯМР (CDC13) 5 7,58 (ушир. с, 1Н), 7,41-7,35 (м, 5Н), 7,08 (ушир. с, 1Н), 6,90 (м, 2Н), 6,59 (м, 1Н), 6,50 (м, 1Н), 4,65 (д, 1Н), 4,45 (д, 1Н) , 4,30 (д, 1Н) , 4,18 (м, 1Н) , 3,20 (м, 1Н) , 2,75 (д, 1Н) . МС (ЕС) m/z 300, 09 tCi7Ha7N04+H]+. Стадия 2: Получение соединения 3. К раствору морфолинона 2 (0,214 г, 0,750 ммоль) в толуоле (10 мл), добавляли по каплям Red-Al (65% раствор в толуоле, 1,5 мл) при 0°С. Реакционную смесь перемешивали при температуре образования льда в течение 4 ч. Избыток Red-Al разрушали капельным добавлением 2М раствора NaOH (5 мл) и подкисляли до 103 значения рН 2 с помощью 6Н НС1. Данный раствор нейтрализовали насыщенным раствором NaHC03 и экстрагировали толуолом (2x10 мл) . Объединенные органические экстракты промывали насыщенным солевым раствором и сушили над безводным Na2S04. Растворитель удаляли при пониженном давлении, и продукт очищали на колонке с силикагелем (этилацетатгметанол, 80:20) для получения соединения морфолина 3 в виде бесцветного твердого вещества (Выход: 0,062 г, 31%), т.пл. 156-158°С. ХН ЯМР (CDC13) 6: 7,457,38 (м, 5Н) , 6,97 (м, 2Н) , 6,58 (м, 1Н) , 6,50 (д, 1Н) , 4,53 (д, 1Н), 4,10 (м, 1Н), 3,95 (м, 1Н) , 3,90 (м, 1Н) , 2,90 (м, 2Н), 2,50 (м, 1Н), 2,42 (м, 1Н) . МС (ЕС) m/z 285,98 [C17H19NO3+H]+. Анализ: подсчитано для Ci7H19N03 (0,5 Н20) С, 69,37; Н, 6,85; N, 4,76. Обнаружено: С, 69,68; Н, 5,45; N, 4,44. Пример 51 СН, (S)-2-[(S)-циклогексил-(2-этокси-фенокси)-метил]-морфолин синтезировали из циклогексилбромида магния и 2-этоксифенола в соответствии с общей методикой С и выделяли в виде смолистого масла. МС (APCI): 320 [М+Н]+. Пример 52 (S)-2- [ (S)-фенил-(2-пиперазин-1-ил-фенокси)-метил]-морфолин синтезировали в соответствии с общими методиками А и В и выделяли в виде смолистого масла. МС (APCI): 354 [М+Н]+. 104 Пример 53 (S)-2-[(S)-(2-метилсульфанил-фенокси)-фенил-метил]-морфолин синтезировали из 2-метансульфанилфенола в соответствии с общей методикой А и выделяли в виде смолистого масла. МС (APCI): 314 [М+Н]+. Пример 54 Хиральный (S)-2-[(S)-(2-метансульфонил-фенокси)-фенил-метил]-морфолин синтезировали из 2-[(2-метансульфанил-фенокси)-фенил-метил] -морфолина в соответствии с следующей методикой: Стадия 1: Исходный амин (250 мг, 0,85 ммоль) растворяли в ТГФ (5 мл) с NaOH (1 М водн., 1,0 мл). К перемешиваемому раствору добавляли ВОС20 (220 мг, 0,98 ммоль) и реакционную смесь перемешивали в течение 1 часа. Реакцию гасили водой (30 мл) и экстрагировали смесью 1:1 гексан:EtOAc (2x20 мл). Объединенные органические экстракты промывали насыщенным солевым рствором (40 мл), сушили над Na2S04, и концентрировали досуха. Материал является чистым за исключением небольшого все еще присутствующего количества ВОС20. Стадия 2: Исходный спирт (270 мг, 0,65 ммоль) растворяли в хлороформе (3,2 мл) и mcpba (290 мг, 1,6 ммоль) добавляли как 105 раствор в хлороформе (4,0 мл) при 0°С. После перемешивания в течение 4 часов, реакционную смесь фильтровали через хлопок в пипетке и экстрагировали 5% водн. NaHC03 (2x10 мл). После концентрации, ЯМР анализ^ неочищенного продукта показывал чистое превращение в единый продукт. Этот продукт очищали на силикагеле (25-70% EtOAc/гексан) для получения продукта в виде бесцветной пены. Стадия 3: Исходное вещество растворяли в 4М НС1 (раствор в диоксане) при 0°С. Реакционную смесь перемешивали в течение 1 ч. Когда исходное вещество было израсходовано (с помощью ТСХ, 1 ч) , реакционную смесь концентрировали досуха и переносили в МеОН (с помощью 5% НОАс). Очистка на ионообменной смоле (SCX, 1 г, вносили в 5% НОАс./МеОН, промывали МеОН, элюировали 1 М NH3 в МеОН) давала бесцветное густое масло, которое содержало, по данным ЯМР, один изомер. Оптическое вращение этого образца (41 мг/мл в МеОН, 100 мм длина пути, -3,713 degrees Arc) составляло -90 градусов и ВЭЖХ анализ образца показал > 98% чистоту. МС (APCI): 330 [М+Н] +. Пример 55 (S)-2-[(S)-(2-циклопентил-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде смолистого твердого вещества. МС (APCI): 338 [М+Н]+. Пример 56 (S)-2-[(S)-(2-циклогексил-фенокси)-фенил-метил]-морфолин 106 синтезировали в соответствии с общей методикой А и выделяли в виде масла. МС (APCI): 352 [М+Н]+. Пример 57 (S)-2-[(S)-(2-дифторметокси-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде масла. МС (APCI): 336 [М+Н]+. Пример 58 (S)-2-{ (S)- [2-(2-фтор-этокси)-фенокси]-фенил-метил}-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде смолистого твердого вещества. МС (APCI): 332 [М+Н] +. (S)-2-[(S)-(4-фтор-2-изобутил-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде смолистого тведого вещества. МС (APCI): 344 [М+Н] +. Хиральный Пример 59 107 Пример 60 (S)-2-[(S)-(2-хлор-б-фтор-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде смолистого твердого вещества. МС (APCI): 322 [М+Н]+. Пример 61 (S)-2-[(S)-(2-циклопропилметил-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде смолистого твердого вещества. МС (APCI): 324 [М+Н] +. Пример 62 Хиральный (S)-2-[(S)-(2,6-дихлор-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде смолистого твердого вещества. МС (APCI): 339 [М+Н]+. Пример 63 _ л,, Хиральны* (S)-2-[(S)-(2-этоксиметил-фенокси)-фенил-метил]-морфолин синтезировали из [2- (морфолин-2-ил-фенил-метокси)-фенил] -метанола в соответствии с общими методиками А и F и выделяли в 108 виде смолистого твердого вещества. МС (APCI): 328 [М+Н]+. Пример 64 Хиральный (2S,3S)-диметил-[2 -(морфолин-2-ил-фенил-метокси)-фенил]-амин синтезировали в соответствии с общей методикой А и выделяли в виде смолистого твердого вещества. МС (APCI): 313 (S)-2-{(S)- [2-(4-фтор-фенокси)-пиридин-3-илокси]-фенил-метил}-морфолин синтезировали из (S)-2-[(S)-(2-бром-пиридин-З-илокси)-фенил-метил]-морфолина в соответствии с общей методикой А реакцией биарильного присоединения общей методики D и выделяли в виде смолистого твердого вещества. МС (APCI): 381 (R)-2-[(S)-(2,6-дифтор-фенокси)-(4-фтор-фенил)-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде фумарата (белое твердое вещество). МС (APCI): 324 [М+Н]+. [М+Н] +. Пример 65 [М+Н] +. Пример 66 109 Пример 67 (R)-2-[(S)-(2-бром-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде фумарата (белое твердое вещество). МС (APCI): 348 [М+Н]+. Пример 6 8 (S)-2-[(S)-(2,4-дифтор-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде фумарата (белое твердое вещество). МС (APCI): 306 [М+Н]+. Пример 69 (S)-2-[(S)-(4-фтор-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде фумарата (белое твердое вещество). МС (APCI): 288 [М+Н]+. Пример 7 0 (R)-2-[(S)-(2-этокси-фенокси)-(3-фтор-фенил)-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде фумарата (белое твердое вещество). МС (APCI): 332 [М+Н]+. (R)-2-[(S)-(2-циклопропил-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде фумарата (белое твердое вещество). МС (APCI): 310 [М+Н]+. Пример 72 (S)-2-(2-фенокси-феноксиметил)-морфолин получали в соответствии с общей методикой D и выделяли в виде гидрохлорида. МС (APCI): 310 [М+Н]+. Пример 73 2-(2'-хлор-бифенил-2-илоксиметил)-морфолин получали с помощью бифенильной версии общей методики D и выделяли в виде гидрохлорида. МС (APCI): 3 04 [М+Н]+. Пример 74 2-(2'-метокси-бифенил-2-илоксиметил)-морфолин получали с помощью бифенильной версии общей методики D и выделяли в виде фумарата. МС (APCI): 300 [М+Н]+. Ill Пример 75 СН, (R) - и (S)-2-(5-фтор-41-метил-бифенил-2-илоксиметил)-морфолин независимо получали из (R) и (S) морфолиновых спиртов с помощью бифенильной версии общей методики D и выделяли в виде фумарата. МС (APCI): 302 [М+Н]+. Пример 76 (R) - и (S)-2-(5,4'-дифтор-бифенил-2-илоксиметил)-морфолин независимо получали из (R) и (S) морфолиновых спиртов с помощью бифенильной версии общей методики D и выделяли в виде фумарата. МС (APCI): 306 [М+Н]+. Пример 77 (R)-2-(2-фенокси-пиридин-З-илоксиметил)-морфолин получали с помощью биарилэфирной версии общей методики D и выделяли в виде фумарата. МС (APCI): 287 [М+Н]+. Пример 78 р Хиральный (S)-2-[3-(4-фтор-фенокси)-пиразин-2-илоксиметил]-морфолин 112 получали с помощью общей методики D из исходного материала, представленного 2,3-дихлорпиразином, и выделяли в виде гидрохлорида. МС (APCI): 287 [М+Н]+. Пример 79 (S)-2- [2-(3,4-дифтор-фенокси)-пиридин-3-илоксиметил]-морфолин получали с помощью биарилэфирной версии общей методики D и выделяли в виде фумарата. МС (APCI): 323 [М+Н]+. Пример 80 (S)-2-((S)-(фенокси-фенил-метил)-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде масла. МС (APCI): 270 [М+Н]+. Пример 81 (S)-2- [ (S)-(4'-фтор-бифенил-2-илокси)-фенил-метил]-морфолин синтезировали в соответствии с общими методиками А и В и выделяли в виде масла. МС (APCI): 364 [М+Н]+. Пример 82 ?Нз (S)-2-[(S)-(41-метил-бифенил-2-илокси)-фенил-метил]- 113 морфолин синтезировали в соответствии с общими методиками А и В и выделяли в виде масла. МС (APCI): 360 [М+Н]+. Пример 83 (S)-2-[(S)-(2-бензилокси-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде масла. МС (APCI): 376 [М+Н]+. Пример 84 (S)-2- [ (S)-(2-фтор-фенокси)-фенил-метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде масла. МС (APCI): 288 [М+Н]+. Пример 85 (2S,3S)- [2-(морфолин-2-ил-фенил-метокси)-фенил]-метанол синтезировали в соответствии с общими методиками А и F и выделяли в виде масла бледножелтого цвета. МС (APCI): 3 00 [М+Н] +. Пример 86 (S)-2- [ (S)-(2'-фтор-бифенил-2-илокси)-фенил-метил]- 114 морфолин синтезировали в соответствии с общими методиками А и В и выделяли в виде масла. МС (APCI): 364 [М+Н]+. Пример 87 (2R,3R)-2-[(2,4-дифтор-фенокси)-пиридин-2-ил-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 307 [М+Н] +. Пример 88 2-(2'-метил-бифенил-2-илоксиметил)-морфолин (рацемат) синтезировали в соответствии с общей методикой D (бифенильная версия) и выделяли в виде соли гидрохлорида. МС (APCI): 284 [М+Н] +. Пример 89 (2R)-2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин синтезировали в соответствии с общей методикой D и выделяли в виде фумарата. МС (APCI): 305 [М+Н]+. 115 Пример 90 (2R)-2-t(R)-(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде белой пены. МС (APCI): 315 [М+Н]+. Пример 91 (R)-2-[(S)-(2-этокси-фенокси)-фенил-метил]-морфолин получали в соответствии с общей методикой С и выделяли в виде пены. МС (APCI): 314 [М+Н]+. Пример 92 Хиральный (S)-2-[(R)-(2-этокси-фенокси)-фенил-метил]-морфолин получали в соответствии с общей методикой С и выделяли в виде пены. МС (APCI): 314 [М+Н]+. Пример 93 2-[(S)-(2S)-морфолин-2-ил(фенил)метокси]бензонитрил синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 294 [М+Н]+. 116 Пример 94 (2S)-2-[(2-хлор-5-фторфенокси)(фенил)метил]морфолин получали в соответствии с общей методикой С и выделяли в виде фумарата. МС (APCI): 321 [М+Н]+. Пример 95 -сн, (2S)-2-[(2-фтор-6-метоксифенокси)(фенил)метил]морфолин получали в соответствии с общей методикой С и выделяли в виде фумарата. МС (APCI): 317 [М+Н]+. Пример 96 (2S)-2-[(S)-(2,5-дифторфенокси)(фенил)метил]морфолин получали в соответствии с общей методикой С и выделяли в виде фумарата. МС (APCI): 305 [М+Н]+. Пример 97 Хиральный (2S)-2-[(S)-фенил(2-пропилфенокси)метил]морфолин получали в соответствии с общей методикой А и выделяли в виде соли фумарата. МС (APCI): 311 [М+Н]+. 117 Пример 98 Хиральный (2S)-2-[(S)-(2-зтилфенокси)(фенил)метил]морфолин получали в соответствии с общей методикой А и выделяли в виде соли фумарата. МС (APCI): 297 [М+Н]+. Пример 99 (2S)-2-[циклопропил(2,4-дифторфенокси)метил]морфолин получали в соответствии с общей методикой С и выделяли в виде смолы (смеси диастереомеров). МС (APCI): 269 [М+Н]+. Пример 100 (2S)-2-[(S)-(2-этоксифенокси)(1-оксидопиридин-2-ил)метил]морфолин получали в соответствии с общей методикой С со следующей дополнительной стадией: исходный амин растворяли в DCM вместе с добавлением МТО и водного Н202. Эту смесь перемешивали при комнатной температуре в течение 79 часов и гасили осторожным добавлением (тщательное выведение газа, выведение тепла, использование очень небольшого количества Мп02) Мп02 и эту пузырящуюся смесь тщательно перемешивали в течение 3 часов до прекращения выделения газа. Фазы разделяли и водную фазу экстрагировали СН2С12 (2Х). Объединенные органические фазы концентрировали для получения чистого продукта. МС (APCI): 331 [М+Н]+. 118 Пример 101 (2S)-2-[1-(2,б-дифторфенокси)-2-фенилэтил]морфолин получали в соответствии с общей методикой Е и выделяли в виде смолы (смеси диастереомеров). МС (APCI): 319 [М+Н]+. Пример 102 (2S)-2- [ (S)- [2-(бензилокси)фенокси] (пиридин-2-ил)метил]морфолин получали в соответствии с общей методикой С и выделяли в виде фумарата. МС (APCI): 376 [М+Н]+. Пример 103 (2S)-2- [ (S)-(2-изопропилфенокси) (пиридин-2-ил)метил]морфолин получали в соответствии с общей методикой Е и выделяли в виде фумарата. МС (APCI): 312 [М+Н]+. Пример 104 (2S)-2-f(IS)-1-(2-этоксифенокси)-бутил]морфолин получали в соответствии с общей методикой Е и выделяли в виде фумарата (смеси диастереомеров). МС (APCI): 279 [М+Н]+. Хфальный 119 Пример 105 (2S)-2- [ (IS)-1-(2-этоксифенокси)-3-метилбутил]морфолин получали в соответствии с общей методикой С и выделяли в виде фумарата (смеси диастереомеров). МС (APCI): 293 [М+Н]+. Пример 106 Я С1Н" O^NH (2S)-2-[(S)-(2,3-дифторфенокси)(3-фторфенил)метил]морфолин и (2S)-2-[(R)-(2,3-дифторфенокси)(3-фторфенил)метил]морфолин получали в соответствии с общей методикой С и выделяли в виде смеси диастереомеров. МС (APCI): 266 [М+Н]+. Пример 107 HjC "jjj^^j Хиральный \J о. н 1 сн, (2S)-2- [ (S)-(2-этоксифенокси) (б-метилпиридин-г-ил) метил ] морфолин получали в соответствии с общей методикой Е и выделяли в виде фумарата. МС (APCI): 328 [М+Н]+. Пример 108 CjHg Х|ф*ЛЬНЫЙ сн, (2S)-2-[(S)-(2-этоксифенокси)(б-метоксипиридин-г-ил ) метил] морфолин получали в соответствии с общей методикой Е и выделяли в виде фумарата. МС (APCI): 344 [М+Н]+. 120 Пример 109 ((2S)-2-{(S)-(6-метоксипиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин получали в соответствии с общей методикой Е и выделяли в виде фумарата. МС (APCI) : 384 [М+Н] +. Пример 110 (2S)-2-[(S)-(2,3-дигидро-1Н-инден-4-илокси)(пиридин-2-ил)метил]морфолин получали в соответствии с общей методикой Е и выделяли в виде сукцината. МС (APCI): 311 [М+Н]+. Пример 111 (2R)-2-[(2,6-дифторфенокси)(4-фторфенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 323 [М+Н]+. Пример 112 (2R)-2-[(2-бромфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 349 [М+Н]+. 121 Пример 113 Хиральный (2S)-2- [ (S)-(2-хлор-6-фторфенокси) (фенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 322 [М+Н]+. Пример 114 (2R)-2-[(2-циклопропилфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 310 [М+Н]+. Пример 115 N,N,Ы-триметил-2-[(S)-(2S)-морфолин-2-ил(фенил)метокси]бензоламиний синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 328 [М+Н]+. Пример 116 Хиральный (2S)-2-[(S)-{[2-(4-фторфенокси)пиридин-Зил] окси} (фенил) метил] морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 381 [М+Н]+. 122 Пример 117 4> н (2S)-2-[(S)-(2-бром-4-фторфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 367 [М+Н]+. Пример 118 (2S)-2-[циклопропил(2-этоксифенокси)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 278 [М+Н]+. Пример 119 (2S)-2- [ (S)-(2-циклопропил-4-фторфенокси)(фенил)метил]морфолин синтезировали в соответствии с общими методиками А и В и выделяли в виде твердого вещества белого цвета. МС (APCI): 328 [М+Н]+. Пример 120 (2S)-2- [ (S)- [2-фторфенокси)] (пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 289 [М+Н]+. 123 Пример 121 IX) (2S)-2-[(R)-[2-фторфенокси)](пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 289 [М+Н]+. Пример 122 Хиральный (2S)-2- [ (S)-(2-циклопропил-4,6-дифторфенокси)(фенил)метил]морфолин синтезировали в соответствии с общими методиками А и В и выделяли в виде твердого вещества белого цвета. МС (APCI): 346 [М+Н]+. Пример 123 ( (2S)-2- [ (2-этоксифенокси) (4-метил-1,З-оксазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI) : 319 [М+Н] +. Пример 124 Hp ^ - <Гч. хнрыьныа (2S)-2-[(S)-[(2-этилпиридин-З-ил)окси](фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 299 [М+Н]+. 124 Пример 125 Хиральный 2- [ (S)-(2S)-морфолин-2-ил(пиридин-2-ил)метокси]бензонитрил синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 296 [М+Н]+. Пример 126 Хиральный (2S)-2-[(S)-(2-изопропоксифенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI) : 329 [М+Н]+. Пример 127 ц -1 Хиральный N. (2S)-2-[(S)-(2-пропилфенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 313 [М+Н]+. Пример 128 Хиральный (2S)-2- [ (S)-(2-бензилфенокси) (пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 361 [М+Н]+. 125 Пример 129 (2S)-2-{(S)-пиридин-2-ил[2-(трифторметокси)фенокси]метил}-морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 355 [М+Н] + Пример 130 Хиральный (2S)-2-[(S)-(2-изопропил-5-метилфенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 327 [М+Н]+. Пример 131 (2S)-2-[(S)-[(2-метилпиридин-З-ил)окси](фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 285 [М+Н] +. Пример 132 (2S)-2- [ (S)-(2-циклопентилфенокси) (пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. 126 МС (APCI): 339 [М+Н]+. Пример 133 Хиральный (2S)-2-{(S)-пиридин-2-ил[2-(трифторметил)фенокси]метил]-морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 33 9 [М+Н] +. Пример 134 (2S)-2-[(2,6-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде фумарата (смеси диастереомеров). МС (APCI) : 311 [М+Н]+. Пример 135 (2S)-2-{(S)-фенил[(2-пропилпиридин-З-ил)окси]метил}морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 313 [М+Н]+. Пример 136 (2S)-2-{1-[(2-этоксипиридин-З-ил)окси]пропил}морфолин синтезировали в соответствии с общей методикой С и выделяли в 127 виде смолистого масла, содержащего смесь диастереомеров. МС (APCI): 267 [М+Н]+. Пример 137 Хиральный (2S)-2-[(S)-[(2-этоксипиридин-З-ил)окси](фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 315 [М+Н] +. Пример 138 и Хиральны" он, (2S)-2-[(S)-(2-этоксифенокси)(З-метилпиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI) : 329 [М+Н]+. Пример 139 Хиральный (2S)-2-{(S)-(З-метилпиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 369 [М+Н]+. 128 Пример 140 Хиральный (2S)-2-[(S)-(2-изопропоксифенокси)(б-метоксипиридин-г-ил ) метил ] морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI) : 359 [М+Н] +. Пример 141 (2S)-2- [ (S)-(4-этилпиридин-2-ил) (2-фтор-6-метоксифенокси)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 347 [М+Н]+. Пример 142 ф-9 сн, (2S)-2-[(S)-(2-этоксифенокси)(4-этилпиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 343 [М+Н]+. Пример 143 (2S)-2-[1-бензофуран-2-ил(2,6-дифторфенокси)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в 129 виде твердого вещества белого цвета, содержащего смесь диастереомеров. МС (APCI): 346 [М+Н]+. Пример 144 сот (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]этил}морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 253 [М+Н]+. Пример 145 Хиральный (2S)-2- [ (S)- [2-(3-фторпропил)фенокси) (фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 330 [М+Н]+. Пример 146 6гг° (2S)-2-[(S)-циклопент-1-ен-1-ил(2,б-дифторфенокси)метил]-морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета, содержащего смесь диастереомеров. МС (APCI): 296 [М+Н]+. Пример 147 (2S)-2-[(R)-циклопент-1-ен-1-ил(2,6-дифторфенокси)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 296 [М+Н]+. 130 Пример 148 (2S)-2-[(2,6-диметоксифенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 330 [М+Н]+. Пример 149 (2S)-2-{l-[(2-этоксипиридин-З-ил)окси]-3-метилбутил}морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 295 [М+Н]+. Пример 150 Хиральный (2S)-2-[(S)-[(2-циклопропилпиридин-Зил) окси] (фенил) метил] морфолин синтезировали в соответствии с общими методиками А и В и выделяли в виде твердого вещества белого цвета. МС (APCI): 311 [М+Н]+. Пример 151 (2S)-2-{1-[2-(4-фторфенокси)фенокси]этил}морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 318 [М+Н]+. 131 Пример 152 (2S)-2-[(S)-(2-хлор-5-фторфенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 324 [М+Н]+: Пример 153 Хиральный (2S)-2-[(S)-(бифенил-2-илокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 347 [М+Н]+. Пример 154 Хиральный (2S)-2- [ (S)-(2-циклопропилфенокси) (пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 311 [М+Н]+. Пример 155 (2S)-2-[(S)-(2-бромфенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 350 [М+Н]+. 132 Пример 156 (2S)-2-[[2-(фторметил)фенокси](фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 302 [М+Н]+. Пример 157 (2S)-2-[(2-этокси-б-фторфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 332 [М+Н]+. Пример 158 Хмральный (2S)-2-[(S)-(2-фтор-6-метоксифенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 319 [М+Н]+. Пример 159 Хиральный ск, (2S)-2-[(S)-(2-этокси-6-фторфенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с методикой Е и выделяли в виде твердого вещества белого МС (APCI): 333 [М+Н]+. общей цвета. 133 Пример 160 (2S)-2- [ (S)-(2,б-дифторфенокси) (пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 307 [М+Н]+. Пример 161 Хиральный (2S)-2- [ (S)- [2-(3-фторпропокси)фенокси] (фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 346 [М+Н] +. Пример 162 (2S)-2-{(IS)-2-циклогексил-1-[(2-этоксипиридин-З-ил ) окси] этил } морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 335 [М+Н]+. Пример 163 (2S)-2-[(2,б-дифторфенокси)(2,3-дигидро-1-бензофуран-7-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. 134 МС (APCI): 348 [М+Н]+. Пример 164 (2S)-2-[(S)-(2-циклопропил-5-фторфенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общими методиками Е и В и выделяли в виде твердого вещества белого цвета. МС (APCI) : 329 [М+Н]+. Пример 165 (2S)-2-[(S)-(2-фтор-б-изопропоксифенокси)(фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 346 [М+Н]+. Пример 166 (2S)-2-[(S)-[(2-метоксипиридин-З-ил)окси](фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 301 [М+Н]+. Пример 167 (2S)-2-[(5-фтор-2-метоксифенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в 135 виде твердого вещества белого цвета. МС (APCI): 318 [М+Н] Пример 168 (2S)-2-[(З-фтор-2-метоксифенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 318 [М+Н]+. Пример 169 (2S)-2-[(2-этокси-5-фторфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 332 [М+Н]+. Пример 170 (2S)-2-[(2-этокси-З-фторфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 332 [М+Н]+. Пример 171 Хиралымй (2S)-2-[(S)-(2-фтор-6-пропоксифенокси)(фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 346 [М+Н] +. 136 Пример 172 =н. <*. (2S)-2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI) : 319 [М+Н]+ . Пример 173 (2S)-2-[(2,6-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 311 [М+Н]+. Пример 174 (2S)-2-{(4-метил-1,3-оксазол-2-ил)[2-(трифторметокси)фенокси]метил}морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 359 [М+Н]+. Пример 175 (2S)-2- [ (2,6-дифторфенокси) (1,З-тиазол-2-ил)метил]-морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 313 [М+Н] +. 137 Пример 176 Хиральный (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]пентил}морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 295 [М+Н]+. Пример 177 (2S)-2-[(2-бромфенокси)(4-метил-1,3-оксазол-2-ил)метил]-морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 354 [М+Н] +. Пример 178 Хмральный (2S)-2-[(S)-(2-фтор-б-метилфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 302 [М+Н]+. Пример 179 Hp vJ3H4 [ <^\ Хиральный (2S)-2- [ (S)-[(2-изопропилпиридин-З-ил)окси] (фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 313 [М+Н] +. 138 Пример 180 (2S)-2 -[(2-этоксифенокси) (1,З-тиазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 321 [М+Н]+. Пример 181 Хиральный (2R)-2-[(R)-(2-этоксифенокси)(пиридин-2-ил)метил]морфолин синтезировали из R морфолинового спирта в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 315 [М+Н]+. Пример 182 (2S)-2-[(S)-[(2-изобутилпиридин-З-ил)окси](фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 327 [М+Н]+. Пример 183 Хиральный (2S)-2-[(S)-(2-фтор-6-изопропилфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 330 [М+Н]+. 139 Пример 184 (2S)-2- [ (S)-(2-циклопропил-6-фторфенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 328 [М+Н]+. Пример 185 (2S)-2-[(S)-(2-бром-б-фторфенокси)(6-метоксипиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 398 [М+Н]+. Пример 186 Хиральный (2S)-2-[(S)-(2-бром-б-фторфенокси)(пиридин-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 368 [М+Н]+. Пример 187 Хиральный (2S)-2-[(S)-(2-бромфенокси)(б-метоксипиридин-г-ил) метил] морфолин синтезировали в соответствии с методикой Е и выделяли в виде твердого вещества белого общей цвета. 140 МС (APCI) : 380 [М+Н] +. Пример 188 СН, Харшьный (2S)-2-[(S)-(2-фтор-6-метоксифенокси)(б-метоксипиридин-г-ил ) метил] морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI) : 349 [М+Н]+. Пример 189 (2S)-2-{l- [ (2-этоксипиридин-З-ил)окси]-2-метилпропил}морфолин синтезировали в соответствии с общей методикой С и выделяли в виде твердого вещества белого цвета. МС (APCI): 281 [М+Н]+. Пример 190 (2S)-2-[(2-циклопропилфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 315 [М+Н]+. Пример 191 (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]бутил}морфолин синтезировали в соответствии с общей методикой С и выделяли в 141 виде твердого вещества белого цвета. МС (APCI): 281 [М+Н]+. Пример 192 Хиральный (2S)-2-[(S)-{[2-(циклопропилметокси)пиридин-Зил) окси} (фенил) метил] морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 341 [М+Н]+. Пример 193 Хмрольный (2S)-2-[(S)-[2-фтор-б-(трифторметил)фенокси](фенил)метил]-морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 356 [М+Н] +. Пример 194 Х|дольный (2S)-2-[(S)-[2-фтор-б-(трифторметокси)фенокси)(фенил)метил]морфолин синтезировали в соответствии с общей методикой А и выделяли в виде твердого вещества белого цвета. МС (APCI): 372 [М+Н]+. Пример 195 (S)-2-[(2-этоксифенокси)(1,З-оксазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в 142 виде твердого вещества белого цвета, содержащего смесь диастереомеров. МС (APCI): 305 [М+Н]+. Пример 196 (S)-2-[(2,6-дифторфенокси)(1,3-оксазол-2-ил)метил]морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета, содержащего смесь диастереомеров. МС (APCI): 297 [М+Н]+. Пример 197 (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]-2-фенилэтил}морфолин синтезировали в соответствии с общей методикой Е и выделяли в виде твердого вещества белого цвета. МС (APCI): 329 [М+Н]+. Пример 198 (2S)-2-[(S)-[4-фтор-2-(метилтио)фенокси)(фенил)метил]-морфолин получали в соответствии с общей методикой Е и выделяли в виде фумарата. МС (APCI): 335 [М+Н]+. Пример 199 (2S)-2-[(S)-(2,6-дифторфенокси)(б-метоксипиридин-2-ил)метил]морфолин получали в соответствии с общей методикой Е и 143 выделяли в виде фумарата. МС (APCI): 337 [М+Н]+. Пример 200 Хиральный (2R,2'R)-2,2'-[пиразин-2,3-диилбис(оксиметилен)]диморфолин получали в соответствии с общей методикой D из 2,3-дихлорпиразина и выделяли в виде гидрохлорида. МС (APCI): 311 СН, (S)-2-[2-этокси-пиридин-3-илоксиметил]морфолин синтезировали с помощью общей методики D и выделяли в виде смолистого масла. МС (APCI): 238 [М+Н]+. Пример 202 (2R)-2-[(2-фтор-6-метоксифенокси)(пиридин-Зил ) метил] морфолин получали, используя общую методику С, из 3-бромпиридина и 2-фтор-6-метоксифенола и выделяли в виде смолистого твердого вещества, содержащего смесь диастереомеров. МС (APCI): 319 [М+Н]+. Примеры фармацевтических композиций В следующих примерах термин "активное соединение" или "активный ингредиент" относится к соединению настоящего изобретения, указанного выше, или подходящей комбинации с другим активным агентом, например, лигандом A2D, атипичным [М+Н]+. Пример 201 144 антипсихотиком SRI, др., и/или фармацевтически приемлемой солью или сольватом, в соответствии с настоящим изобретением, (i) Композиции таблеток Следующие композиции А и В могут быть получены влажной грануляцией ингредиентов от (а) до (с) и от (а) до (d) с раствором повидона, с последующим добавлением стеарата магния и сжатием. Композиция А мг/таблетка мг/таблетка (a) Активный ингредиент 250 250 (b) Лактоза В.Р. 210 26 (c) Крахмальный гликолят 20 12 натрия (d) Повидон В.Р. 15 9 (e) Стеарат магния 5 3_ 500 300 Композиция В мг/таблетка мг/таблетка (a) Активный ингредиент 250 250 (b) Лактоза 150 150 (c) Avicel РН 101 60 26 (d) Крахмальный 20 12 гликолят натрия (e) Повидон В.Р. 15 9 (f) Стеарат магния 5 3 500 300 Композиция С мг/таблетка Активный ингредиент 100 Лактоза 200 Крахмал 50 Повидон 5 Стеарат магния 4 359 Следующие композиции D и Е могут быть получены непосредственным сжатием добавленных ингредиентов. Тип лактозы, 145 используемый в прописи Е, предназначен для непосредственного сжатия. Композиция D мг/таблетка Активный ингредиент 250 Стеарат магния 4 Прежелатинизированный крахмал 146 NF15 400 Композиция Е мг/таблетка Активный ингредиент 250 Стеарат магния 5 Лактоза 145 Avicel 100 500 Композиция F (Композиция с контролируемым высвобождением) мг/таблетка (a) Активный ингредиент 500 (b) Гидроксипропилметилцеллюлоза 112 (Methocel К4М Premium) (c) Лактоза В.Р. 53 (d) Повидон В.Р.С. 28 (e) Стеарат магния 7 700 Данная композиция может быть получена влажной грануляцией ингредиентов от (а) до (с) с раствором повидона, с последующим добавлением стеарата магния и сжатием. Композиция G (таблетка с энтеросолюбильным покрытием) Таблетки с энтеросолюбильным покрытием композиции С могут быть получены покрытием таблеток энтеросолюбильным полимером 25 мг/таблетка, таким как ацетатфталат целлюлозы, поливинилацетатфталат, фталат гидроксипропилметилцеллюлозы, или анионными полимерами метакриловой кислоты и метилового эфира метакриловой кислоты (Eudragit L). Кроме Eudragit L, эти полимеры должны также включать 10% (по массе от количества 146 используемого полимера) пластификатора для предотвращения растрескивания оболочки во время применения или хранения. Подходящие пластификаторы включают диэтилфталат, трибутилцитрат и триацетин. Композиция Н (таблетка с энтеросолюбильным покрытием с контролируемым высвобождением) Таблетки с энтеросолюбильным покрытием композиции F могут быть получены покрытием таблеток таким энтеросолюбильным полимером 50 мг/таблетка, как ацетатфталат целлюлозы, поливинилацетатфталат, фталат гидроксипропилметилцеллюлозы, или анионными полимерами метакриловой кислоты и метилового эфира метакриловой кислоты (Eudragit L). Кроме Eudragit L, эти полимеры должны также включать 10% (по массе от количества используемого полимера) пластификатора для предотвращения растрескивания оболочки во время применения или хранения. Подходящие пластификаторы включают диэтилфталат, трибутилцитрат и триацетин. (ii) Композиции капсул Композиция А Капсулы могут быть получены смешиванием ингредиентов композиции D, указанной выше, и заполнением твердых желатиновых капсул, состоящих из двух частей, полученной смесью. Композиция В (ниже) может быть получена аналогичным образом. Композиция В мг/капсула (a) Активный ингредиент 250 (b) Лактоза В.Р. 143 (c) Крахмальный гликолят натрия 25 (d) Стеарат магния 2 420 Композиция С мг/капсула (a) Активный ингредиент 250 (b) Macrogol 4000 BP 350 600 Капсулы могут быть получены плавлением Macrogol 4000 BP, 147 диспергированием активного ингредиента в расплавленном материале и заполнением им твердых желатиновых капсул, состоящих из двух частей. Композиция D мг/капсула Активный ингредиент 250 Лецитин 100 Арахисовое масло 100 450 Капсулы могут быть получены диспергированием активного ингредиента в лецитине и арахисовом масле и заполнением дисперсией эластичных желатиновых капсул. Композиция Е (капсула с контролируемым высвобождением) мг/капсула (a) Активный ингредиент 250 (b) Микрокристаллическая целлюлоза 125 (c) Лактоза В.Р. 125 (d) Этилцеллюлоза 13 513 Состав капсул с контролируемым высвобождением может быть получен продавливанием смешанных ингредиентов от (а) до (с) с применением пресса, с последующим формованием и высушиванием экструдата. Высушенные шарики покрывают оболочкой, контролирующей высвобождение (d), и заполняют ими твердые желатиновые капсулы, состоящие из двух частей. Композиция F (энтеросолюбильные капсулы) мг/капсула (a) Активный ингредиент 250 (b) Микрокристаллическая целлюлоза 125 (c) Лактоза В.Р. 125 (d) Ацетатфталат целлюлозы 50 (e) Диэтилфталат 5 555 Композиция энтеросолюбильных капсул может быть получена продавливанием смешанных ингредиентов от (а) до (с) с применением пресса, с последующим формованием и высушиванием 148 экструдата. Высушенные шарики покрывают энтеросолюбильной оболочкой (d) , содержащей пластификатор (е) , и заполняют ими твердые желатиновые капсулы, состоящие из двух частей. Композиция G (капсула с энтеросолюбильным покрытием с контролируемым высвобождением) Капсулы с энтеросолюбильным покрытием композиции Е могут быть получены покрытием капсул с контролируемым высвобождением энтеросолюбильным полимером 50 мг/капсула, таким как ацетатфталат целлюлозы, поливинилацетатфталат, фталат гидроксипропилметилцеллюлозы, или анионными полимерами метакриловой кислоты и метилового эфира метакриловой кислоты (Eudragit L) . Кроме Eudragit L, эти полимеры должны также включать 10% (по массе от количества используемого полимера) пластификатора для предотвращения растрескивания оболочки во время применения или хранения. Подходящие пластификаторы включают диэтилфталат, трибутилцитрат и триацетин. (iii) Композиция внутривенной инъекции Активный ингредиент 0,200 г Стерильный апирогенный фосфатный буфер (рН 9,0) до 10 мл Данный активный ингредиент растворяют в большей части фосфатного буфера при 35-40°С, затем доводят до определенного объема и фильтруют через стерильный микропористый фильтр в стерильные ампулы на 10 мл (Тип 1), которые закупоривают стерильными пробками и крышками. (iv) Композиция внутримышечной инъекции Активный ингредиент 0,20 г Бензиловый спирт 0,10 г Гликофурол 75 1,45 г Вода для инъекций до 3,00 мл Данный активный ингредиент растворяют в гликофуроле. Затем добавляют бензиловый спирт и растворяют и доводят водой до 3 мл. Смесь затем фильтруют через стерильный микропористый фильтр и укупоривают в стерильных стеклянных ампулах на 3 мл (Тип 1). (v) Композиция сиропа Активный ингредиент 0,25 г 149 Раствор сорбита 1,50 г Глицерин 1 г Бензоат натрия 0,005 г Ароматизатор 0,0125 мл Вода очищенная до 5,0 мл Бензоат натрия растворяют в части очищенной воды и добавляют раствор сорбита. Данный активный ингредиент добавляют и растворяют. Полученный раствор смешивают с глицерином и затем доводят до требуемого объема с помощью очищенной воды. (vi) Композиция суппозитория мг/суппозиторий Активный ингредиент 250 Твердый жир BP (Witepsol Н15 - Dynamit NoBel) 1770 2020 Одну пятую часть Witepsol Н15 расплавляют в котле с паровой рубашкой при максимальной температуре 45°С. Данный активный ингредиент просеивают через сито 2001 меш и добавляют к расплавленной основе с перемешиванием, с использованием Silverson, обуродованного режущей головкой, до получения однородной дисперсии. Сохраняя смесь при температуре 45°С, к суспензии добавляют оставшийся Witepsol HI 5, которую перемешивают для обеспечения гомогенной смеси. Всю суспензию затем пропускают через сетчатый нержавеющий фильтр 2501 меш и, с постоянным перемешиванием оставляют для охлаждения до 4 0"С. При температуре 38-40°С, аликвоты смеси массой 2,02 г помещают в подходящие пластиковые формы и оставляют суппозитории для охлаждения до комнатной температуры. (vii) Композиция пессарий мг/пессарий Активный ингредиент 250 Безводная декстроза 380 Картофельный крахмал 363 Стеарат магния 1_ 1000 Указанные выше ингредиенты непосредственно смешивают и 150 пессарии готовят сжатием полученной смеси, (viii) Трансдермальная композиция Активный ингредиент 200 мг Спирт USP 0,1 мл Гидроксиэтилцеллюлоза Данный активный ингредиент и спирт USP желируют с гидроксиэтилцеллюлозой и упаковывают в трансдермальное средство с площадью поверхности 10 см2. Все ссылки, приведенные в данном документе включены в их полноте и для всех целей. 151 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы 1: и фармацевтически приемлемые соли или производные, где: А представляет собой О или S; X представляет собой арил, гетероцикл, бензоконденсированный бициклический, -Ci-Сюалкил, -С2-С8алкенил, -С5-С8циклоалкенил, - (СН2) пСз-С9циклоалкил, конденсированный циклоалкил, Н, SCF3, гидрокси-С!-С6алкил, -С1-С6алкокси, -С1-СбалкоксиС1-С6алкокси, - (СН2) П3-С1-С6алкил, -(CH2)nS02- Ci-Сбалкил; где каждая группа необязательно замещена одним или более заместителями, независимо выбранными из -С1-С6алкила, -С3-С8циклоалкила, -Ст.-С6алкокси, арила, гетероцикла, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON (H) Сг-Сбалкила, -CON (Ст.-С6алкил) 2, гидрокси-Сх-Сбалкила, -Ст.-4алкокси, -SCF3, S02, -Ст.-С4алкил-3-С1-С4алкила, -С1-С4алкил-3-, -С1-С4алкилШ'11", NR'R", при условии что, когда X является фенилом, замещенным фенилом, С1-4замещенным алкилом, гало-замещеннымС1-С4алкилом, незамещенным С3-С8циклоалкилом или гало-замещеннымС3-С8циклоалкилом, тогда * и @ являются либо (R,S) или (S,R); R1-R5 выбирают независимо из Н, С1-С6алкила, арила, -С3-С8циклоалкила, -С1-С6алкенила, -С5-С8циклоалкенила, - (СН2) пС3-С8циклоалкила, -С1-С6алкокси, -О-арила, гетероцикла, S02, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN,-CONH2, -CON(H) Сг-С6алкила, - CON (Ci - Сбалкил) 2, гидрокси-С!-С6алкила, -С1-С4алкоксиС1-С6алкила, -SCF3, -С1-С6алкил-802, С1-С4алкил-3-С1-С4алкила, -Ст.-С4алкил-3, -Cl-C4aлкилNR, R", и NR'R" и где две группы из групп R1-R5, связанные с кольцом, могут образовывать бензоконденсированное бициклическое кольцо, содержащее фенильную группу, 152 конденсированную с 5-6-членным карбоциклическим кольцом, или фенильную группу, конденсированную с 5-6-членным гетероциклическим кольцом, содержащим, по меньшей мере, один из гетероатомов N, 0, или S и где каждая из групп -С1-С6алкил, арил, -С3-С8циклоалкил, -С2-С8циклоалкенил, -С5-С8циклоалкенил, -Ci-Сбалкокси, гетероцикл может быть необязательно замещена одной или более из следующих групп: арильной, гетероциклильной, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON(H) Ст.-Сбалкильной, -CON (Ci-Свал кил) 2, гидрокси-С1-С6алкильной, -С1-Сбалкокси, -С^Свалкильной, -SCF3, -Сх-СбалкилБОг, -С1-С4алкил-3- -С1-С4алкильной, -С1-С4алкил-Б-, - Ci-С4 ал килNRIR" и NR'R"; R' и R" независимо представляют собой С1-С6алкил или Н; п представляет собой значение от 1 до 5; * обозначает первый хиральный центр; и @ обозначает второй хиральный центр. 2. Соединение по п.1, где R1 представляет собой С1-С6алкил, галоген, ОН, CN, -SCi-Сбалкил, СН2ОСт_-С6алкил, С3-С8циклоалкил, ИЛИ Ci-СбЭЛКОКСИ . 3. Соединение по п.1, где R1 является CN или -SCx-Сбалкилом. 4. Соединение по п.1, где R3, R4 и R5 не могут быть одновременно замещены. 5. Соединение формулы II: и его фармацевтически приемлемые соли или производные, где: R1 и R6, R7 и R8 независимо выбирают из Н, Ci-Свалкила, арила, -С3-С8циклоалкила, -С2-Сбалкенила, -С5-С8циклоалкенила, - (СН2)пС3-С9циклоалкила, -С1-С6алкокси, -О-арила, гетероцикла, 153 S02, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON (H) С1-Сбалкила, -CON (С1-С6алкил) 2, гидрокси-С1-С6алкила, -С1-С4алкоксиС1-С6алкила, -SCF3, -С1-С6алкил-302, -Сд.-С4алкил-3-С1-С4алкила, -С1-С4алкил-3, -Cl-C4aлкилNR,R" и NR'R", и где каждая из групп С1-С6алкил, арил, -С3-С8циклоалкил, -С2-С8циклоалкенил, -С5-С8циклоалкенил, -С1-С6алкокси, арил, гетероцикл может быть необязательно замещена одной или более из следующих групп: -С1-С6ал киль ной, арильной, гетероциклильной, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON(H) С1-С6алкильной, -CON (С1-С6алкил) 2, гидрокси-С1-С6алкильной, -С1-С4алкокси- С1-С6алкильной, -С1-С6алкокси, -SCF3, -С1-С6алкил302, -С].-С4алкил-S-, -С1-С4алкильной, - Ci - С4ал килNR' R" и NR'R"; R' и R" независимо представляют собой -С1-С6алкил или Н; п представляет собой значение от 1 до 5; R3 представляет собой Н или F; R4 представляет собой Н или F, однако когда R3 является F, R4 не является F; R5 представляет собой Н, галоген, С1-С6алкил, С1-С6алкокси, -S-Ci-Сбалкил, - (СН2) п-0-(СН2) п-, -OCF3 или -SCF3; и * обозначает первый хиральный центр; и @ обозначает второй хиральный центр при условии, что когда R1 представляет собой метил, -О-метил, -О-зтил, С1 и R3-R6 представляет собой Н, тогда * и @ являются либо (S,R) или (R,S), и, кроме того, когда R1 представляет собой -О-метил и R6-R8 представляют собой Н, -О-метил, С1 или метил, тогда * и @ являются либо (S,R) или (R,S). 6. Соединение по п. 5, где R1 представляет собой -С1-С6алкил, галоген, -ОН, -CN, -SCi-Сбалкил, -СН2ОС1-С6алкил, -С3-С8циклоалкил, С1-С6алкокси, пиридил, фенил или замещенный фенил. 7. Соединение по п. 5, где R1 представляет собой F, -С1-С6алкил или -CN. 8. Соединение по п. 5, где R3, R4 и R5 не могут быть одновременно замещены. 9. Соединение формулы III: 154 и фармацевтически и/или его ветеринарно приемлемые соли или производные, где: А представляет собой О; Z представляет собой нефенильный гетероарил, выбранный из пиридина, фурана, тиофена, нафталина, нафтиридина, пиразола, пиразина, пиримидина, тиазола, оксазола, изоксазола, триазола, тетразола; или фенильного кольца, конденсированного с гетероциклом, содержащим N, О или S; где каждый из гетероарилов может быть необязательно замещен одним или более заместителями, независимо выбранными из гетероцикла, -С3-С8циклоалкила, фенила, -С2-С8алкенила, -С5-С8циклоалкенила, - (СН2)пС3-С9циклоалкила, -С5-Сконденсированного циклоалкила, арила, Н, -SCF3, гидрокси-Ci-Сбалкила, -С1-С6алкокси, -О-арила, - (СН2) nS-Ci-Сбалкила, -С1-С6алкил-802, - (СН2) п302-С1-С6алкила, -С1-С6алкил-3-, -С1-С4алкилШ'К" или NR'R", где любая из предшествующих групп необязательно замещена одним или более заместителями, независимо выбранными из -С1-С6алкила, -С3-С8циклоалкила, -С1-С6алкокси, замещенных или незамещенных арилом, гетероциклом, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, -CONH2, -CON (H) Ci-Сбалкилом, -CON (С1-С6алкил) 2, гидрокси-С1-С6алкилом, -SCF3, -С1-С6алкил302, -С1-С4алкил-3-С1-С4алкилом, -С1-С4алкил-3-, -С1-С4алкилШ^" и NR'R"; X представляет собой гетероцикл, арил, -С1-С8алкил, -С2-С8алкенил, -С5-С8циклоалкенил, бензоконденсированный бициклический, -С3-С8циклоалкил, - (СН2) пС3-С8циклоалкил, -С5-С9конденсированный циклоалкил, Н, -SCF3, гидрокси-С1-С6алкил, -С1-С6алкокси, -С!-С6алкил, - (СН2) П3-С1-С6алкил, -(CH2)nS02-С1-С6алкил, где любая из групп необязательно замещена одним или более заместителями, независимо выбранными из -Ci-Сбалкила, -С3-С8циклоалкила, -С1-С6алкокси, арила, гетероцикла, ОН, гало, -CF3, -CHF2, -CH2F, -OCF3, -OCHF2, -OCH2F, -0(CH2)nCF3, -CN, 155 -CONH2, -CON(H) С1-Сбалкила, -CON (С1-С6алкил) 2, гидрокси-С1-Сбалкила, -SCF3, -С1-С6алкил302, -С1-С4алкил-3-С1-С4алкила, -С1-С4алкил-3-, -Cl-C4aлкилNR,R" и NR'R"; R1 и R" независимо представляют собой С1-С6алкил или Н; п представляет собой значение от 1 до 5; * обозначает первый хиральный центр; и @ обозначает второй хиральный центр. 10. Соединение по п.9, где Z представляет собой пиридил. 11. Фармацевтическая композиция, содержащая соединение по любому из пп.1, 5 и 9 и фармацевтически приемлемый носитель. 12. Способ лечения нарушения или состояния, выбранного из группы, состоящей из норэпинефриновой дисфункции, единичных эпизодических или регулярных основных депрессивных состояний, дистимических нарушений, депрессивного невроза и невротической депрессии, меланхолической депрессии, включая анорексию, потерю веса, бессонницу, раннее утреннее пробуждение или психомоторную заторможенность; атипичной депрессии (или реактивной депрессии), включая повышенный аппетит, сонливость, психомоторное возбуждение или возбудимость, зимнюю депрессию и детскую депрессию; биполярных расстройств или маниакальной депрессии, включая биполярное расстройство 1-го типа, биполярное расстройство II-го типа и циклотимическое расстройство; расстройства поведения; расстройства, связанного с агрессивным поведением; расстройств поведения, связанных с умственной отсталостью, аутизмом и расстройством поведения; тревожных расстройств, таких как паническое расстройство с или без агорафобией, агорафобия без панического расстройства, определенные фобии, например, боязни животных, социальная тревожность, социофобия, (включая социальную тревожность), навязчивые состояния и связанные с ними обширные расстройства, стрессовые нарушения, включающие посттравматическое стрессовое нарушение, острое стрессовое нарушение и хроническое стрессовое нарушение, и генерализованные состояния тревожности; пограничных личностных расстройств; шизофрении и других психотических расстройств, например, шизофреноподобных расстройств; шизоаффективных нарушений, бредовых расстройств, 156 кратковременных психотических расстройств, общих психотических расстройств, психотических расстройств с бредом и галлюцинациями, психотических приступов тревожности, психоза, связанного с тревожностью, психотических расстройствх настроения, включая острое основное депрессивное состояние; расстройств настроения, связанных с психотическими нарушениями, включающими острую манию и депрессию, связанную с биполярным расстройством; расстройств настроения, связанных с шизофренией; делирии, деменции и амнестического и других когнитивных или нейродегенеративных расстройств, включающих болезнь Паркинсона (БП) , болезнь Хантингтона, болезнь Альцгеймера, старческое слабоумие, деменцию по типу болезни Альцгеймера, нарушения памяти, потерю дееспособности, мультиинфарктную деменцию и другие деменции, включающие, относящихся к заболеванию ВИЧ, травме головы, болезни Паркинсона, болезни Хантингтона, болезни Пика, болезни Крейтцфельда-Якоба, или относящихся к множественной этиологии; расстройств движений, включающих акинезии, дискинезии, включая семейные пароксизмальные дискинезии, спазмы, синдром де ла Туретта, синдром Скотта, параличи и акинетический ригидный синдром; экстрапирамидальные двигательные расстройства, включая двигательные расстройства, вызванные лечением, включая паркинсонизм, индуцированный нейролептиками, злокачественный нейролептический синдром, острую дистонию, индуцированную нейролептиками, острую акатизию, индуцированную нейролептиками,, отсроченную дискинезию, индуцированную нейролептиками, и индуцированный лечением постуральный тремор; расстройств привыкания и абстинентного синдрома, химических зависимостей и привыкания, включающих зависимости от алкоголя, героина, кокаина, бензодиазепинов, психоактивных веществ, никотина, или фенобарбитала и поведенческие привычки, включающие привычку к игре; нарушений зрения, включающих глаукому и ишемическую ретинопатию; расстройств привыкания к алкоголю, никотину, и другим психоактивным веществам и абстинентного синдрома, нарушения адаптации, включая подавленное состояние, тревожность, сочетание тревожности и подавленного состояния, 157 расстройство поведения и сочетание расстройства поведения и настроения; возрастных нарушений обучаемости и нервно-психических анорексий; апатии; нарушений внимания (или других когнитивных нарушений), обусловленных основными клиническими состояниями, включающими синдром нарушения внимания (СНВ) и синдром дефицита внимания с гиперактивностью (СНВГ) и его узнаваемые подтипы; нейрогенной булимии; синдрома хронической усталости; боли; хронической боли; циклотимического нарушения; депрессии, включающей пубертатную депрессию и малую депрессию; фибромиалгии и других соматических нарушений, включая соматизацию; конверсионных расстройств; болевых расстройств; ипохондрии, дизморфизма; недифференцированного соматоформного расстройства и соматоподобных NOS; недержания, включающего стрессовое недержание; истинного недержания мочи при напряжении; и смешанного недержания; расстройств мочеиспускания; преждевременной эякуляции; расстройств дыхания; интоксикаций, включающих алкогольную зависимость; мании; мигреней; ожирения, включающего снижение веса у пациентов с ожирением или избыточным весом; оппозиционно-вызывающего расстройства; периферической нейропатии; диабетической нейропатии; постгерпетической невралгии; предменструального дисфорического расстройства, включающего предменструальный синдром дисфорического расстройства поздней стадии лютеинизации; нарушений сна, включающих нарколепсию, бессонницу, и энурез; определенных нарушений развития; ингибирования селективного обратного захвата серотонина (СОЗС) синдрома "выхода из игры"; и судорожных нарушений, включающих болезнь Туретта у млекопитающих, включая человека, включающего введение животному, нуждающемуся в таком лечении, количества соединения формулы I, II или III, или соединения по любому из пунктов 1, 5 или 9. 13. Способ лечения синдрома дефицита внимания с гиперактивностью, расстройств, связанных с мочеиспусканием, болью, преждевременной эякуляцией или фибромиалгии, млекопитающих, нуждающихся в нем, который включает введение нуждающемуся млекопитающему терапевтически эффективного 158 количества соединения по любому из пп.1, 5 или 9. 14. Соединение, выбранное из следующих соединений и их фармацевтически приемлемых солей, энантиомеров и диастереомеров: 2-[фенил-(2-трифторметокси-фенокси)-метил]-морфолин; 2-[(2-этилсульфанил-фенокси)-фенил-метил]-морфолин; 2-[(2-изобутил-фенокси)-фенил-метил]-морфолин; 2-[(2-бром-фенокси)-фенил-метил]-морфолин; 2-[фенил-(2-винил-фенокси)-метил]-морфолин; 2-[(2-хлор-фенокси)-фенил-метил]-морфолин; 2-[(2-метоксиметил-фенокси)-фенил-метил]-морфолин; 2-[фенил-(2-трифторметил-фенокси)-метил]-морфолин; 2-[(2-бензил-фенокси)-фенил-метил]-морфолин; 2-[фенил-(2-пиридин-4-ил-фенокси)-метил]-морфолин; 2-[(2-циклопропил-фенокси)-фенил-метил]-морфолин; 2-[(нафталин-1-илокси)-фенил-метил]-морфолин; 2-[фенил-(2-пиридин-3-ил-фенокси)-метил]-морфолин; 2-[(2-фенокси-фенокси)-фенил-метил]-морфолин; этиловый эфир 2-(морфолин-2-ил-фенил-метокси)-бензойной кислоты; 2- [ (41-хлор-бифенил-2-илокси)-фенил-метил]-морфолин; 2-(2-этокси-феноксиметил)-морфолин; 2- [ (2-фтор-фенокси)-фенил-метил]-морфолин; 2-[(2-хлор-4-фтор-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин; 2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил; 2- [ (2-фторфенокси)-пиридин-3-ил-метил]-морфолин; 2-(морфолин-2-ил-пиридин-З-ил-метокси)-бензонитрил; 2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[пиридин-3-ил(2-трифторметокси-фенокси)-метил]-морфолин; 2-[(2-,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин; 2- [ (1-окси-пиридин-2-илокси)-фенил-метил]-морфолин; 2- [ (2'-хлор-бифенил-2-илокси)-фенил-метил]-морфолин; (2-фтор-6-метокси-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[(2-фтор-6-метокси-фенокси)-пиридин-3-ил-метил]-морфолин; 159 2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин 2-{[2-(4-фтор-фенил)-пиридин-3-илокси]-фенил-метил}-морфолин; 2-[(2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; 2-[(2-фтор-фенокси)-(4-фтор-фенил)-метил]-морфолин; 2-[(2,6-дифтор-фенокси)-фенил-метил]-морфолин; 2-[2-циклогексил-1-(2-этокси-фенокси)-этил]-морфолин; 2-[1-(2-этокси-фенокси)-3-метил-бутил]-морфолин; 2-[(2-аллил-фенокси)-фенил-метил]-морфолин; 2-[фенил-(пиридин-3-илокси)-метил]-морфолин; 2-[(2-бром-пиридин-3-илокси)-фенил-метил]-морфолин 2-[фенил-(2-п-толил-пиридин-3-илокси)-метил]-морфолин 2-[(2-хлор-фенокси)-фенил-метил]-морфолин; 2-[(2-изопропил-фенокси)-фенил-метил]-морфолин; 2-[(бензофуран-6-илокси)-фенил-метил]-морфолин; 2-[(2-изопропокси-фенокси)-фенил-метил]-морфолин; 2-[(2-бром-фенокси)-(4-фтор-фенил)-метил]-морфолин; 2-[(бензофуран-5-илокси)-фенил-метил]-морфолин; 2-(фенил-о-толилокси-метил)-морфолин; 2-(морфолин-2-ил-фенил-метокси)-фенол; 2-[циклогексил-(2-этокси-фенокси)-метил]-морфолин; 2-[фенил-(2-пиперазин-1-ил-фенокси)-метил]-морфолин; 2-[(2-метилсульфанил-фенокси)-фенил-метил]-морфолин; 2-[(2-метансульфонил-фенокси)-фенил-метил]-морфолин; 2-[(2-циклопентил-фенокси)-фенил-метил]-морфолин; 2- [ (2-циклогексил-фенокси)-фенил-метил]-морфолин; 2-[(2-дифторметокси-фенокси)-фенил-метил]-морфолин; 2-{[2-(2-фтор-этокси)-фенокси]-фенил-метил}-морфолин; 2-[(4-фтор-2-изобутил-фенокси)-фенил-метил]-морфолин; 2-[(2-хлор-6-фтор-фенокси)-фенил-метил]-морфолин; 2-[(2-циклопропилметил-фенокси)-фенил-метил]-морфолин 2-[(2,б-дихлор-фенокси)-фенил-метил]-морфолин; 2-[(2-этоксиметил-фенокси)-фенил-метил]-морфолин; диметил-[2-(морфолин-2-ил-фенил-метокси)-фенил]-амин; 2-{[2-(4-фтор-фенокси)-пиридин-3-илокси]-фенил-метил} морфолин; 160 2- [ (2, 6-дифтор-фенокси) - (4-фтор-фенил) -метил] -морфолин; 2-[(2-бром-фенокси)-фенил-метил]-морфолин; 2-[(2 , 4-дифтор-фенокси)-фенил-метил]-морфолин; 2-[(4-фтор-фенокси)-фенил-метил]-морфолин; 2-[(2-этокси-фенокси)-(3-фтор-фенил)-метил]-морфолин; 2-[(2-циклопропил-фенокси)-фенил-метил]-морфолин; 2-(2-фенокси-феноксиметил)-морфолин; 2-(21-хлор-бифенил-2-илоксиметил)-морфолин; 2-(2'-метокси-бифенил-2-илоксиметил)-морфолин; 2-(5-фтор-41-метил-бифенил-2-илоксиметил)-морфолин; 2-(5,4'-дифтор-бифенил-2-илоксиметил)-морфолин; 2-(2-фенокси-пиридин-З-илоксиметил)-морфолин; 2- [3-(4-фтор-фенокси)-пиразин-2-илоксиметил]-морфолин; 2-[2-(3,4-дифтор-фенокси)-пиридин-3-илоксиметил]-морфолин; 2-(фенокси-фенил-метил)-морфолин; 2-[(4'-фтор-бифенил-2-илокси)-фенил-метил]-морфолин; 2-[(4'-метил-бифенил-2-илокси)-фенил-метил]-морфолин; 2-[(2-бензилокси-фенокси)-фенил-метил]-морфолин; 2- [ (2-фтор-фенокси)-фенил-метил]-морфолин; [2-(морфолин-2-ил-фенил-метокси)-фенил]-метанол; 2- [ (2'-фтор-бифенил-2-илокси)-фенил-метил]-морфолин; 2-[(2,4-дифтор-фенокси)-пиридин-2-ил-метил]-морфолин; 2-(21-метил-бифенил-2-илоксиметил)-морфолин; 2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин; 2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; 2-[(2-этокси-фенокси)-фенил-метил]-морфолин; 2-[(2-этокси-фенокси)-фенил-метил]-морфолин; 2-[морфолин-2-ил(фенил)метокси]бензонитрил; 2- [ (2-хлор-5-фторфенокси) (фенил)метил]-морфолин; 2-[(2-фтор-6-метоксифенокси)(фенил)метил]-морфолин; 2-[(2,5-дифторфенокси)(фенил)метил]-морфолин; 2-[фенил(2-пропилфенокси)метил]-морфолин; 2- [ (2-этилфенокси) (фенил)метил]-морфолин; 2-[циклопропил(2,4-дифторфенокси)метил]-морфолин; 2-[(2-этоксифенокси)(1-оксидопиридин-2-ил)метил]морфолин; 2-[1-(2,6-дифторфенокси)-2-фенилэтил]морфолин; 161 2-[[2-(бензилокси)фенокси](пиридин-2-ил)метил]морфолин; 2-[(2-изопропилфенокси)(пиридин-2-ил)метил]морфолин; 2-[1-(2-этоксифенокси)бутил]морфолин; 2-[1-(2-этоксифенокси)-3-метилбутил]морфолин; 2-[(2,3-дифторфенокси)(3-фторфенил)метил]морфолин; 2-[(2-этоксифенокси)(б-метилпиридин-2-ил)метил]морфолин; 2-[(2-этоксифенокси)(6-метоксипиридин-2-ил)метил]морфолин; 2-{(6-метоксипиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; 2-[(2,3-дигидро-1Н-инден-4-илокси)(пиридин-2-ил)метил]морфолин; 2-[(2,б-дифторфенокси)(4-фторфенил)метил]морфолин; 2-[(2-бромфенокси)(фенил)метил]морфолин; 2-[(2-хлор-б-фторфенокси)(фенил)метил]морфолин; 2-[(2-циклопропилфенокси)(фенил)метил]морфолин; N,N,Ы-триметил-2-[морфолин-2-ил(фенил)метокси]бензоламиний; 2- [ { [2- (4-фторфенокси)пиридин-Зил] окси} (фенил)метил]морфолин; 2-[(2-бром-4-фторфенокси)(фенил)метил]морфолин; 2-[циклопропил(2-этоксифенокси)метил]морфолин; 2-[(2-циклопропил-4-фторфенокси)(фенил)метил]морфолин; 2- [ [2-фторфенокси)] (пиридин-2-ил)метил]морфолин; 2-[(2-циклопропил-4,6-дифторфенокси)(фенил)метил]морфолин; 2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-[[(2-этилпиридин-З-ил)окси](фенил)метил]морфолин; 2-[морфолин-2-ил(пиридин-2-ил)метокси]бензонитрил; 2-[(2-изопропоксифенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-пропилфенокси)(пиридин-2-ил)метил]морфолин; 2- [ (2-бензилфенокси) (пиридин-2-ил)метил]морфолин; 2-{пиридин-2-ил[2-(трифторметокси)фенокси]метил}морфолин; 2-[(2-изопропил-5-метилфенокси)(пиридин-2-ил)метил]морфолин; 2-[[(2-метилпиридин-З-ил)окси](фенил)метил]морфолин; 2-[(2-циклопентилфенокси)(пиридин-2-ил)метил]морфолин; 162 2-{пиридин-2-ил[2-(трифторметил)фенокси]метил]морфолин; 2-[(2,6-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-{фенил[(2-пропилпиридин-З-ил)окси]метил}морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]пропил}морфолин; 2-[[(2-этоксипиридин-З-ил)окси](фенил)метил]морфолин; 2-[(2-этоксифенокси)(3-метилпиридин-2-ил)метил]морфолин; 2-{(З-метилпиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; 2-[(2-изопропоксифенокси)(б-метоксипиридин-2-ил)метил]морфолин; 2-[(4-этилпиридин-2-ил)(2-фтор-6-метоксифенокси)метил]морфолин; 2-[(2-этоксифенокси)(4-этилпиридин-2-ил)метил]морфолин; 2-[1-бензофуран-2-ил(2,б-дифторфенокси)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]этил}морфолин; 2-[[2-(3-фторпропил)фенокси)(фенил)метил]морфолин; 2-[циклопент-1-ен-1-ил(2,б-дифторфенокси)метил]морфолин; 2-[(2,6-диметоксифенокси)(фенил)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]-3-метилбутил}морфолин; 2-[[(2-циклопропилпиридин-З-ил)окси](фенил)метил]морфолин; 2-{l-[2-(4-фторфенокси)фенокси]этил}морфолин; 2-[(2-хлор-5-фторфенокси)(пиридин-2-ил)метил]морфолин; 2-[(бифенил-2-илокси)(пиридин-2-ил)метил]морфолин; 2-[(2-циклопропилфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-бромфенокси)(пиридин-2-ил)метил]морфолин; 2-[[2-(фторметил)фенокси](фенил)метил]морфолин; 2-[(2-этокси-6-фторфенокси)(фенил)метил]морфолин; 2-[(2-фтор-6-метоксифенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-этокси-6-фторфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2,6-дифторфенокси)(пиридин-2-ил)метил]морфолин; 2-[[2-(3-фторпропокси)фенокси](фенил)метил]морфолин; 2-{2-циклогексил)-1-[(2-этоксипиридин-З-ил) окси]этил}морфолин; 2-[(2,6-дифторфенокси)(2,3-дигидро-1-бензофуран-7-ил)ме тил]морфолин; 163 2-[(2-циклопропил-5-фторфенокси)(пиридин-2-ил)метил]морфолин; 2-[(2-фтор-6-изопропоксифенокси)(фенил)метил]морфолин; 2-[[(2-метоксипиридин-З-ил)окси](фенил)метил]морфолин; 2-[(5-фтор-2-метоксифенокси)(фенил)метил]морфолин; 2-[(З-фтор-2-метоксифенокси)(фенил)метил]морфолин; 2-[(2-этокси-5-фторфенокси)(фенил)метил]морфолин; 2-[(2-этокси-З-фторфенокси)(фенил)метил]морфолин; 2-[(2-фтор-6-пропоксифенокси)(фенил)метил]морфолин; 2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-[(2,6-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-{(4-метил-1,З-оксазол-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; 222 ил)метил]морфолин; 22222222 222 (2,6-дифторфенокси)(1,З-тиазол-2-ил)метил]морфолин; 1-[(2-этоксипиридин-З-ил)окси]пентил}морфолин; (2-бромфенокси)(4-метил-1,З-оксазол-2- (2-фтор-6-метилфенокси)(фенил)метил]морфолин; [(2-изопропилпиридин-З-ил)окси](фенил)метил]морфолин; (2-этоксифенокси)(1,З-тиазол-2-ил)метил]морфолин; (2-этоксифенокси)пиридин-2-ил)метил]морфолин; [(2-изобутилпиридин-З-ил)окси](фенил)метил]морфолин; (2-фтор-б-изопропилфенокси)(фенил)метил]морфолин; (2-циклопропил- б-фторфенокси) (фенил)метил]морфолин; (2-бром-б-фторфенокси)(6-метоксипиридин-2- ил)метил]морфолин; (2-бром-б-фторфенокси)(пиридин-2-ил)метил]морфолин; (2-бромфенокси)(б-метоксипиридин-2-ил)метил]морфолин; (2-фтор-6-метоксифенокси)(6-метоксипиридин-2- ил)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]-2-метилпропил}морфолин; 2-[(2-циклопропилфенокси)(4-метил-1,З-оксазол-2-ил)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]бутил}морфолин; 164 2-[{[2-(циклопропилметокси)пиридин-3-ил]окси}(фенил)метил]морфолин; 2-[[2-фтор-б-(трифторметил)фенокси](фенил)метил]морфолин; 2- [ [2-фтор-6-(трифторметокси)фенокси)(фенил)метил]морфолин; 2-[(2-этоксифенокси)(1,З-оксазол-2-ил)метил]морфолин; 2-[(2,б-дифторфенокси)(1,3-оксазол-2-ил)метил]морфолин; 2-{1-[(2-этоксипиридин-З-ил)окси]-2-фенилэтил}морфолин; 2-[[4-фтор-2-(метилтио)фенокси](фенил)метил]морфолин; 2- [ (2,6-дифторфенокси)(6-метоксипиридин-2-ил)метил]морфолин; 2,2'-[пиразин-2,3-диилбис(оксиметилен)]диморфолин; 2-[2-этокси-пиридин-3-илоксиметил]морфолин; и 2-[(2-фтор-6-метоксифенокси)(пиридин-3-ил)метил]морфолин. 15. Соединения, выбранные из следующих соединений и их фармацевтически приемлемых солей, энантиомеров и диастереомеров: (S)-2-[(S)-фенил-(2-трифторметокси-фенокси)-метил]-морфолин; (S)-2-[(S)-2-этилсульфанил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-(2-изобутил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-(2-бром-фенокси)-фенил-метил]-морфолин; (S)-2- [ (S)-фенил-(2-винил-фенокси)-метил]-морфолин; (S)-2-[(S)-(2-хлор-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-(2-метоксиметил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-фенил-(2-трифторметил-фенокси)-метил]-морфолин; (S)-2-[(S)-(2-бензил-фенокси)-фенил-метил]-морфолин; (S)-2-[(S)-фенил-(2-пиридин-4-ил-фенокси)-метил]-морфолин; (S)-2-[(S)-(2-циклопропил-фенокси)-фенил-метил]-морфолин; (S)-2- [ (S)-(нафталин-1-илокси)-фенил-метил]-морфолин; (S)-2-[(S)-фенил-(2-пиридин-З-ил-фенокси)-метил]-морфолин; (S) -2-[(S)-(2-фенокси-фенокси)-фенил-метил]-морфолин; этиловый эфир (2S,3S)-2-(морфолин-2-ил-фенил-метокси)-бензойной кислоты; (S)-2-[((S)-4'-хлор-бифенил-2-илокси)-фенил-метил] морфолин; (S)-2-(2-этокси-феноксиметил)-морфолин; (R)-2-[(S)-(2-фтор-фенокси)-фенокси)-фенил-метил]-морфолин; (S)-2-[(R)-(2-хлор-4-фтор-фенокси)-пиридин-3-ил-метил]-морфолин; (S)-2-[(R)-(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин; (S)-2-[(S)-(2-этокси-фенокси)-пиридин-2-ил-метил]-морфолин; (2S,3S)-2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил; (2S,3R)-2-(морфолин-2-ил-пиридин-2-ил-метокси)-бензонитрил; (S)-2-[(S)-(2-фторфенокси)-пиридин-3-ил-метил]-морфолин; (2S,3R)-2-(морфолин-2-ил-пиридин-З-ил-метокси)-бензонитрил; (2R,3R)-2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; (2S,3R)-2-[(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(S)-пиридин-3-ил(2-трифторметокси-фенокси)-метил]-морфолин; (R)-2-[(S)-(2-,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(R)-(2-,4-дифтор-фенокси)-пиридин-3-ил-метил]-морфолин; (S)-2-[((S)-1-окси-пиридин-2-илокси)-фенил-метил]-морфолин; (S)-2- [ (S)-(2'-хлор-бифенил-2-илокси)-фенил-метил]-морфолин; (2R,3R)-(2-фтор-6-метокси-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(S)-(2-фтор-6-метокси-фенокси)-пиридин-3-ил-метил] морфолин; (S)-2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин (S)-2-{(S)-[2-(4-фтор-фенил)-пиридин-3-илокси]-фенил- 166 метил}-морфолин; (R)- [ (S) -(2-фтор-фенокси)-(4-фтор-фенил)-метил]- морфолин; (R) - [ (S) -(2-фтор-фенокси)-(4-фтор-фенил)-метил]- морфолин; (S) - [ (S) -(2,б-дифтор-фенокси)-фенил-метил]-морфолин; (S) - [ (S) -2-циклогексил-1-(2-этокси-фенокси)-этил]- морфолин; (2S, 3R) -2- [2-циклогексил-1-(2-этокси-фенокси)-этил]- морфолин; (S) - L (S) -1-(2-этокси-фенокси)-3-метил-бутил]-морфолин; (S) - [ (S) -(2-аллил-фенокси)-фенил-метил]-морфолин; (S) - (S) -фенил-(пиридин-3-илокси)-метил]-морфолин; (S) - :(s) -2-бром-пиридин-3-илокси)-фенил-метил]-морфолин (S) - (S) -фенил-(2-п-толил-пиридин-3-илокси)-метил]- морфолин; (S) - :(s) -2-хлор-фенокси)-фенил-метил]-морфолин; (S) - (S) -2-изопропил-фенокси)-фенил-метил]-морфолин; (R) - (S) -(бензофуран-б-илокси)-фенил-метил]-морфолин; (S) - 2- I (S) -2-изопропокси-фенокси)-фенил-метил]-морфолин; (R) - 2- I (S) -(2-бром-фенокси)-(4-фтор-фенил)-метил]- морфолин; (S) - 2- [ (S) -(бензофуран-5-илокси)-фенил-метил]-морфолин; (S) - 2- I (S) -фенил-о-толилокси-метил)-морфолин; (2S, 3S) -2- (морфолин-2-ил-фенил-метокси)-фенол; (S) - 2- I (S) -циклогексил-(2-этокси-фенокси)-метил]-морфолин; (S) - 2- I (S) -фенил-(2-пиперазин-1-ил-фенокси)-метил]- морфолин; (S) - 2- I (S) -(2-метилсульфанил-фенокси)-фенил-метил]- морфолин; (S) - 2- [ (S) -(2-метансульфонил-фенокси)-фенил-метил]- морфолин; (S) - 2- I (S) -(2-циклопентил-фенокси)-фенил-метил]-морфолин; (S) - 2- I (S) -(2-циклогексил-фенокси)-фенил-метил]-морфолин; (S) - (S) -(2-дифторметокси-фенокси)-фенил-метил]- морфолин; 167 морфолин (S морфолин (S (S морфолин (S (S (2 амин; (S метил} (R морфолин 2-{(S)-[2-(4-фтор-фенокси)-пиридин-3-илокси]-фенил-морфолин; -2- [ (S)-(2,6-дифтор-фенокси)-(4-фтор-фенил)-метил]- морфолин (R (S (R (S (R (S (R (S (S морфолин (S (S морфолин (S морфолин (S -2-{(S)-[2-(2-фтор-этокси)-фенокси]-фенил-метил}- 2- [ (S)-(4-фтор-2-изобутил-фенокси)-фенил-метил]- -2-[(S)-(2-хлор-6-фтор-фенокси)-фенил-метил]-морфолин; -2-[(S)-(2-циклопропилметил-фенокси)-фенил-метил]- -2-[(S)-(2,6-дихлор-фенокси)-фенил-метил]-морфолин; -2- [ (S)-(2-этоксиметил-фенокси)-фенил-метил]-морфолин; ,3S)-диметил-[2-(морфолин-2-ил-фенил-метокси)-фенил]- (R) -2- [ (S) (S) -2- [(S) (S) -2- [ (S) (R) -2- [ (S) -2-2-2-2-2-2-2-2-2Г -2-2Г -2Г -2(S)-(2-циклопропил-фенокси)-фенил-метил]-морфолин; 2-фенокси-феноксиметил)-морфолин; 5-фтор-4'-метил-бифенил-2-илоксиметил)-морфолин; 5-фтор-4'-метил-бифенил-2-илоксиметил)-морфолин; 5,4"-дифтор-бифенил-2-илоксиметил)-морфолин; 5,4'-дифтор-бифенил-2-илоксиметил)-морфолин; 2- фенокси-пиридин-3-илоксиметил)-морфолин; 3- (4-фтор-фенокси)-пиразин-2-илоксиметил]-морфолин; 2-(3,4-дифтор-фенокси)-пиридин-3-илоксиметил]- (S)-фенокси-фенил-метил)-морфолин; (S)-(4'-фтор-бифенил-2-илокси)-фенил-метил]- (S)-(4'-метил-бифенил-2-илокси)-фенил-метил]- (S)-(2-бензилокси-фенокси)-фенил-метил]-морфолин; 168 (S)-2-[(S)-(2-фтор-фенокси)-фенил-метил]-морфолин; (2S,3S)-[2-(морфолин-2-ил-фенил-метокси)-фенил]-метанол; (S)-2-[(S)-(21-фтор-бифенил-2-илокси)-фенил-метил]-морфолин; (2R,3R)-2-[(2,4-дифтор-фенокси)-пиридин-2-ил-метил]-морфолин; (2R)-2-[2-(4-фтор-фенокси)-пиридин-3-илоксиметил]-морфолин; (2R)-2-[(R)-(2-этокси-фенокси)-пиридин-3-ил-метил]-морфолин; (R)-2-[(S)-(2-этокси-фенокси)-фенил-метил]-морфолин; (S)-2-[(R)-(2-этокси-фенокси)-фенил-метил]-морфолин; 2-[(S)-(2S)-морфолин-2-ил(фенил)метокси]бензонитрил; (2S)-2-[(2-хлор-5-фторфенокси)(фенил)метил]-морфолин; (2S)-2-[(2-фтор-6-метоксифенокси)(фенил)метил]-морфолин; (2S)-2-[(S)-(2,5-дифторфенокси)(фенил)метил]-морфолин; (2S)-2-[(S)-фенил(2-пропилфенокси)метил]-морфолин; (2S)-2-[(S)-(2-этилфенокси)(фенил)метил]-морфолин; (2S)-2-[циклопропил(2,4-дифторфенокси)метил]-морфолин; (2S)-2-[(S)-(2-этоксифенокси)(1-оксидопиридин-2-ил)метил]морфолин; (2S)-2-[1-(2,6-дифторфенокси)-2-фенилэтил]морфолин; (2S)-2-[(S)-[2-(бензилокси)фенокси](пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-изопропилфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(IS)-1-(2-этоксифенокси)бутил]морфолин; (2S)-2-[(IS)-1-(2-этоксифенокси)-3-метилбутил]морфолин; (2S)-2-[(S)-(2,3-дифторфенокси)(3-фторфенил)метил]морфолин; (2S)-2-[(R)-(2,3-дифторфенокси)(3-фторфенил)метил]морфолин; (2S)-2-[(S)-(2-этоксифенокси)(б-метилпиридин-г-ил) метил] морфолин; (2S)-2-[(S)-(2-этоксифенокси)(б-метоксипиридин-2-ил)метил]морфолин; 169 (2S)-2-{(S)-(6-метоксипиридин-2-ил)[2-(трифторметокси)фенокси]метил}-морфолин; (2S)-2-[(S)-(2,3-дигидро-1Н-инден-4-илокси)(пиридин-2-ил)метил]морфолин; (2R)-2-[(2,6-дифторфенокси)(4-фторфенил)метил]морфолин; (2R)-2-[(2-бромфенокси)(фенил)метил]-морфолин; (2S)-2-[(S)-(2-хлор-6-фторфенокси)(фенил)метил]-морфолин; (2R)-2-[(2-циклопропилфенокси)(фенил)метил]-морфолин; N, N, N-триметил-2-[(S)-(2S)-морфолин-2-ил(фенил)метокси]бензоламиний; (2S)-2 - [ (S)-{ [2-(4-фторфенокси)пиридин-3-ил]окси}(фенил)метил]-морфолин; (2S)-2-[(S)-(2-бром-4-фторфенокси)(фенил)метил]-морфолин; (2S)-2-[циклопропил(2-этоксифенокси)метил]-морфолин; (2S)-2- [ (S)-(2-циклопропил-4-фторфенокси) (фенил)метил]-морфолин; (2S)-2-[(S)-[2-фторфенокси)](пиридин-2-ил)метил]-морфолин (2S)-2-[(R)-[2-фторфенокси)](пиридин-2-ил)метил]-морфолин (2S)-2-[(S)-(2-циклопропил-4,6-дифторфенокси)(фенил)метил]-морфолин; (2S)-2-[(2-этоксифенокси)(4-метил-1,3-оксазол-2-ил)метил] морфолин; (2S)-2-[(S)-[(2-этилпиридин-З-ил)окси](фенил)метил]-морфолин; 2-[(S)-(2S)-морфолин-2-ил(пиридин-2- ил)метокси]бензонитрил; (2S)-2- [ (S)-(2-изопропоксифенокси) (пиридин-2- ил)метил]морфолин; (2S)-2- [ (S)-(2-пропилфенокси) (пиридин-2-ил)метил]морфолин (2S)-2-[(S)-(2-бензилфенокси)(пиридин-2-ил)метил]морфолин (2S)-2-{(S)-пиридин-2-ил[2-(трифторметокси)фенокси]метил} морфолин; (2S)-2-[(S)-(2-изопропил-5-метилфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-[(2-метилпиридин-З-ил)окси](фенил)метил]-морфолин; 170 (2S)-2-[(S)-(2-циклопентилфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-{(S)-пиридин-2-ил[2-(трифторметил)фенокси]метил]-морфолин; (2S)-2-[(2,6-дифторфенокси)(4-метил-1,З-оксазол-2-ил)метил]-морфолин; (2S)-2-{(S)-фенил[(2-пропилпиридин-З-ил)окси]метил}морфолин; (2S)-2-{1-[(2-этоксипиридин-З-ил)окси]пропил}морфолин; (2S)-2-[(S)-[(2-этоксипиридин-З-ил)окси](фенил)метил]-морфолин; (2S)-2-[(S)-(2-этоксифенокси)(З-метилпиридин-2-ил)метил]-морфолин; (2S)-2-{(S)-(З-метилпиридин-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; (2S)-2- [ (S)-(2-изопропоксифенокси) (6-метоксипиридин-2-ил)метил]-морфолин; (2S)-2- [ (S)-(4-этилпиридин-2-ил) (2-фтор-6-метоксифенокси)метил]-морфолин; (2S)-2-[(S)-(2-этоксифенокси)(4-этилпиридин-2-ил)метил]-морфолин; (2S)-2-[1-бензофуран-2-ил(2,6-дифторфенокси)метил]-морфолин; (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]этил}морфолин; (2S)-2- [ (S)- [2-(3-фторпропил)фенокси) (фенил)метил]-морфолин; (2S)-2-[(S)-циклопент-1-ен-1-ил(2,6-дифторфенокси)метил]-морфолин; (2S)-2-[(R)-циклопент-1-ен-1-ил(2,6-дифторфенокси)метил]-морфолин; (2S)-2-[(2,б-диметоксифенокси)(фенил)метил]-морфолин; (2S)-2-{1-[(2-этоксипиридин-З-ил)окси]-3-метилбутил}морфолин; (2S)-2- [ (S)- [ (2-циклопропилпиридин-З-ил)окси](фенил)метил]-морфолин; (2S)-2-{1-[2-(4-фторфенокси)фенокси]этил}морфолин; 171 (2S ил)метил (2S ил)метил (2S ил)метил (2S (2S (2S (2S ил)метил (2S ил)метил (2S ил)метил (2S морфолин (2S ил)окси] (2S ил)метил (2S ил)метил (2S морфолин (2S морфолин (2S (2S (2S (2S (2S морфолин (2S морфолин (2S -2- [ (S)-(2-хлор-5-фторфенокси) (пиридин-2-морфолин; -2-[(S)-(бифенил-2-илокси)(пиридин-2-морфолин; -2-[(S)-(2-циклопропилфенокси)(пиридин-2-морфолин; -2-[(S)-(2-бромфенокси)(пиридин-2-ил)метил]морфолин; -2-[[2-(фторметил)фенокси](фенил)метил]-морфолин; -2-[(2-этокси-6-фторфенокси)(фенил)метил]-морфолин; -2-[(S)-(2-фтор-6-метоксифенокси)(пиридин-2-морфолин; -2-[(S)-(2-этокси-6-фторфенокси)(пиридин-2-морфолин; -2- [ (S)- (2,6-дифторфенокси) (пиридин-2-морфолин; -2- [ (S)- [2-(3-фторпропокси)фенокси) (фенил)метил]- -2-{(1S)-2-циклогексил-1-[(2-этоксипиридин-З-этил}морфолин; -2-[(2,6-дифторфенокси)(2,3-дигидро-1-бензофуран-7--морфолин; -2-[(S)-(2-циклопропил-5-фторфенокси)(пиридин-2-морфолин; -2-[(S)-(2-фтор-6-изопропоксифенокси)(фенил)метил]- -2-[(S)-[(2-метоксипиридин-З-ил)окси](фенил)метил]- -2-[(5-фтор-2-метоксифенокси)(фенил)метил]-морфолин; -2-[(З-фтор-2-метоксифенокси)(фенил)метил]-морфолин; -2- [ (2-этокси-5-фторфенокси) (фенил)метил]-морфолин; -2-[(2-этокси-З-фторфенокси)(фенил)метил]-морфолин; -2-[(S)-(2-фтор-6-пропоксифенокси)(фенил)метил]- -2-[(2-этоксифенокси)(4-метил-1,З-оксазол-2-ил)метил] -2- [ (2,6-дифторфенокси) (4-метил-1,3-оксазол-2- ил)метил]-морфолин; (2S)-2-{(4-метил-1,З-оксазол-2-ил)[2-(трифторметокси)фенокси]метил}морфолин; (2S)-2-[(2,6-дифторфенокси)(1,З-тиазол-2-ил)метил]-морфолин; (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил )окси]пентил}морфолин; (2S)-2-[(2-бромфенокси)(4-метил-1,З-оксазол-2-ил)метил]-морфолин; (2S)-2-[(S)-(2-фтор-б-метилфенокси)(фенил)метил]-морфолин (2S)-2- [ (S)- [ (2-изопропилпиридин-З-ил)окси] (фенил)метил]-морфолин; (2S)-2-[(2-этоксифенокси)(1,З-тиазол-2-ил)метил]-морфолин (2R)-2-[(R)-(2-этоксифенокси)пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-[(2-изобутилпиридин-З-ил)окси](фенил)метил]-морфолин; (2S)-2-[(S)-(2-фтор-6-изопропилфенокси)(фенил)метил]-морфолин; (2S)-2-[(S)-(2-циклопропил-6-фторфенокси)(фенил)метил]-морфолин; (2S)-2-[(S)-(2-бром-б-фторфенокси)(6-метоксипиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-бром-б-фторфенокси)(пиридин-2-ил)метил]морфолин; (2S)-2-[(S)-(2-бромфенокси)(6-метоксипиридин-2-ил)метил]-морфолин; (2S)-2-[(S)-(2-фтор-6-метоксифенокси)(б-метоксипиридин-2-ил)метил]-морфолин; (2S)-2-{1- [ (2-этоксипиридин-З-ил)окси]-2-метилпропил}морфолин; (2S)-2-[(2-циклопропилфенокси)(4-метил-1,З-оксазол-2-ил)метил]-морфолин; (2S)-2-{(IS)-1-[(2-этоксипиридин-З-ил)окси]бутил}морфолин (2S)-2-[(S)-{[2-(циклопропилметокси)пиридин-Зил) окси} (фенил)метил]-морфолин; (2S)-2-[(S)-[2-фтор-6-(трифторметил)фенокси](фенил)метил] 173 морфолин; (2S)-2-[(S)-[2-фтор-6-(трифторметокси)фенокси)(фенил)метил]-морфолин; (S)-2-[(2-этоксифенокси)(1,З-оксазол-2-ил)метил]-морфолин; (S)-2-[(2,б-дифторфенокси)(1,З-оксазол-2-ил)метил]морфолин; (2S)-2-{(lS)-l-[(2-этоксипиридин-З-ил)окси]-2-фенилэтил}морфолин; (2S)-2-[(S)-[4-фтор-2-(метилтио)фенокси)(фенил)метил]-морфолин; (2S)-2-[(S)-(2,6-дифторфенокси)(б-метоксипиридин-2-ил)метил]-морфолин; (2R,21R)-2,21 -[пиразин-2,3-диилбис(оксиметилен)]диморфолин; (S)-2-[2-этокси-пиридин-З-илоксиметил]-морфолин; и (2R)-2-[(2-фтор-6-метоксифенокси)(пиридин-3-ил)метил]-морфолин. По доверенности 
|